
6 курс / Кардиология / Шляхто_Е_Вред_Кардиология_Национальное_руководство_2019
.pdfХирургическое лечение у бессимптомных пациентов показано при снижении функции ЛЖ (ФВ менее 50%), а также в случае, если КДР ЛЖ более 70 мм или КСР ЛЖ более 50 мм. Эта рекомендация основана на том, что частота развития необратимой дисфункции миокарда выше в тех случаях, когда оперативное лечение откладывают. Напротив, в тех случаях, когда хирургическое лечение выполнено без отсрочки, послеоперационные результаты оказываются очень хорошими. Быстрое негативное изменение параметров, характеризующих функцию желудочков, - еще одно показание к оперативному лечению у бессимптомных пациентов.
ОСОБЕННОСТИ ТАКТИКИ ВЕДЕНИЯ БОЛЬНЫХ С СИНДРОМОМ МАРФАНА И ДРУГИМИ НАСЛЕДСТВЕННЫМИ НАРУШЕНИЯМИ СОЕДИНИТЕЛЬНОЙ ТКАНИ
В случае пограничных размеров аорты во внимание следует принимать семейный и индивидуальный анамнез, возраст пациента и ожидаемый риск оперативного лечения. При наличии ФР (семейный анамнез диссекции, увеличение диаметра более 2 мм в год, тяжелая АН, планируемая беременность) показанием к оперативному лечению является диаметр корня аорты 45 мм и более. При диаметре аорты 40-45 мм имеют значение такие факторы, как быстрый темп роста размеров аорты и отягощенная наследственность, и тогда их наличие является противопоказанием к беременности.
Пациенты с марфаноподобными симптомами, вызванными заболеваниями соединительной ткани, должны лечиться так же, как пациенты с синдромом Марфана. У пациентов с БАК решение об оперативном лечении аневризмы аорты, диаметр которой больше 50 мм, основано на возрасте пациента, размерах тела, сопутствующих заболеваниях, типе хирургического вмешательства и наличии дополнительных ФР (семейный анамнез, системная гипертензия, коарктация аорты или увеличение диаметра корня аорты на 2 мм в год и более). В остальных случаях расширение корня аорты более 55 мм - показание к оперативному лечению независимо от степени АН.
Для пациентов, имеющих показания к хирургической коррекции АН, можно использовать более низкие границы диаметра корня аорты как показания к сопутствующему протезированию аорты (45 мм), в зависимости от возраста, ППТ, этиологии заболевания клапана, наличия двустворчатого аортального клапана, интраоперационной формы и толщины стенки восходящей аорты.
МИТРАЛЬНЫЙ СТЕНОЗ
Этиология
Митральный стеноз (МС) в большинстве случаев является следствием ревматической лихорадки. Ревматическое поражение МК локализуется в области клапанных комиссур, а также на самих створках клапана и хордальном аппарате. Воспалительный процесс приводит к сращению комиссур, фиброзу и кальцификации створок, укорочению и утолщению хорд. Дегенеративные и врожденные стенозы МК встречаются достаточно редко. К другим причинам МС относят карциноид, болезнь Фабри, мукополисахаридоз, подагру, коллагенозы, обструкцию клапана опухолью предсердия или крупной вегетацией.
Патофизиология
Площадь митрального отверстия в норме составляет 4-6 см2, однако при сужении митрального отверстия до 2 см2 сколько-нибудь существенного градиента давления
между ЛП и ЛЖ практически не возникает. При сужении отверстия <1,5 см2 или 1 см2 на единицу ППТ МС принято считать значимым. В таких случаях трансмитральный градиент давления сопровождается повышением давления в ЛП, в легочных венах и капиллярах.
Первоначально градиент давления в состоянии покоя отсутствует и появляется лишь при ФН. Постепенно для повышения давления в малом круге необходима все меньшая нагрузка, и давление становится повышенным в состоянии покоя. Отек легких, связанный с транссудацией из легочных капилляров, развивается при повышении давления заклинивания до 25 мм рт.ст. и более. Трансмитральный градиент зависит от ЧСС и трансмитрального кровотока, а толерантность к ФН различна при различной степени выраженности МС. Ограничение переносимости ФН зависит от величины УО, растяжимости кольца МК и состояния ЛП. Сама по себе ЛГ, столь характерная для МС, определяется не только повышением давления в ЛП, но и морфологическими изменениями легочной сосудистой сети, постепенно формирующимися под влиянием хронической ЛГ. Последняя постепенно приводит к гипертрофии ПЖ и развитию правожелудочковой недостаточности.
Несмотря на то, что сократительная способность ЛЖ сохранена, длительное снижение преднагрузки и увеличение постнагрузки часто приводят к появлению его дисфункции. ФП, являющаяся частой спутницей МС, развивается в результате дилатации ЛП, ревматического повреждения миокарда предсердия, межузловых проводящих путей и СА-узла. ФП усугубляет гемодинамические нарушения из-за потери вклада предсердной сократимости в наполнение ЛЖ и увеличивает риск тромбоэмболических осложнений.
Диагностика
ЖАЛОБЫ, АНАМНЕЗ
Наиболее характерная жалоба пациентов с МС - одышка, в начале появляющаяся при ФН. Одышка связана с повышением давления в ЛП и малом круге кровообращения и может усиливаться при психоэмоциональном напряжении, беременности, инфекционных заболеваниях, как, впрочем, и при любых состояниях и усилиях, сопровождающихся тахикардией. Особую роль в усилении одышки может играть ФП. К другим жалобам, характерным для таких больных, относят перебои в работе сердца, связанные с ПЭ, и кровохаркание, вызванное повышением давления и повреждением сосудов малого круга кровообращения. Предвестник развития ФП - частая ПЭ, которая постепенно сменяется кратковременными пароксизмами ФП с последующим переходом этой аритмии в постоянную форму.
Одно из типичных осложнений МС - тромбоэмболия сосудов большого и малого круга, связанная с образованием тромбов в предсердиях. Для больных с МС и ФП особенно характерны эмболические инсульты. При развитии декомпенсации и присоединении правожелудочковой недостаточности возникают повышенная утомляемость, слабость, дискомфорт в животе из-за гепатомегалии и нарушения функций печени. При МС может встречаться симптом Ортнера - осиплость голоса, связанная с микротравматизацией возвратного нерва из-за увеличения ЛП.
ФИЗИКАЛЬНОЕ ОБСЛЕДОВАНИЕ
При осмотре больных с МС обращает на себя внимание своеобразный румянец на лице, описываемый как «facies mitralis». При пальпации прекардиальной области выявляют
сердечный толчок и эпигастральную пульсацию как результат ГПЖ, развивающейся при развернутой клинической картине порока. Характерное диастолическое дрожание, напоминающее «кошачье мурлыкание», выявляется при пальпации прекардиальной области. Такое дрожание связано с затрудненным выбросом крови из ЛП, что сопровождается возникновением ускоренного турбулентного потока через суженное АВотверстие, вызывающего дрожание верхушки сердца и передней грудной стенки. При миогенной дилатации ЛП и ФП этот пальпаторный симптом исчезает.
При аускультации выявляется громкий «хлопающий» I тон, возникающий при условии сохранения подвижности створок МК. Появление такого тона объясняется быстрым повышением давления и увеличенной площадью соприкосновения створок в недостаточно заполненном ЛЖ. Отсутствие акцентуации I тона может быть связано с сопутствующей митральной регургитацией или ограниченной подвижностью створок при их фиброзе и кальцинозе. Митральный щелчок (МЩ) особенно характерен для МС. Он возникает в момент внезапного прекращения движения створок в полость ЛЖ. Время появления МЩ после II тона характеризует степень МС. Интервал от аортального компонента II тона до МЩ колеблется в диапазоне 0,04-0,12 с, и чем он короче, тем более высокое давление в ЛП и тяжелее МС. МЩ лучше выслушивается над верхушкой при использовании диафрагмы фонендоскопа (высокочастотная составляющая). Не менее характерен для МС диастолический шум, обычно появляющийся сразу после МЩ. При легкой степени МС диастолический шум обычно короткий с пресистолическим усилением при сохраненном СР. Тяжелый МС сопровождается появлением голодиастолического шума. При появлении ЛГ возникают акцент II тона над ЛА и систолический шум недостаточности ТК, который выслушивается над мечевидным отростком и в отличие от шума МН возрастает по интенсивности на высоте вдоха. Кроме того, для ЛГ и пульмональной регургитации характерен шум Грэхема-Стилла, появляющийся в протодиастоле и практически примыкающий ко II тону.
НЕИНВАЗИВНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ
ЭхоКГ - важнейший метод диагностики и оценки степени выраженности МС. Морфологические изменения клапана хорошо видны в двухмерном режиме, который позволяет визуализировать диастолический прогиб створок, вызванный их сращением по комиссурам. Выраженность стеноза принято определять планиметрически при проведении ЭхоКГ исследования в парастернальном сечении по короткой оси (рис. 26.5, см. цв. вклейку).
Планиметрический расчет следует дополнять расчетом площади митрального отверстия по уравнению непрерывности потока при отсутствии значимой митральной регургитации. Морфологическая оценка состояния клапана особенно важна для отбора больных для проведения чрескожной баллонной вальвулопластики. Ее проводят с использованием данных, полученных при трансторакальном ЭхоКГ исследовании с учетом мобильности створок, выраженности утолщения створок и хордального аппарата, а также наличия и степени выраженности кальциноза. Не менее важная ЭхоКГ характеристика состояния клапана при МС - средний диастолический градиент давления на клапане, определяемый с помощью постоянноволновой допплерографии.
Интегральный подход к оценке выраженности МС представлен в табл. 26.1. ЭхоКГ позволяет также оценить давление в ЛА, выявить нередко сопутствующую МС митральную регургитацию, оценить размеры камер сердца.
Несмотря на то, что трансторакальный доступ в большинстве случаев дает достаточную информацию для выбора тактики ведения пациента, перед проведением чрескожной баллонной вальвулопластики следует проводить ЧПЭ исследование, позволяющее исключить наличие тромбов в ЛП и уточнить морфологию МК.
Рентгенография. Признаки изменения размеров тени сердца во фронтальной проекции на ранних стадиях могут отсутствовать, в то время как в боковой проекции выявляют признаки увеличения размеров ЛП. Признаки увеличения дуги ЛА, ПЖ и ПП обычно появляются при тяжелом МС. Прогрессирование признаков декомпенсации порока часто сопровождается признаками интерстициального и альвеолярного отека легких.
ЭКГ позволяет выявить признаки увеличения ЛП, которое проявляется увеличением Pd до 0,12 с и отклонением угла альфа Р влево от +45° до -30°. Вслед за признаками увеличения ЛП и нарушения внутрипредсердной проводимости развивается ФП, обусловленная прогрессирующим растяжением ЛП, развитием фиброза и возрастом больного. Появление на ЭКГ признаков увеличения ПЖ зависит от повышения систолического давления в ПЖ. При давлении 70-100 мм рт.ст., как правило, появляется отклонение ЭОС вправо и увеличение соотношения R:S в правых грудных отведениях более 1,0.
Велоэргометрия позволяет объективизировать физическое состояние пациента в сомнительных случаях, когда клиническая картина не соответствует результатам оценки тяжести МС. Точно так же стресс-ЭхоКГ может помочь оценить динамику градиента давления на МК и изменения давления в ЛА.
ИНВАЗИВНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ
Сегодня, благодаря возможностям ЭхоКГ диагностики, прямые гемодинамические измерения с использованием катетерной техники для оценки состояния больных с МС практически не используют. Согласно принятым стандартам, в предоперационном периоде больным с МС выполняют КАГ.
Естественное течение болезни
В большинстве развивающихся стран МС обычно выявляется у детей и лиц молодого возраста и становится результатом ревматической лихорадки, в то время как в развитых странах МС возникает у лиц 40-50 лет вследствие склеродегенеративных изменений МК. Темпы прогрессирования МС крайне вариабельны и составляют 0,1-0,3 см2 в год. У бессимптомных больных 10-летняя выживаемость составляет 84%, у малосимптомных больных - 42%, у симптомных больных 5-летняя выживаемость составляет 44%. В процессе естественного течения МС возможны как постепенное ухудшение состояния, так и внезапное ухудшение, вызванное одним из возможных осложнений. ФП может развиваться как у симптомных, так и у бессимптомных больных, и ее частота у больных с МС увеличивается с возрастом и увеличением размеров ЛП. Частота тромбоэмболических осложнений нарастает с увеличением возраста, размеров ЛП, степени сужения митрального отверстия, возникновением признаков спонтанного контрастирования в ЛП при проведении ЭхоКГ.
Медикаментозное лечение
Симптомные больные с МС нуждаются в постоянной медикаментозной поддержке. Уменьшение одышки достигают при использовании диуретиков и нитратов пролонгированного действия. β-Адреноблокаторы и БКК позволяют контролировать ЧСС. Антикоагулянтная терапия показана больным с ФП или при признаках спонтанного контрастирования по данным ЭхоКГ. У больных с сохранным СР антикоагулянты показаны при наличии тромбов в ЛП или указаний на тромбоэмболии в анамнезе.
Не следует предпринимать попытки восстановления СР у больных с выраженными признаками МС до проведения оперативного вмешательства. Попытка восстановления СР оправдана при небольшой длительности существования ФП и умеренном увеличении ЛП вскоре после успешно проведенной операции. Больным с МС следует проводить мероприятия, направленные на профилактику ИЭ.
Хирургическое лечение
Баллонная катетерная митральная вальвулопластика (БКМВП) была предложена в 80-х годах прошлого столетия и доказала свою эффективность. Сегодня она рекомендована симптомным больным с МС и площадью митрального отверстия <1,5 см2 (класс рекомендаций I, уровень доказательности В, С). БКМВП приводит к надрыву комиссур и обычно обеспечивает увеличение площади митрального отверстия вдвое, что сразу вызывает улучшение работы МК и снижение давления в ЛП. Частота осложнений варьирует в пределах 1-15% и зависит от состояния больного и опыта хирургической бригады. Сегодня имеются данные о результатах отдаленного послеоперационного периода, которые подтверждают длительную эффективность этой процедуры. При неудовлетворительных результатах БКМВП возникает необходимость хирургического вмешательства. Прогноз отдаленных результатов БКМВП зависит от многих факторов.
К «неблагоприятным» факторам для пациентов как кандидатов на БКМВП относят:
•клинические данные: возраст, комиссуротомии в анамнезе, IV ФК СН, персистирующая форма ФП, значимая ЛГ;
•анатомические характеристики: кальциноз МК, очень маленькое левое АВ-отверстие, значимая трикуспидальная недостаточность (ТН).
Критерии значимого МС:
•площадь митрального отверстия <1 см2;
•средний градиент на МК >10 мм рт.ст.
Проведение БКМВП противопоказано в следующих случаях:
•площадь левого АВ более 1,5 см2;
•умеренная и более МН;
•значимый или двустворчатый кальциноз МК;
•отсутствие комиссуральных сращений;
•значимое поражение аортального клапана и ТК;
•значимое поражение КА, требующее АКШ.
К хирургическим методам лечения больных с выраженным МС относят закрытую комиссуротомию МК, которую до настоящего времени довольно широко используют в
развивающихся странах. Сегодня ее заменила митральная комиссуротомия на открытом сердце с использованием экстракорпорального кровообращения (ЭКК), что позволяет провести полную ревизию аппарата МК и обеспечивает хорошие отдаленные результаты вмешательства.
В случае тяжелого поражения аппарата МК можно выполнять его протезирование с использованием механического искусственного протеза. Операционная летальность при этой операции варьирует в пределах 3-10% и корреллирует с возрастом, ФК, ЛГ и наличием ИБС. Выживаемость больных в послеоперационном периоде во многом зависит от исходного функционального состояния ЛЖ, осложнений, возникающих со стороны протеза (тромбоэмболии) и связанных с необходимостью длительной антикоагулянтной терапии.
Стратегия лечения
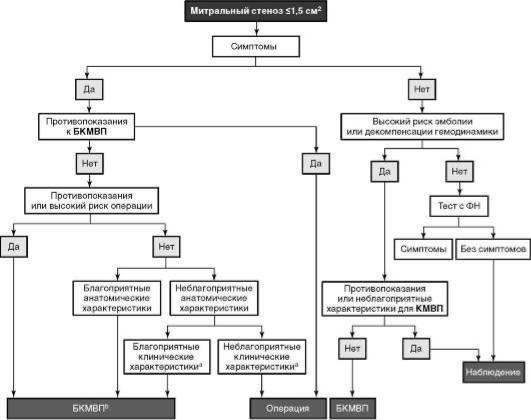
Алгоритм ведения пациентов со значительным МС, рекомендованный ЕОК, представлен на рис. 26.6 [9].
Рис. 26.6. Тактика ведения больных с митральным стенозом. БКМВП - баллонная катетерная митральная вальвулопластика; a - неблагоприятные условия для БКМВП определяются наличием следующих характеристик: клинические характеристики - возраст, комиссуротомия в анамнезе, класс IV NYHA, постоянная форма ФП, тяжелая легочная гипертензия; анатомические характеристики - кальцификация митрального клапана по данным рентгеноскопии, очень маленькая площадь отверстия МК, тяжелая трикуспидальная регургитация; b - хирургическая комиссуротомия может быть выполнена опытной хирургической бригадой или у пациентов, имеющих противопоказания к чрескожной митральной комиссуротомии
СИМПТОМНЫЕ БОЛЬНЫЕ
БКМВП - метод выбора у симптомных больных, имеющих противопоказания к проведению оперативного вмешательства, или у больных молодого возраста с сохранным СР. Однако есть множество факторов, связанных с особенностями анатомической структуры клапанов, которые могут влиять на исход БКМВП. Речь идет о наличии и степени выраженности кальцификации МК, выраженности ХСН, степени сужения отверстия. При наличии противопоказаний к проведению БКМВП (наличие тромбов в ЛП, выраженная кальцификация, выраженный стеноз МК, сочетание МС с поражением аортального клапана и ТК, наличие ИБС) альтернативой чрескожной митральной баллонной комиссуротомии является хирургическое вмешательство по замене МК.
БЕССИМПТОМНЫЕ БОЛЬНЫЕ
Бессимптомным пациентам показана медикаментозная терапия, а при выраженном стенозе - БКМВП. Вальвулопластика показана пациентам с высоким риском развития тромбоэмболических осложнений (тромбоэмболии в анамнезе, спонтанное контрастирование ЛП и пароксизмы ФП). Кроме того, БКМВП показана при высоком риске гемодинамической декомпенсации (систолическое давление в ЛА более 50 мм рт.ст.), при необходимости выполнения внесердечной хирургической операции и планируемой беременности.
ОСОБЫЕ КАТЕГОРИИ ПАЦИЕНТОВ
Речь идет о больных, у которых возникла необходимость в повторной операции при развитии рестеноза. В подобных случаях практически всегда необходима замена клапана. Другие категории пациентов с МС, требующей специальных знаний, - беременные, а также лица старших возрастных групп, поскольку оперативное вмешательство в подобных случаях сопровождается высоким риском развития осложнений. У всех особых категорий пациентов при наличии показаний и при благоприятных анатомических возможностях предпочтительной является чрескожная митральная баллонная комиссуротомия. Оперативное вмешательство целесообразно лишь при отрицательных результатах комиссуротомии.
МИТРАЛЬНАЯ НЕДОСТАТОЧНОСТЬ
Митральная недостаточность (МН) - второе по частоте заболевание клапанного аппарата, требующее оперативного вмешательства [14]. Благодаря развитию хирургической техники и получившим в последние годы широкое распространение реконструктивным операциям, подходы к лечению МН подвергнуты существенному пересмотру.
Этиология
Аппарат МК включает в себя створки, хорды, папиллярные мышцы и митральное кольцо. Нарушения структуры и функции любого из звеньев аппарата МК могут лежать в основе МН. Наиболее частые причины МН - пролапс митрального клапана (ПМК), ревматизм, ИЭ, кальциноз кольца МК, ИБС и КМП. Особенности МН, возникающей при ПМК, будут рассмотрены отдельно. Различают:
•первичную (органическую) МН, при которой аномалии строения аппарата МК лежат в ее основе;
•вторичную (функциональную) МН, возникающую при патологических изменениях ЛЖ.
ПЕРВИЧНАЯ МИТРАЛЬНАЯ НЕДОСТАТОЧНОСТЬ
Первичная МН может развиться при любой патологии, в которую вовлекается один или несколько компонентов аппарата МК. Наиболее частая причина первичной МН - первичный ПМК, сопровождающийся миксоматозной дегенерацией створок. ПМК может быть одним из проявлений ряда менделирующих наследственных нарушений соединительной ткани (ННСТ), таких как синдромы Марфана , Элерса-Данло , но нередко носит спорадический характер и характеризуется аутосомно-доминантным типом наследования и генетической гетерогенностью (см. ниже). Снижение заболеваемости ревматизмом и увеличение продолжительности жизни в промышленно развитых странах постепенно изменили распределение этиологических факторов таким образом, что МН дегенеративной природы сегодня стала наиболее распространенной [14]. Тем не менее ревматизм нередко сопровождается формированием МН, как правило, в сочетании с МС. ИЭ также одна из частых причин развития МН и может вызвать перфорацию створок или отрыв хорд. В основе развития острой первичной МН может лежать и острый ИМ, сопровождающийся разрывом папиллярной мышцы.
ВТОРИЧНАЯ МИТРАЛЬНАЯ НЕДОСТАТОЧНОСТЬ
Развитие МН довольно характерно для больных ИБС. Другая причина вторичной МН - ДКМП, сопровождающаяся растяжением МК и смещением папиллярных мышц, что приводит к нарушению закрытия створок.
Патофизиология
МН характеризуется обратным током крови из полости ЛЖ в ЛП во время систолы желудочков (митральная регургитация). Как было отмечено выше, МН может развиваться при растяжении митрального кольца, избыточных размерах створок клапана, удлинении и разрыве хорд, ремоделировании ЛЖ. Объем регургитации определяется площадью отверстия регургитации, градиентом систолического давления и длительностью систолы.
Острая митральная регургитация
Острая митральная регургитация из-за разрыва папиллярной мышцы может развиться у пациентов с острым ИМ и привести к отеку легких. Точно так же при миксоматозе створок на фоне первичного классического ПМК существует опасность отрыва хорды, удерживающей створку клапана, что сопровождается развитием острой митральной регургитации. При этом резко возрастает давление в ЛП, что сопровождается повышением давления в малом круге кровообращения. Несмотря на увеличение ФВ изза митральной регургитации, УО оказывается сниженным, что приводит к развитию тахикардии, необходимой для поддержания минутного объема кровообращения.
Хроническая митральная недостаточность
МН приводит к изотонической гиперфункции ЛЖ и перегрузке дополнительным объемом. Суммарный выброс из ЛЖ - результат сложения объема крови, выброшенного в аорту и в ЛП. В результате объемная перегрузка зависит от степени выраженности митральной регургитации. Если объем регургитационного потока невелик, гемодинамические сдвиги оказываются мало выраженными и не проявляются клинически. Левые камеры сердца незначительно расширяются, что позволяет вместить дополнительный объем крови и долгие годы компенсировать небольшие нарушения центральной гемодинамики. При значительном объеме митральной регургитации происходит увеличение камер сердца, что в итоге приводит к срыву адаптации и постепенному снижению сократительной способности ЛЖ.
Часть крови, остающаяся в ЛЖ при ослаблении его сократительной способности, приводит к повышению сопротивления к поступлению крови из ЛП, что, в свою очередь, вызывает повышение давления в ЛП и малом круге кровообращения. При декомпенсации хронической МН возрастает постнагрузка и может развиться ХСН.
Диагностика
АНАМНЕЗ
При острой МН больные, как правило, отмечают внезапное появление выраженной одышки, а нередко и развитие удушья с клиникой сердечной астмы. При хронической МН симптомы ХСН могут отсутствовать в течение многих лет. Анамнестические данные позволяют думать о возможности хронической МН у больных, перенесших воспалительные заболевания (ревматизм, системная красная волчанка), ИЭ, а также при поражении клапанного аппарата, связанном с ННСТ (синдромы Марфана и ЭлерсаДанло, первичный ПМК).
ФИЗИКАЛЬНОЕ ОБСЛЕДОВАНИЕ
Физикальное обследование больных с хронической МН позволяет выявить смещение верхушечного толчка влево и вниз. Аускультативная картина характеризуется снижением I тона и систолическим шумом над верхушкой, который обычно примыкает к I тону и проводится в аксиллярную область. Весьма характерно для МН появление III тона, связанного с увеличенным объемом крови, поступающим в полость ЛЖ.
НЕИНВАЗИВНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ
ЭхоКГ должна включать оценку степени тяжести, механизмов митральной регургитации, возможности реконструктивного вмешательства. Критерии оценки тяжести первичной митральной регургитации описаны в табл. 26.2. Оценку объема и эффективной площади отверстия регургитации проводят, исходя из площади проксимальной изоскоростной поверхности (PISA) (рис. 26.7, см. цв. вклейку). Объем более 60 мл или эффективная площадь отверстия более 40 мм2 указывают на тяжелую первичную регургитацию. Для вторичной МН критерии тяжести более мягкие - 30 мл и 40 мм2 соответственно. Окончательный анализ тяжести митральной регургитации требует интегральной оценки результатов допплерэхокардиографии и морфологических параметров. Последствия хронической МН для ЛЖ оценивают с помощью ЭхоКГ путем измерения объемов ЛП, ЛЖ и расчета ФВ. Необходимо помнить, что ФВ включает в себя как поток, направленный в аорту, так и поток крови, направленный назад в ЛП.
Чреспищеводную ЭхоКГ обычно проводят при планировании оперативного вмешательства и для оценки результатов реконструктивной операции.
Стресс-ЭхоКГ позволяет получить количественную оценку митральной регургитации, индуцированной нагрузкой, провести измерение систолического давления в ЛА и функции ЛЖ [15]. Появившиеся в последние годы новые методы исследования, оценка глобальной продольной деформации и региональной сократимости могут быть полезны для ранней диагностики нарушений сократимости и послеоперационной оценки дисфункции ЛЖ.
Один из предикторов исхода МН - нейрогормональная активация, которую оценивают при исследовании уровня МНУП. Значения МНУП >105 мкг/мл дают основание думать о высоком риске развития СН, дисфункции ЛЖ или высоком риске смерти бессимптомных
пациентов с МН [16]. Концентрация МНУП в плазме имеет высокую отрицательную прогностическую ценность и может быть полезной при динамическом наблюдении за бессимптомными пациентами.
Рентгенография при выраженной МН показывает признаки увеличения размеров сердца влево и вверх, признаки застоя крови в малом круге кровообращения.
ЭКГ при МН выявляет признаки увеличения ЛЖ и ЛП. При длительно существующей хронической МН могут появляться признаки увеличения правых отделов сердца, связанные с ЛГ.
ИНВАЗИВНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ
Катетеризация сердца может быть использована при получении противоречивых данных клинического и ЭхоКГ обследований. Ее проведение необходимо в предоперационном периоде.
Естественное течение
Острая митральная регургитация - неотложное состояние и при отсутствии своевременного вмешательства имеет неблагоприятный прогноз. Несмотря на то, что у пациентов с разрывом хорды после периода острой симптоматики клиническое состояние может стабилизироваться, отказ от оперативного вмешательства несет в себе плохой прогноз вследствие последующего развития нарастающей ЛГ.
ХРОНИЧЕСКАЯ МИТРАЛЬНАЯ НЕДОСТАТОЧНОСТЬ
При хронической МН постепенно развиваются признаки срыва адаптации к гиперфункции и ремоделирование левых отделов сердца. При тяжелой бессимптомной хронической митральной регургитации расчетная 5-летняя смертность от любой причины, будь то ВСС, ХСН или новые случаи ФП, требующие медикаментозного лечения, составляет 22-25%, 14-17% и 33-36% соответственно. Дополнительные предикторы неблагоприятного исхода - возраст больного, развитие ФП, тяжелая степень митральной регургитации, ЛГ, расширение легочных вен, увеличение КСО и низкая ФВ
[17].
ФУНКЦИОНАЛЬНАЯ ХРОНИЧЕСКАЯ МИТРАЛЬНАЯ НЕДОСТАТОЧНОСТЬ
Течение функциональной хронической МН зависит от причины, лежащей в основе ее развития. При ИБС и остром ИМ, а также при КМП присоединение функциональной МН вносит свой вклад в неблагоприятный прогноз.
Медикаментозное лечение
При острой МН рекомендуют использование диуретиков и нитратов. Хроническая МН у бессимптомных больных с легкой степенью митральной регургитации не требует специального лечения. Использование вазодилататоров не предупреждает и не замедляет развитие дисфункции ЛЖ. Эти препараты не следует назначать больным, которым рекомендовано оперативное вмешательство. У больных с МН, сочетающейся с АГ, необходимо проводить лечение гипертензии, поскольку последняя увеличивает градиент давления между ЛЖ и ЛП и таким образом способствует увеличению митральной регургитации.
