
6 курс / Кардиология / Аритмии_сердца_Механизмы,_диагностика,_лечение_в_3_х_томах_Том_2
.pdfЭктопическое возникновение аберрантных комплексов
Аберрацию ускользающего возбуждения АВ-соединения можно также объяснить с точки зрения аномальности места его происхождения. Rick считает таким местом волокна Махайма [226]. Позднее Masumi и соавт. [236], а также Lie и соавт. [242] пришли к заключению, что многие из таких возбуждений возникают скорее в ветвях (передняя или задняя ветвь) левой ножки пучка Гиса, нежели в АВ-соединении. При таких возбуждениях следует ожидать появления относительно узких комплексов QRS с признаками неполной блокады правой ножки пучка Гиса, что представляет одну из возможных причин аберрации комплексов АВ-соединения с картиной блокады правой ножки. Однако таким образом нельзя объяснить аберрацию типа блокады левой ножки пучка Гиса и неспецифические типы аберрации. Более того, в этом случае остается без ответа вопрос о механизмах аберрации длительного цикла для синусовых возбуждений.
Влияние парасимпатической нервной системы
Поскольку во многих описанных ранее случаях аберрации наблюдались в сочетании с вагусноопосредованным замедлением синусового ритма, было также выдвинуто предположение, что удлинение QRS- обусловлено прямым депрессивным влиянием ацетилхолина на проведение в системе Гис—Пуркинье [222, 223, 229]. Однако данные об отсутствии угнетающего влияния ацетилхолина на нормальную систему Гис—Пуркинье [25], а также о его способности реально улучшать проведение в угнетенных тканях [251] исключают данное объяснение. Dressier предложил другое объяснение, согласно которому повышение парасимпатической активности вызывает изменение формы комплекса QRS вследствие вагусного сосудосуживающего эффекта [227]. Однако это не позволяет объяснить случаи аберрации, когда влияние парасимпатической активации несомненно отсутствует, например при аберрации наджелудочковых комплексов вскоре после постэкстрасистолических пауз.
Деполяризация в фазу 4
Латентные пейсмекерные клетки. Четвертый возможный механизм аберрации длительного цикла при замедленном синусовом ритме и при ритме ускользания в АВ-со- единении основывается на существовании в системе Гис—Пуркинье большого числа автоматических клеток (латентных водителей ритма), способных к спонтанной диастолической деполяризации [56, 238—241]; возникновение аберрации при этом обусловлено описанной ранее взаимосвязью автоматизма и проводимости (рис. 4.19) [56].
Медленное повышение диастолического потенциала, происходящее при деполяризации в фазу 4, вызывает постепенное, зависящее от потенциала и времени уменьшение Vmax и амплитуды потенциала действия, инициируемого в позднюю фазу диастолы, а также развитие нарушений, аналогичных наблюдаемым в не полностью реполяризованных волокнах (см. рис. 4.19) [56]. Поскольку латентные пейсмекерные клетки имеются практически везде в системе Гис—Пуркинье, ускорение их деполяризации в фазу 4 способно вызывать практически любой тип нарушений предсердно-желудочково- го и внутрижелудочкового проведения, причем конкретная картина аберрации определяется локализацией аномальных волокон и степенью их деполяризации. Во всех случаях, когда такие волокна расположены в ножках пучка Гиса, наблюдаются изменения формы комплекса QRS, которые представляют собой аберрацию. Усиленный автоматизм в дистальных сегментах АВ-узла (зона NH) или в пучке Гиса, который обычно проявляется АВ-блокадой, при развитии продольной диссоциации предсердно-желудочковой проводящей системы может вызвать нарушение внутрижелудочкового проведения и аберрацию. Поскольку такая аберрация обусловлена уменьшением абсолютной величины мембранного потенциала во время фазы 4 потенциала действия, ее называют «блоком в фазу 4» или «аберрацией в фазу 4» [11, 238]. Однако эти термины недостаточно точны, так как они используются для описания аберрации, связанной со стабильным повышением потенциала покоя без медленной диастолической деполяризации.
Massumi [234] составил перечень электрокардиографических характеристик аберрации длительного цикла. Из особенностей природы предложенного механизма следует, что постепенное увеличение длительности сердечного цикла должно сопровождаться усилением аберрантности. Это наглядно показано на рис. 4.18. И наоборот, факторы, замедляющие деполяризацию в фазу 4, предупреждают развитие аберрации длительного цикла и ослабляют или устраняют уже существующую аберрацию. Примером тому служит сокращение синусового цикла при физической активности или под влиянием таких препаратов, как атропин, а также повышение частоты основного ритма сердца вследствие имплантации пейсмекера в случаях брадиаритмии, как и фармакологическое подавление деполяризации в фазу 4. Таким образом, при выяснении причин аберрантности в неясных случаях целесообразно применение воздействий, изменяющих частоту синусового ритма.
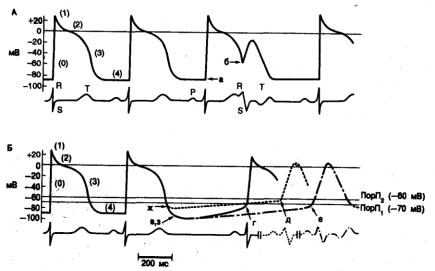
Рис. 4.19. Схематическое изображение трансмембранных потенциалов латентного пейсмекера в системе Гис—Пуркинье и одновременно полученная поверхностная ЭКГ, которые иллюстрируют взаимосвязь автоматизма и проведения.
Фазы потенциала действия обозначены арабскими цифрами от 0 до 4, а ЭКГ-дефлексии — латинскими буквами Р, R, S и Т. А — во время первых трех возбуждений стимуляция проводилась достаточно быстро и деполяризация в фазу 4 оказалась подавленной — ситуация, аналогичная наблюдаемой при синусовом ритме. Мембранный потенциал имеет нормальную величину и остается постоянным во время диастолы (фаза 4). Потенциалы действия, развивающиеся примерно на уровне —90 мВ (а), так же нормальны, как и ЭКГ. Фаза реполяризации третьего возбуждения прерывается преждевременным ответом, который возникает приблизительно на уровне —60 мВ (б) и характеризуется существенным уменьшением амплитуды и Упшг, а также угнетенным проведением, что электрокардиографически проявляется аберрантной формой RS. Б — первые два возбуждения зарегистрированы при той же частоте стимуляции, что и на фрагменте А. Потенциалы действия и ЭКГ нормальны. Третье, четвертое и пятое возбуждения инициируются после развития деполяризации в фазу 4 вследствие сильного снижения частоты стимуляции. Третий потенциал действий, как показано, возникает в клетке при нормализации максимального диастолического потенциала (МДП, —90 мВ) и порогового потенциала (ПорП\, г, приблизи- тельно—70 мВ). Поскольку процесс деполяризации не может уменьшить диастолический потенциал до величины ниже пороговой (ПорП), наблюдаемое в результате снижение амплитуды и Vmax является недостаточным для значительного угнетения проведения, поэтому ЭКГ остается нормальной. Четвертый потенциал действия отражает эффект смещения ПорП к менее отрицательному уровню (ПорП г). Такое смещение позволяет четвертому потенциалу действия инициироваться при значительно более низком потенциале — примерно —60 мВ (д), чем в норме. Снижение амплитуды и У max, а также замедление проведения становятся соответственно более выраженными. Комплекс RS на ЭКГ является аберрантным. Обратите внимание на сходство с преждевременным ответом на фрагменте А, который также инициируется на уровне примерно —60 мВ. Кроме того, следует отметить, что смещение ПорП сопровождается уменьшением МДП (е). Пятый потенциал действия показывает, как изменения реактивности типа представленных на фрагменте Б рис. 4.3 предрасполагают к аберрации вследствие деполяризации в фазу 4 при более отрицательных, чем обычно, потенциалах и при нормальном ПорП. Обратите внимание: хотя это возбуждение возникает на уровне около —70 мВ (ж), амплитуда и Vmax снижены достаточно для замедления проведения и появления аберрации комплекса RS. Это напоминает скорее четвертый ответ, возникающий на уровне примерно —60 мВ (д), нежели третий, хотя он также развивается на уровне —70 мВ (г). Снижение амплитуды и Vmax сверх ожидаемого, а также угнетение проведения для данного уровня потенциала отражают изменение реактивности [56}.
Кроме того, у больных с аберрацией, обусловленной деполяризацией в фазу 4, можно ожидать появления желудочковых экстрасистол, происходящих из области повышенного автоматизма: у больных с аберрацией типа блокады правой ножки пучка Гиса должны возникать экстрасистолы с признаками блокады левой ножки, и наоборот. Выявление экстрасистол соответствующего типа подтверждает обусловленность аберрации длительного цикла усиленным автоматизмом. На рис. 4.17, Б и 4.18 показано развитие аберрации типа блокады левой и правой ножек пучка Гиса в сочетании с наличием желудочковых эктопических сокращений, соответственно с формой блокады правой и левой ножек. На рис. 4.18 также наблюдается одновременное исчезновение аберрации и эктопии.
Электрофизиологические детерминанты. Аберрации, обусловленные деполяриза-
цией в фазу 4 потенциала действия, вероятнее всего, возникнут в условиях усиления автоматизма латентных пейсмекерных клеток в системе Гис—Пуркинье, из которых наиболее очевидны следующие два обстоятельства.
1. Снижение частоты сердечного ритма в результате ослабления активности синусового узла или вследствие таких факторов, как АВ-блокада высокой степени или блокирование предсердной экстрасистолы. Продолжительная диастола дает достаточно времени для развития деполяризации в фазу 4 с последующим снижением уровня диастолического мембранного потенциала, с которым сталкивается распространяющийся импульс (см. рис. 4.19, Б). Это одно из возможных объяснений аберрации, возникающей при снижении частоты ритма до уровня, близкого К собственной частоте возбуждений латентных пейсмекеров АВ-соединения или системы Гис—Пуркинье или ни-
же (^40— 55 уд/мин) (см. рис. 4.17, Б).
2. Прямое усиление автоматизма латентных водителей ритма. Ряд физиологических воздействий, таких как изменения рН, рСО2 и температуры, ишемия, перерастяжение в дилатированном сердце, изменения внеклеточных концентраций ионов, а также многие медикаментозные средства, в том числе сердечные гликозиды, вызывают повышение скорости деполяризации в фазу 4 латентных пейсмекерных клеток системы Гис—Пуркинье [25, 28, 38—47]. Это позволяет объяснить явление, показанное на рис. 4.18, где аберрация возникает при небольшом увеличении длительности цикла и при такой частоте синусового ритма, которая обычно не обеспечивает значительной деполяризации латентных пейсмекерных клеток в фазу 4.
Учитывая большое количество автоматических клеток в сердце, а также существование целого ряда физиологических и фармакологических факторов, угнетающих активность синусового узла или повышающих автоматизм латентных пейсмекеров, можно сделать вывод, что данный тип аберрации должен быть достаточно обычным. Однако имеющиеся в литературе данные не подтверждают этого заключения. Это особенно касается больных с клинически здоровым сердцем, так как в большинстве случаев явление описано в органически пораженном сердце.
Анализ связи между мембранным потенциалом и скоростью проведения [56, 115] позволяет объяснить этот явный парадокс. Как отмечалось ранее, проведение возбуждения обычно поддерживается и даже несколько улучшается до тех пор, пока мембранный потенциал не становится меньше — 70 мВ, чему способствуют следующие факторы: 1) уменьшение тока, необходимого для возбуждения (т. е. повышение возбудимости), по мере приближения диастолического потенциала к пороговому уровню; 2) увеличение константы длины вследствие повышения сопротивления мембраны при деполяризации в фазу 4. Оба фактора способствуют повышению эффективности электротонического распространения тока и компенсируют снижение Удах при деполяризации [56]. Поскольку пороговый потенциал в нормальных волокнах Пуркинье близок к —70 мВ [116], деполяризация в фазу 4 не способна уменьшить диастолический мембранный потенциал до менее отрицательной величины: при потенциале выше порогового обязательно возникнет спонтанное возбуждение, а значит, и желудочковая экстрасистола. Поэтому в нормальном миокарде деполяризация в фазу 4 вряд ли вызовет медленное проведение и аберрацию (см. рис. 4.19, Б).
Однако в некоторых особых условиях деполяризация в фазу 4 способна вызывать значительное уменьшение диастолического потенциала, вполне достаточное для, развития аберрации, причем одно из таких условий может выполняться и в нормальном миокарде. На рис. 4.20 показана активность латентных пейсмекерных клеток, в которых скорость деполяризации в фазу 4 повышена; она лишь немного ниже скорости диастолической деполяризации клеток синусового узла. При таких близких частотах возбуждение синусового узла может достигнуть латентной пейсмекерной клетки в момент приближения ее диастолического потенциала к пороговому уровню. Так как по-
роговый потенциал определяет переход между диастолой (фаза 4) и быстрой деполяризацией (фаза 0) следующего потенциала действия, при его достижении происходит быстрое нарастание скорости деполяризации и резкое уменьшение мембранного потенциала за очень короткое время (10—20 мс). В таких условиях даже очень небольшие вариации во времени прихода распространяющегося импульса, которые обусловлены либо изменением синусового ритма, либо скоростью диастолической деполяризации латентных пейсмекерных клеток, приведут к значительным изменениям уровня мембранного потенциала в момент прихода импульса и, следовательно, изменяет его проведение. Соответственно этому, небольшое увеличение длительности синусового цикла обусловит значительную аберрацию проведения. И наоборот, столь же небольшое его уменьшение способно нормализовать проведение. Аналогично небольшие изменения скорости деполяризации в фазу 4 латентных пейсмекерных клеток повлияют на проведение в отсутствие каких-либо изменений частоты синусового ритма. Этот механизм позволяет объяснить изменения проведения практически от комплекса к комплексу, а также развитие интермиттирующей аберрации При наджелудочковом ритме ускользания и вариабельность форм комплексов, возникающих вблизи аналогичных интервалов ускользания (см. рис. 4.18, Г).
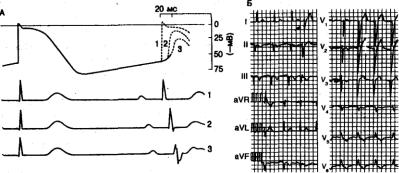
Рис. 4.20. Аберрантность длительного цикла, связанная с медленной диастолической деполяризацией.
А — трансмембранные потенциалы латентного пейсмекера, зарегистрированные в правой ножке пучка Гиса, показывают, каким образом деполяризация в фазу 4 может привести как к аберрантности длительного цикла, так и к аберрации проведения в отсутствие заметных изменений синусового ритма даже в нормальном сердце. Скорость деполяризации в фазу 4 в клетках правой ножки предположительно повышена до уровня, несколько меньшего, чем частота синусового ритма. Такая близость частот позволяет распространяющемуся синусовому импульсу достигнуть клеток ножки пучка в тот момент, когда их диастолический потенциал приближается к уровню порогового потенциала. Этот период (переход фазы 4 в фазу нарастания следующего потенциала действия) характеризуется быстрым увеличением скорости деполяризации и существенным снижением потенциала в течение короткого времени (20 мс). Поэтому даже небольшие изменения времени прихода распространяющегося возбуждения, обусловленные изменениями частоты синусового ритма или скорости деполяризации латентного пейсмекера клетки, будут сопровождаться выраженным различием в величине потенциала в этот момент, что приведет к вариабельности формы ответа и его дальнейшего распространения. Обратите внимание на постепенное уменьшение амплитуды и Vm,, трех ответов (I, 2 и 3), инициированных с возрастающей задержкой (шаг 20 мс), а также на усиливающееся угнетение проведения (определяется по ЭКГ-изменениям QRS). Ответ 1 возникает непосредственно перед появлением порогового потенциала и распространяется нормально. Ответы 2 и 3 характеризуются возрастающей аберрантностью типа блокады правой ножки вследствие ее активации при все более положительных потенциалах. Небольшие временные различия не обнаруживаются на стандартной ЭКГ, так что вариации формы QRS определяются как возникающие в отсутствие изменений частоты ритма. Наличие этого механизма обеспечивает также разумное объяснение типа изменений формы QRS в каждом последовательном возбуждении, который показан на рис. 4.18. Б — стандартная ЭКГ в 12 отведениях у больного 68 лет с ишемической болезнью сердца, демонстрирующая появление и исчезновение аберраций типа блокады левой ножки в отсутствие явных изменений частоты синусового ритма (см. отведения V1—V6). Выявление такой вариабельности вместе со спонтанными желудочковыми экстрасистолами, характеристики которых указывают на их левостороннее происхождение (см. отмеченные стрелками комплексы в отведениях I—III), позволяет предположить, что аберрации могут быть обусловлены ускорением деполяризации в фазу 4 в латентном водителе ритма, расположенном в левой ножке пучка Гиса. Обсуждение в тексте.
Учитывая результаты, полученные при исследовании ишемического и патологически измененного миокарда, следует отдельно рассмотреть еще два условия возникновения нарушений проведения и аберрации, а именно: 1) смещение порогового потенциала к уровню ниже —70 мВ, что позволяет мембранному потенциалу в процессе
деполяризации понизиться до уровня, при котором проведение существенно ухудшится [56]; 2) изменения соотношения реактивности, аналогичные показанным на рис. 4.3, Б и снижающие степень, при которой автоматические клетки должны деполяризоваться до замедления проведения с последующим блокированием. На рис. 4.19, Б, например, существенные нарушения проведения могли бы появиться скорее при деполяризации до —70 мВ, нежели до —60 мВ. Для возникновения аберрации также должно быть достаточно меньшего увеличения длительности цикла. Стоит отметить, что экспериментальное воспроизведение нарушений проведения, связанных с постепенной деполяризацией изолированных волокон Пуркинье в фазу 4, обычно сопровождается изменениями зависимости реполяризации от времени и потенциала, что проявляется снижением максимального диастолического потенциала и генерализованной гипополяризацией кардиомиоцитов [56], а также смещением потенциала за нулевой уровень [56J. Эти изменения иллюстрирует рис. 4.19, Б. Верхний и средний фрагменты рис. 4.21 позволяют объяснить изменения формы комплекса QRS на рис. 4.18с точки зрения зависящих от длительности цикла изменений диастолического потенциала в клетках латентных пейсмекеров правой ножки пучка Гиса. Ввиду небольших изменений длительности цикла, сопровождающихся появлением и исчезновением аберрации, здесь предполагается ускорение деполяризации в фазу 4 вследствие ишемии, а также вызванное деполяризацией смещение порогового потенциала к менее отрицательным значениям или упомянутые ранее изменения реактивности миокарда. Дальнейшее подтверждение значимости этих факторов для развития аберрации длительного цикла было получено El-Sherif и соавт. [252] при исследовании нарушений проведения в системе Гис — Пуркинье собаки после перевязки коронарной артерии. Важная роль изменений возбудимости, зависимых от длительности цикла, в развитии аберрации этого типа подчеркивалась другими исследователями [150].
Осцилляторная активность. Предполагается также, что нарушения проведения могут быть связаны с осцилляторной активностью, вызванной деполяризацией, или с другими типами этой активности [30, 253]. Если циклические изменения мембранного потенциала, обусловленные осцилляторной активностью, происходят достаточно медленно, обеспечивая тем самым изменения электрофизиологических свойств мембраны, то создаются условия для возникновения нарушений проведения, аналогичных наблюдаемым при деполяризации в фазу 4 латентных пейсмекерных клеток. Так, относительно медленные колебания мембранного потенциала, связанные с действием сердечных гликозидов [253], могут сопровождаться циклическими изменениями Ушах и скорости проведения в фазу диастолы. С другой стороны, быстрые колебания должны обусловить более однородное угнетение свойств мембраны до уровня, обеспечивающего усреднение потенциала при осцилляторной активности. Это в свою очередь приведет к изменениям возбудимости и проведения, более характерным для ситуации с низким потенциалом покоя, чем для повышенного автоматизма. Данные о существовании относительно медленной Осцилляторной активности во многих препаратах ишемического и патологически измененного миокарда (см. рис. 4.4) и о наличии во многих спонтанно активных клетках изменений порогового потенциала [77] и реактивности [74, 75, 77, 87], облегчающих развитие медленного проведения, указывают на потенциальную значимость такой активности как причины нарушений проведения. Определенное значение имеют и сообщения о наличии связи между осцилляторной активностью и вариабельной местной блокадой в подобных препаратах [74, 75, 77, 87,
91—93].
Антиаритмические препараты и аберрация длительного цикла. Все антиаритми-
ки, используемые в настоящее время, угнетают деполяризацию в фазу 4 потенциала действия латентных пейсмекерных клеток и, следовательно, должны влиять на аберрантность длительного цикла. Однако к такому выводу следует относиться с определенной осторожностью. Ярким примером служат хинидин и прокаинамид, действие которых на нарушения проведения в фазу 4 представляется весьма парадоксальным [40, 256, 257]. С одной стороны, в терапевтической концентрации они ослабляют или устраняют автоматизм латентных пейсмекеров. Это предотвращает развитие аберрации (или устраняет уже имеющуюся). С другой стороны, прямое блокирующее действие этих препаратов на Na+-кaнaлы [45, 46, 146, 221] способно облегчить развитие аберрации или усилить уже существующую аберрацию. Их суммарное влияние на проведение и аберрантность зависит от того, насколько благотворное подавление деполяризации в фазу 4 превышает прямое угнетение проведения. При низких концентрациях их прямое угнетающее влияние на проведение может быть столь небольшим, что замедление деполяризации в фазу 4 приведет к улучшению проведения и ослаблению аберрантности. С другой стороны, при высоких концентрациях этих препаратов может

преобладать угнетающее влияние на проведение. Кроме того, хинидин и прокаинамид в высокой концентрации способны уменьшить диастолический потенциал, облегчив тем самым развитие автоматизма, связанного с деполяризацией [40, 254, 255].
Рис. 4.21. Альтернативный механизм возникновения аберраций при ускорении деполяризации в фазу 4 латентного клеточного пейсмекера в отсутствие значительных изменений частоты синусового ритма.
Показан также возможный механизм «сверхнормального» внутрижелудочкового проведения. Слева приведена упрощенная схема проводники системы, аналогичная представленной на рис. 4.1, А. Кривые показывают трансмембранные потенциалы, зарегистрированные в синусовом узле (СУ), пучке Гиса (Гис) и правой ножке пучка (ПНП); ниже дана ЭКГ во И отведении. Верхний фрагмент (контрольные условия): частота синусового ритма в нормальном диапазоне. Латентные пейсмекеры в пучке Гиса и его правой ножке не подвергаются деполяризации в фазу 4, ЭКГ в норме. Средний фрагмент: синусовый ритм не изменяется. Автоматизм латентного пейсмекера в правой ножке усиливается до степени, лишь немного уступающей таковой синусового узла. Одновременно отмечается смещение порогового потенциала до менее отрицательного, чем в норме, уровня, а также угнетение реактивности. В результате амплитуда и Vmах ответа, возникающего в клетках правой ножки, значительно снижаются и проведение угнетается. На ЭКГ наблюдается блокада правой ножки пучка Гиса. Нижний фрагмент: предсердная экстрасистола достигает клеток правой ножки в тот момент, когда диастолический потенциал имеет максимальную величину. Следовательно, амплитуда и Vmax превосходят таковые основного возбуждения, что соответствует улучшению проведения в правой ножке по сравнению с основным возбуждением. Форма QRS соответственно менее аберрантна, чем во время основного возбуждения («сверхнормальное» внутрижелудочковое проведение). Обсуждение в тексте.
Если аберрантность фазы 4 в ишемическом или поврежденном миокарде обусловлена изменением электрофизиологических свойств большого количества частично деполяризованных, спонтанно активных волокон, то восстановление максимального диастолического потенциала до более отрицательной величины может способствовать уг-
нетению автоматизма и ослаблению аберрантности. Такое действие оказывают катехоламины [56, 77, 254, 255]. Однако они одновременно усиливают автоматизм нормальных латентных водителей ритма, что уменьшает целесообразность их применения.
Сверхнормальное проведение
Для объяснения по крайней мере некоторых случаев аберрантности длительного цикла была предложена концепция «сверхнормального внутрижелудочкового проведения» [235, 246—249]. Этот термин обозначает улучшение проведения импульсов, возникающих в раннюю фазу диастолы у больных с предшествующими нарушениями проведения [3—5, 19, 20, 238, 241, 248]. Было предложено несколько объяснений этого явления [3—5, 19, 20, 238, 241—248], которое фактически заключается в исчезновении аберрации. Парадоксально то, что одной из причин сверхнормального проведения является деполяризация в фазу 4 латентных пейсмекерных клеток системы Гис—Пуркинье
[56, 238, 241, 248, 258].
Так как автоматические клетки начинают деполяризоваться сразу же по окончании реполяризации, мембранный потенциал максимален в начале цикла, а затем он постепенно уменьшается.
Поэтому потенциалы действия, возникающие в терминальную фазу реполяризации и сразу после ее завершения, имеют большую амплитуду и Vmax и проводятся быстрее инициируемых в более поздние фазы цикла. Таким образом, в случаях, когда ухудшение внутрижелудочкового проведения вызвано усилением деполяризации в фазу 4, форма комплексов QRS ранних преждевременных возбуждений может быть ближе к нормальной, чем форма QRS основного ритма. Такого рода изменения в пучке Гиса вызывают сверхнормальное АВ-проведение. На рис. 4.21 (нижний фрагмент) схематически показано, каким образом деполяризация в фазу 4 вызывает сверхнормальное внутрижелудочковое проведение и приводит к аберрантности длительного цикла. Примечательно, что синусовые комплексы, замыкающие длительные циклы, имеют признаки блокады правой ножки пучка Гиса, тогда как сверхнормально проведенные ранние предсердные преждевременные возбуждения, по-видимому, нормально конфигурированы.
Аберрация без существенных изменений длительности цикла
Аберрация может также возникать при минимальных или даже вовсе не заметных изменениях длительности цикла и при нормальной или сниженной частоте сердечного ритма. По-видимому, первый такой случай был описан в 1913 г. сэром Томасом Льюисом [259], определившим это явление как «нестабильный блок» ножки Пучка Гиса. В настоящее время используется множество других терминов, в том числе «интермиттирующая блокада ножки пучка», «транзиторная блокада ножки пучка», «непостоянная блокада ножки пучка», «обратимая блокада ножки пучка», «частотнозависимая блокада ножки пучка» и «частотнозависимая аберрация» {161, 172, 179, 223, 224, 260— 262]. Хотя точные цифры пока не известны, аберрация этого типа, без сомнения, довольно обычна для заболеваний сердца, причем описаны аберрации типа блокады как правой, так и левой ножки [161, 172, 179, 180, 223, 224, 260— 263]. Однако в отличие от аберрантности короткого и длинного циклов здесь, безусловно, преобладает картина блокады левой ножки пучка Гиса. Клиническое значение аберрантности этого типа практически то же, что и у других типов, но по сравнению с аберрантностью длительного цикла она даже в большей степени означает наличие существенной патологии проводящей системы и служит предвестником постоянного блока ножки пучка Гиса. Практически все известные случаи описаны у больных с серьезным забо-
леванием сердца [161, 172, 179, 180, 223, 224, 260—263].
На рис. 4.15, Г, 4.15, Б, 4.18, В, 4.20, А и 4.22, Б представлены типичные случаи интермиттирующего блока правой и левой ножек пучка Гиса без изменений (или при минимальных изменениях) длительности основного цикла при нормальной физиологической частоте ритма сердца. Как и при других типах аберрантности [179, 180], появление и исчезновение аберрантных комплексов этого типа наблюдается при разной длительности цикла. Кроме того, стойкие признаки блока ножки обычно появляются сразу же; степень аберрантности варьирует лишь минимально или вовсе не изменяется (см. рис. 4.15, Г, 4.20, А и 4.22, Б). Однако в некоторых случаях возможны ее существенные вариации. Например, как показано на рис. 4.18, Г, один
из двух циклов в 0,76 с заканчивается желудочковым комплексом нормальной формы, а другой — обнаруживает некоторое запаздывание терминального зубца S, указывающее на неполную блокаду правой ножки. Увеличение цикла сверх 0,76 с приводит к дальнейшему усилению аберрации, что завершается картиной полной блокады правой ножки см. рис. 4.18, А, Б и В).
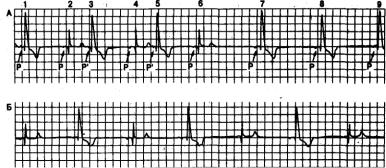
Рис. 4.22. Запись, Полученная при холтеровском мониторировании больного 70 лет с гипертонической болезнью, осложненной предсердной эктопией и полиморфной аберрантностью вследствие блокады правой ножки пучка Гиса.
А — брадикардия синусового узла и аритмия прерываются тремя преждевременными возбуждениями предсердий (возбуждения I, 3 и 5) по типу бигеминии. Возбуждения в конце коротких циклов (1, 3 и 5), как и возбуждения в конце длительных циклов (7, 8 и 9), обнаруживают полную блокаду правой ножки пучка. Возбуждения в конце постэктопических циклов (2, 4 и 6), промежуточных по своей длительности, показывают неполную блокаду правой ножки. Б — синусовый ритм с признаками чередования неполной и полной блокады правой ножки, которое не .связано явно с изменением длительности цикла, причем колебания длительности цикла в среднем не превышают 0,04 с. Обсуждение в тексте.
Электрофизиологические детерминанты аберрации
Аберрантность, возникающая при минимальных изменениях длительности цикла или без каких бы то ни было изменений, означает, что распространяющийся импульс встречает на своем пути ткани с вариабельной рефрактерностью на протяжении всего сердечного цикла или большей его части. Это довольно трудно объяснить только на основании зависимых от длительности цикла изменений рефрактерности или диастолического потенциала.
Выше были перечислены физиологические и фармакологические факторы, способные повлиять на мембранный потенциал и рефрактерность независимо от длительности цикла. Учитывая преимущественное возникновение аберрации этого типа у больных с , серьезным заболеванием сердца или проводящей системы, особое внимание следует уделить изменениям электрофизиологических свойств, связанным с ишемией и патологическими процессами. Изменения, наблюдаемые в ишемических и пораженных тканях сердца, в целом предрасполагают к увеличению рефрактерности на протяжении всего сердечного цикла. Это подтверждается существованием в измененном миокарде большого количества клеток с пониженным диастолическим потенциалом, усиленным автоматизмом и вариабельным увеличением реполяризации, поскольку такие изменения облегчают прохождение распространяющегося импульса на участках с низким потенциалом в течение всего сердечного цикла независимо от его длительности. Дополнительным фактором является увеличение рефрактерного периода, превышающее длительность реполяризации (см. рис. 4.6). Эти факторы вместе с ослаблением зависимости длительности потенциала действия от продолжительности цикла (см. рис. 4.13 и 4.14) и увеличением времени, необходимого для установления новой стабильной длительности (см. рис. 4.13), усиливают и продлевают депрессивное влияние на проведение и рефрактерность, связанную с реполяризацией, даже при очень небольших изменениях частоты ритма. Еще одним фактором может быть изменение реактивности миокарда, аналогичное показанному на рис. 4.3, Б, так как оно способствует замедлению проведения даже при незначительном уменьшении мембранного потенциала в любой момент сердечного цикла.
Важную роль играет влияние лекарственных препаратов. Ряд основных кардиоактивных препаратов, особенно антиаритмики в высокой концентрации (например, амиодарон и хинидиноподобные препараты), вызывают изменения длительности потенциала действия, реактивности миокарда, проведения и диастолического потенциала, способствуя развитию аберрации как во время реполяризации, так и в фазу 4. Усиление или ослабление таких эффектов при различных концентрациях препаратов приводит к возникновению вариаций формы QRS, независимо от длительности цикла. Такие препараты применяются главным образом у больных с заболеванием сердца, что может скрывать потенциальное значение их побочного действия из-за синергизма эффектов препаратов и влияния электрофизиологических изменений, связанных с заболеванием.
На рис. 4.19, Б, 4.20, А и 4.21 схематически представлены два возможных механизма возникновения аберраций проведения из-за деполяризации в фазу 4, которые не зависят от длительности цикла. Оба механизма уже обсуждались в связи с аберрантностью длительного цикла. Первый механизм участвует в ускорении деполяризации в фазу 4 латентных пейсмекерных клеток одновременно с угнетением реактивности вовлеченных тканей (см. рис. 4.19, Б и 4.21); второй — предполагает возбуждение латентных пейсмекерных клеток в тот момент, когда они уже в значительной степени претерпели быстрые изменения потенциала перед спонтанной активацией (т. е. вблизи порогового уровня потенциала; см. рис. 4.20), и способен действовать даже в нормальном сердце. Поскольку эти механизмы обеспечивают развитие аномалий проведения в отсутствие существенных изменений основного цикла, они позволяют объяснить различия в форме комплексов QRS, замыкающих 0,76-секундные циклы на рис. 4.18, Г. Так как дальнейшее увеличение цикла (свыше 0,76 с) приводит к постепенному усилению аберрации (см. рис. 4.18, А—-В) и у больного отмечаются также преждевременные желудочковые возбуждения с признаками блока левой ножки пучка Гиса, это подтверждает заключение о том, что различия в форме двух комплексов QRS на рис. 4.18, Г отражают изменение уровня диастолического потенциала в правой ножке вследствие вариабельности деполяризации в фазу 4. На рис. 4.19, Б показана интермиттирующая блокада левой ножки пучка Гиса, которая сопровождается преждевременными желудочковыми комплексами с признаками блокады правой ножки; это предполагает, что данная картина обусловлена вариабельностью усиления автоматизма, но уже в системе левой ножки.
Записи на рис. 4.12, полученные на препарате папиллярной мышцы человека при регулярной стимуляции с периодом 1000 мс, дают несколько необычный пример возникновения аберраций вследствие изменений электрофизиологических свойств пораженных тканей сердца без изменения длительности цикла. На всех трех фрагментах видно, что реполяризация в фазу 3 потенциала действия прерывается спонтанной преждевременной деполяризацией (см. рис. 4.12, возбуждения а, б и в). Экстравозбуждение «а» приводит к развитию аберрантного распространяющегося ответа (аберрантность короткого цикла), а в момент прихода возбуждений «б» и «в» уровень потенциала оказывается столь низким, что возникают лишь локальные ответы. Постэкстрасистолические возбуждения (комплексы 1, 2 и 3) также характеризуются уменьшением амплитуды и Vmах, а их проведение, по-видимому, замедлено. Если бы подобные изменения происходили в соответствующих частях проводящей системы, они сопровождались бы аберрацией. Поскольку преждевременные ответы «б» и «в» не способны распространяться в остальных областях сердца и вызвать экстрасистолу, которая повлияла бы на основной ритм, изменения формы постэкстрасистолических комплексов 2 и 3 воспринимаются как возникающие в отсутствие изменений длительности цикла.
Описанное выше изменение формы комплекса QRS является, вероятно, вариантом аберрации короткого цикла, так как первый постэктопический цикл короче интервала между основными возбуждениями из-за преждевременного ответа. Хотя причины изменения характеристик постэктопических комплексов неясны, наилучшее объяснение, по-видимому, заключается в том, что рефрактерность в пораженном миокарде может значительно превышать период завершения реполяризации, а преждевременные ответы способствуют еще большему замедлению процесса восстановления возбудимости.
Аберрантность смешанного типа
Из сказанного ранее следует, что основные типы аберрантности можно объяснить в рамках какого-либо одного механизма или, во всяком случае, одного главно-
го механизма. Такое обобщение справедливо для большинства случаев аберрантности короткого цикла, особенно в нормальном сердце. Однако это, вероятно, в целом непригодно для объяснения аберраций, наблюдаемых в отсутствие существенных изменений длительности цикла, или в случаях возникновения аберрации разных типов у одного и того же больного (см. рис. 4.17 и 4.22). В таких случаях приходится предполагать наличие одновременно двух иди нескольких механизмов.
Одновременному проявлению двух (или более) механизмов аберрации, по-види- мому, способствует существование сложной взаимосвязи нескольких электрофизиологических переменных. Это, в частности, относится к связи между деполяризацией в фазу 4 автоматических клеток, диастолическим потенциалом, длительностью потенциала действия и проведением [56]. Деполяризация в фазу 4 вызывает снижение ко- нечно-диастолического потенциала автоматических клеток с последующим уменьшением амплитуды и Vmax потенциалов действия вовлеченных волокон и угнетением проведения, что предрасполагает к аберрантности длительного цикла [56, 238—241]. Так как временные характеристики реполяризации и длительность потенциала действия зависят также от величины потенциала (см. рис. 4.3, А, 4.7 и 4.14), уменьшение диастолического потенциала при деполяризации в фазу 4 может влиять на эти переменные (см. рис. 4.19, Б) и, следовательно, на развитие аберрантности короткого цикла. Точнее говоря, поскольку ответы, инициированные в частично деполяризованных волокнах, характеризуются сокращением ранней и увеличением! терминальной стадии реполяризации, ускорение деполяризации в фазу 4 также может создать условия, благоприятные для аберрантности короткого цикла. Если деполяризация в фазу 4 протекает бесконтрольно и конечно-диастолический потенциал снижается до достаточно низкого уровня, то изменения реполяризации в отношении времени и потенциала могут развиваться таким образом, что максимальный диастолический потенциал начнет уменьшаться, за чем может последовать общая гипополяризация клетки [56]. Потенциалы действия, возникающие в таких волокнах, имеют характеристики медленных ответов со всеми вытекающими отсюда последствиями — угнетением реактивности ткани, увеличением периодов рефрактерности и уменьшением зависимости длительности потенциала действия от продолжительности цикла. Могут наблюдаться и различные типы осцилляторной активности. Такая комбинация изменений увеличит период сердечного цикла, в течении которого может возникнуть аберрация. А зона нормального проведения, наоборот, уменьшится. По мере сокращения зоны нормального проведения, появление аберрации становится все более независимым от длительности цикла и момента возбуждения в цикле. Кульминацией процесса станет возникновение аберрации без каких-либо заметных изменений (или с минимальными изменениями) длительности цикла с последующим постоянным блоком ножки пучка Гиса.
Можно привести множество других примеров того, как взаимосвязь ряда электрофизиологических параметров обусловливает изменения, предрасполагающие- к одновременному проявлению нескольких клеточных механизмов аберрантности. Дополнительные предрасполагающие факторы включают независимое возникновение изменений Двух или более электрофизиологических параметров в одной и той же области или, на разных участках АВ-проводящей системы вследствие влияния кардиоактивных препаратов, ишемии и других заболеваний, перерастяжения стенок и т. д. К этому же ряду факторов относят изменения кабельных свойств сердечных волокон. Изменения удельного сопротивления и емкости мембраны, а также внутреннего сопротивления, могут существенно повлиять на скорость проведения во всех фазах сердечного цикла. Однако пока неясно, в какой степени нарушения проведения обусловлены реальными изменениями кабельных свойств. Тем не менее по причинам, изложенным ранее, было бы неразумным предполагать, что изменения сопротивления мембраны и внутриклеточного пространства не являются важными факторами, определяющими нарушения проведения в таких ситуациях, как перерастяжение, изменения вегетативного тонуса и внеклеточной концентрации ионов (особенно калия), воздействие некоторых кардиоактивных препаратов, и (что наиболее важно) при ишемии и заболевании сердца.
Гипотеза об одновременном существовании нескольких механизмов аберрантности оказалась полезной для объяснения ряда особенностей проведения, которые иначе было бы невозможно понять, а именно: возникновение аберрации в необычные моменты времени в сердечном цикле, аберрации при нормальном ритме сердца и с минимальными или нечеткими признаками зависимости от длительности цикла, а также аберрантность различных типов (см. рис. 4.17 и 4.22) и форм (см. рис. 4.8 и 4.9) у одного и того же больного. При объяснении случаев интермиттирующей блокады ножки пучка Гиса и пароксизмальной АВ-блокады с признаками зависимости от длительности как короткого, так и продолжительного цикла и с транзиторным развитием
