
5 курс / Инфекционные болезни / Доп. материалы / Лечение_ВИЧ_инфекции,_К_Хоффман,_Дж_К_Роктрох,_Б_С_Кампс
.pdf
Лечение ВИЧ-инфекции. 2005 год 265
Профилактика при высоком риске (многоплодные роды, преждевременные роды)
При многоплодных родах новорожденным рекомендуется профилактика зидовудином в течение 4 недель. Недоношенные также должны получить невирапин: однократно, если мать получила невирапин до родов, или двукратно, если мать не получила невирапин. Если от приема невирапина матерью до рождения ребенка прошло менее часа, ребенок должен получить первую дозу невирапина в первые 48 ч после рождения (Stringer, 2003). Если мать принимала невирапин в составе комбинированной схемы АРТ, дозу для новорожденного нужно удвоить до 4 мг/кг в связи с возможной индукцией ферментов. Кроме того, новорожденные должны получить расширенную профилактику зидовудином по схеме для недоношенных (см. выше) длительностью 4-6 недель.
Таблица 8. Исследования АРВ профилактики у новорожденных
|
Препарат |
|
Средняя суточная доза |
|
Частые побочные |
|
|
|
|
|
|
эффекты |
|
|
Зидовудин |
|
8 мг/кг в 4 приема; у недоношенных с |
Анемия, нейтропения. |
|
|
|
(Ретровир™) |
|
ГВ< 35 нед 4 мг/кг в 2 приема, с 15-го |
В комбинации с ламивудином — |
|
|
|
|
|
дня 6 мг/кг * в 3 приема, у недоно- |
токсичность для митохондрий |
|
|
|
|
|
шенных с ГВ < 30 нед 6 мг/кг в 3 |
|
|
|
|
|
|
приема с |
|
|
|
|
|
|
29-го дня |
|
|
|
|
Ламивудин (Эпи- |
|
4 мг/кг в 2 приема у новорожденных |
Нарушения со стороны ЖКТ, рво- |
|
|
|
вир™) |
|
(< 30 сут) |
та, в комбинациях с другими пре- |
|
|
|
|
|
|
|
паратами — токсичность для ми- |
|
|
|
|
|
|
тохондрий. |
|
|
|
|
|
|
Не применяется у недоношенных |
|
|
|
|
|
|
|
|
|
Диданозин (Ви- |
|
100 мг/м2 в 2 приема с |
Диарея, панкреатит, в комбинации |
|
|
|
декс™) |
|
14-го дня |
с другими препаратами — токсич- |
|
|
|
|
|
|
|
ность для митохондрий |
|
|
Ставудин (Зе- |
|
1 мг/кг в 2 приема с рождения до 13 |
В комбинации с другими препара- |
|
|
|
рит™) |
|
дня, затем 2 мг/кг в 2 приема с 14-го |
тами — токсичность для митохон- |
|
|
|
|
|
дня |
дрий |
|
|
|
Абакавир (Зиа- |
|
До 4 мг/кг в 2 приема; > 1 мес 16 мг/кг |
Реакции гиперчувствительности |
|
|
|
ген™) |
|
в 2 приема (исследование) |
(не возобновлять), токсичность |
|
|
|
|
|
|
|
для митохондрий, лактацидоз |
|
|
|
|
|
|
|
|
|
Невирапин (Ви- |
|
2-4 мг/кг однократно или 120 мг/м2 в |
Сыпь, гепатотоксичность, при кли- |
|
|
|
рамун™) |
|
течение 14 сут, затем 7-8 мг/кг или |
нически выраженной гепатоток- |
|
|
|
|
|
240 мг/м2 в 2 приема, максимальная |
сичности не возобновлять |
|
|
|
|
|
доза 400 мг/м2 |
|
|
|
|
Нелфинавир |
|
80 мг/кг в 2 приема (исследование) с 1 |
Побочные эффекты со стороны |
|
|
|
(Вирасепт™) |
|
и 6 нед; 110-150 мг/кг в 2 или 3 прие- |
ЖКТ, особенно диарея |
|
|
|
|
|
ма в течение 2 мес |
|
|
|
|
|
|
|
|
|
|
|
Ритонавир (Нор- |
|
350 мг/м2 однократно или 700 мг/м2 в |
Гипербилирубин-емия, желудоч- |
|
|
|
вир™) |
|
2 приема в течение 4 недель (иссле- |
но-кишечные нарушения |
|
|
|
|
|
дование) |
|
|
|
Исследования
(P)ACTG 076, 316, 321, 353, 354, 358;
HIVNET 012 III
PACTG 331(PI)
PACTG 358
PACTG 239, 249;
HIV-NAT
PACTG 332, 356;
HIV-NAT
PACTG 321
PACTG 316, 356,
HIVNET 012
PACTG 353, 356
PENTA 7
PACTG 354
ГВ — гестационный возраст; (P)ACTG = (Pediatric) AIDS Clinical Trial Group — испытание Отдела по клиническим исследованиям СПИДа (у детей); HIV-NAT = HIV-Netherlands Australia Thailand Research Collaboration — Сотрудничество по исследованию ВИЧ-инфекции в Нидерландах, Австралии и Таиланде.
*За исключением зидовудина для доношенных новорожденных дозы получены из исследований. По возможности, не одобренные АРВ препараты у новорожденных нужно использовать в рамках клинических испытаний.
Профилактика при высоком риске вертикальной передачи
У новорожденных с дополнительными факторами риска рекомендуется комбинированная профилактика зидовудином в сочетании с ламивудином. Факторами высокого риска являются преждевременное излитие околоплодных вод, амнионит, высокая вирусная нагрузка у матери перед родами, отсутствие профилактики, режущая травма ребенка во время кесарева сечения, а также аспирация геморрагической амниотической жидкости из ЖКТ или дыхательных путей ребенка.
266 Беременность и ВИЧ-инфекция
Мероприятия в случаях, когда во время беременности и в родах профилактика не проводилась
Комбинированную профилактику зидовудином в сочетании с ламивудином нужно начинать в первые 6-12 ч после рождения ребенка. Кроме того, рекомендуется перинатальная профилактика удвоенной дозой невирапина.
Если ВИЧ-инфекция диагностирована только после родов, профилактика, начатая в первые 48 ч после рождения намного эффективнее, чем профилактика, начатая после третьих суток (частота вертикальной передачи 9,2% против 18,4%; Wade, 1998). Однако даже позднее начало профилактики зидовудином лучше, чем отсутствие профилактики (18,4% против 26,6%) (табл. 7).
Дальнейшие исследования профилактики ВИЧ-инфекции у новорожденных
Обзор исследований фармакокинетики у новорожденных приведен в табл. 8 (Ronkavilit, 2001 & 2002 и
др.).
Исследования
Для постоянного совершенствования лечения ВИЧ-инфекции у беременных и АРВ профилактики вертикальной передачи ВИЧ необходимо тщательно регистрировать все клинические данные. В США действует регистр «Антиретровирусная терапия во время беременности», который помогает отслеживать все возможные тератогенные эффекты антиретровирусных средств на основе сообщений о клинических случаях у новорожденных, подвергавшихся действию АРВ препаратов:
Antiretroviral Pregnancy Registry, Research Park, 1011 Ashes Drive, Wilmington NC28405; контактная информация: http://www.apregistry.com/contact.htm.
Литература
1.Acosta EP, Bardeguez A, Zorrilla C, et al. Pharmacokinetics of saquinavir plus low dose ritonavir in human immunodeficiency virusinfected pregnant women. Antimicrob Agents Chemother 2004; 48: 430-6.
2.Alimenti A, Burdge DR, Ogilvie GS, et al. Lactic acidemia in human immunodeficiency virus-uninfected infants exposed to perinatal exposed to perinatal antiretroviral therapy. Pediatr Infect Dis 2003; 22: 782-9.
3.Barret B, Tardieu M, Rustin P, et al. Persistent mitochondrial dysfunction in HIV-1-exposed but uninfected infants: clinical screening in large prospective cohort. AIDS 2003; 17: 1769-85.
4.Bekerman K, Covington D, Garcia P, et al. Association between antiretroviral therapy during pregnancy and prematurity/low birth weight. 11th Conference on Retroviruses and Opportunistic Infections. February 8-11, 2004, San Francisco, USA.
5.Bristol-Myers warns of AIDS drugs use. AIDS Read 2001; 11: 82
6.Bryson Y, Stek A, Mirochnik M, et al for the PACTG 353 Team. Pharmacokinetics, antiviral activity and safety of nelfinavir (NFV) in combination with ZDV/3TC in pregnant HIV-infected women and their infants: PACTG 353 cohort 2. 9th Conference on Retroviruses & Opportunistic Infections, Seattle, WA, February 24-28, 2002 (Abstract 795-W).
7.Bulterys M, Jamieson DJ, O‘Sullivan MJ, et al. Rapid HIV-1 testing during labour: a multi-centre study. JAMA 2004; 292: 269-71.
8.Capparelli E, Mirochnick M, Dankner WM, et al. Zidovudine pharmacokinetics in premature infants exposed to human immunodeficiency virus. J Pediatr 2003; 142: 47-52.
9.Centers for Disease Control (CDC). Recommendations for use of antiretroviral drugs in pregnant HIV-1-infected women for maternal health and interventions to reduce perinatal HIV-1 transmission in the United States. February 24, 2005. http://www.aidsinfo.nih.gov
10.Centers for Disease Control (CDC). Guidelines for the use of antiretroviral agents in HIV-infected adults and adolescents. Recommendations of the panel on clinical practices for treatment of HIV. MMWR 2002; 51 (RR-7): 1-55. Update October 29, 2004 ). http://www.aidsinfo.nih.gov
11.Coll O, Fiore S, Floridia M, et al. Pregnancy and HIV infection: a European consensus on management. AIDS. 2002; 16 Suppl 2: 1-18.
12.Connor EM, Sperling RS, Gelber R, et al. Reduction of maternal-infant transmission of HIV type 1 with zidovudine treatment. N Engl J Med 1994; 331:1173-80.
13.Cooper ER, Charurat M, Mofenson L, et al. Combination antiretroviral strategies for the treatment of pregnant HIV-1-infected women and prevention of perinatal HIV-1 transmission. J Aquir Immune Defic Syndr 2002; 29: 484-94.
14.Deutsche AIDS-Gesellschaft (DAIG), Österreichische AIDS-Gesellschaft (ÖAG), Robert Koch Institut et al. Deutsch-Österreichische Empfehlungen zur HIV-Therapie in der Schwangerschaft. Stand Mai 2003. http://www.rki.de/INFEKT/AIDS_STD/BR_LINIE/BR_LINIE.HTM
15.Einstein FH, Wright RL, Trentacoste R, et al. The impact of protease inhibitors on maternal serum screening analyte levels in pregnant women who are HIV positive. Am J Obstet Gynecol 2004, 191: 1004-1008.
16.European Collaborative Study. HIV-infected pregnant women and vertical transmission in Europe since 1986. AIDS 2001; 15: 761-70.
17.European Collaborative Study. Exposure to antiretroviral therapy in utero or early life: the health of uninfected children born to HIV-infected women. J Acquir Immune Defic Syndr 2003; 32: 380-7.
18.Hill JB, Sheffield JS, Zeeman GG, Wendel GD. Hepatotoxicity with antiretroviral treatment of pregnant women. Obstet Gynecol 2001; 98: 909-11.
19.Hollwitz B, Gingelmaier A, Gröger S, et al. Course of pregnancy and foetal outcome of 594 HIV-exposed pregnancies in German reference centers 1999-2003. 15th International AIDS Conference, Bangkok, 2004. Abstract ThPeE7973.
20.Ioannidis JP, Abrams EJ, Ammann A, et al. Perinatal transmission of HIV type I by pregnant women with RNA virus loads < 1000 copies/ml. J Infect Dis 2001; 183: 539-45.
Лечение ВИЧ-инфекции. 2005 год 267
21.Jackson JB, Mracnz M, Guay L, et al. Identification of the K103N resistance mutation in Ugandan women receiving nevirapine to prevent HIV-1 vertical transmission. AIDS 2000; 14: 111-5.
22.Kosel BW, Beckerman KP, Hayashi S, et al. Pharmacokinetics of nelfinavir and indinavir in HIV-1-infected pregnant women. AIDS 2003; 17: 1195-9.
23.Mandelbrot L, Landreau-Mascaro A, Rekacewicz C, et al. Lamivudine-zidovudine combination for prevention of maternal-infant transmission of HIV-1. JAMA 2001; 285: 2083-93.
24.Marcollet A Goffinet F, Firtion G, et al. Differences in postpartum morbidity in women who are infected with the HIV after elective cesarean delivery, emergency cesarean delivery, or vaginal delivery. Am J Obstet Gynecol 2002; 186: 784-9.
25.Marzolini C, Rudin C, Decostered LA, et al. Transplacental passage of protease inhibitors at delivery. AIDS 2002; 18: 889-93.
26.Palumbo P, Holland B, Dobbs T, et al. Antiretroviral resistance mutations among pregnant HIV type I-infected women and their newborns in the United States: Vertical transmission and clades. J Infect Dis 2001; 184: 1120-6.
27.Mofenson LM, Lu M, Pacheco S, et al. Perinatal antiretroviral (ARV) exposure and effect on hematopoiesis in HIV-exposed, uninfected children: the women and infants transmission study (WITS). 15th International AIDS Conference, Bangkok, 2004. Abstract ThPeB7024.
28.Rongkavilit C, Thaithumyanon P, Chuenyam T, et al. Pharmacokinetics of stavudine and didanosine coadministered with nelfinavir in HIVexposed neonates. Antimicrob Agents Chemother 2001; 45: 3585-90.
29.Rongkavilit C, van Heeswijk RP, Limpongsanurak S, et al. Dose-escalation study of the safety and pharmacokinetics of nelfinavir in HIVexposed neonates. J Aquir Immune Defic Syndr 2002; 29:455-63.
30.Sarner L, Fakoya A. Acute onset lactic acidosis and pancreatitis in the third trimester of pregnancy in HIV-1 positive women taking antiretroviral medication. Sex Transm Infect 2002; 78: 58-9.
31.Schäfer A. HIV und Schwangerschaft. L’Age-Stehr J, Helm EB (Hrsg). AIDS und die Vorstadien. Ein Leitfaden für Praxis und Klinik. Springer Verlag 2001; Bd 1 III.10 : 1-18.
32.Scott GB, Rodman JH, Scott WA, et al. Pharmacokinetics and virologic response to ritonavir (RTV) in combination with zidovudine (ZDV) and lamivudine (3TC) in HIV-1-infected pregnant women and their infants. 9th Conference on Retroviruses & Opportunistic Infections 2002, Seattle. Abstract 794
33.Shapiro D, Tuomola R, Pollack H, et al. Mother-to-child transmission risk according to antiretrovirals, mode of delivery, and viral load in 2895 U.S. women (PACTG 367). 11th Conference on Retroviruses & Opportunistic Infections 2004, San Francisco. Abstract 99.
34.Stek A, Mirochnik M, Capparelli E, et al. Reduced lopinavir exposure during pregnancy. Preliminary pharmacokinetic results from PACTG 1026. 15th International AIDS Conference, Bangkok. Abstract ThPeE7981.
35.Stringer JS, Sinkala M, Chapman V, et al. Timing of the maternal drug dose and risk of perinatal HIV transmission in the setting of intrapartum and neonatal single dose nevirapine. AIDS 2003; 17: 1165-69.
36.Tarantal AF, Castillo A, Ekert JE, et al. Fetal and maternal outcome after administration of tenofovir to gravid rhesus monkeys (Macaca mulatta). J Aquir Immune Defic Syndr 2002; 29: 207-20.
37.The Italian Register for HIV Infection in Children. Rapid disease progression in perinatally infected children born to mothers receiving zidovudine monotherapy during pregnancy. AIDS 1999; 13: 927-33.
38.The Perinatal Safety Review Working Group. Nucleoside exposure in the children of HIV-infected women receiving antiviral drugs: absence of clear evidence for mitochondrial disease in children who died before 5 years of age in five United States cohorts. J Aquir Immune Defic Syndr Hum Retrovirol 2000; 15: 261-8.
39.Thorne C, Newell M, and European Collaborative Study. Pregnancy outcome in ART-treated HIV-infected women in Europe. 11th Conference on Retroviruses & Opportunistic Infections, San Francisco, 2004. Abstract 98.
40.Tuomala RE, Shapiro D, Mofenson LM, et al. Antiretroviral therapy during pregnancy and the risk of an adverse outcome. N Eng J Med 2002, 346: 1863-70.
41.Vigano A, Bianchi R, Schneider L, et al. Lack of hyperlactataemia and impaired mitochondrial DNA content in CD4+ cells of HIV-uninfected infants exposed to perinatal antiretroviral therapy. 11th Conference on Retroviruses & Opportunistic Infections. San Francisco, 2004. Abstract 94.
42.Vocks-Hauck M. HIV-Infektion und AIDS bei Neugeborenen, Kindern und Jugendlichen. In L’Age-Stehr J, Helm EB (Hrsg). AIDS und die Vorstadien. Ein Leitfaden für Praxis und Klinik. Springer Verlag 2001; Bd 1 III.11: 1-49.
43.Wade NA, Bearkhead GS, Warren BL, et al. Abbreviated regiments of zidovudine prophylaxis and perinatal transmission of the HIV. N Engl J Med 1998; 339: 1409-14.
44.Watts DH, Balasubramanian R, Maupin RT, et al. Maternal toxicity and pregnancy complications in human immunodeficiency virus-infected women receiving antiretroviral therapy: PACTG 316. Am J Obstet Gynecol 2004; 190: 506-16.
268 Антиретровирусная терапия у детей
11. Антиретровирусная терапия у детей
Тим Ниехаес и Гермиона Лайалл
Особенности ВИЧ-инфекции у детей
Дети — это не маленькие взрослые, и ВИЧ-инфекция у них протекает не так, как у взрослых. Это касается и передачи ВИЧ, и естественной вирусологической динамики, и зрелости иммунной системы и клинических проявлений инфекции. Назначая АРВ препараты детям, нужно учитывать несколько факторов, в частности действие зидовудина и других препаратов во внутриутробном периоде и возрастные особенности фармакокинетики, кроме того у детей особого внимания требует помощь в соблюдении назначений.
Более 95% детей инфицированы в результате перинатальной передачи ВИЧ от матери ребенку (ПМР, или вертикальный путь). Случаи заражения при переливании крови, употреблении инъекционных наркотиков и половым путем встречаются гораздо реже. В большинстве случаев (75-90%) ВИЧ передается перед родами или во время родов, и лишь небольшая часть ПМР (10-25%) приходится на внутриутробный период. Передача ВИЧ при кормлении грудью имеет важное значение в странах с ограниченными ресурсами, однако в развитых странах встречается редко, так как в них ВИЧ-инфицированным женщинам настоятельно рекомендуют отказаться от кормления грудью. Благодаря подробному изучению вертикальной передачи ВИЧ была разработана высокоэффективная профилактика ПМР, которая позволила значительно сократить частоту передачи ВИЧ до 2% и менее. И все же случаи вертикальной передачи ВИЧ еще встречаются:
если ВИЧ-статус матери неизвестен; если проведен неполный курс профилактики ПМР;
если беременная не имела доступа к профилактике ПМР.
В отсутствие АРТ ВИЧ-инфекция у детей, заразившихся вертикальным путем, протекает по одному из двух вариантов: у 10-25% детей инфекция быстро прогрессирует с развитием СПИДа и смертельных осложнений на первом году жизни, а у 75-90% детей инфекция прогрессирует значительно медленнее и средний возраст развития СПИДа составляет 8 лет. Сегодня прогрессирование инфекции зависит в основном от эффективности АРТ.
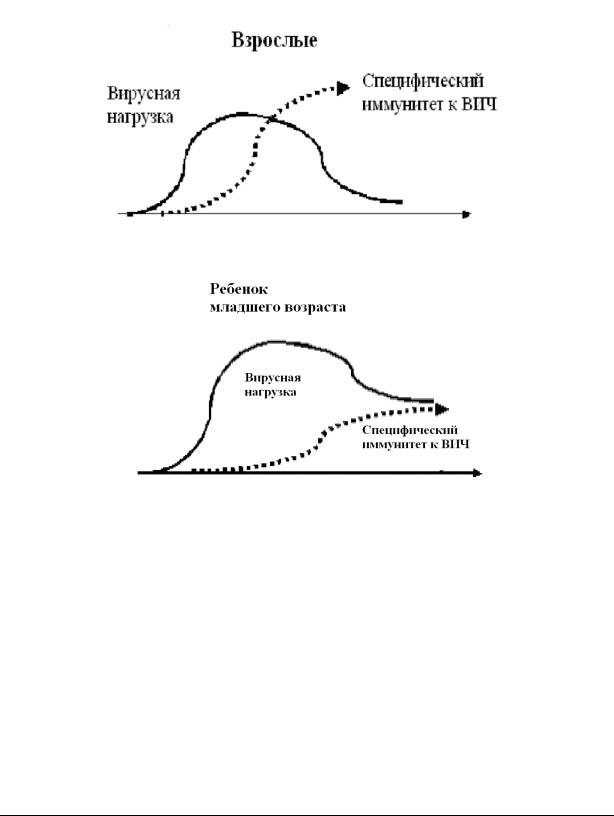
Обычно при рождении вирусная нагрузка составляет менее 10 000 мл-1, затем в течение двух месяцев она медленно растет до 100 000 мл-1 и потом медленно снижается к 4-5 годам. Такая динамика вирусной нагрузки существенно отличается от динамики у взрослых, у которых в течение нескольких месяцев после острой фазы ВИЧ-инфекции наблюдается быстрый подъем и быстрое снижение вирусной нагрузки
(рис. 1).
У детей высокая вирусная нагрузка связана с соматическим ростом лимфатической системы и неспособностью незрелой иммунной системы ребенка к специфическому иммунному ответу на ВИЧ. При оценке иммунитета у детей очень важно сравнивать число лимфоцитов CD4 с возрастными нормами (например, среднее число лимфоцитов у шестимесячного ребенка составляет 3,0 х 109 л-1). На первом году жизни число лимфоцитов у детей очень высокое, к 6 годам жизни оно снижается и становится таким как у взрослых (табл. 1).
Клинические проявления ВИЧ-инфекции у детей тоже отличаются от проявлений у взрослых. У взрослых типичными проявлениями острой фазы ВИЧ-инфекции и сероконверсии служат лихорадка, боль в горле, увеличение лимфоузлов и мононуклеозоподобный синдром. У детей с перинатальным заражением ВИЧ лихорадочной фазы не бывает. Клинически выраженную инфекцию классифицируют в зависимости от тяжести симптомов (табл. 2). С появлением АРТ эти симптомы стали редкостью. Если АРТ эффективна, оппортунистические инфекции у детей развиваются редко. Однако у детей, у которых ВИЧ-инфекция выявлена при обследовании по поводу каких-либо нарушений (например у детей, рожденных женщинами с неизвестным ВИЧ-статусом и поэтому не получавших АРВ профилактики), оппортунистические инфекции еще наблюдаются.
Лечение ВИЧ-инфекции. 2005 год 269
Рисунок 1. Различия в естественной динамике вирусной нагрузки и специфическом иммунном ответе на ВИЧ у детей младшего возраста и взрослых.
Таблица 1. Пересмотренная классификация ВИЧ-инфекции у детей, 1994 г.: иммунологические категории в зависимости от абсолютных и относительных уровней лимфоцитов CD4 в разных возрастных группах*
|
|
|
< 12 мес |
|
|
|
1-5 лет |
|
|
|
6-12 лет |
|
|
|
|
Иммунологическая |
|
мкл-1 |
|
(%) |
|
мкл-1 |
|
(%) |
|
мкл-1 |
|
(%) |
|
|
|
|
|
|
|
|
|
|||||||
|
категория* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Категория 1: нет им- |
|
≥ 1500 |
|
(≥ 25) |
|
≥ 1000 |
|
(≥ 25) |
|
≥ 500 |
|
(≥ 25) |
|
|
мунодефицита |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Категория 2: |
750-1499 |
(15-24) |
500-999 |
(15-24) |
200-499 |
(15-24) |
|
||||||
|
умеренный иммуно- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
дефицит |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Категория 3: |
< 750 |
(< 15) |
< 500 |
(< 15) |
< 200 |
(< 15) |
|
||||||
|
тяжелый иммуноде- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
фицит |
|
|
|
|
|
|
|
|
|
|
|
|
|
* С изменениями по: CDC. 1994 Revised classification system for human immunodeficiency virus infection in children less than 13 years of age. MMWR 1994; 43 (No. RR-12): p. 1-10.

270 Антиретровирусная терапия у детей
Диагностика ВИЧ-инфекции у детей младше 18 мес.
Таблица 2. Пересмотренная классификация ВИЧ-инфекции у детей, 1994 г.: клинические категории
Категория N: бессимптомное течение
Дети, у которых отсутствуют клинические проявления, обусловленные ВИЧ-инфекцией, или у которых есть только одно патологическое состояние категории A.
Категория A: легкое симптоматическое течение
Дети, у которых выявлено не менее двух патологических состояний, перечисленных ниже, но нет ни одного состояния категорий B и C:
•Лимфаденопатия (лимфоузлы >0,5 см в более чем двух областях; симметричное двустороннее увеличение лимфоузлов = одна область)
•Гепатомегалия
•Спленомегалия
•Дерматит
•Паротит
•Рецидивирующие или стойкие инфекции верхних дыхательных путей, синусит или средний отит
Категория B: умеренное симптоматическое течение
Дети, у которых выявлены обусловленные ВИЧ-инфекцией симптомы и заболевания, не отнесенные к категориям A и
C. Примеры состояний и заболеваний категории B (список не полный):
•Анемия (<80 г/л), нейтропения (<1000 мкл-1) и тромбоцитопения (<100 000 мкл-1) сохраняющиеся >30 дней
•Бактериальный менингит, пневмония или сепсис (единичный эпизод)
•Стойкий (>2 месяцев) кандидоз полости рта и глотки (молочница), у детей старше 6 месяцев
•Кардиомиопатия
•Цитомегаловирусная инфекция, развившаяся у новорожденного (в первый месяц жизни ребенка)
•Рецидивирующая или хроническая диарея
•Гепатит
•Рецидивирующий стоматит, вызванный вирусом простого герпеса (более двух эпизодов в течение года)
•Бронхит, пневмония или эзофагит, вызванные вирусом простого герпеса, у новорожденного (в первый месяц жизни)
•Опоясывающий лишай (либо не менее двух эпизодов, либо с поражением более одного дерматома)
•Лейомиосаркома
•Лимфоидная интерстициальная пневмония (ЛИП) или гиперплазия легочных лимфоузлов
•Нефропатия
•Нокардиоз
•Стойкая лихорадка (более месяца)
•Токсоплазмоз у новорожденного (в первый месяц жизни)
•Диссеминированная форма ветряной оспы (осложненное течение)
Категория C: тяжелое симптоматическое течение
Дети, у которых выявлено любое состояние из перечисленных в определении СПИДа для эпиднадзора от 1987 г., за исключением лимфоидной интерстициальной пневмонии (она относится к критериям категории B).
•Тяжелые бактериальные инфекции, сочетанные или рецидивирующие (т. е. любое сочетание по крайней мере двух инфекционных заболеваний в течение двух лет, диагноз которых был подтвержден результатами посевов), следующих локализаций: септицемия, пневмония, менингит, инфекция костей или суставов, абсцесс внутреннего органа или любой полости организма (за исключением среднего отита, поверхностных абсцессов кожи и слизистых, а также инфекций, связанных с наличием постоянного катетера).
•Кандидоз пищевода или дыхательных путей (бронхов, трахеи, легких).
•Диссеминированный кокцидиоидомикоз (при наличии любого очага инфекции вне шейных и прикорневых лимфоузлов и легочной ткани).
•Внелегочный криптококкоз.
•Криптоспоридиоз или изоспориаз с диареей длительностью более месяца.
•Цитомегаловирусная инфекция у новорожденного (в течение первого месяца жизни), с поражением любых органов, кроме печени, селезенки или лимфоузлов.

Лечение ВИЧ-инфекции. 2005 год 271
•Энцефалопатия (в отсутствие других заболеваний, способных привести к аналогичным проявлениям), в течение двух и более месяцев наблюдается и прогрессирует по крайней мере один из следующих симптомов: а) задержка психомоторного развития или утрата ранее приобретенных навыков, умственная отсталость (по стандартным шкалам оценки развития или нейропсихологическим тестам); б) задержка развития головного мозга или приобретенная микроцефалия (по данным измерений окружности головы) или атрофия коры головного мозга (детям старше 2 лет показаны регулярные исследования с помощью КТ или МРТ); в) приобретенное симметричное двигательное расстройство, проявляющееся по крайней мере двумя из следующих нарушений: парез, патологические рефлексы, атаксия или нарушения походки.
•Инфекция, вызванная вирусом простого герпеса: герпетические изъязвления кожи и слизистых, не заживающие в течение месяца, или герпетические бронхит, пневмония, эзофагит любой продолжительности у ребенка старше 1 месяца.
•Диссеминированный гистоплазмоз (с поражением любого органа, кроме легких, прикорневых и шейных лимфоузлов).
•Саркома Капоши.
•Первичная лимфома ЦНС.
•Лимфома Беркитта (лимфома из мелких клеток с нерасщепленными ядрами), или диффузная В-крупноклеточная лимфома (иммунобластная, диффузная гистиоцитарная) или лимфома неизвестного иммунологического фенотипа.
•Диссеминированный или внелегочный туберкулез, вызванный Mycobacterium tuberculosis.
•Диссеминированная микобактериальная инфекция, вызванная Mycobacterium spp., кроме Mycobacterium tuberculosis (с поражением любого органа, кроме легких, кожи, прикорневых и шейных лимфоузлов).
•Диссеминированная инфекция, вызванная Mycobacterium avium-intracellulare или Mycobacterium kansasii (вне лег-
ких, кожи, прикорневых и шейных лимфоузлов).
•Пневмоцистная пневмония.
•Прогрессирующая мультифокальная лейкоэнцефалопатия.
•Рецидивирующая септицемия (кроме Salmonella typhi).
•Церебральный токсоплазмоз, развившийся у ребенка старше месяца.
•ВИЧ-кахексия (выраженная задержка физического развития ребенка при отсутствии других заболеваний, которые способны вызывать аналогичные симптомы): а) упорная потеря веса на >10% исходного, ИЛИ б) снижение кривой «вес/возраст» с пересечением по крайней мере двух процентилей (например, 95-го, 75-го, 50-го, 25-го, 5-го процентилей) диаграммы у ребенка в годовалом возрасте и старше, ИЛИ в) сохранение в течение 30 дней и более кривой «вес/рост» на уровне 5-го процентиля ПЛЮС а) хроническая диарея (т. е. жидкий стул не реже 2 раз в сутки в течение 30 дней и более), ИЛИ б) постоянная или периодическая лихорадка в течение 30 дней и более (по данным регулярных измерений температуры тела).
*Centers for Disease Control and Prevention. 1994 Revised classification system for human immunodeficiency virus infection in children less than 13 years of age. MMWR, 1994. 43 (No. RR-12): p. 1-10.
Диагностика ВИЧ-инфекции у ребенка старше 18 мес
Диагностика ВИЧ-инфекции проводится аналогично диагностике у взрослых (см. гл. «Тестирование на ВИЧ»).
Когда начинать АРТ
Принимая решение о начале АРТ у ребенка, нужно помнить о следующем:
Обычно в экстренном начале лечения ВИЧ-инфекции у детей нет необходимости. Чтобы решить, начинать ВААРТ или нет, отведите столько времени, сколько требуется.
Слишком раннее начало АРТ несет риск длительных побочных эффектов и раннего истощения ограниченного резерва АРВ препаратов, которые можно безопасно использовать у детей. Поэтому многие специалисты откладывают лечение у детей, у которых нет симптомов, вирусная нагрузка низкая и нет иммунодефицита. Показания к АРТ определяются числом лимфоцитов CD4, вирусной нагрузкой и клиническими критериями.
В метаанализе 17 исследований (Dunn D., «HIV Paediatric Prognostic Markers Collaborative Study Group HPPMC cohort»), в которые вошел 3941 ребенок, в том числе дети не получавшие АРТ или получавшие монотерапию зидовудином, вирусная нагрузка и число лимфоцитов CD4 были признаны независимыми прогностическими маркерами развития терминальной стадии инфекции, СПИДа и смерти (Dunn, 2003).
По данной большой когорте детей была разработана компьютерная программа, с помощью которой можно оценить риск развития СПИДа и риск смерти в течение 6 и 12 мес в соответствии с возрастом ре-

272 Антиретровирусная терапия у детей
бенка и числом лимфоцитов CD4 или вирусной нагрузкой («PENTA Calculator» http://www.ctu.mrc.ac.uk/penta/hppmcs/calcProb.htm). Обновленные европейские и американские рекомендации по АРТ были опубликованы в 2004 г. (PENTA, 2004 http://www.ctu.mrc.ac.uk/penta/ http://aidsinfo.nih.gov/guidelines/)
Рекомендации PENTA основаны на оценке оптимального начала терапии в разных возрастных группах в соответствии с числом лимфоцитов CD4 и вирусной нагрузкой при исследовании вышеупомянутой когорты HPPMC; цель лечения — поддерживать риск развития СПИДа на уровне менее 10% в год и риск смерти мене 5% в год (табл. 3 и 4).
Таблица 3. Рекомендации PENTA по началу АРТ ( http://www.ctu.mrc.ac.uk/penta/guidelines.htm)
Дети первого года жизни
1. Клинические показания
Начинать АРТ у всех детей со стадией B или C (СПИД) по классификации CDC.
2. Другие показания
Начинать АРТ у всех детей с долей лимфоцитов CD4 <25-35%.
Настоятельно рекомендуется начинать АРТ при вирусной нагрузке >1 млн мл-1.
Многие специалисты назначают АРТ всем детям первого года жизни, независимо от наличия или отсутствия симптомов.
Дети 1-3 лет
1. Клинические показания
Начинать АРТ у всех детей со стадией C.
2. Другие показания
Начинать АРТ у всех детей с долей лимфоцитов CD4 <20%.
Настоятельно рекомендуется начинать АРТ при вирусной нагрузке >250 000 мл-1.
Дети 4-8 лет
1. Клинические показания
Начинать АРТ у всех детей со стадией C.
2. Другие показания
Начинать АРТ у всех детей с долей лимфоцитов CD4 <15%.
Настоятельно рекомендуется начинать АРТ при вирусной нагрузке >250 000 мл-1.
Дети 9-12 лет
1. Клинические показания
Начинать АРТ у всех детей со стадией C.
2. Другие показания
Начинать АРТ у всех детей с долей лимфоцитов CD4 <15%, однако в отличие от детей младшего возраста в экстренном начале лечения нет необходимости.
Настоятельно рекомендуется начинать АРТ при вирусной нагрузке >250 000 мл-1.
Подростки 13-17 лет
1. Клинические показания
Начинать АРТ у всех подростков со стадией C.
2. Другие показания
Начинать АРТ у всех подростков с числом лимфоцитов CD4 200-350 мкл-1.

Лечение ВИЧ-инфекции. 2005 год 273
Таблица 4. Принятые в США рекомендации по использованию АРВ препаратов для лечения ВИЧ-инфекции у детей
(http://aidsinfo.nih.gov/guidelines).
А. Показания у началу АРТ у детей младше 12 мес жизни
|
Клиническая категория |
|
|
Доля лимфоцитов CD4 |
Вирусная |
Рекомендации |
|
|
|
|
|
нагрузка 1 |
|
|
Симптоматические тече- |
|
< 25 % |
|
|
|
|
ние (клиническая катего- |
или |
|
(иммунологическая катего- |
Любая |
Начать лечение |
|
рия A, B или C) |
|
|
рия 2 или 3) |
|
|
|
Бессимптомное течение |
|
> 25 % |
|
Можно начать лечение2 |
|
|
и |
|
(иммунологическая катего- |
Любая |
||
|
(клиническая категория N) |
|
|
рия 1) |
|
|
|
|
|
|
|
|
|
1У детей первого года жизни вирусная нагрузка выше, чем у детей более старшего возраста и взрослых. Поскольку высокая вирусная нагрузка на первом году жизни отмечается и у детей с быстрым прогрессированием болезни, и с медленным, в этом возрасте ее затруднительно использовать в качестве показания к АРТ.
2Поскольку у детей первого года жизни ВИЧ-инфекция прогрессирует быстрее, чем у более старших детей и взрослых, некоторые специалисты назначают лечение всем ВИЧ-инфицированным детям в возрасте до 6 мес или до 12 мес независимо от их клинических, вирусологических и иммунологических показателей.
Б. Показания к началу АРТ у детей в возрасте 1 год и старше
Клиническая катего- |
|
Доля лимфоци- |
|
Вирусная |
Рекомендации |
рия |
|
тов CD4 |
|
нагрузка |
|
СПИД (стадия C) |
или |
< 15% |
|
Любая |
Начать лечение |
|
|
(иммунологиче- |
|
|
|
|
|
ская категория 3) |
|
|
|
Легкое или умеренное |
или |
15-25% 1 |
или |
>100 000мл-1 2 |
Можно начать лечение |
симптоматическое те- |
|
(иммунологиче- |
|
|
|
чение (стадия A или B) |
|
ская категория 2) |
|
|
|
|
|
|
|
|
|
Бессимптомное тече- |
и |
> 25% |
и |
<100 000 мл-1 2 |
Многие специалисты откла- |
ние (стадия N) |
|
(иммунологиче- |
|
|
дывают лечение, но при- |
|
|
ская категория 1) |
|
|
стально наблюдают за кли- |
|
|
|
|
|
ническими, иммунологиче- |
|
|
|
|
|
скими и вирусологическими |
|
|
|
|
|
параметрами |
1Многие специалисты начинают АРТ при доле лимфоцитов CD4 15-20%, а у детей с долей лимфоцитов CD4 21-25% откладывают лечение и тщательно наблюдают ребенка.
2Вирусная нагрузка, которая служит показанием к АРТ у детей без клинических и иммунологических нарушений, остается спорной; некоторые специалисты начинают лечение бессимптомной инфекции у детей с вирусной нагрузкой
50000-100 000 мл-1.
Общие вопросы лечения ВИЧ-инфекции у детей
Лечение детей антиретровирусными препаратами становится все более сложным. Чтобы лечение было успешным, требуется сотрудничество различных специалистов и членов семьи ребенка.
Антиретровирусная терапия не бывает успешной без хорошего соблюдения назначений. В проспективном исследовании PACTG 377 критерием соблюдения назначений было отсутствие пропусков в приеме препаратов за последние 3 дня. При использовании этого критерия, соблюдали назначения только 70% детей (125 детей за 48 недель наблюдения; Van Dyke, 2002). Эти данные показывают, что постоянное мотивирование детей и ухаживающих за ними взрослых имеет очень большое значение. Расписание ежедневного приема препаратов нужно подробно обсудить с ухаживающими за ребенком взрослыми и согласовать его с распорядком дня и недели. Необходимо установить четкие цели лечения, например, прием 90% предписанных доз. Необходимо обучать пациента и членов семьи по вопросам, связанным с АРВ препаратами. У подростков добиться соблюдения назначения бывает особенно сложно. В этом возрасте за соблюдением назначений нужно следить особенно тщательно, привлекать психологов и социальных работников. В некоторых случаях для обучения приему препаратов и оценки переносимости лечения помогает короткая госпитализация в начале АРТ.
Для оценки соблюдения назначений можно использовать фармакологический мониторинг. Определение уровней препаратов в крови помогает также оценить эффективность АРВ препаратов, их индивидуальную фармакокинетику и риск токсичности.
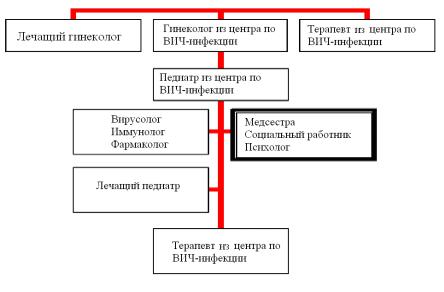
274 Антиретровирусная терапия у детей
Рисунок 2. Многопрофильный подход к оказанию помощи ВИЧ-инфицированным детям и их семьям.
Данных о фармакокинетике АРВ препаратов у детей очень мало, поэтому рекомендуется включать детей в текущее исследование PENTA14 (http://www.pentatrials.org). Измерение концентраций препаратов в плазме помогает скорректировать дозы и предотвратить занижение концентрации и токсичность.
Наблюдение за детьми, получающими АРТ обязательно должно включать регулярные физикальное и лабораторные исследования. Ведением таких детей должны заниматься врачи, имеющие опыт лечения ВИЧ-инфекции у детей и проведения АРТ. Прежде чем начинать или менять АРТ нужно получить результаты исследования не менее двух отдельно взятых проб крови. Вирусная нагрузка и число лимфоцитов CD4 могут меняться из-за инфекций и вакцинации. Поэтому не рекомендуется принимать решения на основе данных, полученных в течение 14 сут после инфекции или вакцинации.
Стратегия
Существующими средствами добиться излечения ВИЧ-инфекции пока нельзя. У некоторых детей вирусная нагрузка остается ниже измеримого уровня в течение нескольких лет, и специфические антитела к ВИЧ у них не определяются. Однако даже у них ВИЧ можно обнаружить с помощью ультрачувствительного анализа (Persaud, 2004). Поэтому риск и пользу АРТ необходимо соотносить у каждого ребенка индивидуально. АРТ с перерывами в лечении или плохим соблюдением назначений может принести больше вреда, чем пользы. Решение о начале терапии имеет для ребенка и его семьи кардинальное значение. Обычно это означает, что ребенок должен будет принимать АРВ препараты всю жизнь. Плановые перерывы в лечении у детей и подростков в контролируемых испытаниях не изучались. Ретроспективный анализ неплановых перерывов в лечении у детей показал значительное снижение доли лимфоцитов CD4 на 6,6% в год (Gibb, 2004). Изучение плановых перерывов в лечении ВИЧ-инфекции у детей в зависимости от числа лимфоцитов CD4 сегодня проводится в рамках исследования PENTA (Pediatric European
Network for Treatment of AIDS) (PENTA11).
В табл. 5 показаны схемы АРТ, рекомендуемые для детей. В американском исследовании PACTG 338, в которое вошли 297 детей, было показано, что схемы, содержащие ИП, эффективнее, чем двухкомпонентные схемы, содержащие 2 НИОТ. Кажется целесообразным начинать лечение со схем, содержащих две группы препаратов (2 НИОТ + ИП или 2 НИОТ + ННИОТ), чтобы сохранить одну или две группы препаратов для будущих замен АРТ. Если при лечении не будет достигнуто полное подавление вируса, высока вероятность перекрестной устойчивости к ННИОТ и ИП. Поэтому сохранение резервной группы препаратов может быть полезным для долгосрочной эффективности лечения. Однако в недавнем исследовании PACTG 256 активная тактика с использованием 3 групп препаратов (НИОТ + ННИОТ + ИП) привела к высокоэффективному и длительному снижению вирусной нагрузки (у 72% больных в течение более 4 лет), особенно у детей, у которых лечение было начато рано (< 3 мес) (Luzuriaga, 2004). В связи с
