
4 курс / Дерматовенерология / Клиническая_дерматология_и_венерология_2020_06
.pdf
Точка зрения |
Point of view |
Препараты группы ингибиторов ИЛ-17 снижают высвобождение провоспалительных цитокинов и хемокинов, приводящих к развитию хронического воспаления, способствующего ускоренному созреванию кератиноцитов. Отличительной особенностью препаратов этой группы является относительно низкая иммуногенность [9].
Cras melius fore, или Закат классической терапии
Тяжелое течение псориаза предполагает системную терапию. Благодаря своей безопасности и эффективности моноклональные антитела в последние годы получили широкое распространение. Так, например, клинические исследования показали высокую эффективность ингибиторов ФНО-α в лечении бляшечного псориаза. Терапия препаратами этой группы позволила достигнуть PASI 75 у 80% пациентов всего за 16 нед [10].
Биологическая терапия неуклонно заменяет классическую и фототерапию. В последние годы все реже стали использоваться такие препараты, как метотрексат, микофенолата мофетил, циклоспорин, ацитретин, а количество кабин в странах Западной Европы резко сократилось [11].
Однако в назначении биологической терапии есть свои особенности. Одной из таковых является феномен иммуногенности и, в частности, образование антилекарственных антител (anti drug antibodies — ADA). Иммуногенность — это способность чужеродного вещества (антигена, в данном случае лекарственного препарата) вызывать в организме гуморальный или клеточный иммунный ответ [12].
Различают желательную и нежелательную иммуногенность. Желательная иммуногенность обычно связана с применением вакцин, где инъекция антигена (вакцины) вызывает иммунный ответ против патогена (вируса, бактерии, токсина), защищая организм от будущего воздействия [13].
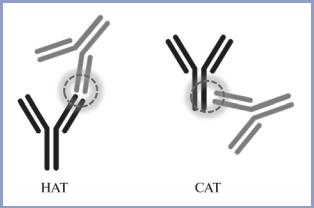
Кроме того, принципы иммуногенности стали широко применяться в онкологии, где конъюгаты антитело—лекарственное средство (ADC) произвели революцию в области химиотерапии рака. В отличие от традиционных методов лечения, повреждающих здоровые ткани при повышении дозы, ADC используют моноклональные антитела (mAb) для специфического связывания ассоциированных с опухолью целевых антигенов и доставки высокоэффективного цитотоксического агента. Антитела оказывают свое терапевтическое действие путем связывания с опухолеспецифическими или ассоциированными с опухолью антигенами клеточной поверхности. После связывания mAb убивает опухолевую клетку одним или несколькими из следующих механизмов:
—отмена передачи сигналов опухолевыми клетками, что приводит к апоптозу;
—модуляции функции Т-клеток через антите- ло-зависимую клеточную цитотоксичность (ADCC) (рис. 1), модуляции функции макрофагов (ADCP), комплемент-зависимую цитотоксичность (CDC) или комплемент-зависимую клеточно-опосредованную цитотоксичность (CDCC);
—оказание ингибирующего воздействия на сосудистую сеть и строму опухоли.
Рис. 1. Этапы антитело-зависимой клеточной цитотоксичности (antibody-dependent cell cytotoxicity — ADCC).
Fig. 1. Stages of antibody-dependent cell cytotoxicity (ADCC).
Russian Journal of Clinical Dermatology and Venereology 2020, Vol. 19, No. 6 |
937 |
Точка зрения |
Point of view |
В тканях организма ADC связываются со своими антигенами-мишенями и интернализуются через рецептор-опосредованный эндоцитоз, что обусловливает высвобождение цитотоксина и приводит к апоптотической гибели раковых клеток. Успех будущих ADC зависит от улучшения выбора цели, повышения потенции цитотоксинов, разработки более стойких соединений в молекуле ADC и преодоления лекарственной устойчивости опухоли [14].
Одним из наиболее показательных примеров нежелательной иммуногенности является формирование ADAs при назначении биологической терапии. В этом случае иммуногенность является побочным эффектом и представляет собой иммунный ответ организма на терапевтический антиген (например, рекомбинантный белок или моноклональное антитело). Вырабатываемые при этом антитела инактивируют терапевтические эффекты лечения и в редких случаях вызывают другие побочные эффекты, такие как реакция гиперчувствительности во время инъекции [15]. Другие неблагоприятные последствия, связанные с образованием иммунных комплексов, включают сывороточную болезнь, реакцию Артуса, бронхоспазм или тромбоэмболические осложнения [16].
Чаще всего лекарственная молекула вызывает иммунный ответ из-за слабого сродства с белками организма, в результате чего молекулы препарата воспринимаются иммунной системой как чужеродные [17]. Иммунная система организма может обнаружить даже наименьшее различие в молекулярной структуре экзогенного вещества и вызвать выработку антител (преимущественно класса IgG4), которые приводят к активации системы комплемента и/или фагоцитозу для их устранения [18].
Иммунологические механизмы формирования ADAs
«Наивная» B-клетка посредством эндоцитоза и процессинга антигена презентирует сигнальные пептиды на молекулах HLA класса II на поверхности клетки. Далее Т-клетки с рецептором, специфичным для представленных пептидов антигена, будут взаимодействовать с активированными В-клетками и давать сигналы, необходимые для переключения класса иммуноглобулина с IgM на IgG. Цитокины дополнительно активируют В-клетки и стимулируют дифференцировку В-клеток в плазматические клетки, секретирующие антитела. Некоторые из активированных В-клеток дифференцируются в клетки памяти, способные быстро реагировать на повторный вызов специфического антигена путем образования короткоживущих плазматических клеток. Далее в герминативном центре лимфатического узла посредством селекции только В-клетки с высокой аффинностью к антигену проходят отбор и завершают свое созревание. Т-зависимые антитела обычно имеют высо-
кие титры и существуют довольно продолжительное время.
Выработка антител возможна также по Т-неза- висимому пути: «наивные» В-клетки могут быть активированы с помощью тяжелых углеводных цепей, содержащих несколько антигенных детерминант. Такой сигнал способствует активации В-клеток с образованием и высвобождением низких титров IgM. Но поскольку Т-клетки остаются не задействованными, переключение классов Ig не произойдет, такие антитела существуют непродолжительное время.
Исходя из особенностей своего строения, ADA могут быть направлены против различных структур антитела: против аллотипических участков (легкой
итяжелых цепей константной области) или против специфических эпитопов идиотипических структур (в вариабельной области). Именно поэтому у одного пациента могут выявляться различные типы ADAs, которые нацелены на различные участки молекулы одного и того же терапевтического препарата [19].
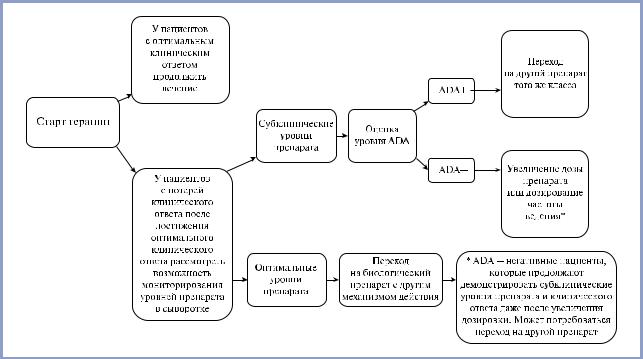
На основании функциональных особенностей принято выделять 2 различных типа ADA: нейтрализующие (НАТ) и ненейтрализующие (связывающие — САТ) (рис. 2). Первые прикрепляются непосредственно к сайту связывания лекарственного антитела, тем самым нейтрализуя его терапевтическую активность [20]. В то время как последние прикрепляются к антителу в области, которая не имеет решающего значения в его терапевтическом потенциале,
илекарственная молекула частично сохраняет свою функцию [21].
Иммуногенность препарата определяется тремя группами факторов: структурой препарата, терапевтическим алгоритмом и свойствами макроорганизма.
1.Прежде всего иммуногенность препарата зависит от его химической структуры и происхождения [22]. Так, химерные антитела, например, инфликсимаб, могут вызывать продуцирование анти-
Рис. 2. Нейтрализующие (НАТ) и ненейтрализующие/связывающие антитела (САТ).
Fig. 2. Neutralizing antibodies (NAB) and non-neutralizing/binding antibodies (BAB).
938 |
Клиническая дерматология и венерология 2020, Т. 19, № 6 |

Точка зрения Point of view
тел, направленных против Fab-участков, включающих |
рата в месте инъекции, замедляя его клиренс и по- |
||||||
мышиные фрагменты. В свою очередь, адалимумаб — |
тенцируя образование белковых агрегатов. |
||||||
полностью человеческое антитело, может индуциро- |
3. Наконец, иммуногенность зависит от индиви- |
||||||
вать иммунный ответ только против эпитопов вариа- |
дуальных особенностей макроорганизма и характера |
||||||
бельной области лекарственной молекулы, что суще- |
его коморбидных расстройств [24]. |
|
|
||||
ственно снижает воздействие ADAs. |
|
Доказано, что антитела против биологическо- |
|||||
В основе молекулярной структуры нетакимаба |
го препарата вырабатываются в течение первых не- |
||||||
используются иммуноглобулины ламы, содержащие |
скольких недель после введения лекарственного |
||||||
тяжелые цепи (VHH-цепи). Эти почти полностью гу- |
препарата. Согласно данным литературы, у 90% па- |
||||||
манизированные части молекулы сохранили лишь |
циентов, получающих иФНО-α, ADAs обнаружива- |
||||||
несколько участков в CDR-регионах, которые от- |
ются в течение 24 нед от начала терапии [25]. В связи |
||||||
вечают за прочность связывания с антигеном. Про- |
с инактивацией ADA части молекул лекарства коли- |
||||||
цесс генной модификации позволил присоединить |
чество свободных молекул может быть значительно |
||||||
легкие человеческие цепи иммуноглобулина к мо- |
снижено, что вызывает изменение фармакокинети- |
||||||
лекуле препарата, что привело к снижению имму- |
ки и фармакодинамики препарата [26]. У пациентов, |
||||||
ногенности. |
|
|
получавших иксекизумаб, частота выявления связы- |
||||
2. Помимо химической структуры на иммуно- |
вающих антител составила 17,4%, из них 6% облада- |
||||||
генность лекарственного средства влияют и другие |
ли нейтрализующей активностью, у 1% пациентов, |
||||||
факторы. Так, риск развития иммунизации зависит |
получавших секукинумаб, выявлены связывающие |
||||||
от фармакологической дозировки, путей и частоты |
антитела, из них в 50% — нейтрализующие [27, 28]. |
||||||
введения лекарственной молекулы, а также от дли- |
По данным российских исследователей, к нетакима- |
||||||
тельности терапии. Доказано, что прерывистое лече- |
бу связывающие ADAs выявлены менее чем в 0,5% |
||||||
ние низкими дозами препарата приводит к возник- |
случаев, при этом нейтрализующие антитела отсут- |
||||||
новению иммуногенности чаще, чем непрерывная |
ствовали [29]. Степень иммуногенности различных |
||||||
терапия высокими дозами того же лекарственно- |
биологических молекул, согласно данным офици- |
||||||
го средства [23]. Среди основных способов введе- |
альных регистров, представлена в таблице. |
||||||
ния наиболее приоритетными являются внутривен- |
Опыт клинической практики показал, что суще- |
||||||
ные инфузии. В свою очередь, подкожный и внутри- |
ствуют особые профили пациентов, для которых им- |
||||||
мышечный пути введения способствуют выработке |
муногенность является решающим фактором, ока- |
||||||
ADAs из-за процессинга молекул антигена антиген- |
зывающим непосредственное влияние на результа- |
||||||
презентирующими клетками в таких иммуноком- |
тивность лечения. |
|
|
||||
петентных органах, как кожа или мышечная ткань. |
Так, например, ожирение является фактором |
||||||
Биораспределение и клиренс терапевтических мо- |
риска в развитии псориаза. Висцеральная жировая |
||||||
лекул в макроорганизме также могут влиять на риск |
ткань способствует продукции адипокинов и про- |
||||||
развития иммуногенности. Подкожное и внутримы- |
воспалительных цитокинов, таких как ФНО-α, IL-6, |
||||||
шечное введения способствуют накоплению препа- |
IL-17. В связи с этим особое значение приобретают |
||||||
Степень иммуногенности различных биологических молекул |
|
|
|
|
|||
Degree of immunogenicity of various biological molecules |
|
|
|
|
|||
|
|
|
|
|
|
||
Биологическая |
Структура молекулы |
Количество исследований |
Число пациентов, |
ADA’s, % |
|||
молекула |
с участием препарата |
участвовавших в исследовании |
|||||
|
|
|
|||||
Адалимумаб |
Полностью гуманизированное |
|
4 |
1194 |
6–46 |
|
|
|
моноклональное антитело |
|
|
|
|
|
|
Бродалумаб |
Полностью гуманизированное |
|
1 |
160 |
5–9,8 |
||
|
моноклональное антитело |
|
|
|
|
|
|
Цертолизумаба |
Пегилированный Fab-фрагмент |
|
1 |
188 |
4–25 |
||
пэгол |
гуманизированного |
|
|
|
|
|
|
|
моноклонального антитела |
|
|
|
|
|
|
Этанерцепт |
Растворимый рецептор |
|
4 |
2138 |
1,1–18,3 |
||
Голимумаб |
Полностью гуманизированное |
|
1 |
405 |
5,4 |
|
|
|
моноклональное антитело |
|
|
|
|
|
|
Инфликсимаб |
Химерное моноклональное |
|
5 |
675 |
19,5–51,5 |
||
|
антитело |
|
|
|
|
|
|
Секукинумаб |
Полностью человеческое |
|
2 |
413 |
1 |
|
|
|
моноклональное антитело |
|
|
|
|
|
|
Нетакимаб |
Гуманизированное |
|
1 |
213 |
0,5 |
|
|
|
моноклональное антитело |
|
|
|
|
|
|
Устекинумаб |
Полностью человеческое |
|
3 |
2328 |
3,8–5,1 |
||
|
моноклональное антитело |
|
|
|
|
|
|
Russian Journal of Clinical Dermatology and Venereology 2020, Vol. 19, No. 6 |
939 |
Точка зрения |
Point of view |
функции макрофагов и гистиоцитов висцеральной |
нумаб) при псориазе с одновременным назначени- |
жировой ткани, количество которых значительно |
ем метотрексата [34]. Другие системные препараты |
увеличивается при ожирении. Эта особенность лежит |
классической терапии используются несколько ре- |
в основе развития «псориатического марша» и объ- |
же и назначаются в каждом случае с учетом сомати- |
ясняет частоту развития псориаза у пациентов с ожи- |
ческого состояния пациента и наличия сопутству- |
рением [30]. Доказано влияние на фармакокинети- |
ющих патологий. Имеются сведения об успешном |
ку и клиренс биологических препаратов у пациентов |
применении циклоспорина [35], азатиоприна [36] |
с избыточной массой тела, характеризующееся сни- |
для профилактики и инактивации выработки ADAs |
жением эффективности биологической терапии [31]. |
при длительном использовании препаратов моно- |
Наиболее распространенными и эффективными |
клональных антител. |
способами преодоления феномена ADAs являются: |
Согласно клиническим рекомендациям по при- |
— увеличение дозы и частоты введения ГИБП. |
менению биологической терапии в случае вторичной |
Такая практика широко применяется за рубежом, |
утери клинического ответа в первую очередь следует |
методики описаны в руководящих документах (guide- |
измерить сывороточный уровень активного препа- |
lines), однако и на территории РФ доза препарата мо- |
рата. Если он ниже минимального терапевтического, |
жет быть увеличена согласно инструкции по меди- |
рекомендуется увеличить дозу и/или кратность при- |
цинскому применению в случае недостаточного кли- |
ема препарата. Если же сывороточный уровень пре- |
нического ответа [32]; |
парата в норме, к терапии добавляют адъювантный |
— альтернативная химическая молекула другого |
препарат, направленный на подавление выработки |
биологического препарата; |
антител против лекарственной молекулы. В некото- |
— применение в качестве адъювантной тера- |
рых случаях целесообразно применение другого мо- |
пии цитостатиков, антиметаболитов, иммуносу- |
ноклонального антитела (рис. 3) [37]. |
прессоров (метотрексат, циклоспорин, азатиоприн). |
|
По данным статистического исследования 5 круп- |
Выводы |
ных регистров PSONET 2017 г., метотрексат являет- |
|
ся наиболее часто используемой молекулой в ком- |
1. Существует множество причин ускользания |
бинации с биологическими препаратами класса |
клинического ответа при лечении биологически- |
ингибитор ФНО (адалимумаб) и IL-12/23 (устеки- |
ми препаратами. Одной из наиболее значимых яв- |
нумаб) [33]. В литературе есть также данные об оп- |
ляется иммуногенность, характеризующаяся выра- |
тимизации лечения ингибитором IL-17А (секуки- |
боткой ADAs. |
Рис. 3. Терапевтический алгоритм при развитии вторичной лекарственной невосприимчивости. |
|
Fig. 3. A therapeutic algorithm with the development of secondary drug resistance.
940 |
Клиническая дерматология и венерология 2020, Т. 19, № 6 |
Точка зрения |
Point of view |
2.Снижая клиренс в сыворотке крови, ADAs влияют на фармакокинетику препарата и обусловливают вторичную лекарственную невосприимчивость.
3.В случае ускользания эффекта от биологической терапии определение количественной оценки ADAs в сыворотке крови имеет стратегическое значение для подбора и продолжения успешной терапии. Для того чтобы отложить формирование ADA и из-
ЛИТЕРАТУРА/REFERENCES
1.Armstrong AW, Aldredge L, Yamauchi PS. Managing patients with psoriasis in the busy clinic: practical tips for health care practitioners. J Cutan Med Surg. 2016;20:196-206.
2.Lecluse LLA, et al. Extent and clinical consequences of antibody formation against adalimumab in patients with plaque psoriasis. Arch Dermatol. 2010; 146:127-132.
3.Кубанов А.А., Самцов А.В. и др. Нетакимаб — новый ингибитор ИЛ17а: результаты 12 недель клинического исследования III фазы BCD- 085-7/PLANETA у пациентов со среднетяжелым и тяжелым вульгарным псориазом. Вестник дерматологии и венерологии. 2019;95(2):15-28. Kubanov AA, Samtsov AV, Khairutdinov VR, et al. Netakimab — new IL17a inhibitor: 12-week results of phase III clinical study BCD-085-7/PLANE- TA in patients with moderate-tosevere plaque psoriasis. Vestnik dermatologii i venerologii. 2019;95(2):15-28. (In Russ.).
4.Авдеева А.С., Артюхов А.С., Дашинимаев Э.Б. и др. Динамика показателей цитокинового профиля на фоне применения биоаналога ритуксимаба (Ацеллбия, «БИОКАД») и оригинального препарата (МабТера, «Ф. Хоффманн-Ля Рош» ЛТД., Швейцария) в терапии ревматоидного артрита. Научно-практическая ревматология. 2019;57(1):46-55. Avdeeva AS, Artyukhov AS, Dashinimaeva EB, et al. Changes of cytokine profile measures during the treatment of rheumatoid arthritis with rituximab biosimilar (Acellbia, BIOCAD) and the original drug (MabThera, F. Hoff- mann-La Roche Ltd., Switzerland). Nauchno-Prakticheskaya Revmatologiya = Rheumatology Science and Practice. 2019;57(1):46-55. (In Russ.).
5.Manis JP. Overview of therapeutic monoclonal antibodies. https://www.uptodate.com/contents/overview-of-therapeutic-monoclo- nal-antibodies
6.Lim LL, Fraunfelder FW, & Rosenbaum JT. Do tumor necrosis factor inhibitors cause uveitis? A registry-based study. Arthritis & Rheumatism. 2007; 56(10):3248-3252.
7.Monaco C, Nanchahal, J, Taylor P & Feldmann M. Anti-TNF therapy: past, present and future. International Immunology. 2014;27(1):55-62.
8.Tumor Necrosis Factor Inhibitors. Handbook of Disease Burdens and Quality of Life Measures. 2010;4341-4341.
9.Blair HA & Dhillon S. Secukinumab: A Review in Ankylosing Spondylitis. Drugs. 2016;76(10):1023-1030.
10.Menter A, Gordon KB, Leonardi CL, Gu Y & Goldblum OM. Efficacy and safety of adalimumab across subgroups of patients with moderate to severe psoriasis. Journal of the American Academy of Dermatology. 2010;63(3): 448-456.
11.Florek AG, Wang CJ & Armstrong AW. Treatment preferences and treatment satisfaction among psoriasis patients: a systematic review. Archives of Dermatological Research. 2018;310(4):271-319.
12.Chen DY, Chen YM, Tsai WC, et al. Significant associations of antidrug antibody levels with serum drug trough levels and therapeutic response of adalimumab and etanercept treatment in rheumatoid arthritis. Ann Rheum Dis; e-pub ahead of print 17 January 2014.
13.Van Brummelen EMJ, Ros W, Wolbink G, Beijnen JH, & Schellens JHM. Antidrug Antibody Formation in Oncology: Clinical Relevance and Challenges. The Oncologist. 2016;21(10):1260-1268.
14.Peters C & Brown S. Antibody-drug conjugates as novel anti-cancer chemotherapeutics. Bioscience Reports. 2015;35(4):e00225-e00225.
15.Sethu S, Govindappa K, Alhaidari M, Pirmohamed M, Park K & Sathish J. Immunogenicity to Biologics: Mechanisms, Prediction and Reduction. Archivum Immunologiae et Therapiae Experimentalis. 2012;60(5):331-344.
16.Jani M, Barton A, Warren RB, Griffiths CEM & Chinoy H. The role of DMARDs in reducing the immunogenicity of TNF inhibitors in chronic inflammatory diseases. Rheumatology. 2013;53(2):213-222.
бежать необходимости перехода на новый препарат, а следовательно, и новую иммунизацию, рекомендуется использовать правильные дозы, планировать лечение в долгосрочной перспективе и использовать иммуносупрессивный адъювант.
Авторы заявляют об отсутствии конфликта интересов. The authors declare no conflict of interest.
17.Brinks V, Jiskoot W and Schellekens H. Immunogenicity of therapeutic proteins: The use of animal models. Pharm Res. 2011;28:2379-2385.
18.Sethu S, Govindappa K, Alhaidari M, Pirmohamed M, Park K & Sathish J. Immunogenicity to Biologics: Mechanisms, Prediction and Reduction. Archivum Immunologiae et Therapiae Experimentalis. 2012;60(5):331-344.
19.Bendtzen Klaus. Anti-TNF-α biotherapies: perspectives for evidence-based personalized medicine. Immunotherapy. 2012;4(11):1167-1179.
20.Schellekens H.. The immunogenicity of therapeutic proteins. Discovery Medicine. 2010;9(49):560-564.
21.van Schouwenburg Pauline A, et al. Adalimumab elicits a restricted anti-idi- otypic antibody response in autoimmune patients resulting in functional neutralisation. Annals of the rheumatic diseases. 2013;72(1):104-109.
22.Bartelds Geertje M, et al. Development of antidrug antibodies against adalimumab and association with disease activity and treatment failure during long-term follow-up. JAMA. 2011;305(14):1460-1468.
23.Parenky Ashwin, et al. New FDA draft guidance on immunogenicity. 2014; 499-503.
24.Menting SP, van Lümig PPM, de Vries, A-CQ, van den Reek JMPA, van der Kleij D, de Jong EMGJ, ... Lecluse LLA. Extent and Consequences of Antibody Formation Against Adalimumab in Patients With Psoriasis. JAMA Dermatology. 2014;150(2):130.
25.Jullien D, Prinz JC & Nestle FO. Immunogenicity of Biotherapy Used in Psoriasis: The Science Behind the Scenes. Journal of Investigative Dermatology. 2015;135(1):31-38.
26.Reich K, Jackson K, Bal, S, Garces S, Kerr L, Chua L, ... Blauvelt A. Ixekizumab Pharmacokinetics, Anti-Drug Antibodies, and Efficacy through 60 Weeks of Treatment of Moderate to Severe Plaque Psoriasis. Journal of Investigative Dermatology. 2018;138(10):2168-2173.
27.Reich K, Blauvelt A, Armstrong A, Langley RG, de Vera A, Kolbinger F, Bruin G. Secukinumab, a fully human anti-interleukin-17A monoclonal antibody, exhibits low immunogenicity in psoriasis patients treated up to 5 years. Journal of the European Academy of Dermatology and Venereology.
2019;33(9):1733-1741.
28.Бакулев А.Л., Самцов А.В., Кубанов А.А. и др. Долгосрочная эффективность и безопасность препарата нетакимаб у пациентов со среднетяжелым и тяжелым вульгарным псориазом. Результаты открытого продленного клинического исследования II фазы BCD-085-2-EXT.
Вестник дерматологии и венерологии. 2019;95(3):54-64.
Bakulev AL, Samtsov AV, Kubanov AA I dr. Long-term efficacy and safety of netakimab in patients with moderate-to-severe psoriasis. Results of phase II open-label extension clinical study BCD-085-2-ext. Vestnik dermatologii i venerologii. 2019;95(3):54-64. (In Russ.).
29.De Simone Clara, et al. Immunogenicity of anti-TNFα therapy in psoriasis: a clinical issue? Expert opinion on biological therapy. 2013;13.12:1673-1682.
30.Owczarczyk-Saczonek, Agnieszka, and Waldemar Placek. Compounds of psoriasis with obesity and overweight. Postepy Higieny i Medycyny Doswiadczalnej (Online). 2017;71.1:761-772.
31.Gisondi Paolo, Micol Del Giglio and Giampiero Girolomoni. Considerations for systemic treatment of psoriasis in obese patients. American journal of clinical dermatology. 2016;17.6:609-615.
32.https://www.vidal.ru/drugs/cosentyx
33.Busard CI, et al. Biologics combined with conventional systemic agents or phototherapy for the treatment of psoriasis: real-life data from PSONET registries. Journal of the European Academy of Dermatology and Venereology.
2018;32.2:245-253.
34.Kostaki Dimitra, et al. Optimizing Secukinumab Treatment in Psoriasis with Concomitant Methotrexate Administration: Minireview and A Case Report.
Case Reports in Dermatology. 2019;11.1:17-22.
Russian Journal of Clinical Dermatology and Venereology 2020, Vol. 19, No. 6 |
941 |
Точка зрения |
Point of view |
35.Katsuyama Atsuko, et al. Long-term efficacy and safety of infliximab and cyclosporine combination therapy for refractory uveoretinitis in Behçet’s disease. Clinical Ophthalmology (Auckland, NZ). 2019;13:521.
36.Roblin Xavier, et al. Addition of azathioprine to the switch of anti-TNF in patients with IBD in clinical relapse with undetectable anti-TNF trough le-
vels and antidrug antibodies: a prospective randomised trial. Gut. 2020; 69.7:1206-1212.
37.Carrascosa J-M, et al. Clinical relevance of immunogenicity of biologics in psoriasis: implications for treatment strategies. Journal of the European Academy of Dermatology and Venereology. 2014;28.11:1424-1430.
Поступила в редакцию 08.10.20
Received 08.10.20
Принята к печати 15.10.20
Accepted 15.10.20
942 |
Клиническая дерматология и венерология 2020, Т. 19, № 6 |
Косметология |
Cosmetology |
Клиническая дерматология и венерология |
Russian Journal of Clinical Dermatology and Venereology = |
2020, Т. 19, № 6, с. 943-952 |
Klinicheskaya dermatologiya i venerologiya 2020, Vol. 19, No. 6, pp. 943-952 |
https://doi.org/10.17116/klinderma202019061943 |
https://doi.org/10.17116/klinderma202019061943 |
Обоснованный выбор комплексной программы коррекции возрастных изменений лица с применением инъекционных и лазерных технологий
© Н.Г. КАЛАШНИКОВА1, Е.В. ПОЗДЕЕВА2
1Сеть клиник «Линлайн», Москва, Россия;
2Сеть клиник «Линлайн», Екатеринбург, Россия
РЕЗЮМЕ
Возрастные изменения лица многоуровневые и многокомпонентные. Очевидно, что воздействовать одним методом на все звенья про-
исходящих возрастных изменений на лице не представляется возможным. Поэтому сочетание методов с различными механизмами
действия и реализацией эффектов на разных уровнях патогенетически обосновано и перспективно. Сочетание различных методов коррекции инволютивых изменений лица широко используется в клинической косметологической практике, но существующей дока-
зательной базы явно недостаточно для создания единого алгоритма указанной коррекции. Критерии комплексной оценки лица, явля-
ющейся основой индивидуального плана коррекции инволютивных изменений, не определены. На основании анализа проведенных
исследований и личного опыта авторов предложены основополагающие принципы выбора таргетной терапии, сочетающей инъекции
ботулотоксина, препаратов на основе гиалуроновой кислоты (ГК) и лазерное/световое лечение и позволяющей реализовать патогенетически обоснованный подход к эстетической коррекции инволютивных изменений лица. Комплексная эстетическая оценка с анали-
зом геометрических пропорций, анатомо-морфологических особенностей структурных тканей, степени возрастных изменений кожи
и формы лица, удельного веса влияния этих факторов на общую клиническую картину — основа для выбора таргетных методов кор-
рекции, которые необходимо включить в индивидуальный план ведения для достижения оптимального результата и высокого уровня
удовлетворенности пациента проведенной терапией.
Ключевые слова: лазер, IPL, гиалуроновая кислота, филлеры, ботулотоксин, комбинированный подход, эстетическая коррекция, возрастные изменения лица.
Калашникова Н.Г. — https://orcid.org/0000-0001-5250-9288 Поздеева Е.В. — https://orcid.org/0000-0002-5507-9751
Автор, ответственный за переписку: Калашникова Н.Г. — e-mail: kalashnikovaline@mail.ru
КАК ЦИТИРОВАТЬ:
Калашникова Н.Г., Поздеева Е.В. Обоснованный выбор комплексной программы коррекции возрастных изменений лица
с применением инъекционных и лазерных технологий. Клиническая дерматология и венерология. 2020;19(6):943–952. https://doi. org/10.17116/klinderma202019061943
Reasonable choice of a complex program for correction of age-related facial changes using injection and laser technologies
© N.G. KALASHNIKOVA1, E.V. POZDEEVA2
1«Linline» Clinic Chain, Moscow, Russia;
2«Linline» Clinic Chain, Ekaterinburg, Russia
ABSTRACT
Age-related changes in the face are multilevel and multicomponent. It is obvious that it is impossible to influence by one method on all aspects of the occurring age-related changes on the face. Therefore, the combination of methods that have different mechanisms of action and realize the effect at different tissue levels is pathogenetically substantiated and it is promising. The combined approach is currently already widely used in practice of nonsurgical aesthetic medicine, but they can rather be characterized as art, since the accumulated scientifically proven base is insufficient due to the fact that this area is difficult to study. Currently, the criteria for a comprehensive face assessment, which is the basis for an individual correction plan, remain undefined. The fundamental principles of the choice of targeted therapy, including a combination of botulinum toxin, fillers HA and laser/light treatment, are proposed based on the analysis of the accumulated research and personal experience of the authors. In the next article, we will present a set of practical recommendations on how to combine these methods in complex programs.
Keywords: laser, light treatment, hyaluronic acid, fillers, botulinum toxin, combined approach, nonsurgical aesthetic medicine, age-related facial changes.
Kalashnikova N.G. — https://orcid.org/0000-0001-5250-9288
Pozdeeva E.V. — https://orcid.org/0000-0002-5507-9751
Corresponding author: Kalashnikova N.G. — e-mail: kalashnikovaline@mail.ru
Russian Journal of Clinical Dermatology and Venereology 2020, Vol. 19, No. 6 |
943 |

Косметология |
Cosmetology |
TO CITE THIS ARTICLE:
Kalashnikova NG, Pozdeeva EV. Reasonable choice of a complex program for correction of age-related facial changes using injection and laser technologies. Russian Journal of Clinical Dermatology and Venereology = Klinicheskaya dermatologiya i venerologiya. 2020;19(6):943–952.
(In Russ.). https://doi.org/10.17116/klinderma202019061943
Возрастные изменения лица многоуровневые
имногокомпонентные [1—3] включают структурное старение соединительной, жировой, мышечной
икостной тканей, что сопровождается потерей эластичности, растяжением кожи и связочного аппарата с формированием излишков мягких тканей, перераспределением последних и их смещением в пространстве относительно друг друга, снижением опоры для мягких тканей за счет уменьшения скелетной поддержки и уменьшения объемов глубоких жировых пакетов. Суммарный результат всех происходящих процессов отражается в клинической картине старения ухудшением качества покровной ткани, трансформацией формы лица и изменением мимики. Анализ проводимых исследований способствует пониманию динамики и взаимодействия происходящих процессов [2]. Накопленные данные позволяют перейти от симптоматической эстетической терапии к анатомо-патогенетическому подходу, реализующему результат, максимально приближенный к естественному [2], и не только корректировать имеющиеся признаки старения, восстанавливая характеристики молодого лица, но и оказывать влияние на темпы их проявления. Очевидно, что воздействовать одним методом на все звенья происходящих возрастных изменений на лице невозможно. Поэтому сочетание методов с различными механизмами действия, реализующими эффект на разных тканевых уровнях, патогенетически обосновано и перспективно. К настоящему времени опубликован ряд работ, посвященных комбинированному подходу к эстетической коррекции инволютивных изменений лица, демонстрирующих актуальность этого направления [2—4].
Современный арсенал косметологии включает широкий спектр различных методов, среди которых наибольшей популярностью пользуются инъекции препаратов ботулинического токсина, филлеров на основе гиалуроновой кислоты (ГК) и высокоэнергетические световые методы, что отражается в представленных статистических данных за 2018 г. (6,1, 3,7 и 0,6 млн процедур соответственно) и их динамике за последние годы в мировой практике [5]. Сочетание этих методов уже широко используется в клинической косметологической практике, однако их скорее можно охарактеризовать как искусство ввиду ограниченной доказательной базы, поскольку данная область сложна для изучения [2, 6].
Обзор и анализ публикаций по комбинированному подходу к коррекции возрастных изменений, накопление опыта важны для определения критериев сочетания различных методов, что, в свою оче-
редь, позволит практикующим врачам более уверенно применять комбинированный подход в своей практике с большей эффективностью и высоким профилем безопасности.
Бесспорно, что результат комплексной программы коррекции будет зависеть от совокупности целого ряда факторов:
—особенностей действия, степени агрессивности и глубины эффекта используемого физического воздействия [3, 7, 8];
—состава и уровня расположения тканевого наполнителя [3, 7, 8];
—полноты и адекватности оценки клинической картины, определения показаний и обоснованного выбора соответствующей индивидуальной программы [4, 7, 8];
—последовательности применения аппаратных
иинъекционных методов, временного интервала между ними [3, 7, 8].
Лазеры и источники интенсивного импульсного света
В основе действия высокоэнергетических лазерных методов лежит способность веществ кожи (хромофоров) поглощать световое излучение с различной степенью в зависимости от длины его волны. При поглощении происходит трансформация световой энергии в другие виды энергии, что позволяет избирательно разрушать целевую мишень. В зависимости от типа преобразованной энергии взаимодействие лазера с биологическими тканями характеризуется тремя видами эффектов: фототермическим (преобразование энергии фотонов в тепло), фотомеханическим (при высоких значениях энергии 108–109 Вт/см2 происходят процессы ионизации, сопровождающиеся взаимодействием электрических полей, диэлектрическими реакциями, ударными волнами и разрывом тканей) и фотохимическим (энергия фотонов вызывает химические реакции в клетках без изменения температуры) [9].
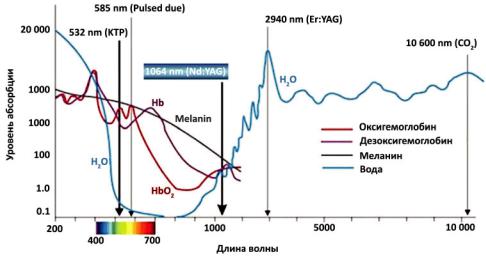
Основными хромофорами кожи являются окси-, дезоксигемоглобин, меланин и вода, коэффициенты поглощения которых хорошо изучены для излучения различных длин волн. На основании спектрограммы (рис. 1) осуществляется выбор типа лазера для получения желаемого лечебного эффекта и глубины его реализации.
Процедуры по омоложению кожи направлены на восстановление ее внешнего вида, характерного для более молодого возраста. В настоящее время с этой целью применяются практически все
944 |
Клиническая дерматология и венерология 2020, Т. 19, № 6 |
Косметология |
Cosmetology |
|
|
|
|
Рис. 1. Спектры поглощения хромофоров кожи.
Fig. 1. Absorption spectra of major chromophores in skin.
известные виды лазеров, генерирующих излучение в видимом, ближнем, среднем и дальнем инфракрасном диапазоне, и источники интенсивного импульсного света (ИИИС) [10—13].
В зависимости от степени термического воздействия лазеры подразделяются на аблятивные, которые нарушают целостность эпидермиса за счет выпаривания поверхностных тканей, и неаблятивные, вызывающие меньший термический эффект (коагуляцию) без нарушения целостности кожных покровов. Оба типа лазеров используются как с воздействием полным световым пятном, так и фракционно [10—13].
Аблятивные лазеры генерируют излучение с высоким коэффициентом поглощения излучения водой, что способствует термическому повреждению кожи, стимулирующему регенеративные процессы с ремоделированием структуры внеклеточного матрикса. Коагуляция на уровне дермы может достигать глубины от 150 до 300 микрон в зависимости от типа лазера и физических параметров излучения [10]. Результатом такого воздействия является обновление и оптимизация поверхностного рельефа кожи, удаление кератоза и эпидермальных новообразований, повышение тонуса и эластичности кожи с уменьшением количества и глубины морщин, излишков мягких тканей за счет сокращения кожного лоскута. К абляционным лазерам относятся углекислотный (CO2) лазер с длиной волны 10 600 нм, эрбий-иттрий-алюминиево-гра- натовый лазер Er:YAG 2940 нм и лазер на иттрий- скандий-галлиевом гранате, легированный эрбием Er:YSGG 2790 нм.
Фотоомоложение с применением неаблятивных лазеров и ИИИС принято подразделять на 2 ти-
па [10]: I тип направлен на коррекцию сосудистой и пигментной патологии, II тип — на восстановление структуры кожи. Лазерные устройства, излучающие свет, преимущественно поглощаемый гемоглобином и меланином, используют для I типа фотоомоложения, длины волн: 532, 585–595, 694, 755, 800–810, 940, 1064 нм. Для II типа фотоомоложения применяют лазерные устройства, излучающие свет среднего и дальнего инфракрасного диапазона, который поглощается водой, длины волн: 1320, 1440, 1450, 1540, 1550, 1900–2000 нм, а также PDL-лазер с длиной волны 585–595 нм, поглощаемой в большей степени гемоглобином, но оказывающей достоверно доказанное стимулирующее действие на неоколлагенез и внеклеточный матрикс [10].
ИИИС в отличие от лазеров генерируют излучение, включающее сразу множество длин волн (420– 1400 нм) с различной длительностью импульса, оно не имеет направленности луча, временной и пространственной синхронизации. Широкий диапазон света поглощается одновременно сразу несколькими хромофорами кожи, что снижает селективность взаимодействия. Использование отсекающих фильтров позволяет выделять узкий спектр излучения и повышать избирательность воздействия при применении ИИИС для фотоомоложения I или II типа, но в целом селективность их остается ниже, чем у лазеров [12, 13].
Глубина воздействия излучения определяется его поглощением и проникновением, которые зависят от основных физических параметров: длины волны, режима генерации и длительности импульса, диаметра светового пятна и плотности мощности. При лазерном воздействии на ткани необходимо учитывать следующие закономерности:
Russian Journal of Clinical Dermatology and Venereology 2020, Vol. 19, No. 6 |
945 |

Косметология Cosmetology
— проникающая способность светового излуче- |
мягких тканей в зависимости от типа излучения и ре- |
ния обратно пропорциональна коэффициенту по- |
жима его генерации недостаточно. Такая задача яв- |
глощения основным хромофором при данной длине |
ляется трудоемкой с учетом многообразия применя- |
волны, соответственно, с увеличением длины волны |
емых на практике лазерных и световых технологий. |
до среднего инфракрасного диапазона глубина про- |
Инъекционные препараты гиалуроновой кислоты |
никновения нарастает (в диапазоне 532–1064 нм свет |
|
на длине волны 1064 нм проникает в ткань наибо- |
Инъекции препаратов на основе ГК занимают |
лее глубоко [14]), далее за счет возрастания коэф- |
второе место среди нехирургических эстетических |
фициента поглощения излучения водой — умень- |
процедур [5, 21]. С этой целью применяются 2 ви- |
шается [14]; |
да препаратов: |
— чем длительнее импульс, тем больше проник- |
— нестабилизированная ГК используется для |
новение света в ткани [14]; |
биоревитализации в технике интрадермальных мно- |
— чем больше диаметр светового пятна, тем |
жественных микроинъекций; |
глубже проникновение излучения, для ширины лу- |
— ГК, имеющая перекрестные связи между мо- |
ча 10 мм достигается критическая точка, при кото- |
лекулами, выполняет роль тканевого наполнителя. |
рой дальнейшее увеличение ширины луча использу- |
Применение ГК для биоревитализации направ- |
емого лечебного устройства не влияет на проникно- |
лено на поддержание или восстановление структуры |
вение света в ткани [14, 15]; |
кожи, повышение ее сияния и уменьшение пигмен- |
— с увеличением плотности мощности светово- |
тации, связанной с фотостарением [22]. ГК повыша- |
го излучения глубина проникновения света возрас- |
ет уровень гидратации благодаря ее гидрофильным |
тает [14]. |
свойствам, позволяющим притягивать и удерживать |
Большинство лазерных технологий и ИИИС реа- |
молекулы воды [22]. Увлажнение кожи происходит |
лизуют свои эффекты относительно поверхностно — |
не только поверхностно, но и в глубоких слоях ко- |
1,5–5 мм (уровень дермы и поверхностный слой ги- |
жи [22, 23], что способствует повышению ее ярко- |
подермы) [10—14]. Однако метод математического |
сти и уменьшению глубины морщин [23, 24]. Вну- |
моделирования, используемый при оценке, показы- |
трикожные микроинъекции ГК стимулируют фибро- |
вает лишь глубину проникновения света, а не уро- |
бласты, воссоздавая физиологические условия [23], |
вень теплового эффекта, который он оказывает при |
увеличивается синтез внеклеточного матрикса (кол- |
взаимодействии с тканью [14]. |
лагена, эластина, эндогенной ГК), что способству- |
Более того, технический прогресс, расширяя воз- |
ет повышению тонуса, эластических свойств кожи |
можности и показания, выходит за рамки ранее ис- |
и омоложению ее внешнего вида [25, 26]. Улучшения |
пользуемых стандартных режимов лазерного излу- |
возникают уже после первого сеанса (через 2 нед) |
чения за счет вариации временных, энергетических |
и продолжаются после каждой последующей про- |
параметров, пространственного моделирования све- |
цедуры [22]. Предполагается полезность выполне- |
тового потока и позволяет достигать более глубоких |
ния биоревитализации перед процедурами лазерного |
тканевых уровней. Уникальные режимы примене- |
омоложения, в которых вода является целевым хро- |
ния Er:YAG-лазера, ранее стандартно используемо- |
мофором. Однако достоверных данных, подтвержда- |
го только для абляции, реализуют эффект на уров- |
ющих или опровергающих это наблюдение, пока нет. |
не SMAS: |
Препараты связанной ГК выполняют роль на- |
— интраоральное применение Er:YAG-лазера |
полнителей и считаются золотым стандартом био- |
2940 нм в SMOOTH-режиме (неаблятивное фрак- |
материала для коррекции мягких тканей лица [27]. |
ционное воздействие) [16, 17]; |
Филлеры на основе ГК используются чаще все- |
— Er:YAG-лазер 2940 нм с технологией простран- |
го [5, 21, 28], что объясняется широким ассортимен- |
ственно-модулированной абляции (SMA) вызывает |
том доступных продуктов, простотой использова- |
акустическое микротравмирование тканей на глуби- |
ния и возможностью их биодеградации [27]. Фил- |
не до 6 мм [18—20]. |
леры на основе ГК различаются реологическими |
Таким образом, лазерные технологии, применя- |
свойствами, которые определяются особенностями |
емые для омоложения, многообразны. Уровень про- |
производственного процесса и физико-химически- |
никновения света в большей степени определяет- |
ми свойствами продуктов [29]: концентрацией ГК, |
ся длиной волны, но также зависит от совокупно- |
длиной их цепей, характером и количеством свя- |
сти других физических параметров. Однако степень |
зей между цепями, наличием добавок и размером |
агрессивности физического воздействия определя- |
частиц [30]. Реологические свойства наполнителей |
ется не уровнем проникновения света, а выражен- |
включают эластичность (G’) — степень восстановле- |
ностью фотобиологического эффекта (фототермиче- |
ния исходной формы геля после деформации и ко- |
ского, фотомеханического, фотохимического). Пока |
гезивность — силу притяжения между частицами пе- |
достоверных данных для оценки степени агрессив- |
рекрестно-связанной ГК. Эти свойства препаратов |
ности лазерного воздействия на различной глубине |
определяют показания к их применению и уровень |
946 |
Клиническая дерматология и венерология 2020, Т. 19, № 6 |
