
- •ПРЕДИСЛОВИЕ ПЕРЕВОДЧИКА
- •ПРЕДИСЛОВИЕ
- •СПИСОК СОКРАЩЕНИЙ
- •1. Введение
- •1.1. Освещение по Кёлеру
- •1.1.1. Принципы метода
- •1.1.2. Предварительная проверка оборудования
- •1.2. Установка света по Кёлеру
- •2.1. Преломление
- •2.1.1. Числовая апертура
- •2.2. Отражение, поглощение и пропускание
- •2.3. Флуоресценция/фосфоресценция
- •2.4. Поляризация
- •2.5. Дифракция
- •2.5.1. Тестовые пластинки Аббе
- •2.5.2. Формирование первичного изображения
- •2.5.3. Разрешающая способность
- •2.5.4. Роль конденсора в разрешении микроскопа
- •2.5.5. Увеличение
- •2.5.6. Увеличение и разрешение
- •4. Поле зрения
- •5. Резюме
- •6. Литература для дальнейшего чтения
- •1. Введение
- •1.1. Определение контраста
- •2. Светлопольная микроскопия
- •3. Фазовый контраст
- •3.2. Дифрагированный свет в фазовом контрасте
- •4. Темнопольная микроскопия
- •4.1. Освещение по Рейнбергу
- •4.2. Темнопольные конденсоры высокого разрешения
- •4.3. Темнопольное изображение
- •5. Поляризованный свет
- •5.1. Использование одиночного поляризатора
- •5.2. Использование скрещенных поляризаторов
- •5.2.2. Направление двулучепреломления
- •6.3. Интерференционная отражательная микроскопия
- •6.3.2. Физические основы метода
- •6.3.3. Интерпретация результатов
- •7.1. Красители
- •7.2. Использование светофильтров
- •7.3. Срезы
- •7.4. Качество препарата
- •8. Другие методы
- •8.1. Дисперсионное окрашивание
- •10. Благодарности
- •11. Литература
- •ФИКСИРОВАНИЕ ИЗОБРАЖЕНИЯ
- •1. Введение
- •2. Рисование
- •3. Фотомикрография
- •4.1. Разрешение
- •4.2. Разрешающая способность и размер отпечатка
- •4.4. Освещение
- •5. Микроскоп для фотомикрографии
- •5.1. Штатив микроскопа
- •5.2. Оптика
- •5.2.1. Числовая апертура и увеличение объективов
- •5.2.2. Исправление аберраций
- •5.2.4. Иммерсионные объективы
- •5.2.5. Глубина резкости
- •5.2.6. Кривизна поля зрения
- •5.2.7. Типы конденсоров
- •5.2.8. Чистка линз
- •6. Камера для фотомикрографии
- •6.1. Выбор размера пленки
- •6.3. Специальная фотомикрографическая камера
- •6.4. Микроскопы со встроенными фотосистемами
- •6.5. Камера с мехами
- •7. Наведение на фокус и определение экспозиции
- •7.1. Наведение на фокус
- •7.2. Определение экспозиции
- •7.3. Контроль экспозиции
- •8. Выбор условий для фотомикрографии
- •8.1. Фотографический процесс
- •8.1.1. Чувствительность пленки
- •8.1.2. Зернистость
- •8.1.3. Контрастность
- •8.2. Черно-белая фотомикрография
- •8.3. Цветная фотомикрография
- •8.3.1. Цветные отпечатки или слайды
- •8.3.2. Печать со слайдов
- •8.3.3. Цветовая температура
- •8.3.4. Коррекция цветовых искажений
- •8.3.6. Выбор чувствительности пленки
- •8.4. Поляроидные клетки
- •8.4.2. Камера Поляроид SX70
- •8.4.3. Поляроидные слайды
- •8.5. Хранение неэкспонированной пленки
- •9. Фотомакрография
- •9.1.1. Стереомикроскопы для фотомикрографии
- •9.1.2. Макроскопы
- •9.1.3. Фотомакрографические объективы
- •9.2. Освещение для фотомакрографии
- •9.3. Определение экспозиции при фотомакрографии
- •10. Завершение процесса фотомикрографии
- •10.1. Содержание записей
- •10.2. Хранение негативов
- •10.3. Хранение слайдов
- •10.4. Монтаж слайдов
- •10.5. Хранение отпечатков
- •10.6. Определение и указание увеличения
- •11. Практическое руководство
- •11.2. Начальная калибровка экспонометра
- •12. Литература для дальнейшего чтения
- •ИММУНОГИСТОХИМИЯ
- •1. Введение
- •2. Антитела
- •2.1. Структура иммуноглобулинов
- •2.2. Поликлональная антисыворотка
- •2.3. Моноклональные антитела
- •2.4. Очистка антител
- •2.5. Специфичность реакций антител
- •2.6. Хранение антител
- •3.1. Выбор условий обработки ткани
- •3.2. Выявление скрытых антигенов
- •4. Выбор способа мечения
- •4.1. Флуоресцентные метки
- •4.2. Ферментные метки
- •4.2.1. Пероксидаза хрена
- •4.2.2. Щелочная фосфатаза
- •4.2.3. Глюкозооксидаза
- •4.2.4. Галактозидаза
- •4.3. Коллоидное золото
- •4.4. Выбор метки
- •5. Методы окраски
- •5.1. Прямой метод
- •5.2. Непрямой метод
- •5.4. Системы с использованием биотин — авидина
- •5.5. Другие методы
- •6. Экспериментальные методы
- •6.1. Общее описание метода
- •6.2. Выбор правильного разведения антител
- •6.3. Флуоресцентные метки
- •6.4. Пероксидаза
- •6.4.1. Ингибирование эндогенного фермента
- •6.5. Щелочная фосфатаза
- •6.5.1. Блокирование эндогенного фермента
- •6.5.2. Мера предосторожности
- •6.6. Глюкозооксидаза
- •6.7. Галактозидаза
- •6.9. Некоторые общие процедуры
- •6.9.1. Покрытие предметных стекол
- •6.9.2. Дополнительное окрашивание
- •7.1. Контрольные препараты
- •7.2. Решение проблем
- •9. ДНК-зонды для гибридизации in situ
- •9.1. Принцип метода гибридизации
- •9.2. Экспериментальная процедура
- •9.2.1. Выявление Y-хромосомы
- •9.2.2. Выявление цитомегаловируса
- •10. Цитологические препараты
- •11. Количественная оценка
- •12. Оборудование
- •13. Благодарности
- •14. Литература
- •ГИСТОХИМИЯ И СВЕТОВАЯ МИКРОСКОПИЯ
- •1. Введение
- •1.1. Объекты для гистохимического окрашивания
- •1.1.1. Что такое окрашивание?
- •2. Приготовление и хранение срезов препаратов
- •2.1. Необходимые характеристики препарата
- •2.2. Методы приготовления и хранения препаратов
- •2.2.1. Получение тонких слоев
- •3. Что можно выявлять? Некоторые примеры
- •3.1. Выявление химических свойств
- •3.1.1. Химические фрагменты
- •3.1.2. Специфические вещества
- •3.1.3. Классы веществ
- •3.2. Выявление биологических объектов
- •3.2.1. Биологические объекты
- •3.2.2. Биологические процессы
- •3.3. Морфологические исследования
- •4. Выбор методов
- •5.1. Оценка селективности методов
- •5.2. Оценка локализации окрашивания
- •5.4. Оценка чистоты реагентов
- •5.5. Номенклатура реагентов
- •6. Что необходимо для гистохимической работы
- •6.1. Оборудование и материалы
- •6.2. Как научиться работать?
- •7. Почему используются гистохимические методы
- •8. Благодарности
- •ФЛУОРЕСЦЕНТНАЯ МИКРОСКОПИЯ
- •1. Введение
- •2. Флуорохромы
- •3. Флуоресцентный микроскоп
- •3.1. Способы освещения
- •3.1.1. Освещение проходящим светом
- •3.1.2. Освещение падающим светом
- •3.2. Источники света
- •3.3. Домики для ламп
- •3.4. Фильтры
- •3.4.1. Возбуждающие фильтры
- •3.4.2. Запирающие фильтры
- •3.4.3. Цветные светоделительные зеркала
- •3.5. Объективы и окуляры
- •4. Применение флуоресцентных красителей
- •4.1. Нуклеиновые кислоты
- •4.1.1. Прижизненное окрашивание флуорохромами
- •4.2. Иммунофлуоресценция
- •4.3. Флуоресценция нейромедиаторов
- •4.4. Двойное окрашивание
- •5. Микрофлуориметрия
- •5.1. Введение
- •5.2. Стандарты флуоресценции
- •5.3. Оборудование
- •5.3.1. Инвертированные микрофлуориметры
- •5.3.2. Сканирующие микрофлуориметры
- •5.4. Измерения содержания ДНК
- •5.4.1. Оборудование
- •5.4.2. Подготовка материала
- •5.4.3. Процедура окрашивания
- •5.4.4. Проведение измерений
- •6. Анализ изображения при флуоресценции
- •7. Сканирующая лазерная микроскопия
- •8. Литература
- •МИКРОМЕТРИЯ И АНАЛИЗ ИЗОБРАЖЕНИЯ
- •1. Введение
- •2. Простая микрометрия
- •2.1. Измерения длины
- •2.1.3. Окуляр-микрометр сдвига
- •2.1.4. Другие методы измерения длины
- •2.2 Измерения углов
- •2.3. Измерение толщины
- •2.4. Счетные камеры
- •2.4.2. Техника работы с гемоцитометром
- •3.1.1. Определение АA в двухфазном препарате
- •3.2. Принципы измерения площади поверхности
- •4. Измерения с использованием дигитайзера
- •5.2. Измерения с помощью компьютера
- •6. Приборы и математическое обеспечение работ
- •7. Литература
- •ВИДЕОМИКРОСКОПИЯ
- •1. Видеомикроскопия и оборудование для нее
- •1.1. Введение
- •1.1.1. Видеоусиление
- •1.1.2. Видеоинтенсификация
- •1.1.3. Цифровая обработка изображения
- •1.2.1. Условия ограниченного числа фотонов
- •1.3. Различные методы видеомикроскопии
- •1.3.1. Видеомикроскопия с усилением
- •1.3.2. Аналоговое усиление контраста
- •1.3.3. Цифровая обработка изображения
- •1.4.1. Камеры и контроллеры камер
- •1.4.5. Видеопроцессорные платы
- •1.4.6. Монофункциональные процессоры
- •1.4.7. Взгляд в будущее
- •1.5. Условия, налагаемые на микроскоп
- •1.6. Как соединить телекамеру с микроскопом
- •2.1. Различные виды VEC-микроскопии
- •2.2. Приготовление препаратов
- •2.3. Получение изображения
- •2.4. Интерпретация изображений
- •2.5. Типичные применения и ограничения метода
- •2.5.1. Светлопольная микроскопия
- •2.5.2. Темнопольная микроскопия
- •2.5.4. Фазовый контраст
- •2.5.5. Поляризационная микроскопия
- •2.5.7. Отражательная контрастная микроскопия
- •2.5.8. Флуоресцентная микроскопия
- •2.5.9. Примеры применения в биологии и биохимии
- •3.1. Введение
- •3.2. Процесс формирования изображения
- •3.2.1. Условия, касающиеся микроскопа
- •3.2.2. Получение статических изображений
- •3.2.3. Получение изображений подвижных объектов
- •3.3. Типичные приложения
- •3.3.2. Картирование отношений
- •3.3.4. Визуализация молекул
- •3.3.6. Люминесценция
- •3.3.7. Нейробиология
- •4.1. Пространственные измерения
- •4.2. Измерения по интенсивности
- •5.1. Видеозапись и редактирование
- •5.1.1. Стандарты видеотехники
- •5.1.2. Форматы видеопленок
- •5.1.3. Качество видеопленок
- •5.1.4. Видеомагнитофоны
- •5.1.5. Видеомагнитофоны с цейтраферной записью
- •5.1.6. Запись при видеомикроскопии
- •5.1.8. Копирование и редактирование видеозаписей
- •5.2.1. Оборудование
- •5.3. Перенос видеозаписей в видеофильм
- •5.4. Рисование с монитора
- •6. Благодарности
- •7. Литература
- •1. Введение
- •2. Классификация сегментов хромосом
- •2.1. Гетерохроматиновые сегменты
- •2.2. Эухроматиновые сегменты
- •2.3. Ядрышковые организаторы
- •2.4. Кинетохоры
- •4.2. G-окрашивание
- •4.2.1. ASG-метод
- •4.2.3. Метод Галлимора и Ричардсона
- •4.3. R-окрашивание
- •4.4. Q-окрашивание
- •4.4.1. Q-окрашивание с помощью акрихина
- •4.5.2. Процедура окраски
- •5.1. Окрашивание ДАФИ/дистамицином
- •5.2.1. Метод культивирования клеток
- •5.2.2. Методика окраски
- •5.3.2. Синхронизация с помощью БУДР [39]
- •5.3.3. Синхронизация с помощью ФУДР [13, 40]
- •6. Наблюдение и регистрация сегментов хромосом
- •6.3. Фотографирование сегментированных хромосом
- •6.4.1. Получение профилей сегментов
- •6.4.2. Отражательная микроскопия
- •6.4.3. Измерение полиморфизма хромосом
- •7. Благодарности
- •8. Литература
- •9. Литература для дальнейшего чтения
5. Микрофлуориметрия
5.1. Введение
Микрофлуориметрия — это метод измерения света, испускаемого флуоресцирующим объектом, например клеткой или клеточной органеллой. Интенсивность флуоресценции прямо пропорциональна поглощению света при условии, что локальное поглощение света веществом незначительно [30]. Таким образом, при слабом локальном поглощении испускаемый свет пропорционален концентрации флуоресцирующего вещества. При высоких уровнях поглощения два явления вызывают снижение флуоресценции. Первое — это появление эффекта внутреннего фильтра, которое обусловлено снижением энергии возбуждающего света в более удаленных от источника света слоях. Поскольку при высоких уровнях локального поглощения слои, расположенные ближе к источнику света, поглощают значительную долю возбуждающего света, то глубоко расположенные слои не могут быть адекватно освещены. Вторая причина состоит в том, что существует явление повторного поглощения, то есть испускаемая флуоресценция частично поглощается в препарате окружающими слоями [30, 31]. Последнее может происходить потому, что в большинстве случаев спектры поглощения и флуоресценции частично перекрываются. Все это приводит к снижению уровня флуоресценции. Чтобы избежать этого явления,, измерения флуоресценции надо проводить за пределами области перекрывания спектров при большей длине волны спектра испускания.
Во флуоресцентной микроскопии по интенсивности флуоресценции целого объекта можно оценить его размер. Поскольку суммарная флуоресценция является суммой локальных интенсивностей, то нет необходимости проводить сканирование, как это требуется при измерениях поглощения. Однако интенсивность измеряемой флуоресценции прямо зависит от интенсивности возбуждающего света, так что показания, считываемые с пустого пятна, которые будут соответствовать интенсивности нежелательного возбуждающего света, а также собственной флуоресценции препарата и частей оптики, не могут служить опорным сигналом. Таким образом, для того чтобы получать показания флуоресценции в разное время или с различных препаратов, следует поддерживать на постоянном уровне интенсивность возбуждающего света.
5.2. Стандарты флуоресценции
Примером стандарта является урановое стекло, обладающее сильной желто-зеленой флуоресценцией [32]. Процедура измерения состоит в следующем.
1.Включите поджиг лампы эпиосвещения (НВО 100) и ждите 20 мин, не начиная измерений.
2.Поместите кусок уранового стекла 25X50 мм и толщиной 2 мм (марки GG17 или 21, Schott, ФРГ) на столик микроскопа.
3.Погрузите масляно-иммерсионный объектив в каплю нефлуоресцирующего масла на стекле. Будьте внимательны и используйте для калибровки всегда один и тот же масляно-иммерсионный объектив. Фильтры и другие оптические детали также должны быть всегда одни и те же.
4.Используйте измерительную диафрагму диаметром 2 мм.
5.Используйте максимальные показания, когда объектив практически касается стекла.
6.Перед каждым измерением иммунофлуоресценции отрегулируйте источник питания по фотоумножителю так, чтобы все время получать с уранового стекла одни и те же показания.
Другими стандартами для измерений могут служить микрокапилляры и шарики определенного размера или объема с известной концентрацией флуорохрома [33, 34].
Кроме того, стандарты необходимы для контроля реакции флуоресцентного окрашивания. В качестве такого стандарта можно использовать препарат, окрашенный определенным образом и содержащий клетки с известным количеством окрашиваемого вещества. Примером является использование диплоидных клеток в качестве стандарта для измерения содержания ДНК.
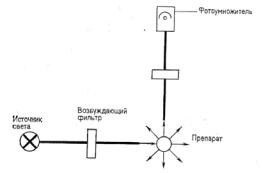
Рис. 6.6. Схема хода лучей при микрофлуориметрии.
5.3. Оборудование
Микрофлуориметр обычно состоит из флуоресцентного микроскопа и прикрепленного к нему
124
светочувствительного устройства — фотоумножителя (рис. 6.6). Приборы для микрофлуориметрии желательно иметь с двумя системами освещения: для проходящего и для падающего света. Падающий свет в основном используется для измерений интенсивности флуоресценции, так как функции освещения и наблюдения оказываются совмещенными в объективе. Когда достигнута точная фокусировка объектива, условия возбуждения при перемещении стекла на столике микроскопа будут воспроизводимыми. Как только фокус наведен на новый участок препарата, автоматически достигаются оптимальные условия для измерений. Установка для воспроизведения условий освещения и измерений нижнего конденсора вместе с объективом более сложна, чем установка одного объектива. Кроме того, нижнее освещение может быть использовано, что еще более важно, для поиска объектов, которые требуется измерять.
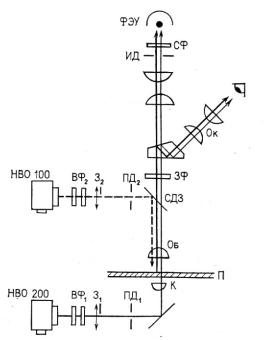
Рис. 6.7. Схема микроскопа, снабженного системой для наблюдения флуоресценции при освещении проходящим светом и системой для измерения флуоресценции при освещении падающим светом. ВФ — возбуждающие фильтры; 3 — затвор; ПД — полевая диафрагма; К — светлополышй конденсор; П — препарат; Об — объектив; СДЗ — дихроичное (светоделительное) зеркало; ЗФ — запирающий фильтр; Ок
— окуляр; ИД — измерительная диафрагма; СФ — селективный фильтр; ФЭУ — фотоэлектронный умножитель НВО 100 и НВО 200 — ртутные лампы мощностью 100 и 200 Вт.
Типичный микрофлуориметр схематично представлен на рис. 6.7. Идущее снизу низкоинтенсивное освещение от лампы накаливания или дуговой ртутной лампы, снабженной толстым возбуждающим фильтром, позволяет проводить поиск флуоресцирующих объектов, не вызывая их обесцвечивания. В условиях очень эффективного собирания света, которое достигается с помощью оптики с большой числовой апертурой и небольшим увеличением, интенсивность нижнего света может быть очень низкой. Это позволяет также полностью открыть полевую диафрагму для того, чтобы видеть все поле зрения и облегчить поиск клеток, которые необходимо измерять. Эпиосвещение для измерений дает ртутная лампа высокого давления НВО 100, работающая от хорошо стабилизированного источника постоянного тока. Для уменьшения количества нежелательного возбуждающего света требуется применять специальные возбуждающие и запирающие фильтры, а также СДЗ. Непосредственно перед ФЭУ устанавливается второй фильтр, который пропускает флуоресценцию только вне области перекрывания спектров возбуждения и испускания. Желателен объектив с умеренным увеличением и с большой числовой апертурой, собирающий много света. Полевую диафрагму эпиосвещения надо открывать лишь ненамного больше, чем измерительную диафрагму, чтобы предупредить нежелательное обесцвечивание препарата в остальной части поля зрения микроскопа сильным светом, используемым для измерений флуоресценции. Измерительную диафрагму с переменным диаметром можно настроить таким образом, чтобы она охватывала только интересующее вас изображение, что позволит избежать неточностей, вносимых фоновым светом. Например, в системах MPVII (Leitz) илиМРОЗ (Zeiss) измеряемое поле видно как освещенное пятно, накладывающееся на микроскопическое изображение. В автоматизированных измерительных микроскопах световой поток может быть переключен с помощью электронных затворов [35, 36]. Во время поиска нижний электронный затвор остается открытым. Процедура измерения начинается с нажатия кнопки, включающей электронную систему. Затвор на пути проходящего света теперь закрывается, и на короткое время (от 0,001 до 1 секунды) открывается затвор на пути падающего света. Присоединение микрофлуориметра к системам анализа и записи сигнала позволяет осуществлять автоматизированный вывод данных.
5.3.1. Инвертированные микрофлуориметры
У инвертированных микроскопов объектив располагается под столиком, что позволяет наблюдать клетки на дне ячеек непосредственно в панелях. Эти микроскопы могут также быть снабжены системами проходящего и падающего света. На приборах данного типа источники освещения падающим светом располагаются под
125
