

Глава16 Комбинированныеповрежденияприполитравме |
|
481 |
|
|
|
ститерморегуляцииорганизмапритяжелойтравмеишоке,ипроявляетсяпрогрессированием функциональных расстройств основных систем жизнеобеспечения. Первичная постагрессивная реакция на охлаждение реализуется компенсаторной тахикардией,тахипноэ,увеличениемдиуреза,однако,еслигипотермияпрогрессирует – развиваются признаки дезадаптации: брадикардия и гипотензия, угнетение сознания, дыхания и мочеотделения, двигательной активности. Таким образом, прогрессирующая гипотермия является патологическим состоянием, которое без адекватныхлечебныхмероприятийнередкообусловливаетгибельпострадавшего.
Клиническиепроявления.Традиционноразличаюттристепенитяжестиобщегоохлаждения(замерзания):
•Легкая степень – адинамическая – развивается при снижении кожной температуры до 32°С, а ректальной – до 35°-33°С. Пациенты в сознании, жалуются на боль в местах повреждений и отморожений, на ощущение замерзания; они адинамичны, вялы, сонливы, речь затруднена, кожа в виде«гусиной»,бледнаяс«мраморной»синюшностью,возможныозноб и мышечная дрожь. Параметры пульса, АД и дыхания в пределах нормальныхзначений.
•Средней тяжести – ступорозная – при снижении кожной температуры до 28°-26°С, ректальной – до 32°-30°С. Сознание сохранено, но угнетено вплоть до сопора, контакт формальный: выраженная сонливость, бессмысленный взгляд, отсутствие мимики, возникает состояние «обманчивого комфорта» и пострадавшие засыпают. Кожа холодная, бледная с «мраморным» окрашиванием, движения резко затруднены – оцепенение.Прогрессируютбрадикардия,гипотензия–науровне100-80 mmHg,дыхание редкоеиповерхностное.
•Тяжелая степень – судорожная – температура тела снижается до 26°С и ниже, ректальная – до 29°С и ниже. Сознание отсутствует. Кожа бледная, холодная. Конечности приведены к туловищу, попытки распрямить их встречают сопротивление, мышцы брюшной стенки напряжены. Характерны судороги, тризм с прикусыванием языка. Пульс редкий, определяется на сонных или бедренных артериях, выраженная гипотензия, дыхание редкое и поверхностное, зрачки сужены, слабо реагируют на свет. Высокийрискразвитияфибрилляциижелудочков.
Диагностика. Своевременная диагностика общего переохлаждения при тяжелой травме на ранних этапах возможна только при исходной настороженности и целенаправленном выявлении характерных признаков. Ключевым критерием констатации системной гипотермии является уровень ректальной температуры. Важным аспектом для объективизации всего диагностического поиска является раннеесогреваниепациента.
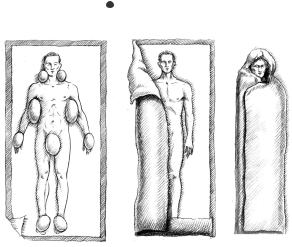
Неотложная помощь. Пациентам, доставленным в терминальном состоянии констатировать летальный исход без согревания недопустимо, т.к. с нормализациейтемпературыфункциижизнеобеспечения«умершего»пациентамогутполностью восстанавливаться.Проведение сердечно-легочнойреанимацииприкритическойги-

Глава16 Комбинированныеповрежденияприполитравме |
|
483 |
|
|
|
В программе хирургической коррекции отморожений традиционно используется выжидательная тактика до окончательного отграничения некротических тканей. Однако при политравмах часто необходима ранняя хирургическая обработка ран, некрэктомия или ампутация, что определяется у этой категории пациентов высоким риском развития фатальных гнойно-септических осложнений или раневогоистощения.
Нараннихэтапахлечения,дочеткогоотграничениянекротическихтканейвыполняют этапную хирургическую обработку с удалением эпидермальных пузырей
иместным лечением ран водорастворимыми многокомпонентными мазями. У пациентов с влажным струпом и при угрозе развития влажной гангрены используют влажно-высыхающие повязки с растворами антисептиков и физические методы подсушивания струпа (инфракрасное облучение, обдувание теплым воздухом). На ткани с мумифицированным струпом при нецелесообразности расширенных некрэкромийнакладываютсухуюстерильнуюповязку.
Радикальную некрэктомию у пациентов с политравмой при отморожениях ІІI- ІVстепенивыполняютна2-3неделелеченияпослеокончательногоформирования сухого некроза, выявления четкой демаркации и при незначительном реактивном воспалениивзонепоражений.Однакоунекоторыхбольныхужевраннемреактивномпериодепрогрессируютпризнакивлажнойгангрены,выраженный реактивный отек при отсутствии четкой демаркации, признаки гнилостной инфекции в пораженныхтканях.Нарастающаяинтоксикацияиугрозагенерализациихирургической инфекции определяют необходимость выполнения радикального хирургического вмешательствавболееранниесроки.
Таким образом, проблема хирургической коррекции глубоких и распространенныхотморожений аналогичнапозначимости исложноститаковойприглубоких
ираспространенныхожогах.
Влияние комбинированного термического поражения на динамику травма-
тической болезни при политравме. Наличие у пациентов с политравмой дополнительного поражающего термического фактора всегда определяет развитие ярко выраженного синдрома взаимного отягощения повреждений, который сохраняет свою значимость на протяжении всей динамики травматической болезни. Терми-


Глава |
раневая инфекция и Гнойно- |
|
17 |
септические осложнения |
|
при политравме |
||
|
Проблема гнойно-септических осложнений у пострадавших с политравмой становится актуальной с 5-7 суток после травмы – в конце острого периода травматической болезни, когда патогенетические факторы раневой инфекции приобретают абсолютную доминирующую роль и сохраняют ее в течение нескольких недель. Нормализация функций основных систем жизнеобеспечения в остром посттравматическом периоде достигается аутокатаболизмом структурных элементов и истощением адаптационно-компенсаторных механизмов. Реакция иммунореактивной системы на тяжелую механическую политравму проявляется начальными признаками гиперреактивности, с последующим стойким постагрессивным иммунодефицитом, в условиях которого развитие гнойной инфекции сопряжено с высокой вероятностью ее генерализации. Наиболее подвержены возникновению гнойных осложнений и сепсиса пациенты с обширным травматическим разрушением мышц, подкожной жировой клетчатки, повреждениям кишечника, поджелудочной железы, органов малого таза, минно-взрывных и огнестрельных ранениях (Рис. 17.1, см. цв. вкл.). У пострадавших с политравмой гнойно-инфекционные осложнения развиваются в 16-41% наблюдений, а генерализованная гнойная инфекция или сепсис – в 2,8-16,5% наблюдений. Гнойно-септические осложнения являются основной причиной смерти пострадавших в этом периоде травматической болезниидостигаютвструктурелетальностиприполитравме10%(7-25%).
Патогенез гнойно-септических осложнений. При тяжелом течении травмати-
ческой болезни антимикробная резистентность организма резко ослаблена. После перенесенных ранних функциональных расстройств на фоне истощения компенсаторных реакций резко повышается проницаемость естественных антимикробных барьеров,такихкаккожа,слизистыеоболочкикишечникаилегких.Упострадавших отмечается снижение показателей как клеточного, так и гуморального иммунитета: уменьшается содержание Т и В-лимфоцитов, иммуноглобулинов (Ig G, Ig M); нарастает концентрация циркулирующих иммунных комплексов. Увеличивается лейкоцитоз, снижаются защитные функции нейтрофилов, хемотаксис, фагоцитарнаяактивность,развиваетсядисфункциясистемымононуклеарныхфагоцитовиистощениесистемыкомплимента.
Все перечисленные изменения естественной антибактериальной резистентности соответствуют состоянию вторичного иммунодефицита и способствуют генерализации гнойной инфекции. При политравме меняется патогенез местной гнойной инфекции и условия в ране. В очагах травматической деструкции расстройства местногокровообращенияиишемиятканейрезкоснижает«критический»уровень бактериальной обсемененности, необходимый для развития гнойных осложнений: с 105 до 102 микробных тел в 1г ткани. При этом основными возбудителями


Глава17 Раневаяинфекцияигнойно-септическиеосложненияприполитравме 487
Раневаяинфекцияигнойно-септическиеосложненияприполитравме 487
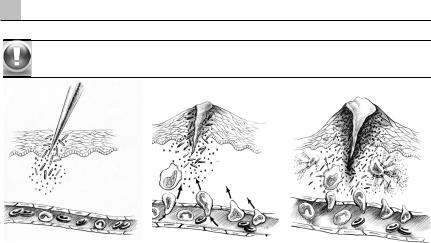
альтерация: в зоне активной воспалительной реакции оказываются и нежизнеспособныетканииткани,обсемененныемикроорганизмами.
Высвобождающиеся тканевой тромбопластин,гистамин,биогенные амины и целый каскадмедиатороввоспалениявызываютнарушениямикроциркуляции,повышаютпроницаемостьсосудовивыходвтканинейтрофилов,макрофаговилимфоцитов.Наличиебольшого количества некротизированных тканей сопровождается быстрым размножением, повышением вирулентнтности и патогенности микроорганизмов, так как значительная частьфагоцитов«отвлечена»наутилизациюсобственныхпогибшихтканей.Врезультате даже незначительная обсемененность тканей микроорганизмами создает преобладание количества последних над функционирующими фагоцитами. Неспособность местных иммунокомпетентных клеток подавить инфекцию определяют необходимость срочного привлечениякочагубактериальнойальтерациидополнительныхиммунных«резервов».
Активированные иммунокомпетентные клетки посредством выработки и экскреции сигнальных веществ – медиаторов, которые представлены кахектином (TNFα), интерлейкинами (ІL-1, -6), интерфероном (INFγ) и др. усиливают местную воспалительную реакцию. Во избежание гематогенного распространения и генерализации инфекции отток крови из зоны воспаления уменьшается периориентацией артерио-венозной пер- фузиитканейнаартерио-лимфатическую.Парезпрекапиллярныхиспазмпосткапилляр- ных сфинктеров ведет к переполнению кровью обменных капилляров, что проявляется местнойгиперемией.Резкоувеличиваетсяпроницаемостькапилляров,взонувоспаления устремляются с током жидкости иммуноглобулины, опсонины-маркеры фагоцитоза, активномигрируютмоноциты,нейтрофилы,лимфоцитыит.п.Результатомдеятельности макрофагов является не только очищение раны от тканевого детрита и микроорганизмов, но и регуляция воспалительной реакции медиаторами воспаления, которые определяют проницаемость стенки капилляров, интенсивность миграции форменных элементоввткани.Однакодоминируютсредимигрирующихиммунокомпетентныхкле- токименнонейтрофилы–своеобразная«группабыстрогореагирования».Врезультате развивается отек и лейкоцитарная инфильтрация поврежденных тканей. Макрофаги
инейтрофилы активно поглощают лизированные нейтрофилами нежизнеспособные ткани, микроорганизмы, продукты бактериального распада, включая и погибшие лейкоциты, очищают рану и при благоприятном течении воспалительная реакция стихает. Однакофагоцитарнаяактивностьмакрофаговинейтрофиловограниченакакразмером поглащаемых микроорганизмов и их фрагментов, так и их количеством. Если фагоцитарный потенциал уступает массиву подлежащих фагоцитозу объектов, нейтрофилы поражают их «объемным взрывом» – дегранулируют, выбрасывая в окружающее пространство активные радикалы кислорода и лизосомальные ферменты для повреждения
ивнеклеточного переваривания антигенного материала. Массовая дегрануляция и лизис нейтрофилов образует экссудат с высокой протеолитической активностью, который способен разрушать как микроорганизмы и некротические ткани, так и собственные жизнеспособные тканевые структуры. В результате такого поражения чужеродных и собственных тканей появляются полости, образованные на месте лизиса структурных элементов, в которые стекает экссудат с высокой протеолитическою активностью и тканевойдетрит–образовываетсягной.Сливающиесявцентреочагавоспаленияполо- сти формируют абсцесс (Рис. 17.2). Одновременно на внешних границах первичного очага иммунокомпетентные клетки, формируют лейкоцитарный вал – временный биологический барьер, который располагается на границе жизнеспособных и некротизированных тканей.

Глава17 Раневаяинфекцияигнойно-септическиеосложненияприполитравме 489
Раневаяинфекцияигнойно-септическиеосложненияприполитравме 489
Фазарегенерацииначинаетсясостиханиемместнойвоспалительнойреакции и очищением раны от некротизированных тканей. Ключевым морфологическим элементомэтойфазыявляетсяразвитиегрануляционнойткани,котораяпостепен- нозаполняетполостьраны–раневойдефект.
Формирование грануляционной ткани осуществляется фибробластами и эндотелием капилляров. Фибробласты мигрируют к краям раны и продуцируют соединительнотканные волокна. Из эндотелия формируются новые капилляры, врастающие в края раны. Грануляции имеют вид блестящих розовых или малиново-красных мелкозернистых образований, при повреждении легко кровоточат. Разрастание соединительнотканных волокон (колагена) делает края раны более плотными. При осложненном (инфекция) течении раневого процесса грануляции вялые, багрово-синюшные, крупнозернистые, склонныкгипертрофии,задерживаютэпителизациюкраевраны.
Продолжительность регенерации определяется несколькими факторами: объемом раневого дефекта, требующего заполнения грануляциями; активностью раневой инфекции, эффективностью тканевых репаративных процессов и может длиться от нескольких дней до нескольких недель и даже месяцев (синдром замершей раны). При политравме истощение адаптационно-компенсаторных механизмов в остром периоде травматической болезни приводит к значительному затягиванию процессов регенерации, а при обширных раневых дефектах и развитии раневой инфекции даже к раневому истощению. Поэтому наложение швов или пластическое закрытие ран в фазу регенерации способно значительно сократить раневыепотерииускоритьпроцессзаживления.
Фаза реорганизации рубца и эпителизации характеризуется активной эпите-
лизациейкраевраныиконцентрическимсокращениемкраевистенокраны.Доказано,чтоширинакраевого«наползающего»эпителиальногоободканеможетпревышать 6-15 мм, поэтому обширные раневые дефекты требуют своевременного пластическогозакрытияран.
Раневой процесс заканчивается заживлением раны. Традиционно различают заживлениепервичным,вторичнымнатяжениемиподструпом.
Заживление первичным натяжением происходит при отсутствии видимого отстояния краев раны друг от друга, как правило, при линейных ранах. При этом края раны и/или раневой канал слипаются и прорастают соединительной тканью с последующим формированием небольшого, часто малозаметного рубца. Заживление раны первичным натяжением возможно при небольших линейных раневых дефектах, отсутствии зияния раны и плотном соприкосновении краев, отсутствии очагов размозжения и некроза тканей, гематом, и, конечно, при малой микробной обсемененности раны (менее 105 микробных тел в 1 г ткани), исключающем развитие раневой инфекции. Адекватные условия для заживления ран первичным натяжением создаются при закрытии ран швами после ранней первичной хирурги- ческойобработки(ПХО),впервые6-8часовпослеранения.
Вторичным натяжением заживают зияющие раны, которые имеют значительныйдефекттканей,астенкиикраяраныотстоятдруготдруганаболееилименее значительном расстоянии, при наличии обширных очагов некротизированных


 Хирургияповрежденийприполитравмемирногоивоенноговремени
Хирургияповрежденийприполитравмемирногоивоенноговремени Хирургияповрежденийприполитравмемирногоивоенноговремени
Хирургияповрежденийприполитравмемирногоивоенноговремени Хирургияповрежденийприполитравмемирногоивоенноговремени
Хирургияповрежденийприполитравмемирногоивоенноговремени Хирургияповрежденийприполитравмемирногоивоенноговремени
Хирургияповрежденийприполитравмемирногоивоенноговремени Хирургияповрежденийприполитравмемирногоивоенноговремени
Хирургияповрежденийприполитравмемирногоивоенноговремени