
11
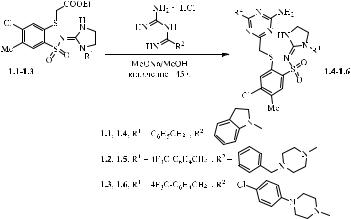
Так, в работе [6] при взаимодействии сложных эфиров (1.1–1.3) с
соответствующими гидрохлоридами бигуанидов в растворе метилата натрия в метаноле (MeONa/MeOH) при кипячении с обратным холодильником в течение 45 ч
был получен ряд 2-[(4-амино-6-R2-1,3,5-триазин-2-ил)метилтио]-N-(1-R1-
имидазолидин-2-илиден)-4-хлор-5-метилбензолсульфонамидов (1.4–1.6; Схема 1.1).
Схема 1.1
Влияние соединений 1.4–1.6 на жизнеспособность трёх линий опухолевых клеток HCT-116 (карцинома кишечника человека), MCF-7 (аденокарцинома протоков молочной железы человека) и HeLa (аденокарцинома шейки матки человека), а также клеток неопухолевого происхождения — НаСаТ (кератиноциты)
проводилось с использованием МТТ-теста. Авторы [6] определяли IC50 после 72 ч
инкубации клеток; в качестве препарата сравнения использовался цисплатин.
Результаты МТТ: соединение 1.4 (R1 = бензил, R2 = индолин) — IC50 = 6 мкМ для
HCT-116, IC50 = 7 мкМ для MCF-7; соединение 1.5 (R1 = 4-трифлорометилбензил, R2
= 4-бензилпиперазин) — IC50 = 5 мкМ для HCT-116, IC50 = 8 мкМ для HeLa;
соединение 1.6 (R1 = 4-трифторметилбензил, R2 = хлор) — IC50 = 5 мкМ для HCT116, IC50 = 6 мкМ для MCF-7. Значения IC50 соединений 1.4–1.6 по отношению к клеточной линии НаСаТ составило 33, 22 и 21 мкМ, соответственно.
В другой работе конденсацией между бигуанидом и различными сложными эфирами были синтезированы 1,3,5-триазиновые производные метформина (1.7–1.9) [7]. Авторы проводили синтез без выделения и очистки промежуточных продуктов,

12
используя гидрохлорид бигуанида, метоксид натрия (NaOMe) в метаноле (Схема
1.2).
Схема 1.2
Далее оценивалась цитотоксическая активность соединений 1.7–1.9 in vitro по отношению к двум клеточным линиям карциномы кишечника человека (HCT-116 и
SW620). Все синтезированные производные 1,3,5-триазина проявляли сопоставимую или более высокую цитотоксичность, по сравнению с цисплатином.
Соединение 1.7 проявило цитотоксичность с IC50 = 59,1 ± 1,5 мкМ для клеточной линии SW620 и 59,4 ± 1,7 мкМ для клеточной линии HCT-116. Напротив,
цитостатический эффект соединений 1.8 и 1.9 был очень низким и составлял не более 5–20 %. Далее в работе [7] синтезировали наноформу соединения 1.7,
инкапсулированного в наночастицы цитрата кальция (1.7а) (Схема 1.3).
Схема 1.3
Авторами был предложен метод синтеза с использованием бинарного растворителя EtOH-вода. Добавление 1,3,5-триазина 1.7 к водно-этанольному раствору хлорида кальция и цитрата натрия на воздухе при энергичном перемешивании при комнатной температуре приводило к образованию наночастиц
1.7а [6].
При разработке наноматериалов, используемых для адресной доставки лекарств важно изучать контролируемое высвобождение лекарственного средства при физиологических условиях. Как анаэробный, так и аэробный гликолиз приводят к накоплению Н+ во внеклеточном пространстве опухолей, вызывая выраженное закисление межклеточной жидкости в области микроокружения опухоли [8],
поэтому высвобождение вещества 1.7 изучали в кислой среде при pH 5,0 и 3,0 и в

13
нейтральной среде (pH 7,4) для сравнения. Исследование in vitro показало, что наночастицы 1.7а реагируют на изменение pH среды с контролируемым высвобождением триазина 1.7. Через 24 ч высвобождалось 80,0 %, 48,8 % и 30,0 %
соединения 1.7 при pH 3,0, pH 5,0 и pH 7,4, соответственно.
Другим успешным примером синтеза биологически активных 1,3,5-триазинов из производных бигуанида является исследование, проведённое Котайер и соавт. [9].
Синтез производных 4-амино-6-(ариламино)-1,3,5-триазина-2-карбогидразида проводили в две стадии из солей гидрохлорида арилбигуанида. На первой стадии проводилась нейтрализация соли 1.8 с использованием метоксида натрия в метаноле с последующей её реакцией с диметилоксалатом в кипящем метаноле. Это приводило к образованию промежуточных метил-4-амино-6-(ариламино)-1,3,5-
триазин-2-карбоксилатов (1.9–1.11) с выходом в 83–92 % после перекристаллизации из метанола. Реакция промежуточных соединений (1.9–1.11) с гидразингидратом в кипящем этаноле приводила к получению целевых 2,4,6-тризамещённых-1,3,5-
триазинов (1.12–1.14) (Схема 1.4).
Схема 1.4
Изучение цитотоксичности синтезированных 4-амино-6-(ариламино)-1,3,5-
триазин-2-карбогидразидов (1.12–1.14) в диапазоне концентраций 0–125 мкМ проводили на семи опухолевых клеточных линиях человека: аденокарциномы яичников (OV90), карциномы яичников (A2780), аденокарциномы лёгкого (A549),
карциномы лёгкого (H1299), аденокарциномы молочной железы (MCF-7 и MDA- MB-231) и аденокарциномы толстой кишки (HT29). Обобщённые данные со значениями IC50 представлены в Табл. 1.1. Анализ данных по цитотоксичности соединений 1.12–1.14 показывает, что их активность сопоставима c цитотоксической активностью соединения 1.15, являющегося ингибитором убиквитин-
конъюгирующего фермента Е2В (Rad6B; Рис. 1.2). Rad6B активирует белок

14
клеточной адгезии β-катенин, который отвечает за злокачественную прогрессию
клеток рака молочной железы.
Табл. 1.1. Значения IC50 (мкМ) замещённых производных 4-амино-6-(ариламино)- 1,3,5-триазин-2-карбогидразида.
Номер |
OV90 |
A2780 |
MCF-7 MDA- |
A549 |
H1299 |
HT-29 |
|
соединения |
|
|
|
MB231 |
|
|
|
|
|
|
|
|
|
|
|
1.12 |
75,0 |
7,3 |
5,9 |
2,6 |
7,8 |
65,0 |
3,3 |
1.13 |
80,0 |
14,7 |
6,2 |
7,6 |
5,2 |
65,0 |
5,4 |
1.14 |
85,0 |
36,6 |
8,8 |
24,6 |
7,5 |
30,0 |
4,6 |
1.15 |
60,0 |
7,8 |
5,0 |
4,6 |
7,2 |
45,0 |
8,3 |
|
|
|
|
|
|
|
|
Рис. 1.2. Химическая структура ингибитора убиквитин-конъюгирующего фермента Е2В (Rad6B).
Интересные данные по цитотоксической активности триазинового цикла описываются в работе [10], где были представлены методы получения производных
2-(4-амино-6-(4-(2-хлорфенил)пиперазин-1-ил)-1,3,5-триазин-2-ил)ацетонитрила
1.16 как прекурсора в синтезе амино-4-{[4-(2-R'-фенил)пиперазино]-1,3,5-триазин- 6-ил}ацетонитрила 1.17. Целевые соединения получали взаимодействием N-
карбамимидоил-4-(2-хлорфенил)пиперазин-1-карбоксимидамида и этилцианоацетата в метанольном растворе при комнатной температуре.
Промежуточный 2-амино-4-(4-арилпиперазино)-1,3,5-триазин 1.16,
связанный непосредственно с циановиниловым фармакофором, использовался для последующей реакции с 5-нитро-2-фуральдегидом в реакции конденсации Кневенагеля, катализируемой триэтиламином, с получением (E)-2-(4-амино-6-(4-
фенилпиперазин-1-ил)-1,3,5-триазин-2-ил)-3-(5-нитрофуран-2-ил)акрилонитрила
1.17 с выходом 57 % (Схема 1.5).

15
Схема 1.5
Скрининг цитотоксической активности проводился на 10 опухолевых клеточных линиях человека: цервикальной аденокарциноме шейки матки (SISO),
плоскоклеточной карциноме пищевода (KYSE-520, KYSE-70, KYSE-510),
крупноклеточной карциноме лёгкого (LCLC-103H), карциноме мочевого пузыря
(RT-4), карциноме мочевыводящих путей (RT-112 и RT-5637), карциноме поджелудочной железы (YAPC и DAN-G). Среди производных триазина наибольшая цитотоксическая активность была обнаружена для соединения 1.17,
которое в арильном кольце содержит хлор (IC50 1,66 мкМ для RT-4, 1,05 мкМ для
RT-112, 0,92 мкМ для RT-5637, 0,92 мкМ для KYSE-70, 0,45 мкМ для KYSE-510, 0,95 мкМ для KYSE-520, 0,72 мкМ для YAPC, 0,86 мкМ для DAN-G, 0,90 мкМ для
SISO и 0,89 мкМ для LCLC-103H), что свидетельствует о перспективности введения галогеновых заместителей в структуру 1,3,5-триазинов.
Джунаид и соавт. использовали микроволновый синтез для получения 6,N2-
диарил-1,3,5-триазин-2,4-диаминов (Схема 1.6) [11].

16
Схема 1.6
Реакция между цианогуанидином, ароматическими альдегидами и ариламинами в присутствии соляной кислоты под действием микроволнового облучения приводила к образованию продуктов перегруппировки Димрота, которые в свою очередь претерпевают спонтанное дегидрирование и ароматизацию с получением 6, N2-диарил-1,3,5-триазин-2,4-диаминов (1.18 и 1.19) (Схема 1.6).
Полученные соединения были исследованы на антипролиферативную активность в отношении клеточной линии карциномы простаты человека DU145 (C
= 10 мкМ). Было показано, что соединения 1.18 и 1.19 ингибировали пролиферацию клеток более, чем на 45 %.
1.2.Реакции нуклеофильного замещения атомов хлора в производных
2,4,6-трихлор-1,3,5-триазина
Рассмотрен метод, который заключается в последовательном нуклеофильном замещении атомов хлора в присутствии основания (Схема 1.7). Исходным соединением является 2,4,6-трихлор-1,3,5-триазин (цианурхлорид, ТХТ).
Схема 1.7
Несмотря на широкое распространение представленного метода синтеза, в
нем имеются существенные недостатки, в основном связанные с жёсткими условиями нуклеофильного замещения третьего атома хлора и низкими выходами тризамещённого продукта [12,13].

17
1.2.1. Реакции 2,4,6-трихлор-1,3,5-триазина с аминами различной природы
Первым продуктом замещения атомов хлора в ТХТ был N2,N2,N4,N4,N6,N6-
гексаметил-1,3,5-триазин-2,4,6-триамин (альтретамин), который был одобрен FDA
под торговой маркой Hexalen® для лечения рака яичников [14,15]. Синтез целевого тризамещённого ТХТ проводили диметиламинированием ТХТ водным раствором
40 %-ного диметиламина и гидроксида калия в 1,4-диоксане в одну стадию с получением альтретамина (1.20) с высоким выходом (Схема 1.8) [16,17].
Схема 1.8
В организме животных и человека альтретамин подвергается окислительному
N-деметилированию с образованием гидроксиметильных производных. Показано,
что именно гидроксиметилмеламины ответственны за цитотоксическую и противоопухолевую активность альтретамина [18]. Альтретамин действует как алкилирующий агент, однако детальный механизм его противоопухолевого действия неизвестен. Альтретамин предположительно повреждает опухолевые клетки за счёт образования формальдегида, как продукта N-деметилирования при участии цитохрома P450. При пероральном приёме альтретамин метаболизируется в печени, образуя в основном моно- и дидеметилированные метаболиты. В
опухолевых клетках происходят последовательные реакции деметилирования и высвобождения формальдегида in situ. Показано, что альтретамин способен ковалентно взаимодействовать с остатками гуанина и цитозина, входящими в состав ДНК [19]. Альтретамин после перорального приёма хорошо всасывается и подвергается быстрому деметилированию в печени, вызывая значительное снижение концентрации действующего вещества в плазме. В последующих исследованиях у пациентов с рецидивирующим раком яичников после монотерапии препаратом Hexalen® в течение 14, 21 или 28-дневного цикла было достигнуто 6
полных клинических ответов и 2 частичных ответа при общей частоте ответов 18 %,
с продолжительностью от 2 до 36 месяцев. У некоторых пациентов регрессия опухоли сопровождалась улучшением общего состояния [20].

18
Авторами работы [21] был успешно проведён синтез производных тиомочевины, например, соединение 1.22 (без выделения промежуточных продуктов) с выходами до 71 %. Реакцию ТХТ с двумя эквивалентами замещённых аминов проводили при добавлении NaOH, предотвращая подкисление реакционной смеси с получением дизамещённого продукта 6-хлор-N2,N4-дифенил-1,3,5-триазин- 2,4-диамина 1.21 (Схема 1.9).
Схема 1.9
На следующей стадии авторы осуществили синтез целевых гибридных соединений на основе реакции между соединением 1.22, ацетофеноном и этил-3-
оксобутаноатом с использованием Bi(NO3)3 (Схема 1.10).
Схема 1.10
Цитотоксическая активность этил 1-(4,6-бис(фениламино)-1,3,5-триазин-2-
ил)-6-метил-4-фенил-2-тиоксо-1,2,3,4-тетрагидропиримидин-5-карбоксилата 1.23
оценивалась в экспериментах in vitro в отношении клеточных линий: HeLa, MCF-7, HL-60 (клетки промиелоцитарного лейкоза человека), HepG2 (клеточная линия гепатоцеллюлярной карциномы человека) и MCF-12A (эпителиальная клеточная линия, полученная из протоков молочной железы человека) методом МТТ.
Цисплатин, использовался в качестве препарата сравнения. Результаты показали,
что соединение 1.23 проявляет умеренную активность в отношении клеточных линий HeLa (IC50 = 96,6 ± 0,5 мкМ), MCF-7 (IC50 = 87,4 ± 0,8 мкМ), HL-60 (IC50 = 83,7
± 0,3 мкМ), однако не проявляет активности в отношении клеточной линии MCF-

19
12A, что говорит о селективности цитотоксического действия полученного производного 1,3,5-триазина.
Продолжая рассматривать варианты синтеза биологически активных 1,3,5-
триазинов, хотелось бы выделить исследование по синтезу 2,4-диамино-6-арил- 1,3,5-триазинов, которые были получены с использованием твердофазного синтеза
[22]. Различная реакционная способность аминирования моноарилзамещённых триазинов приводит к тому, что амин, связанный со смолой, селективно замещает хлор в неочищенной реакционной смеси с получением триазина 1.24. Затем третий атом хлора замещается амином в среде ДМФА при высокой температуре (Схема
1.11). Отщепление смолы проводилось обработкой 50 % трифторуксусной кислотой в дихлорметане. Таким образом, были получены 2,4-диамино-6-арил-1,3,5-триазины
1.25–1.27.
Схема 1.11
Большинство полученных соединений продемонстрировали антипролиферативную активность в отношении клеточных линий миелогенного лейкоза (K562), аденокарциномы предстательной железы человека (PC-3 и HO8910).
В частности, соединение 1.26 проявляло заметную ингибирующую активность со

20
значениями IC50 1,01, 2,23 и 1,06 мкМ в отношении клеточных линий K562, PC-3 и HO8910, соответственно.
Успешным оказалось проведение синтеза β-лактамов, к которым присоединён диморфолинотриазиновый фрагмент [23]. Исходное соединение 4,4'-(6-хлор-1,3,5-
триазин-2,4-диил)диморфолин (1.28) было синтезировано из ТХТ в ацетоне и обработано смесью триэтиламина и морфолина при −10◦C с получением аддукта
1.28. Последующая реакция 1.28 с 4-нитроанилином в присутствии карбоната калия и ДМФА приводила к образованию тризамещённого триазина 1.29, в котором нитрогруппа подвергалась восстановлению с образованием соединения 1.30 (4,6-
диморфолино-N-(4-нитрофенил)-1,3,5-триазин-2-амин; Схема 1.12).
Схема 1.12
Затем полученные из 1.30 основания Шиффа 1.31 вступали в реакцию с замещёнными уксусными кислотами в присутствии триэтиламина и тозилхлорида в различных молярных соотношениях с получением цис-β-лактамов 1.32–1.33 с
выходами 75–90 % (Схема 1.13).
Схема 1.13
Влияние полученных β-лактам-триазинов на клеточные линии HEK293, SW-
1116, HepG2 и MCF-7 оценивалось с использованием МТТ теста [23].
Примечательно, что ни для одного из описанных соединений не наблюдалось ингибирующей активности по отношению к клеткам неопухолевого происхождения
