

11
желчные камни только в 30% имеющихся случаев.
Лечение
1.Хенодезоксихолевая кислота в дозе 1 г/сут. Вызывает снижение осаждения ХС
ирастворение ХС камней. Камни размером с горошину без билирубиновых наслое-
ний растворяются в течение полугода.
2.Ингибирование ГМГ-S-КоА-редуктазы (ловастатин) – снижает в 2 раза синтез
ХС.
3.Адсорбция ХС в желудочно-кишечном тракте (холестираминовые смолы,
Questran) и предотвращение его всасывания.
4.Подавление функции энтероцитов (неомицин) – снижение всасывания жиров.
5.Хирургическое удаление подвздошной кишки и прекращение реабсорбции
желчных кислот.
Всасывание липидов.
Происходит в верхнем отделе тонкого кишечника в первые 100 см.
1.Короткие жирные кислоты всасываются без каких либо дополнительных механизмов, напрямую.
2.Другие компоненты образуют мицеллы с гидрофильным и гидрофобным
слоями. Размеры мицелл в 100 раз меньше самых мелких эмульгированных жировых капелек. Через водную фазу мицеллы мигрируют к щеточной каемке слизистой
оболочки.
Относительно самого механизма всасывания липидов нет устоявшегося представления. Первая точка зрения заключается в том, что мицеллы проникают внутрь
клетки целиком путем диффузии без затраты энергии. В клетках происходит распад
мицелл и выход желчных кислот в кровь, ЖК и МАГ остаются и образуют ТАГ. По другой точке зрения, поглощение мицелл идет пиноцитозом.
И, наконец, в-третьих, возможно проникновение в клетку только липидных ком-
понентов, а желчные кислоты всасываются в подвздошной кишке. В норме всасывается 98% пищевых липидов.
Нарушения переваривания и всасывания могут возникать
•при болезнях печени и желчного пузыря, поджелудочной железы, стенки кишечника,
•повреждении энтероцитов антибиотиками (неомицин, хлортетрациклин);
•избытке кальция и магния в воде и пище, которые образуют соли желчных кислот, препятствуя их функции.
Ресинтез липидов
Это синтез липидов в стенке кишечника из посту-
пающих сюда экзогенных жиров, частично могут использоваться и эндогенные жирные кислоты.
При синтезе триацилглицеролов поступившая
жирная кислота активируется через присоединение ко-

12
энзима А. Образовавшийся ацил-S-КоА участвует в реакциях синтеза триацилглице-
ридов по двум возможным путям.
Первый путь – 2-моноацилглицеридный, происходит при участии экзогенных 2- МАГ и ЖК в гладком эндоплазматическом ретикулуме: мультиферментный комплекс
триглицерид-синтазы формирует ТАГ
При отсутствии 2-МАГ и высоком содержании ЖК активируется второй путь,
глицеролфосфатный механизм в шероховатом эндоплазматическом ретикулуме. Источником глицерол-3-фосфата служит окисление глюкозы, так как пищевой глице-
рол быстро покидает энтероциты и уходит в кровь.
Холестерол этерифицируется с использованием ацилS-КоА и фермента АХАТ. Реэтерификация холестерола напрямую влияет на его всасывание в кровь. В настоящее время ищутся возможности подавления этой реакции для снижения концентрации ХС в крови.
Фосфолипиды ресинтезируются двумя путями – с использованием 1,2-МАГ для синтеза фосфатидилхолина или фосфатидилэтаноламина, либо через фосфатидную кислоту при синтезе фосфатидилинозитола.
Транспорт липидов
Липиды транспортируются в водной фазе крови в составе особых частиц – липопротеинов. Поверхность частиц гидрофильна и сформирована белками, фосфолипидами и свободным холестеролом. Триацилглицеролы и эфиры холестерола составляют гидрофобное ядро.
Белки в липопротеинах обычно называются апобелками, выделяют несколько их типов – А, В, С, D, Е. В каждом классе липопротеинов находятся соответствующие ему апобелки, выполняющие структурную, ферментативную и кофакторную функции.
Липопротеины различаются по соотноше-
нию триацилглицеролов, холестерола и его
эфиров, фосфолипидов и как класс сложных белков состоят из четырех классов.
•хиломикроны (ХМ);
•липопротеины очень низкой плотности (ЛПОНП, пре-β-липопротеины, пре-β-ЛП);
•липопротеины низкой плотности (ЛПНП, β-липопротеины, β-ЛП);
•липопротеины высокой плотности (ЛПВП, α-липопротеины, α-ЛП).
Транспорт триацилглицеролов
Транспорт ТАГ от кишечника к тканям осуществляется в виде хиломикронов, от печени к тканям – в виде липопротеинов очень низкой плотности.

13
Хиломикроны
Общая характеристика
•формируются в кишечнике из ресинтезированных жиров,
•в их составе 2% белка, 87% ТАГ, 2% ХС, 5% эфиров ХС, 4% фосфолипидов. Ос-
новным апобелком является апоВ-48.
•в норме натощак не обнаруживаются, в крови появляются после приема пищи,
поступая из лимфы через грудной лимфатический проток, и полностью исчеза-
ют через 10-12 часов.
•не атерогенны
Функция
Транспорт экзогенных ТАГ из кишечника в ткани, запасающие и исполь-
зующие жиры, в основном жировую
ткань, легкие, печень, миокард, лактирующую молочную железу, костный
мозг, почки, селезенку, макрофаги
Утилизация
На эндотелии капилляров вышепе-
речисленных тканей находится фер-
мент липопротеинлипаза, прикреп-
ленная к мембране гликозаминогликанами. Она гидролизует ТАГ, находящиеся в составе хиломикронов до свободных
жирных кислот и глицерина. Жирные кислоты перемещаются в клетки, либо остаются в плазме крови и в комплексе с альбумином разносятся с кровью в другие ткани. Липопротеинлипаза способна удалить до 90% всех ТАГ, находящихся в хиломикроне или ЛПОНП. После окончания ее работы остаточные хиломикроны попадают в
14
печень и разрушаются.
Липопротеины очень низкой плотности
Общая характеристика
•синтезируются в печени из эндогенных и экзогенных липидов
•8% белка, 60% ТАГ, 6% ХС, 12% эфиров ХС, 14% фосфолипидов Основным белком является апоВ-100.
•в норме концентрация 1,3-2,0 г/л
•слабо атерогенны
Функция
Транспорт эндогенных и экзогенных ТАГ от печени в ткани, запасающие и ис-
пользующие жиры.
Утилизация
Аналогично ситуации с хиломикронами, в тканях они подвергаются воздействию
липопротеинлипазы, после чего остаточные ЛПОНП либо эвакуируются в печень, либо превращаются в еще одну разновидность липопротеинов – липопротеины низ-
кой плотности (ЛПНП).

15
МОБИЛИЗАЦИЯ ЖИРОВ
В состоянии покоя печень, сердце, скелетные мышцы и другие ткани (кроме
эритроцитов и нервной ткани) более 50% энергии получают из окисления жирных кислот, поступающих из жировой ткани благодаря фоновому липолизу ТАГ.
Гормонзависимая активация липолиза
При напряжении организма (голодание, длительная мышечная работа, охлаж-
дение) происходит гормон-зависимая активация ТАГ-липазы адипоцитов. Кроме
ТАГ-липазы, в адипоцитах имеются еще ДАГ- и МАГ-липазы, активность которых высока и постоянна, однако в покое она не проявляется из-за отсутствия субстратов.

16
В результате липолиза образуются свободный глицерол и жирные кислоты. Глицерол с кровью доставляется в печень и почки, эдесь фосфорилируется и превращается в метаболит гликолиза глицеральдегидфосфат. В зависимости от ус-
ловий ГАФ может включаться в реакции глюконеогенеза (при голодании, мышечной нагрузке) или окисляться до пировиноградной кислоты.
Жирные кислоты транспортируются в комплексе с альбуминами плазмы крови
•при физической нагрузке – в мышцы
•при голодании – в большинство тканей и около 30% захватываются печенью.
При голодании и физической нагрузке после проникновения в клетки жирные ки-
слоты вступают на путь β-окисления.

17
β- окисление жирных кислот
Реакции β-окисления происходят
вмитохондриях большинства клеток организма. Для окисления использу-
ются жирные кислоты, поступающие
вцитозоль из крови или при внутриклеточном липолизе ТАГ.
Прежде, чем проникнуть в мат-
рикс митохондрий и окислиться, жирная кислота должна активировать-
ся. Это осуществляется присоедине-
нием коэнзима А.
Ацил-S-КоА является высокоэнер-
гетическим соединением. Необрати-
мость реакции достигается гидролизом дифосфата на две молекулы
фосфорной кислоты пирофосфори-
лазой.
Ацил-S-КоА-синтетазы находятся
в эндоплазматическом ретикулу-
ме, на наружной мембране митохондрий и внутри них. Существует ряд синтетаз, специфичных к разным жирным кислотам.
Ацил-S-КоА не способен прохо-
дить через митохондриальную мем-
брану, поэтому существует способ его переноса в комплексе с витами-
ноподобным веществом карнити-
ном. На наружной мембране митохондрий имеется фермент карнитин-
ацил-трансфераза I.
После связывания с карнитином жирная кислота переносится через
мембрану транслоказой. Здесь, на внутренней стороне мембраны, фер-
мент карнитин-ацил-трансфераза II
вновь образует ацил-S-КоА который
вступает на путь β-окисления.
Процесс β-окисления состоит из 4-х реакций, повторяющихся цикли-
чески. В них последовательно проис-
ходит окисление 3-го атома углерода (β-положение) и в результате от жир-
ной кислоты отщепляется ацетил-S- КоА. Оставшаяся укороченная жирная кислота возвращается к первой
реакции и все повторяется снова, до
тех пор, пока в последнем цикле образуются два ацетил-S-КоА.
18
Окисление ненасыщенных жирных кислот
При окислении ненасыщенных жирных кислот возникает потребность клетки в
дополнительных ферментах изомеразах. Эти изомеразы перемещают двойные связи в жирнокислотных остатках из γ- в β-положение, переводят природные двойные
связи из цис- в транс-положение.
Таким образом, уже имеющаяся двойная связь готовится к β-окислению и пропускается первая реакция цикла, в которой участвует ФАД.
Окисление жирных кислот с нечетным числом углеродных атомов
Жирные кислоты с нечетным числом углеродов поступают в организм с расти-
тельной пищей и морепродуктами. Их окисление происходит по обычному пути до
последней реакции, в которой образуется пропионил-S-КоА. Суть превращений пропионил-S-КоА сводится к его карбоксилированию, изомеризации и образованию
сукцинил-S-КоА. В этих реакциях участвуют биотин и витамин В12.
Энергетический баланс β-окисления.
При расчете количества АТФ, образуемого при β-окислении жирных кислот необ-
ходимо учитывать
•число циклов β-окисления. Число циклов β-окисления легко представить исходя из представления о жирной кислоте как о цепочке двухуглеродных звеньев. Число разрывов между звеньями соответствует числу циклов β-окисления. Эту же величину можно подсчитать по формуле n/2 -1, где n – число атомов углерода в кислоте.
•количество образуемого ацетил-S-КоА – определяется обычным делением числа атомов углерода в кислоте на 2.
•наличие двойных связей в жирной кислоте. В первой реакции β-окисления происходит образование двойной связи при участии ФАД. Если двойная связь в жирной кислоте уже имеется, то необходимость в этой реакции отпадает и ФАДН2 не образуется. Остальные реакции цикла идут без изменений.
•количество энергии, потраченной на активацию
Пример 1. Окисление пальмитиновой кислоты (С16).
Для пальмитиновой кислоты число циклов β-окисления равно 7. В каждом цикле образуется 1 молекула ФАДН2 и 1 молекула НАДН. Поступая в дыхательную цепь, они "дадут" 5 молекул АТФ. В 7 циклах образуется 35 молекул АТФ.
Так как имеется 16 атомов углерода, то при β-окислении образуется 8 молекул ацетил-S-КоА. Последний поступает в ЦТК, при его окислении в одном обороте цик-
ла образуется 3 молекулы НАДН, 1 молекула ФАДН2 и 1 молекула ГТФ, что эквива-
лентно 12 молекулам АТФ. Всего 8 молекул ацетил-S-КоА обеспечат образование 96 молекул АТФ.
Двойных связей в пальмитиновой кислоте нет.
На активацию жирной кислоты идет 1 молекула АТФ, которая, однако, гидролизуется до АМФ, то есть тратятся 2 макроэргические связи.
Таким образом, суммируя, получаем 96+35-2=129 молекул АТФ.
Пример 2. Окисление линолевой кислоты.
Количество молекул ацетил-S-КоА равно 9. Значит 9×12=108 молекул АТФ.
Число циклов β-окисления равно 8. При расчете получаем 8×5=40 молекул АТФ.
В кислоте имеются 2 двойные связи. Следовательно в двух циклах β-окисления
не образуется 2 молекулы ФАДН2, что равноценно 4 молекулам АТФ. На активацию жирной кислоты тратятся 2 макроэргические связи.
Таким образом, энергетический выход 108+40-4-2=142 молекулы АТФ.
19
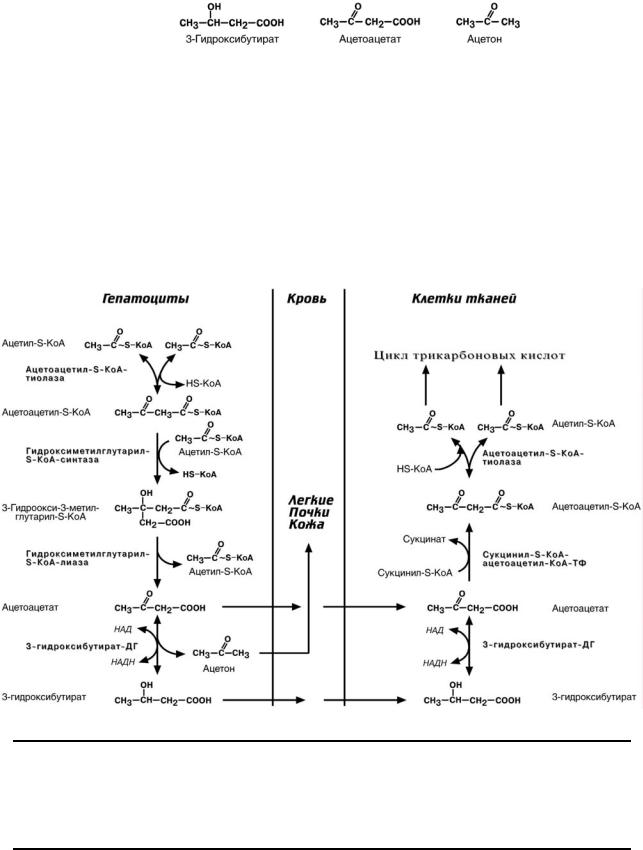
Кетоновые тела
К кетоновым телам относят три соединения близкой структуры.
Синтез кетоновых тел происходит только в печени, клетки всех остальных тканей
(кроме эритроцитов) являются их потребителями.
Стимулом для образования кетоновых тел служит поступление большого коли-
чества жирных кислот в печень. Как уже указывалось, при состояниях, активирующих
липолиз в жировой ткани, около 30% образованных жирных кислот задерживаются печенью. К этим состояниям относится голодание, сахарный диабет I типа, длитель-
ные физические нагрузки, богатая жирами диета. Также кетогенез усиливается при
катаболизме аминокислот, относящихся к кетогенным (лейцин, лизин) и к смешанным (фенилаланин, изолейцин, тирозин, триптофан и т.д.).
Нормальные показатели |
|
|
Кровь |
0,1-0,6 ммоль/л |
менее 0,01 г/л |
Моча |
менее 5 ммоль/л |
0,02-0,05 мг/сут |
При голодании синтез кетоновых тел ускоряется в 60 раз (до 0,6 г/л), при сахарном диабете I типа – в 400 раз (до 4 г/л).
20
Регуляция окисления жирных кислот и кетогенеза
1. Зависит от соотношения инсулин/глюкагон. При уменьшении отношения возрастает липолиз, усиливается накопление жирных кислот в печени, которые активно
поступают в реакции β-окисления.
2.При накоплении цитрата и высокой активности АТФ-цитрат-лиазы (см далее) образующийся малонил-S-КоА ингибирует карнитин-ацил-трансферазу, что препят-
ствует поступлению ацил-S-КоА внутрь митохондрий. Имеющиеся в цитозоле моле-
кулы ацил-S-КоА поступают на этерификацию глицерина и холестерола, т.е. на синтез жиров.
3.При нарушении регуляции со стороны малонил-S-КоА активируется синтез
кетоновых тел, так как в попавшая в митохондрию жирная кислота может только окисляться до ацетил-S-КоА. Избыток ацетильных групп переправляется на синтез
кетоновых тел.
ЗАПАСАНИЕ ЖИРОВ
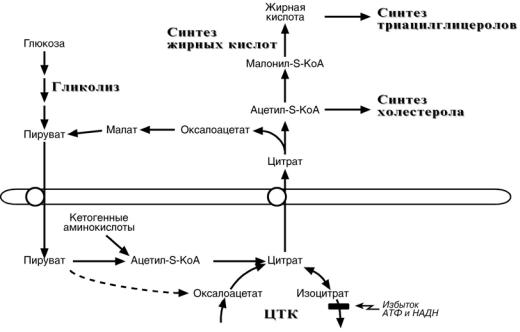
Реакции биосинтеза липидов идут в цитозоле клеток всех органов. Субстратом
для синтеза жиров de novo является глюкоза, которая попадая в клетку, окисляется по гликолитическому пути до пировиноградной кислоты. Пируват в митохондриях декарбоксилируется в ацетил-S-КоА и вступает в ЦТК. Однако, в состоянии покоя, при
отдыхе, при наличии достаточного количества энергии в клетке реакции ЦТК (в част-
ности, изоцитратдегидрогеназная реакция) блокируются избытком АТФ и НАДН. В результате накапливается первый метаболит ЦТК – цитрат, перемещающийся в ци-
тозоль. Образованный из цитрата ацетил-S-КоА далее используется в биосинтезе
жирных кислот, триацилглицеролов и холестерола.
