
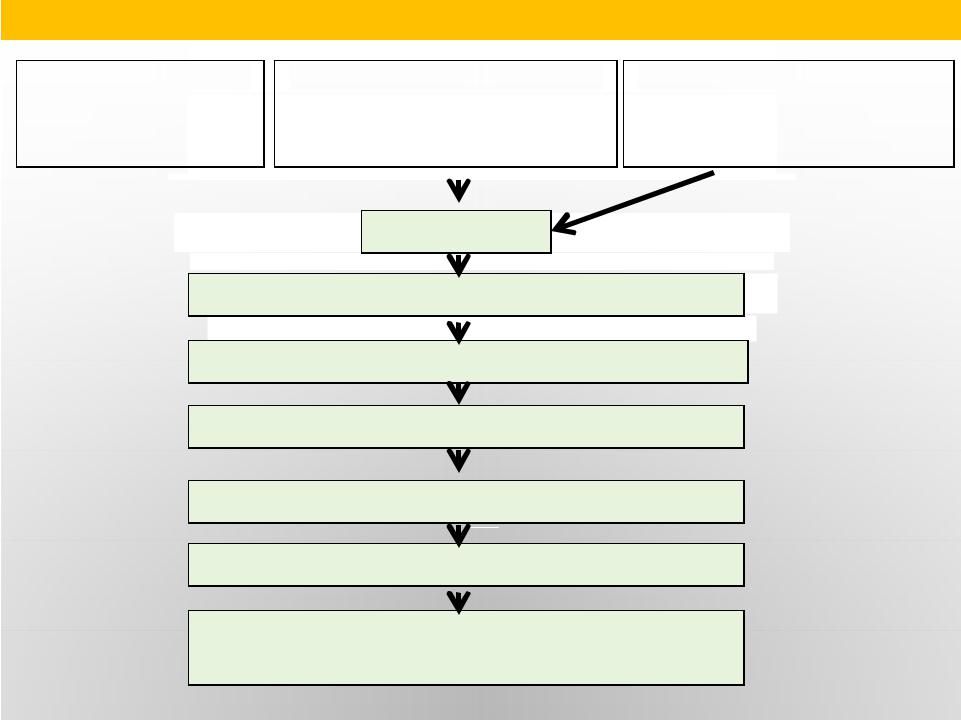
Причины и механизмы развития рахита
|
|
Нарушение всасывания |
|
Снижение активности |
Недостаток УФ |
|
жирорастворимых |
|
гидроксилаз |
|
|
витаминов |
|
|
Дефицит D3
Нарушение образования кальцитриола
Нарушение всасывания Са в кишечнике
Снижение концентрации Са в крови
Стимуляция секреции паратгормона
Вымывание Са из костей
Нарушение образования костной ткани,
деформация скелета

Гипервитаминоз D
Гипервитаминоз D (интоксикация витамином D) - состояние, обусловленное как прямым токсическим действием препарата на клеточные мембраны, так и повышенной концентрацией в крови солей кальция, откладывающихся в стенках сосудов внутренних органов, в первую очередь почек и сердца.
Острая интоксикация витамином D - нейротоксикоз или кишечный токсикоз: резко снижен аппетит, жажда, рвота, быстро уменьшается масса тела, развивается обезвоживание, появляются запоры (возможен неустойчивый и жидкий стул). У некоторых детей регистрируют кратковременную потерю сознания, возможны тонико-клонические судороги.
Хроническая интоксикация витамином D возникает на фоне длительного (6-8 мес и более) применения препарата в превышающих физиологическую
потребность дозах. Клиническая картина выражена менее отчётливо и
включает повышенную раздражительность, плохой сон, слабость, боли в суставах, постепенное нарастание дистрофии, преждевременное закрытие
большого родничка, изменения со стороны сердечно-сосудистой и мочевой
систем.

Кальцитонин
Природа гормона
Пептидный гормон, содержит 32 аминокислоты, секретируется
парафолликулярными клетками щитовидной железы (С-клетками) при повышении концентрации Са2+ в крови.
Механизм действия
Рецептор кальцитонина - трансмембранный белок (7 трансмембранных сегментов). Связывание кальцитонина сопровождается активацией
аденилатциклазной системы, фосфоинозитольного и Са 2+-зависимого
внутриклеточных сигнальных путей.
Эффекты Вызывает угнетение активности остеокластов и остеоцитов и ингибирует
резорбцию костной ткани. Стимулирует остеобласты.
В почках кальцитонин усиливает экскрецию фосфатов, ионов кальция
и натрия, угнетает активность 1α-гидроксилазы, что уменьшает синтез
кальцитриола.
В тонкой кишке кальцитонин тормозит всасывание кальция.
Кальцитонин - антагонист ПТГ.
Уровень секреции кальцитонина зависит от концентрации эстрогенов.
При дефиците эстрогенов (менопауза или заболевания яичников) секреция кальцитонина снижается, что способствует ускоренной резорбции костной ткани и приводит к остеопорозу и переломам костей.

Лекция « МЕТАБОЛИЗМ ГЕМА И ОБМЕН ЖЕЛЕЗА»
Авторы – доцент Т.А.Титова и доцент Е.С.Зыкова
|
|
|
СИНТЕЗ ГЕМА |
|
|
Гем является |
простетической группой |
гемоглобина, |
миоглобина, |
||
цитохромов, |
а |
также |
коферментом |
каталазы, |
пероксидазы, |
цитохромоксидазы. Гем синтезируется в большинстве клеток, за исключением эритроцитов. Железо, необходимое для синтеза гема, поступает с пищей или освобождается при распаде гема.
Гем состоит из иона Fe+2 , входящего в структуру порфирина, который состоит из 4-х пиррольных колец, связанных между собой метеновыми «мостиками». Порфирины могут отличаться заместителями в пиррольных кольцах. Гем гемоглобина содержит протопорфирин IХ, имеющий два винильных, четыре метильных радикала и два остатка пропионовой кислоты
(рис.1).
Рис. 1.
Субстратами для синтеза гема являются глицин, сукцинил-КоА и Fe+2 Первая и три последние реакции синтеза идут в матриксе митохондрий, а остальные – в цитоплазме.

В матриксе митохондрий из глицина и сукцинил-КоА под действием пиридоксальфосфат зависимого фермента 5-аминолевулинатсинтазы образуется 5-аминолевулиновая кислота, которая поступает в цитоплазму. В цитоплазме фермент 5-аминолевулинатдегидратаза катализирует конденсацию двух молекул 5-аминолевулината с образованием порфобилиногена. Далее из двух молекул порфобилиногена последовательно образуются промежуточные метаболиты порфириногены. Последний из них поступает в митохондрии и превращается в протопорфирин IХ. Фермент феррохелатаза присоединяет Fe+2 к протопорфирину IХ и таким образом образуется гем (рис.2).
Рис. 2.
Две первые реакции синтеза гема аллостерически ингибирует гем по принципу отрицательной обратной связи. Синтез аминолевулинатсинтазы индуцирует Fe+2 . В свою очередь сам гем индуцирует синтез α- и β- полипептидных цепей гемоглобина (рис.3).

Рис. 3.
Нарушения синтеза гема могут быть наследственными и приобретенными. Они сопровождаются повышением содержания промежуточных метаболитов синтеза гема, а также продуктов их окисления в клетках и называются порфириями. Эти вещества поступают в мочу, окрашивая ее в красный цвет. При генетических дефектах ферментов, катализирующих превращения промежуточных метаболитов синтеза гема порфириногенов, наблюдаются наследственные порфирии. Порфириногены являются нейротоксинами и ускоряют образование активных форм кислорода, которые стимулируют перекисное окисление липидов (ПОЛ) и разрушение мембран клеток. Легкие формы порфирий могут протекать бессимптомно, но прием лекарств, являющихся индукторами синтеза 5- аминолевулинатсинтазы (сульфаниламиды, барбитураты, стероиды) могут вызвать обострение болезни. Порфирии сопровождаются нейропсихическими расстройствами, нарушениями ретикулоэндотелиальной системы, фотосенсибилизацией.
ОБМЕН ЖЕЛЕЗА
Железо входит в состав гемсодержащих белков и ферментов (миоглобина, гемоглобина, цитохромов, цитохромоксидазы, пероксидазы, каталазы), железофлавопротеинов ( NADH-дегидрогеназы, сукцинатдегидрогеназы, ксантиноксидазы, ацил-КоАдегидрогеназы) и железосодержащих белков трансферрина и ферритина.
В организме здорового человека содержится 3-4г железа. Оно поступает с пищей или освобождается при распаде гема и железосодержащих белков. В пище содержится Fe+2 и Fe+3 . Наиболее богаты железом печень и почки животных, яйца, мясо. В растительных продуктах железа содержится меньше, вместе с тем им относительно богаты овсянка, персики, грибы,

гранаты. Однако в растениях железо связано с фитиновой кислотой и поэтому плохо усваивается.
Ионы железа легко вступают в окислительно-восстановительные реакции и образуют хелатные соединения со многими веществами. Это может привести к изменению их свойств и функций. Поэтому железо транспортируют и депонируют особые белки. По крови железо транспортирует трансферрин, а в клетках депонирует ферритин. При связывании железа с белками оно окисляется, а при освобождении из белков
– восстанавливается. В суточном количестве пищи содержится около 20 мг железа, а всасывается не более 2 мг. В полости кишечника железо освобождается из белков и органических солей пищи. В клетки слизистой кишечника всасывается закисное железо - Fe+2 . Витамин С восстанавливает железо и улучшает его усвоение. В клетках слизистой кишечника избыток железа соединяется с белком апоферритином, который окисляет железо и превращается в ферритин. Поступающее из клеток кишечника в кровь железо окисляется ферментом плазмы крови ферроксидазой. В крови Fe+3 транспортирует белок трансферрин. В клетках железо используется для синтеза железосодержащих белков или депонируется в ферритине (рис.4).
Рис. 4.
Ферритин это олигомерный белок, состоящий из 24 протомеров. Они образуют полую сферу, внутри которой может содержаться около 3000 ионов железа в составе гидроксифосфата. Ферритин окисляет Fe+2 . В белковой части этого белка есть каналы, через которые железо может поступать и выходить из полости сферы.
Из организма в сутки со слущенным эпителием выводится около 1 мг железа.
При нарушениях метаболизма железа возникают железодефицитная анемия или гемохроматоз.
Железодефицитная анемия развивается при недостатке железа в организме, который может возникнуть при частых кровотечениях, анацидном
гастрите, беременности, родах, язвах и опухолях желудочно-кишечного тракта, снижении всасывания железа в кишечнике. При этой анемии уменьшается размер эритроцитов, снижается интенсивность их окраски, содержание гемоглобина в крови, насыщение железом трансферрина, содержание ферритина в клетках. Причина этих изменений – снижение синтеза гема, гемоглобина и апоферритина из-за дефицита железа. Больных лечат лекарствами, содержащими железо.
Гемохроматоз - это наследственное заболевание, которое сопровождается повышением всасывания железа в кишечнике. При этом железо откладывается в белковой части ферритина, который в результате этого превращается в гомосидерин. Накопление гранул гомосидерина в клетках печени, селезенки, поджелудочной железы приводит к гемохроматозу. Содержание железа в организме больных может достигать 40 г. Накопление железа в клетках поджелудочной железы приводит к сахарному диабету, в гепатоцитах – к циррозу печени, в кардиоцитах – к сердечной недостаточности. Больных лечат кровопусканиями и препаратами, связывающими железо.
КАТАБОЛИЗМ ГЕМА
Наибольшее количество гема содержит гемоглобин, который находится в эритроцитах. Они циркулируют в крови около 120 дней, а затем распадаются в клетках ретикулоэндотелиальной системы селезенки, костного мозга и печени.
В процессе распада гема можно выделить несколько последовательных этапов (рис.5).

Гемоглобин
Гем
Гемоксигеназная система
Биливердин
Биливердинредуктаза
Билирубин
Непрямой билирубин
Билирубин
2УДФ-глюкуронат
Глюкуронилтрансфераза I и II
Рис. 5.
•В клетках ретикулоэндотелиальной системы гемоглобин под действием фермента гемоксигеназы превращается в вердоглобин. Вердоглобин состоит из глобина, Fe+2 и линейного тетрапиррола биливердина. Теряя глобин и железо, он превращается в желчный пигмент желто-зеленого цвета биливердин.
•Биливердинредуктаза восстанавливает биливердин в желчный пигмент красного цвета билирубин, который поступает в кровь.
•В крови гидрофобный билирубин соединяется с белком альбумином. Билирубин, связанный с альбумином, называют непрямым (неконъюгированным), так как он не дает положительную качественную реакцию (розовое окрашивание) с диазореактивом. Непрямой билирубин плохо растворим в воде, токсичен и не обнаруживается в моче, так как связан
сальбумином.
•Неконъюгированный билирубин поступает в клетки печени. В эдоплазматическом ретикулуме гепатоцитов билирубин под действием фермента глюкуронилтрансферазы соединяется с глюкуроновой кислотой с образованием диглюкуронидбилирубина. Диглюкуронидбилирубин называют прямым билирубином. Он растворим в воде, не токсичен и взаимодействует с диазореактивом. Около 75% прямого билирубина из
