

4)Ресинтез ЭХС в энтероцитах: а) активация жирной кислоты:
б) взаимодействие холестерола и ацил-KoA:
АХАТ – ацил-холестерол-ацил-трансфераза.
5)ЭХС и небольшое кол-во свободного ХС включаются в состав ХМнезр..
6)Через лимфу ХМнезр. поступают в кровь, где происходит их «созревание».
7)Зрелые ХМ подвергаются действию ЛП-липазы => образуются ХМост..
8)ХМост. взаимодействуют с ЛПНП-рецепторами печени и поглощаются печенью с помощью рецептор-опосредованного эндоцитоза.
(Лигандами ЛПНП-рецепторов служат белки апо B и апо E).
9)Компоненты |
ХМост. |
расщепляются |
лизосомальными ферментами. |
|
|
Освобождающийся ХС включается в общий фонд ХС в организме.

Синтез эндогенного холестерола в печени и транспорт его в ткани
Холестерол синтезируется из ацетил-КоА в основном в печени (80% всего ХС).
Также ХС синтезируется: в клетках кишечника, коре надпочечников, коже и др. тканях.
Исходный субстрат: ацетил-КоА Необходимый кофермент: NADPH. Источник энергии: АТФ.
! Все вещества, необходимые для синтеза ХС образуются в реакциях катаболизма глюкозы.
Синтез ХС происходит в абсорбтивный период, в цитозоле и эндоплазматическом ретикулуме клеток печени одновременно с синтезом жирных кислот и ТАГ.
Реакции синтеза ХС до образования сквалена происходят в цитозоле, остальные реакции – в мембранном слое ЭР, т.к. сквален и последующие метаболиты не растворимы в воде.

Схема синтеза холестерола:
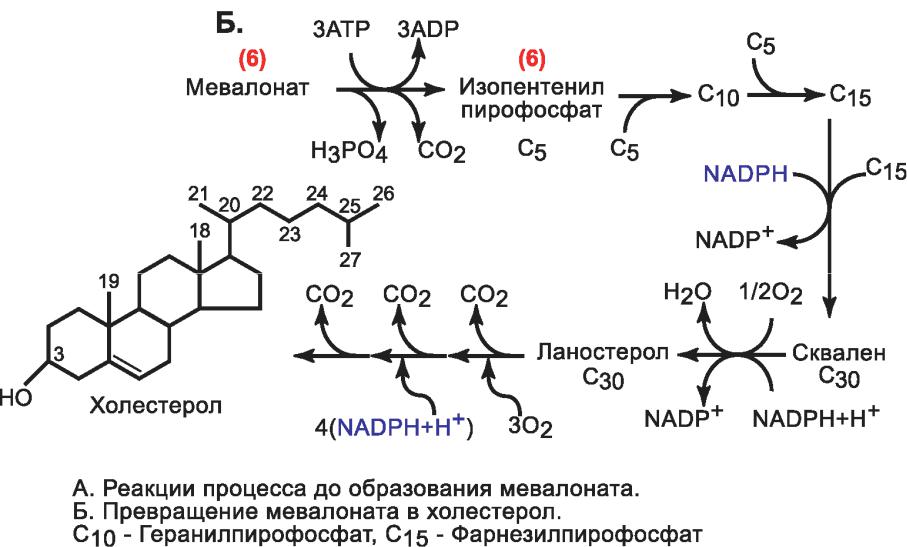

Регуляция синтеза ХС в печени:
Регуляторный фермент синтеза ХС в печени – ГМГ-КоA-редуктаза.
ГМГ-КоA-редуктаза – гликопротеин, пронизывающий мембрану ЭР, активный центр которого выступает в цитозоль.
2 способа регуляции действия ГМГ-КоА-редуктазы:
1) регуляцияактивностифермента:
Фосфорилирование и дефосфорилирование.
ГМГ-КоA-редуктаза – активна в дефосфорилированной форме и активируется в абсорбтивный период при участии инсулина.
Ингибируется – путем фосфорилирования под действием глюкагона (в постабсорбтивный период и при голодании).
2)регуляцияколичествафермента:
а) регуляция на уровне транскрипции:
Стероиды – холестерол и желчные кислоты – подавляют транскрипцию гена ГМГ-КоА-редуктазы и синтез этого фермента.
Эстрогены – индукторы синтеза ГМГ-КоА- редуктазы – повышают синтез этого фермента.
б) регуляция протеолиза ГМГ-КоА-редуктазы:
ХС, желчные кислоты, оксипроизводные ХС и кортикостероиды стимулируют протеолиз молекул ГМГ-КоА-редуктазы, т.е. деградацию функционально активного фермента.


Большая часть синтезированного ХС и ЭХС удаляется из печени в составе ЛПОНП.
ЛПОНП содержат 55% ТАГ, фосфолипиды и апобелки (в основном: апо В-100).
В крови ЛПОНП созревают, подвергаются действию ЛП-липазы и превращаются сначала в ЛППП, а затем в ЛПНП.
После этого → белки апо E и апо C-II переносятся
обратно из ЛПНП в ЛПВП.
ЛПНП – основная транспортная форма ХС, в которой он доставляется в ткани.
~ 70% ХС и ЭХС в крови находятся в составе ЛПНП.
Из крови ЛПНП поступают в печень (~ 75%) и другие ткани и доставляют в них ХС.
Захват ЛПНП из кровотока происходит всеми тканями организма с помощью ЛПНП-рецепторов:
ЛПНП-рецепторы помимо ЛПНП могут также захватывать из крови ЛППП, ЛПОНП и ХМост..
ЛПНП-рецепторы взаимодействуют своим N-концевым
гидрофобным доменом с белками апоB (B48 и B100) и апоE
на поверхности липопротеинов (в основном: ЛПНП).
После этого → ЛП поглощаются тканями с помощью
рецептор-опосредованного эндоцитоза.
«Обратный» транспорт холестерола
В«обратном» транспорте ХС, т.е. выведении избытка ХС из тканей и крови в печень, главную роль играют ЛПВП.
Впечени образуются незрелые ЛПВП – ЛПВПпредшественники (ЛПВПпредш.)
Они имеют дисковидную форму и состоят из бислоя фосфолипидов, с включенными в него белкамиапопротеинами (A-I, С-П, Е).
ЛПВПпредш. практически не содержат ХС.
Вначале, поступая в кровь, ЛПВПпредш. отдают белки апо C-II и апо E ХМ и ЛПОНП.
Затем, ЛПВПпредш. принимают холестерол с мембран клеток и поверхности других липопротеинов (в основном: ЛПНП).
Для этого к поверхности ЛПВП прикрепляется фермент лецитин-холестерол-ацилтрансфераза (ЛХАТ), поступающий в ЛПВП из крови.
Активатор ЛХАТ – белок апо A-I, который располагается на поверхности ЛПВП.
ХС перемещается в оболочку ЛПВПпредш. путем облегченной диффузии при участии белка ABC1
(АТФ-связывающий кассетный белок).
ХС, поступающий в оболочку ЛПВПпредш. вступает в реакцию этерификации, которую катализирует ЛХАТ:

В результате этой реакции образуются ЭХС, которые погружаются в гидрофобное ядро ЛПВП.
Таким образом, в оболочке ЛПВПпредш. освобождается место для поступления следующей порции ХС.
По мере наполнения гидрофобного ядра эфирами холестерола ЛПВПпредш. приобретают сферическую форму и превращаются в ЛПВП3:
Образованный лизолецитин связывается с альбумином и уносится с поверхности ЛПВП3 током крови.
Далее происходит обмен ЭХС на ТАГ между ЛПВП3 и ЛПОНП или ЛППП.
ЭХС поступают из ЛПВП3 на ЛПОНП или ЛППП с помощью апоD-белка – «белка, переносящего ЭХС» (БПЭХ).
А обратно из ЛПОНП или ЛППП – ЛПВП3 получают ТАГ и фосфолипиды.
=> ЛПВП увеличиваются в размере и превращаются в ЛПВП2.
ЛПВП2 подвергаются действию печеночной липазы, которая гидролизует жиры в ЛПВП2, и превращается обратно в ЛПВП3, которые могут продолжать забирать ХС из тканей и ЛП.
Поступление ЭХС, собранных с помощью ЛПВП, в печень происходит несколькими путями:
1)ЛПОНП и ЛППП под действием ЛП-липазы превращаются в ЛПНП, которые доставляют ХС в печень;
2)ЛПВП2 взаимодействуют со "скэвенджер"- рецепторами печени и ЭХС переносятся
непосредственно с ЛПВП2 в гепатоциты после действия на ЛПВП2 печеночной липазы;
3)В меньшей степени: Взаимодействие ЛПВП2 со специфическими рецепторами печени, комплементарными белкам апо E и апо A-I и поглощение их путем рецептор-опосредованного эндоцитоза.
