

В последнем цикле: получается сразу 2 Ацетил-KoA.
=> Количество циклов β-окисления составляет:
 , где n – общее число С-атомов в молекуле ЖК.
, где n – общее число С-атомов в молекуле ЖК.
Кол-во Ацетил-KoA = кол-ву циклов + 1 =  .
.
Σ Кол-во АТФ, образующегося при β-окислении
равно: 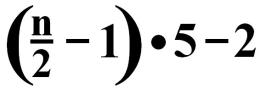
5 – кол-во АТФ, образованного в каждом цикле
(FADH2 → 2 АТФ и 1 NADH + H+ → 3 АТФ)
=> 2 +3 = 5 АТФ
2 – энергия 2-х макроэргических связей АТФ используется на активацию ЖК в цитозоле.
Σ Кол-во АТФ, образующегося при полном аэробном
катаболизме ЖК до CO2 и H2O:
12 – кол-во АТФ, которое образуется при окислении Ацетил-KoA в цикле Кребса.

Кол-во АТФ при окислении ненасыщенной ЖК:
где m – кол-во = связей в молекуле ЖК.
Регуляция β-окисления
Скорость окисления жирных кислот зависит от: а) V цикла Кребса;
б) отношения NADH / NAD+ (потребности клетки в энергии);
в) поступления О2 в ткани (гемоглобин, эффект Бора); г) доступности коферментов:
– NAD+ |
(витамин РР) |
|
– FAD |
( |
В2) |
– НSКоА |
( |
В5 – пантотеновая кислота) |
д) доступности субстрата – Ацил-KoA.
Регуляторный фермент β-окисления – Карнитинацилтрансфераза I.
=> регулируется не собственно β-окисление, а транспорт ацильного остатка из цитозоля в митохондрии.
Активаторы: АДФ, АМФ, Ацил-KoA
Ингибиторы: АТФ, Малонил-KoA (в основном:
в печени).
Гормональная регуляция окисления ЖК в печени
В клетках печени одновременно происходит и синтез и окисление ЖК.
Малонил-KoA (основной субстрат синтеза ЖК) →
основной аллостерический ингибитор Карнитинацилтрансферазы I.

Кол-во Малонил-KoA регулируется гормонами: Адреналином, Глюкагоном и Инсулином.
1. ситуация:
В постабсорбтивный период, при голодании и при стрессе:

2. ситуация:
В абсорбтивный период:
При участии Инсулина происходит дефосфорилирование Ацетил-KoA-карбоксилазы.
=> ↑ V синтеза ЖК => ↑ конц-ия Малонил-KoA => ингибируется Карнитинацилтрансфераза I => ↓ V β-
окисления ЖК.
Кетоновые тела
1.Синтез кетоновых тел.
Всинтез кетоновых тел включается часть молекул Ацетил-KoA, которые образуются в ходе β-окисления.
Синтез кетоновых тел происходит в митохондриях печени:

! Конц-ия в крови β-гидроксибутирата >> конц-ии
Ацетоацетата, т.к. равновесие реакции: Ацетоацетат←→ β-гидроксибутират сдвинуто → из-за ↑ конц-ии NADH, образующегося в ходе β-окисления.
Основные Кетоновые тела: Ацетоацетат и β- гидроксибутират.
3-е кетоновое тело – ацетон тканями не используется.
В норме: синтез кетоновых тел незначительно ↑ в
постабсорбтивный период.
Их конц-ия в крови при этом составляет ~ 1-3 мг/дл.
Синтез кетоновых тел ↑↑:
а) при голодании; б) длительной физической нагрузке (стрессе);
в) диете, богатой ТАГ, но с низким кол-вом углеводов ("кремлевская" диета);
г) сахарном диабете.
Конц-ия кетоновых тел в крови: При длительном голодании ~ 50 мг/дл При сахарном диабете ~ 300 мг/дл
Регуляция синтеза кетоновых тел:
При голодании и физической нагрузке:
Гормоны Глюкагон (или Адреналин) через АЦ-систему ↑ распад жира из жировой ткани →
→ЖК поступают в кровь и транспортируются в комплексе с альбумином в печень →
→В печени ↑ V β-окисления ЖК и образуется большое кол-во Ацетил –KoA и NADH (↑ Ацетил –KoA; ↑ NADH).
Ацетил-KoA в печени может вступать в 2 процесса:
1.Синтез кетоновых тел (происходит только в печени);
2.Цикл Кребса
Но, в условиях голодания (стресса): V цикла Кребса в печени существенно снижена по 2 причинам:
1)Ингибирование регуляторных ферментов цикла Кребса ↑ конц-иями АТФ и NADH (аллостерическое
ингибирование)
2)Утечка оксалоацетата из митохондрий в цитозоль клеток печени на глюконеогенез => ↑ накопление Ацетил-KoA и ↓ конц-ия Оксалоацетата.
Из 1 и 2 причин => избыток Ацетил-KoA используется на синтез кетоновых тел.

Митохондрии печени Голодание, стресс:
Синтез |
β-окисление ЖК |
кетоновых тел |
ЦТК 














 Ацетил-KoA
Ацетил-KoA
Пируват |
|
|
|
Оксалоацетат |
|
NADH + H+ |
|
|
||||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
||||||
|
|
|
|
NAD+ |
||||||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
Малат |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Внутренняя |
|
|
|
|
|
|
|
|
|
|
|
|
мембрана митохондрии |
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Цитозоль |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
печени |
|
|
|
|
|
|
|
|
Малат |
|||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
NAD+ |
||
|
|
|
|
|
|
|
|
|
|
|||
Глюкоза |
|
Глюконеогенез |
|
|
NADH + H+ |
|||||||
|
|
|||||||||||
|
|
|
|
|
|
|
Оксалоацетат |
|||||
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|||||
Регуляторный фермент синтеза кетоновых тел: ГМГ- KoA-синтаза.
Ингибитор фермента: HS-KoA.
При голодании и стрессе: при участии Глюкагона (Адреналина) происходит мобилизация ТАГ из жировой ткани => ↑ поток ЖК в печень и образуется
Ацил-KoA.
Далее происходит перенос ацильных остатков через внутреннюю мембрану митохондрий в матрикс.
В матриксе митохондрий: HS-KoA используется в процессе β-окисления, а также происходит
взаимодействие Ацил-карнитина с HS-KoA => => ↓ конц-ия HS-KoA =>
=> не происходит ингибирования ГМГ-KoA-синтазы и происходит ↑ V синтеза кетоновых тел.
