

|
|
|
CH OPO H |
|
|
CH OPO H |
||||||||||||||
|
|
|
|
2 O3 |
2 |
CH2OH +АТФ + Мg 2+ |
|
|
2 |
O3 2 |
|
CH2OPO3H2 |
||||||||
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
H |
|
OH |
|
Фосфофруктокиназа |
|
|
H |
|
OH |
|
|
|
||||
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
OH |
|
|
OH |
АДФ |
H |
|
|
|
O |
|
||||||
|
|
|
||||||||||||||||||
|
|
|
|
|
H |
|
|
|
|
|
OH |
H |
||||||||
фруктозо-6-фосфат |
|
|
|
|
|
|
|
фруктозо-1,6-бисфосфат |
||||||||||||
Фруктозо-6-фосфат фосфорилируется по первому углеродному
атому ферментом фосфофруктокиназой за счет АТФ. Реакция необра-
тима. Фосфофруктокиназа Ã аллостерический фермент, активность которого регулируется: активируется АДФ и АМФ и тормозится АТФ и цитратом. Реакция протекает в присутствии ионов Mg. Эта стадия ли-
митирует скорость всего процесса распада. Таким образом, на активность фосфофруктокиназы (а соответственно на скорость распада глюкозы) влияет отношение АТФ/АМФ в цитозоле клетки. Фруктозо-1,6-
бисфосфат, образовавшийся в этой реакции, далее расщепляется альдолазой на две фосфотриозы: 3-фосфоглицериновый альдегид и диокси-
ацетонфосфат, которые являются изомерами по отношению друг к другу. Под действием триозофосфатизомеразы они легко превращаются друг в друга, но дальнейшим превращениям подвергается 3-
фосфоглицериновый альдегид, и по мере его убыли происходит превращение диоксиацетонфосфата в его изомер (хотя образуется 95% диоксиацетонфосфата и только 5% 3-фосфоглицеринового альдегида). Поэтому можно считать, что молекула фруктозо-1,6-бисфосфата распадается на 2 молекулы 3-фосфоглицеринового альдегида.
|
|
|
H O |
|
|
|
|
|
|
H |
|
|
|
|
|
|
2OPO3H2 |
|
|
|
диоксиаце |
лицериновый |
|
||||
|
|
|
альдегид |
|
||
|
|
|
аза |
|
|
|
|
|
+НS-фермент-НАД |
|
|
|
|
H |
O |
Дегидрогеназа 3-фосфо- |
H OH |
фермент––НАД |
+ |
|
глицеринового альдегида |
||||||
C |
|
C S |
|
|||
2 H C OH |
|
2 H C OH |
|
|
||
CH2OPO3H2 |
CH2OPO3H2 |
|
||||
|
|
|
фермент-субстратный |
|
||
|
|
|
комплекс |
|
|
|
152

3-фосфоглицериновый альдегид взаимодействует с дегидрогеназой 3-фосфоглицеринового альдегида. Это сложный фермент с четвер-
тичной структурой. Построен из четырех идентичных субъединиц. В каждой полипептидной цепи в активный центр фермента входит SН-
группа остатка цистеина. Каждая полипептидная цепь прочно соединена с молекулой НАД. НАД защищает фермент от термоинактивации, протеолитического расщепления. Таким образом, в ферменте есть четыре структурно независимых каталитических центра. При взаимодействии дегидрогеназы с 3-фосфоглицериновым альдегидом образуется фер- мент-субстратный комплекс типа тиополуацеталя. Происходит окисле-
ние этого комплекса с переносом протонов и электронов к НАД, т.е. происходит окисление альдегида в кислоту, а энергия окисления аккумулируется в макроэргической связи.
O |
|
|
|
|
O |
|||||
C ~ S фермент––НАД!Н+Н+ |
C ~ S фермент––НАД+ |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
2 H C OH |
|
+ 2НАД+ 2 H C OH |
|
|
||||||
CH2OPO3H2 |
|
|
|
|
CH2OPO3H2 |
|
|
|||
|
|
|
|
|||||||
|
|
|
|
|
||||||
|
2НАД!Н+Н+ |
|||||||||
|
|
|
|
|
|
|
|
|||
Протоны и электроны с НАД+, прочно связанного с ферментом, переносятся на свободный цитоплазматический НАД+, а макроэргическая связь закрепляется фосфатом с образованием 1,3-
бисфосфоглицериновой кислоты. Фермент освобождается из комплекса.
|
|
|
|
O |
|
+2АДФ |
|
|
|
|
|
|
|
|
|
|
|
|
Фосфоглицерат- |
|
|
COOH |
|||||
|
|
|
|
C O ~ PO3H2 |
|
киназа |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 HC OH |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|||
+2Н3РО4 |
2 HC |
OH |
|
|
|
||||||||
CH2OPO3H2 |
|
+2АТФ |
|
CH2OPO3H2 |
|||||||||
НS-ФЕРМ-НАД+ |
|
|
|||||||||||
|
|
|
|
1,3-бисфоглицериновая |
|
3-фосфоглицериновая |
|||||||
|
|
|
|
|
кислота |
|
|
|
кислота |
||||
Фосфоглицераткиназа переносит фосфатный остаток, богатый энергией, на АДФ с образованием АТФ и 3-фосфоглицериновой кислоты. Таким образом, энергия окисления 3-фосфоглицеринового
альдегида в кислоту аккумулируется в макроэргических связях АТФ.
Синтез АТФ, связанный с переносом на АДФ фосфата из высокоэнергетических соединений, образовавшихся в результате внутримолекулярных превращений субстратов, называется субстратным фосфорилированием.
В 3-фосфоглицериновой кислоте фосфоглицеромутаза переносит фосфатную группировку во 2-ое положение, и образуется 2-
фосфоглицериновая кислота. Фермент енолаза отщепляет от нее воду, и образуется фосфоенолпируват.
153

Фосфоглице- |
|
|
COOH |
|
|
|
|
|
|
COOH |
||||||||||
ромутаза |
|
|
|
|
Енолаза |
|
|
|
||||||||||||
|
|
|
|
|
||||||||||||||||
|
|
|
||||||||||||||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
2 C |
|
O ~ PO3H2 |
|
|||
|
|
|
HC |
|
|
O |
|
PO H |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
3 |
2 |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
CH OH |
|
|
Н2О CH2 |
||||||||||||
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
2-фосфоглицериновая |
|
|
фосфоенолпировиноградная |
|||||||||||||||
|
|
|
|
кислота |
|
|
|
|
|
|
кислота |
|||||||||
При отщеплении воды связь с фосфатом становится макроэргической. Енолаза активируется Mg2+ и Mn2+, ингибируется фторидом.
Пируваткиназа переносит фосфатный остаток, богатый энергией, с фосфоенолпирувата на АДФ, и образуются еще две молекулы АТФ (субстратное фосфорилирование). Реакция необратима. В результате образуются две молекулы пировиноградной кислоты.
+ 2АДФ |
|
|
COOH |
|
|
|
|
|
COOH |
|||||
Пируваткиназа |
|
|
|
|
|
|
|
|||||||
|
|
|
||||||||||||
|
||||||||||||||
|
|
2 C |
|
OH |
|
|
|
2 C |
|
O |
||||
2АТФ |
|
|
|
|
|
|||||||||
|
|
|
|
|
||||||||||
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CH |
|
|
|
CH3 |
||||||||||
|
|
|
|
|
||||||||||
|
|
2 |
|
пировиноградная кислота |
||||||||||
|
|
|
|
|
|
|
|
|||||||
Таким образом, в результате специфического пути превращения глюкозы в цитозоле клеток образуются две молекулы пировиноградной кислоты, две молекулы восстановленного кофермента НАД (2НАД!Н+Н+) и 4 молекулы АТФ, однако 2 молекулы АТФ были израсходованы на фосфорилирование глюкозы и фруктозо-6-фосфата. Поэтому 4-2=2 АТФ – энергетический баланс распада молекулы глюкозы на две молекулы пировиноградной кислоты.
Аэробный распад глюкозы
В аэробных условиях (а большинство тканей в организме получают энергию за счет аэробных процессов) образовавшиеся в цитоплазме продукты – пировиноградная кислота и восстановительные эквиваленты (НАД!Н+Н+) переносятся в митохондрии.
Пировиноградная кислота вступает в митохондриях в общий путь катаболизма: подвергается окислительному декарбоксилированию с образованием ацетил-КоА, который окисляется в цикле трикарбоновых кислот до СО2 и Н2О.
Наружная мембрана митохондрий хорошо проницаема для большинства низкомолекулярных соединений. Внутренняя мембрана проницаема для воды, небольших нейтральных молекул (глицерофосфат, жирные кислоты с короткой углеродной цепью), непроницаема для катионов Na+, К+, анионов Cl– и других, сахаров, большинства аминокислот, НАД, НАД!Н+Н+, НАДФ, НАДФ!Н+Н+ и др. Обмен между цито-
154

плазмой и внутренней средой митохондрий представляет сложный процесс, осуществляющийся с помощью особых переносчиков. Специальный переносчик обеспечивает перенос молекул пирувата по механизму симпорта с протоном.
Основным механизмом переноса восстановительных эквивалентов из цитоплазмы в митохондрии (протонов и электронов, восстановивших НАД на стадии окисления 3-фосфоглицеринового альдегида) является малат- оксалацетатный челночный механизм.
Он заключается в восстановлении в цитоплазме щавелевоуксусной кислоты в малат, для которого есть переносчик во внутренней мембране митохондрий. В матриксе митохондрий малат окисляется митохондриальной малатдегидрогеназой до щавелевоуксусной кислоты. Восстановившийся при этом кофермент НАД отдает протоны и электроны в полную дыхательную цепь. Образуется вода и 3 АТФ.
|
|
Цитоплазма |
+ |
|
|
|
|
|
|
|
|
Митохондрия + НАД+ |
|
|
|
|
||||||||
|
COOH |
+ НАД!Н+Н |
|
|
|
COOH |
|
|
|
|
|
COOH |
митохондриальная |
|
COOH |
|||||||||
|
малатдегидрогеназацитоплазматическая HC |
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
||||||||||||||||||||||
C |
|
O |
|
|
|
OH |
|
|
|
HC |
|
|
|
OH |
малатдегидрогеназа |
C |
|
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
CH2 |
|
|
|
|
CH2 |
НАД!Н+Н+ |
|
|
||||||||||
|
|
|
|
|||||||||||||||||||||
|
|
+ |
|
|
|
|
|
|
|
CH2 |
||||||||||||||
COOH |
НАД |
|
COOH |
|
|
|
COOH |
+ ½О2 |
COOH |
|||||||||||||||
|
Щук |
|
|
|
Малат |
|
|
|
|
|
|
|
|
+ 3АДФ |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ 3Н3РО4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
НАД++Н2О+3АТФ |
|
|
|
|
|
Энергетический баланс аэробного окисления молекулы глюкозы
Специфический путь распада глюкозы в цитозоле приводит к образованию 2 молекул пирувата, 2 АТФ и 2 НАД!Н+Н+.
Две молекулы пирувата в митохондриях подвергаются окислительному декарбоксилированию с образованием двух молекул ацетил- КоА и шести молекул АТФ (3х2=6 АТФ). Ацетил-КоА окисляется в
цикле трикарбоновых кислот и при этом образуются: 3 АТФ – при окислении изоцитрата;
3 АТФ – при окислительном декарбоксилировании -кетоглутарата; 2 АТФ – при окислении сукцината; 3 АТФ – при окислении малата;
1 АТФ – при субстратном фосфорилировании;
12 АТФ.
Таким образом, полное окисление молекулы пирувата дает 15 АТФ (из них 12 образуются при окислении ацетил-КоА в цикле трикарбоновых кислот), окисление 2 молекул – 30 АТФ.
Перенос протонов и электронов от 2 молекул НАД!Н+Н+ из цито-
155

плазмы в митохондрию малат-оксалацетатным челночным механизмом к О2 дает еще 6 АТФ.
2+30+6=38 АТФ
Итак, полное окисление молекулы глюкозы в аэробных условиях до СО2 и Н2О приводит к образованию 38 АТФ.
Лекция 13
АНАЭРОБНЫЙ РАСПАД ГЛЮКОЗЫ. СПИРТОВОЕ БРОЖЕНИЕ. МЕТАБОЛИЗМ ЭТАНОЛА.
ГЛЮКОНЕОГЕНЕЗ. ПЕНТОЗОФОСФАТНЫЙ ЦИКЛ
Анаэробный распад глюкозы
Напомним, что аэробный распад глюкозы – это предельное ее окисление до СО2 и Н2О, а анаэробный гликолиз – это специфический
путь катаболизма, т.е. часть аэробного распада глюкозы и термины ана-
эробный распад и анаэробный гликолиз совпадают.
В анаэробных условиях и в клетках, не имеющих митохондрий (зрелые эритроциты), образовавшаяся пировиноградная кислота восстанавливается лактатдегидрогеназой до лактата с использованием НАД!Н+Н+, образовавшегося при окислении 3-фосфоглицеринового альдегида в 1,3-бисфосфоглицериновую кислоту.
|
CH3 |
|
+ НАД!Н+Н+ |
|
CH3 |
||
|
|
Лактатдегидрогеназа |
|
|
|
||
C O |
|
|
|
HC |
OH + НАД+ |
||
|
|
|
|||||
COOH |
|
НА Н+Н+ |
|
|
COOH |
||
|
|
||||||
пируват |
|
|
|
|
|
лактат |
|
НАД играет роль промежуточного переносчика протонов и электронов от 3-фосфоглицеринового альдегида к пирувату. Этот процесс
получил название гликолитической оксидоредукции.
Энергетический баланс анаэробного гликолиза: молекула глю-
козы в анаэробных условиях распадается на 2 молекулы лактата. При этом образуются 4 АТФ, но 2 АТФ затрачиваются на фосфорилирование глюкозы и фруктозо-6-фосфата. Поэтому энергетическая эффектив-
ность процесса составляет 2 АТФ.
156

Если в анаэробных условиях распаду подвергается гликоген, то образуются 3 АТФ.
Анаэробный гликолиз протекает во всех тканях и играет роль пути получения энергии, но его значение для разных органов различно. Следует отметить, что в живых тканях анаэробных условий не бывает. Определение «анаэробный» в данном случае указывает лишь на то, что кислород в этом процессе не используется.
Анаэробный гликолиз используется для получения энергии:
1)В условиях ограниченной доставки кислорода в ткани (при интенсивной мышечной работе, гипоксии, ишемии органов и тканей).
2)В клетках с малым количеством митохондрий (мозговой слой почек, лейкоциты).
3)В клетках, не имеющих митохондрий (в зрелых эритроцитах это единственный путь образования АТФ).
Спиртовое брожение
В дрожжевых клетках и микроорганизмах, подобных им, анаэробный распад углеводов протекает сходно с гликолизом за исключением конечных стадий. Первые стадии до образования пировиноградной кислоты идут одинаково. При спиртовом брожении пируват подвергается декарбоксилированию ферментом пируватдекарбоксилазой, имеющей кофермент тиаминпирофосфат и требующей ионов Mg2+. При этом об-
разуется уксусный альдегид, который восстанавливается в этанол алкогольдегидрогеназой с использованием НАД!Н+Н+, образовавшегося при окислении 3-фосфоглицеринового альдегида в 1,3-бисфосфогли-
цериновую кислоту.
CH3 |
+ТПФ, Mg2+ |
CH |
Алкоголь- |
CH3 + НАД+ |
||||||||||
дегидрогеназа |
||||||||||||||
|
|
|
Пируватдекарбоксилаза |
|
3 |
|||||||||
|
|
|
|
|||||||||||
|
|
|
|
|
|
O+ НАДН+Н+ |
|
|
|
|||||
C |
|
O |
|
|
|
|||||||||
|
|
|
C |
|
CH2OH |
|||||||||
|
|
|
|
|
||||||||||
|
|
|
|
|||||||||||
|
|
|
|
СО2 |
|
|
|
|
|
|
||||
COOH |
H |
|
|
|
|
|||||||||
|
|
|
|
ацетальдегид |
|
|
этанол |
|||||||
Таким образом, конечными продуктами спиртового брожения являются этанол и СО2.
Метаболизм этанола в организме
В организме человека и животных этанол может образоваться как метаболит (эндогенный), а в организм человека может поступить извне (экзогенный).
Всасывание поступившего этанола происходит в желудке (20%) и
157

вкишечнике (80%). Метаболизм этанола осуществляется тремя ферментативными системами: алкогольдегидрогеназой (80%), микросомальной этанолокисляющей системой (МЭОС – 15%) и каталазой (5%).
Алкогольдегидрогеназа наиболее активно метаболизирует этанол
впечени, затем в слизистой кишечника, почках и легких. Фермент преимущественно локализован в цитозоле клеток, но около 10% – в эндоплазматической сети и митохондриях. В активном центре содержит атомы цинка, которые участвуют в каталитическом акте и стабилизируют четвертичную структуру фермента. В результате окисления этанола образуется ацетальдегид.
|
|
|
|
+НАД+ |
|
CH3 |
|||
CH |
Алкогольдегидрогеназа |
C |
|
O |
|||||
|
|||||||||
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
CH2OH НАДН+Н+ |
|
|
|
|
|||
|
|
|
|||||||
|
|
H |
|
|
|||||
Этот же продукт образуется и при окислении этанола МЭОС и каталазой.
|
|
|
МЭОС |
|
CH3 |
|||
CH |
+НАДФН+Н++О2 |
C |
|
O + 2Н2О |
||||
|
||||||||
|
||||||||
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
НАДФ+ |
|
|
|
|
|
|
|
|
||||||
|
|
H |
|
|
||||
|
|
|
Каталаза |
|
CH3 |
|||
CH |
C |
|
O + 2Н2О |
|||||
+Н2О2 |
|
|||||||
|
||||||||
|
|
3 |
|
|
|
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
||||
|
|
|
H |
|
|
|||
В качестве донора протонов и электронов микросомальная этанолокисляющая система использует НАДФ!Н+Н+.
Образующийся ацетальдегид далее окисляется ацетальдегиддегидрогеназой в уксусную кислоту, которая активируется путем присоединения к коферменту А, и активная форма уксусной кислоты – ацетил-
КоА вступает в цикл трикарбоновых кислот, где окисляется.
CH |
Ацетальдегиддегидрогеназа |
|
|
|
|
|||||||||||
|
|
3 |
|
+НАД |
+ |
|
|
+НS-КоА+АТФ |
|
CH3 |
||||||
|
|
|
||||||||||||||
C |
|
O |
|
|
|
|
|
|
CH3 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
НАД!Н+Н |
+ |
|
|
|
|
АМФ Н4Р2О7 |
|
O |
||
H |
|
|
|
|
|
COOH |
C ~ SKoA |
|||||||||
ацетальдегид |
|
|
уксусная кислота |
|
|
ацетил-КоА |
||||||||||
В сутки в тканях человека образуется и окисляется 1-9 г этанола.
Полагают, что его предшественниками являются пировиноградная кислота, некоторые аминокислоты (треонин, -аланин), дезоксирибоза.
158
Содержание эндогенного этанола повышается при неврозах, шизофрении, сахарном диабете, заболеваниях почек, в условиях гипоксии и при физической нагрузке, может повышаться при избыточном потреблении углеводов с пищей.
Независимо от пути окисления этанола в организме промежуточным продуктом его распада является ацетальдегид, который обладает сильным токсическим действием. Обычно его концентрация чрезвычайно мала. При употреблении этанола содержание токсичного ацетальдегида несоизмеримо возрастает, что приводит к структурно-
функциональным изменениям в клетках тканей.
Взаимоотношения аэробного и анаэробного путей распада глюкозы
Еще в XIX веке Л. Пастером было открыто явление, получившее
впоследствии название «эффект Пастера» и заключавшееся в том, что дыхание всегда приводит к снижению скорости анаэробного гликолиза, т.е. подавляет брожение. При этом снижается потребление глюкозы и не происходит накопления лактата.
Этот эффект объясняется тем, что:
1.Цитоплазматический НАД!Н+Н+ окисляется с помощью малат- оксалацетатной системы, и в конкуренции за НАД!Н+Н+ с лактатдегид-
рогеназой выигрывает челночный механизм.
2.Фосфофруктокиназа – аллостерический фермент, активность которого стимулируется АДФ, подавляется АТФ и цитратом. При высоком содержании АТФ, характерном для окислительного фосфорилирования, фосфофруктокиназа тормозится.
3.В конкурентной борьбе за АДФ между фосфоглицераткиназой, пируваткиназой и митохондриальной системой окислительного фосфорилирования выигрывает последняя, т.к. обладает более высоким сродством к АДФ. Фосфорилирование АДФ в митохондриях происходит при более низких концентрациях, чем субстратное фосфорилирование в цитоплазме.
Глюконеогенез
В количественном отношении в биосфере одним из важнейших биосинтетических процессов является биосинтез глюкозы и других углеводов. Фотосинтезирующие организмы образуют огромные количества углеводов из СО2 и Н2О (крахмал, целлюлозу и другие полисахариды
из гексоз). В клетках животных организмов синтез углеводов идет из таких предшественников как лактат, аминокислоты, глицерин.
Синтез глюкозы из неуглеводных предшественников – лактата,
159
аминокислот, глицерина (в узком смысле – из аминокислот) называется глюконеогенезом, протекает в печени и корковом веществе почек. В этот процесс могут быть вовлечены вещества, которые способны превратиться в пируват или любой другой метаболит глюконеогенеза. Запасов гликогена в организме достаточно для удовлетворения потребностей в глюкозе в период между приемами пищи. Цель глюконеогенеза – поддержание уровня глюкозы в крови после истощения запасов гликогена в печени при длительной физической работе или длительном голодании. При длительной физической работе субстратами для глюконеогенеза служат лактат, поступающий из мышечной ткани, и глицерин – из жировой ткани. При длительном голодании с этой целью используются аминокислоты, поступающие из мышечной ткани вследствие распада белков, и глицерин – из жировой ткани.
Ворганизме человека и животных после интенсивной мышечной работы активно происходит синтез глюкозы, гликогена из лактата.
Лактат, образовавшийся в мышцах, вымывается кровью и достав-
ляется ею в печень. Превращение пирувата в глюкозу происходит по пути, обратному анаэробному гликолизу. Из 11 реакций гликолиза восемь легко обратимы и используются в глюконеогенезе, но 3 киназ-
ные реакции необратимы: 1) пируваткиназная, 2) фосфофруктокиназная
и3) гексокиназная, в глюконеогенезе они называются обходными путя-
ми гликолиза.
Вцитозоле клеток лактатдегидрогеназой лактат превращается в пировиноградную кислоту, которая транспортируется в митохондрии.
Здесь 1/5 часть ее окисляется до СО2 и Н2О, давая энергию для превра-
щения остальных 4/5 в глюкозу.
Реакция превращения фосфоенолпирувата в пируват, катализи-
руемая пируваткиназой, необратима ( G макроэргической связи фос-
фоенолпирувата – 61,9 кДж/моль). Поэтому для ее преодоления необходима затрата энергии. В митохондриях остальные 4/5 пирувата подвергаются карбоксилированию пируваткарбоксилазой (с коферментом биотином) с затратой АТФ. Образующийся оксалацетат восстанавливается в малат, который с помощью переносчика транспортируется в цитоплазму, где окисляется цитоплазматической малатдегидрогеназой вновь до щавелевоуксусной кислоты. Последняя подвергается декарбоксилированию фосфоенолпируваткарбоксикиназой с участием ГТФ, и образуется фосфоенолпируват. Это первый обходной путь гликолиза.
160
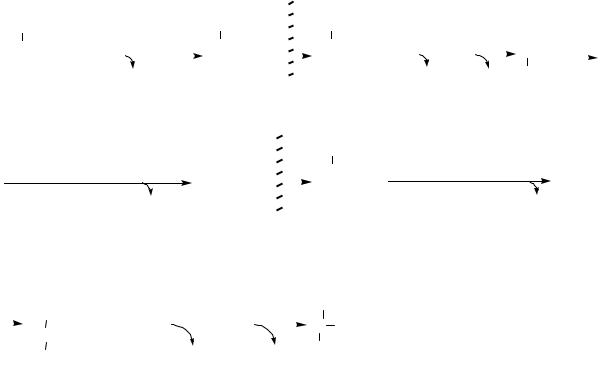
|
|
|
|
+ НАД+ |
Цитоплазма |
|
|
Митохондрия |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
CH3 |
Лактат- |
|
|
CH3 |
|
|
|
CH3 |
Пируваткарбоксилаза |
COOH |
||||||||||||
|
дегидрогеназа |
|
|
|
|
|
|||||||||||||||||
HC |
|
|
OH |
|
C |
|
O |
|
|
C |
|
O |
+ СО2 + АТФ + Mg2+ |
|
|
|
|
|
|||||
|
|
|
|
|
CH2 |
|
|||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
COOH |
НАД!Н+Н+ |
|
COOH |
|
|
COOH |
АДФ + Н3РО4 |
C |
|
O |
||||||||||||
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
||||
|
|
|
|
|
|
|
|
|
|
|
Цитоплазма |
|
|
|
|
щук |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
Малатде- |
|
COOH |
|
|
|
|
|
COOH |
+ НАД+ |
|
|||||||||||||||
|
гидрогеназа |
+НАДН+Н+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 Малатдегидрогеназа |
||||||||||
CH2 |
|
|
|
|
|
||||||||||||||||||||||
|
|
(митохонд- |
НАД+ |
HC |
|
|
|
OH |
|
|
|
|
|
HC |
|
|
|
OH |
(цитоплазма- |
НАД!Н+Н+ |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
риальная) |
|
|
|
|
|
|
|
|
|
|
|
тическая) |
|||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||
COOH |
|
|
|
|
|
|
COOH |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
малат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
COOH |
Фосфоенолпируват- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
карбоксикиназа |
|
|
|
|
|
|
|
CH2 |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
CH2 |
+ГТФ |
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
C O ~ PO3H2 |
|
|||||||||||||||||||
|
|
C |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
COOH |
ГДФ |
СО2 |
COOH |
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
фосфоенолпируват |
|
||||||||
Фосфоенолпируват превращается далее по пути обратному гликолизу при участии тех же ферментов до образования фруктозо-1,6- бисфосфата. Далее следуют необратимые фосфофруктокиназная и гек-
сокиназная реакции. Для их обращения используются специальные ферменты: дефосфорилирование фруктозо-1,6-бисфосфата осуществляется фосфатазой фруктозо-1,6-бисфосфата, глюкозо-6-фосфата – глюко- зо-6-фосфатазой. Это второй и третий обходные пути гликолиза.
Ряд аминокислот, называемых гликопластическими (глицин, аланин, серин, цистеин, треонин, метионин, валин, глютаминовая и аспарагиновая кислоты, аргинин, триптофан, гистидин, пролин), в результате специфических путей превращаются в пируват, щавелевоуксусную или-кетоглутаровую кислоты, которые используются для глюконеогенеза. Глицерин включается в этот процесс на стадии образования 3-
фосфоглицеринового альдегида.
Между распадом глюкозы (гликогена) в мышцах и глюконеогенезом в печени существует тесная взаимосвязь для координации работы этих тканей в интересах всего организма. При распаде гликогена в печени образуется глюкоза, которая кровью доставляется в мышцы, где используется для синтеза гликогена или с энергетической целью при мышечной работе с образованием лактата в анаэробных условиях. Лактат из мышечной ткани кровотоком доставляется в печень, где используется для синтеза глюкозы и гликогена. Этот цикл превращений назван глюкозо-лактатным или циклом Кори.
161
