
стратного фосфорилирования также относится катализируемое сукцинил- КоА-синтетазой (сукцинилтиокиназой) образование ГТФ в цикле Кребса:
СООН |
|
|
|
СООН |
||||
|
|
|
|
|
СН2 |
|
|
|
СН |
|
|
|
|
|
|
||
|
2 |
+ ГДФ + фосфат |
Сукцинил-СоА-синтетаза |
|
СН2 |
+ ГТФ + HS |
|
CoA |
СН |
|
|
||||||
|
|
|
|
|
||||
|
2 |
|
|
|
О |
|
|
|
|
О |
|
|
|
|
|
|
|
С ~ SCoA |
С ОН |
|||||||
Сукцинил-СоА |
Сукцинат |
|||||||
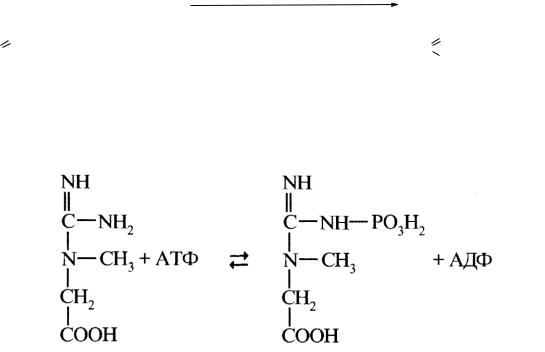
В мышцах в процессе мышечного сокращения активно протекает еще одна реакция субстратного фосфорилирования, катализируемая креатинфосфаткиназой.
Эта реакция обратима и в условиях покоя идет образование креатинфосфата из АТФ и креатина, а в процессе мышечной работы накопленный креатинфосфат отдает фосфорильную группу на АДФ с образованием АТФ, необходимого для процессов мышечного сокращения.
Реакции субстратного фосфорилирования являются важным источником получения АТФ, особенно в анаэробных условиях. Для эукариотов главным источником АТФ является окислительное фофорилирование, использующее энергию электронов, освобождающихся при дегидрировании субстратов, при восстановлении кислорода, через реализацию трансмембранного протонного градиента потенциала.
Дегидрирование субстратов и восстановление кислорода (образование воды) как основной источник энергии для синтеза АТФ
АТФ – чрезвычайно важная молекула клетки. Она непрерывно синтезируется и используется. Энергия для синтеза АТФ поступает от субстратов, отдающих электроны в ходе их дегидрирования. Электроны извлекаются из субстратов в ходе гликолиза и гликогенолиза (в цитозоле), при окислении жирных кислот и в общих путях метаболизма: при преобразовании пирувата в ацетил-КоА и в цикле трикарбоновых кислот (в митохондриальном матриксе). Молекулы НАДН и ФАДН2 переносят эти электроны в дыхательную цепь, локализованную во внутренней митохондриальной мембране. Энергия этих электронов используется для создания трансмембранного протонного градиента потенциала, используемого для синтеза АТФ.
11
ОБЩИЕ ПУТИ КАТАБОЛИЗМА
Общие пути катаболизма начинаются с пирувата, который превращается в молекулу ацетил-СоА под действием сложного мультифетментного пируватдегидрогеназного комплекса в митохондриях. Затем молекула аце- тил-СоА подвергается полному окислению в цикле трикарбоновых кислот, где из двууглеродного фрагмента уксусной кислоты извлекаются 8 электронов. Эти электроны в составе молекул НАДН и ФАДН2 вовлекаются в процесс окислительного фосфорилирования, где синтезируется АТФ и образуется Н2О. К общим путям катаболизма относят: окислительное декарбоксилирование пировиноградной кислоты, цикл трикарбоновых кислот, окислительное фосфорилирование.
Окислительное декарбоксилирование пировиноградной кислоты
Транспорт пирувата. Поступление пирувата в митохондрии (транспорт пирувата) обеспечивает специальная белковая транспортная система, локализованная во внутренней митохондриальной мембране. Пируват поступает в митохондрии из цитозоля совместно с протонами по механизму сопряженного транспорта. Движущей силой при этом является энергия протонного градиента.
Строение пируватдегидрогеназного комплекса. Пируватдегидрогеназный комплекс состоит из 512 субъединиц объединенных в сложный мультиферментный комплекс. В его состав (рис. 3) входят 3 фермента: пируватдегидрогеназа (Е1), дигидролипоамидацилтрансфераза (Е2) и дигидролипоамиддегидрогеназа (Е3), а также 5 коферментов : тиаминдифосфат (ТДФ), липоевая кислота (связанная через свою карбоксильную группу с ε- аминогруппой лизина, входящего в состав фермента – дигидролипоамидацилтрансферазы, и далее называемая липоамид), ФАД, НАД+ и СоА. Три кофермента (ТДФ, липоамид и ФАД) ковалентно связаны в активных центрах ферментов Е1, Е2 и Е3 соответственно, а НАД+ и СоА выполняют роль вторых субстратов в химических реакциях (мигрирующие коферменты).
Особенностью ферментов и белков комплекса является то, что все ферменты и белковые компоненты мультиферментного комплекса кодируются в ядерной ДНК и синтезируются в цитозоле. После их поступления в митохондриальный матрикс (при этом затрачивается энергия АТФ и протонного градиента) они подвергаются финальному фолдингу с помощью митохондриальных шаперонов, приобретают функциональную активность и объединяются в мультиферментный комплекс.
Последовательность реакций в пируватдегидрогеназном комплексе. В этом комплексе происходит преобразование пирувата в ацетил-СоА, содержащий макроэргическую тиоэфирную связь и удаление из пирувата 2-х электронов в составе молекулы НАДН.
Для превращения пирувата в ацетил-СоА необходимы 5 реакций (1-5
12
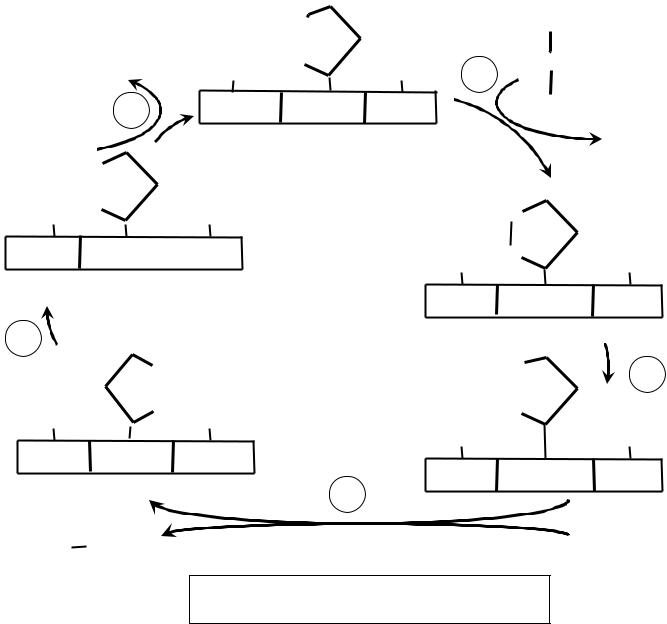
на рис.3). |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
S |
|
|
|
|
|
СООН |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ТДФ |
S |
ФАД |
1 |
С=О |
|
||||
НАДН + Н+ |
|
|
|
|
|
|
|
|||||
|
5 |
Е1 |
|
Е2 |
Е3 |
|
|
|
СООН |
|
||
НАД+ |
|
|
|
|
|
|
|
|
|
|
|
СО2 |
|
S |
|
|
|
|
|
CH3 |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
ТДФ |
S |
ФАДН2 |
|
|
НО |
|
|
СН |
S |
|
||
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Е1 |
|
Е2 |
Е3 |
|
|
|
|
ТДФ |
S |
ФАД |
||
|
|
|
|
|
|
|
|
|
Е1 |
Е2 |
Е3 |
|
4
|
SH |
|
|
О HS |
|
2 |
|
|
|
|
|
║ |
|
||
|
|
|
|
|
|
||
ТДФ |
SH |
ФАД |
CH3 |
|
C ~ S |
|
|
|
|
|
|||||
|
|
|
ТДФ |
|
ФАД |
||
Е1 |
Е2 |
Е3 |
|
|
|
|
|
|
|
|
|
Е1 |
Е2 |
Е3 |
|
|
O |
|
3 |
|
|
|
|
|
║ |
|
|
|
|
|
|
CH3 |
C ~ S-СоА |
|
|
|
|
|
СоА-SH |
Рис.3 Реакции пируватдегидрогеназного
комплекса
1. Реакция декарбоксилирования пирувата.
Значение декарбоксилирования пирувата для извлечения энергии из молекулы исключительно велико. Три углеродных атома пирувата имеют разную степень окисления. Углерод метильной группы (-СН3) имеет степень окисления –3 и, следовательно, в дальнейшем при его окислении до СО2 (С+4) можно получить 7 электронов. Углерод кето-группы (›С=О) окислен значительно (степень окисления +2) при его окислении до СО2 можно извлечь 2 электрона. А углерод карбоксильной группы окислен почти полностью (+3). Поэтому карбоксильная группа это до некоторой степени балластная часть молекулы с позиции извлечения энергии, окисление этого углерода может дать лишь 1 электрон. Удаление карбоксильной группы (т.е. реакцию декарбоксилирования) катализирует фермент пируватдегидрогеназа в активном
13
центре которого локализован тиаминдифосфат – кофермент декарбоксилирования.
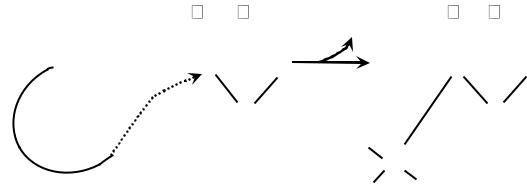
1.В активном центре фермента происходит прямое взаимодействие двух атомов углерода с образованием между ними ковалентной связи. Это взаимодействие обусловлено разноименностью зарядов, которыми обладают углерод кето-группы пирувата с одной стороны и атом углерода тиазольного кольца тиаминпирофосфата с другой.
2.На этой стадии Е1 (пируватдегидрогеназа) переносит атом водорода
идвухуглеродный ацетильный фрагмент (СН3-СО-) на молекулу липоевой кислоты, локализованную в активном центре фермента Е2 (дигидролипоамидацетилтрансферазы). При этом в активном центре фермента образуется ацетилтиоэфир липоамида, а восстановление при этом липоамида способствует извлечению еще 1 электрона (от 2-го углеродного атома пирувата.
СН3 |
N+ |
|
СО2 |
N+ |
| |
║ |
|
|
║ |
+δС=О-δ |
+ - C |
|
|
C |
| |
Н+ |
|
|
|
СООН |
S |
|
S |
|
|
|
|
СН3 |
|
|
|
|
С |
|
|
|
|
НО |
Н |
|
Фрагмент |
|
|
|
Пируват |
тиазольного |
Промежуточное соединение в |
||
|
кольца |
активном центре фермента |
||
Рис.4 Схема реакции декарбоксилирования пирувата
3.В этой реакции СоА-SH атакует тиоэфирную связь в активном центре
фермента Е2, разрывает еѐ и присоединяет к себе двухуглеродный ацетильный фрагмент (СН3-СО-). Происходит образование ацетил~СоА, который покидает активный центр фермента Е2 (дигидролипоамидацетилтрансферазы). При этом оба атома серы липоевой кислоты полностью восстановлены.
4.В этой реакции фермент Е3 (дигидролипоамиддегидрогеназа) катализирует перенос двух атомов водорода с восстановленного липоамида, нахо-
дящегося в активном центре фермента Е2 на кофермент ФАД, локализованный в своѐм активном центре. При этом в активном центре фермента Е3 образуется ФАДН2.
5.В активный центр дегидрогеназы (Е3) пируватдегидрогеназного комплекса входит НАД+ и присоединяет к себе 2 электрона и протон от кофермента ФАДН2 и в форме НАДН переносит их в процесс окислительного фос-
14
форилирования.
Связь окислительного декарбоксилирования пирувата с процессом окислительного фосфорилирования
При превращении пирувата в ацетил-СоА происходит образование НАДН, транспортирующего электроны в дыхательную цепь. Пара электронов в процессе окислительного фосфорилирования может участвовать в синтезе АТФ с образованием до 2,5 моль АТФ на 2 моль электронов. Усиление распада АТФ в клетке ведет к повышению концентрации АДФ и ускорению окисления НАДН в дыхательной цепи. Повышение концентрации НАД+, в свою очередь, стимулирует окислительное декарбоксилирование пирувата. Напротив, повышение концентрации АТФ и НАДН снижает скорость этого процесса.
Таким образом, изменения отношений АДФ/АТФ и НАДН/НАД+ - важнейшие внутриклеточные регуляторные сигналы, отражающие энергетические потребности клетки и регулирующие скорость окислительного декарбоксилирования пирувата. Каталитическая активность пируватдегидрогеназного комплекса снижается, когда в клетках имеется достаточно ―топлива‖ в виде жирных кислот и ацетил~СоА.
Регуляция пируватдегидрогеназного комплекса (ПДК)
Регуляция пируватдегидрогеназного комплекса (ПДК) имеет важное значение для обеспечения цикла трикарбоновых кислот ―топливными‖ молекулами ацетил-СоА. Точная регуляция этого комплекса имеет важное значение в связи с невозможностью обратного преобразования ацетил-СоА в пируват, т.к. ферменты, необходимые для этого в организме человека отсутствуют.
Активность ПДК регулируется различными способами: доступностью субстратов, ингибированием продуктами реакции, аллостерическим путѐм, путѐм ковалентной модификации (табл. 2).
Активность пируватдегидрогеназного комплекса увеличивается при повышении концентрации АДФ, внутриклеточного кальция, под влиянием гормонов: инсулина и адреналина.
При повышении концентрации АДФ ПДК находится в нефосфорилированной активной форме. Этот эффект усиливается при повышении концентрации внутриклеточного кальция, который активирует фосфатазу ПДК. Такой механизм активации ПДК особенно важен в мышцах и жировой ткани. Активация ПДК происходит также под влиянием инсулина. Один из эффектов инсулина – повышение концентрации внутримитохондриального кальция, это приводит к активированию ПДК. В клетках миокарда ПДК активируется адреналином.
15
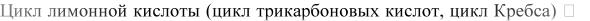
Табл. 2 Регуляция активности пируватдегидрогеназного комплекса
Ковалентная |
Осуществляется фосфорилированием и дефосфорилиро- |
модификация: |
ванием. |
|
В состав ПДК входят 2 регуляторных субъединицы: ки- |
|
наза ПДК – фосфорилирует ферменты комплекса и |
|
инактивирует ПДК; а фосфатаза – дефосфорилирует |
|
ферменты, превращая ферментативный комплекс в ак- |
|
тивную форму. |
Ингибирование |
Продукты пируватдегидрогеназной реакции аллостери- |
продуктами |
чески активируют киназу ПДК. Активированная киназа |
реакции: |
фосфорилирует и инактивирует ферменты комплекса. |
|
Таким образом, при накоплении НАДН и ацетил-СоА |
|
тормозится превращение пирувата в ацетил-СоА. Так, |
|
например, в печени при голодании: |
|
- из жирового депо в печень поступают жирные кисло- |
|
ты, из которых образуется ацетил-СоА; |
|
- в присутствии высокомолекулярных жирных кислот |
|
ингибирование ПДК усиливается. Пируват при этом не |
|
окисляется и может быть использован для синтеза глю- |
|
козы (в процессе глюконеогенеза). |
Аллостерический |
Пируват аллостерически активирует нефосфорилиро- |
путь: |
ванную форму ПДК, действуя согласно с другими суб- |
|
стратами НАД+ и СоА. |
|
Цикл лимонной кислоты |
заключительный этап катаболизма, локализованный в матриксе митохондрий. В нем 4-х углеродное соединение оксалоацетат конденсируется с 2-х углеродным ацетильным компонентом, который вносит в процесс молекула ацетил-СоА, с образованием 6-ти углеродной трикарбоновой кислоты (цитрата). Далее цитрат подвергается изомеризации и окислению с последующим декарбоксилированием (не путать с окислительным декарбоксилированием) образовавшегося оксалосукцината.
Образующееся при этом 5-ти углеродное соединение α-оксоглутарат (α-кетоглутарат) при окислительном декарбоксилировании превращается в 4- х углеродное соединение сукцинат. Дальнейшие превращения сукцината приводят к регенерированию оксалоацетата. Поэтому одна молекула оксалоацетата может многократно использоваться для окисления ацетильных остатков. Два атома углерода включаются в цикл в виде ацетильного компонента и 2 атома углерода покидают цикл в виде двух молекул СО2.
Таким образом, двухуглеродный фрагмент молекулы ацетил-СоА подвергается полному окислению. 8 электронов, ранее принадлежащих молекуле ацетил~СоА, покидают цикл в связанной форме: в виде трех молекул НАДН
16
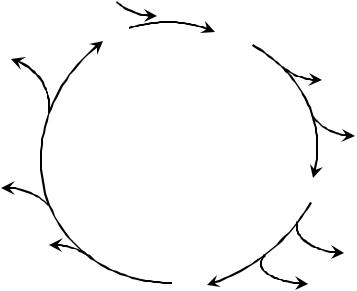
и одной ФАДН2. Затем они переносятся в процесс окислительного фосфорилирования, где энергия каждой пары электронов переносимых НАДН, преобразуется в энергию макроэргических связей – до 2,5 моль АТФ на 2 моль электронов. А энергия пары электронов переносимых ФАДH2, ведет к образованию до 1,5 моль АТФ на 2 моль электронов. Всего в процессе окислительного фосфорилирования при окислении этих переносчиков электронов образуется до 9 молекул АТФ. Одна макроэргическая связь генерируется в самом цикле в форме молекулы ГТФ (равноценной АТФ). Итого, теоретически до 10 моль АТФ может быть генеририровано при окислении 1 моль двухуглеродного фрагмента ацетил~КоА в цикле трикарбоновых кислот сопряженном с процессом окислительного фосфорилирования.
|
Цикл трикарбоновых кислот - циклический |
|
биохимической процесс был открыт в 1937 |
C2 |
году Гансом Кребсом и А. Сент Дьерди |
|
|
|
|
С4 |
С6 |
НАДН |
НАДН |
|
CO2 |
ФАДH2 |
С5 |
ГТФ |
НАДН |
С4 |
CO2 |
Рис. 5 Схема цикла трикарбоновых кислот. В цикл входят молекулы ацетил~СоА, а покидают 8 электронов на своих мобильных переносчиках в составе НАДН и ФАДН2.
Реакции цикла трикарбоновых кислот
1.Реакция образования цитрата (лимонной кислоты). Эта реакция представляет собой альдольную конденсацию с последующим гидролизом, которую катализирует цитрат-синтаза. При расщеплении тиоэфирной связи освобождается коэнзим А и выделяется значительная тепловая энергия. Равновесие в реакции сильно сдвинуто вправо.
2.Превращение цитрата в изоцитрат. Изомеризация цитрата осуществляется путем дегидратации с последующей гидратацией. В результате происходит взаимоперемещение Н и ОН. Фермент назван аконитазой, поскольку промежуточное соединение цис-аконитат не покидает активный центр фермента.
17
3. Реакция окисления изоцитрата катализируется изоцитратдегидрогеназой, сопровождается декарбоксилированием образующегося оксалосукцината и ведет к образованию α-оксоглутарата (α-кетоглутарата). НАД+ в реакции играет роль второго субстрата захватывая пару электронов и в форме НАДН вовлекает их в процесс окислительного фосфорилирования. Самая медленная реакция цикла. Аллостерически активируется АДФ.
1. РЕАКЦИЯ КОНДЕНСАЦИИ. |
|
|
|
||
|
О |
|
|
СН2—СОО- |
|
|
║ |
|
|
│ |
|
О═С—СОО- + С—СН3 + Н2О |
НО—С—СОО-+ HS—КоА + H+ |
||||
│ |
│ |
ЦИТРАТ- |
|
│ |
|
Н2С—СОО- S—СоА |
СИНТАЗА |
СН2—СОО- |
|
||
ОКСАЛО- АЦЕТИЛ-CoA |
|
ЦИТРАТ |
|
||
АЦЕТАТ |
|
|
|
|
|
2. ПРЕВРАЩЕНИЕ ЦИТРАТА В ИЗОЦИТРАТ |
|
|
|||
СОО- |
|
СОО- |
|
СОО- |
|
│ |
Н2О |
│ |
Н2О |
│ |
|
Н—С—Н |
|
Н—С |
|
Н—С—ОН |
|
│ |
|
║ |
|
|
│ |
-ООС—С—ОН |
|
-ООС—С |
|
-ООС—С—Н |
|
│ |
АКОНИТАЗА |
│ |
АКОНИТАЗА |
│ |
|
СН2 |
|
СН2 |
|
|
СН2 |
│ |
ДЕГИДРАТАЦИЯ │ |
ГИДРАТАЦИЯ |
│ |
||
СОО- |
|
СОО- |
|
СОО- |
|
ЦИТРАТ |
ЦИС-АКОНИТАТ |
ИЗОЦИТРАТ |
|||
3. РЕАКЦИЯ ОКИСЛЕНИЯ ЦИТРАТА |
|
|
|
||
СОО- |
+ H+ |
СОО- |
|
|
СОО- |
│ |
NAD+ NADH |
│ |
H+ |
CO2 |
│ |
Н—С—Н |
Н—С—Н |
|
Н—С—Н |
||
│ |
|
│ |
|
|
│ |
Н—С—СОО- |
Н—С—СОО- |
|
Н—С—Н |
||
│ |
|
│ |
|
|
│ |
Н—С—ОН |
|
С=О |
|
|
С=О |
│ |
|
│ |
|
|
│ |
СОО- |
|
СОО- |
|
|
СОО- |
ИЗОЦИТРАТ |
ОКСАЛОСУКЦИНАТ |
α-ОКСОГЛУТОРАТ |
|||
ФЕРМЕНТ – ИЗОЦИТРАТ-ДЕГИДРОГЕНАЗА
4. РЕАКЦИЯРис.6ОКИСЛИТЕЛЬНОГО. Начальные реакции циклаДЕКАРБОКСИЛИРОВАНИЯтрикарбоновых кислот
18
4. Реакция катализируется α-оксоглутарат дегидрогеназным комплексом (мультиферментный комплекс), который структурно и функционально сходен с пируватдегидрогеназным комплексом. Механизм этой реакции сходен с механизмом превращения пирувата в ацетил-СоА. В состав комплекса
также входят 5 коферментов: тиаминдифосфат (ТДФ), липоамид, ФАД, НАД+ и СоА.
α-ОКСОГЛУТОРАТ + NAD+ + КоА  СУКЦИНИЛ~КоА + CO2 + NADH
СУКЦИНИЛ~КоА + CO2 + NADH
α-ОКСОГЛУТОРАТ ДЕГИДРОГЕНАЗНЫЙ КОМПЛЕКС
α-Оксоглутарат-дегидрогеназный комплекс отличается от пируватде- гидрогеназного комплекса тем, что в нем отсутствует сложная система регуляции активности. Равновесие реакции сильно сдвинуто вправо, в сторону образования сукцинил~СоА. Биохимическое значение реакции состоит в удалении карбоксильной группы (–СОО-) поскольку атом углерода в ней почти полностью окислен, тем не менее при ее декарбоксилировании извлекаются 2е- при превращении ее в молекулу углекислого газа.
5. РЕАКЦИЯ СУБСТРАТНОГО ФОСФОРИЛИРОВАНИЯ
СУКЦИНИЛ~СоА + Ф + ГДФ  СУКЦИНАТ + ГТФ + СоА
СУКЦИНАТ + ГТФ + СоА
СОО- |
|
СОО- |
|
│ |
|
│ |
|
СН2 |
|
СН2 |
|
│ |
+ Ф + ГДФ |
│ |
+ ГТФ + СоА-SH |
СН2 |
|
СН2 |
|
│ |
|
│ |
|
С═О |
|
СОО- |
|
ς |
|
|
|
S-СоА
ФЕРМЕНТ – СУКЦИНАТТИОКИНАЗА (СУКЦИНИЛ-СоА-СИНТЕТАЗА)
Рис.7 Реакция субстратного фосфорилирования
5. В этой реакции для синтеза ГТФ используется энергия молекулы сукцинил-СоА. Энергия разрыва тиоэфирной связи в молекуле сукцинилСоА всего на 9% превышает ту энергию, которая необходима для фосфорилирования ГДФ с образованием ГТФ. Поэтому реакция легко обратима. Однако равновесие процесса сдвинуто вправо, поскольку ГТФ далее входит в
19
реакцию переноса своей фосфатной группы на АДФ с образованием АТФ, который расходуется в клеточных процессах.
ГТФ + АДФ ↔ ГДФ + АТФ
Эту реакцию катализирует нуклеозидфосфаткиназа.
На этом заканчивается первая стадия цикла трикарбоновых кислот.
ВТОРАЯ СТАДИЯ ЦИКЛА ТРИКАРБОНОВЫХ КИСЛОТ: (РЕГЕНЕРИРОВАНИЕ ОКСАЛОАЦЕТАТА)
|
|
|
6. |
|
7. |
8. |
|
СОО- |
|
СОО- |
|
СОО- |
НАДН |
СОО- |
|
│ |
ФАД |
ФАДH2 │ |
Н2О |
│ НАД+ + H+ |
│ |
||
СН2 |
|
С—Н |
|
НO—С—Н |
|
С═О |
|
│ |
|
║ |
|
│ |
|
│ |
|
СН2 |
|
Н—С- |
|
Н—С—Н |
|
СН2 |
|
│ |
|
│ |
|
│ |
|
│ |
|
СОО- |
|
СОО- |
|
СОО- |
|
СОО- |
|
СУКЦИНАТ |
ФУМАРАТ |
|
МАЛАТ |
ОКСАЛОАЦЕТАТ |
|||
6. |
РЕАКЦИЯ ОКИСЛЕНИЯ |
(СУКЦИНАТ-ДЕГИДРОГЕНАЗА) |
|||||
7. |
РЕАКЦИЯ ГИДРАТАЦИИ |
|
(ФУМАРАЗА) |
|
|
||
8. |
РЕАКЦИЯ ОКИСЛЕНИЯ |
|
(МАЛАТ - ДЕГИДРОГЕНАЗА) |
||||
Рис. 8 Реакции второй стадии цикла трикарбоновых кислот
6.Фермент сукцинат-дегидрогеназа, действующий в 6-й реакции – флавопротеин, содержащий ковалентно присоединенный ФАД в своем активном центре. В отличие от других ферментов цикла трикарбоновых кислот сукци- нат-дегидрогеназа прочно закреплена во внутренней митохондриальной мембране. Фермент состоит из двух субъединиц, одна из которых содержит ФАД. В состав двух субъединиц включены железо-серные центры. В одной
субъединице в форме - Fe2S2, а в другой в форме – Fe4S4. Оба железо-серных центра сопряжены с компонентами дыхательной цепи и участвуют в транспорте электронов.
7.Реакцию гидратации катализирует фермент фумарат-гидратаза (фумараза), локализованный в матриксе митохондрий. Особенностью реакции является абсолютная субстратная специфичность этого фермента. Фермент катализирует гидратацию только транс-формы фумарата.
8.Заключительную реакцию цикла трикарбоновых кислот катализирует НАД-зависимая малат-дегидрогеназа, локализованная в митохондриальном матриксе. Особенность реакции состоит в том, что в ней равновесие сильно сдвинуто влево.
Поскольку оксалоацетат, синтезируемый в этой реакции постоянно расходуется на образование цитрата (цитрат-синтазная реакция), то в интактных
20
