
4 курс / Акушерство и гинекология / Гинекология 2010 №01
.pdf
И Н Ф Е К Ц И О Н Н О - В О С П А Л И Т Е Л Ь Н Ы Е З А Б О Л Е В А Н И Я В А М Б У Л АТ О Р Н О Й П РА К Т И К Е
|
лах живота (96,2%), тошноту (43,0%), |
ем симптомов и нарушением репроду- |
Т-хелперов (CD4), Т-супрессоров |
||||
|
гноевидные выделения из половых пу- |
ктивной функции. |
(CD8), а также хелперно-супрессорно- |
||||
|
тей (43,8%), повышение температуры |
В первые дни с начала лечения ско- |
го отношения (Тх/Тс), кроме субпопу- |
||||
|
тела до 38°С (34,1%). Среди сопутству- |
рость купирования обострения воспа- |
ляции нормальных киллеров (CD16), |
||||
|
ющих и ранее перенесенных экстра- |
лительного процесса, ассоциирован- |
доля которых была увеличена, и суб- |
||||
|
генитальных заболеваний у обследо- |
ного с хламидийной инфекцией, в |
популяции В-клеток (CD19), числен- |
||||
|
ванных наиболее часто встречались |
обеих группах (основной и контроль- |
ность которой была нормальной |
||||
|
хронический гастрит, цистит, тонзил- |
ной) была одинаковой, но уже начи- |
(табл. 2). |
||||
|
лит, что свидетельствует о наличии в |
ная с 3-х суток больных с выраженной |
После проведенной терапии в ос- |
||||
|
организме больных нескольких оча- |
положительной динамикой в 1-й груп- |
новной группе соотношение Тх/Тс |
||||
|
гов инфекции и возможности их взаи- |
пе было больше, чем во 2-й (56,1 и |
увеличилось, что, по-видимому, обу- |
||||
|
модействия. |
44,8% соответственно). |
словлено иммунокорригирующим |
||||
|
В группе женщин с сальпингоофо- |
Согласно полученным данным на- |
влиянием Кипферона®. В группе срав- |
||||
|
ритом, ассоциированным с хламидия- |
рушения в ИФН-статусе у женщин с |
нения отмечено снижение значений |
||||
|
ми, нарушения менструальной функ- |
воспалительными заболеваниями вну- |
соотношения Тх/Тс (см. табл. 2). |
||||
|
ции отмечались в среднем в 30% слу- |
тренних половых органов, ассоции- |
С целью оценки гуморального звена |
||||
|
чаев, что, возможно, связано с наруше- |
рованными с хламидиями, довольно |
иммунитета, перед началом лечения |
||||
|
нием функции яичников на фоне хро- |
значительны, тяжело поддаются имму- |
было выявлено, что концентрация IgG |
||||
|
нического воспалительного процесса. |
нокоррекции и выражаются в наруше- |
и IgА в сыворотке крови не выходила |
||||
|
Гинекологическая заболеваемость в |
нии индуцированной продукции α- и |
за пределы нормы, в отличие от уров- |
||||
|
группе больных женщин была выше, |
γ-ИФН (табл. 1). У женщин, обследо- |
ня IgM, который был повышен. Как из- |
||||
|
чем в группе здоровых. Выше была ча- |
ванных в ходе данного исследования, |
вестно, увеличение концентрации IgM |
||||
|
стота как заболеваний, непосредст- |
индуцированная продукция α- и γ- |
связывают с острым воспалительным |
||||
|
венно связанных с хроническим вос- |
ИФН была резко снижена (α-ИФН в |
процессом. В нашем исследовании на |
||||
|
палительным процессом в органах ма- |
11–14 раз, γ-ИФН в 15–19 раз). |
фоне лечения в обеих группах проис- |
||||
|
лого таза (бесплодие, эндометрит, |
Все взятые под наблюдение женщи- |
ходило снижение концентрации это- |
||||
|
трубная беременность), так и опосре- |
ны имели устойчиво низкий уровень |
го иммуноглобулина: в 1-й группе до |
||||
|
дованно связанных с хроническим |
ИФН в крови. |
нормальных значений, во 2-й остава- |
||||
|
воспалением (нарушения менструаль- |
По показателям иммунного статуса |
лось несколько повышенным (табл. 3). |
||||
|
ной функции, апоплексия яичника, эк- |
группы обследованных женщин зна- |
Особое внимание в нашей работе |
||||
|
топия шейки матки). |
чительно отличались. У больных как |
было уделено изучению состояния ло- |
||||
|
У всех обследованных пациенток |
основной, так и контрольной группы |
кального иммунитета в цервикальном |
||||
|
наблюдалась типичная картина обост- |
по сравнению со здоровыми женщи- |
канале, который рассматривался в ка- |
||||
|
рения хронического двустороннего |
нами определялось снижение относи- |
честве одного из основных защитных |
||||
|
сальпингоофорита, который в боль- |
тельной и абсолютной численности |
барьеров человеческого организма на |
||||
|
шинстве случаев проявился сочетани- |
лимфоцитов в целом, Т-клеток (CD3), |
пути инфекционных агентов. |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
И Н Ф Е К Ц И О Н Н О - В О С П А Л И Т Е Л Ь Н Ы Е З А Б О Л Е В А Н И Я В А М Б У Л АТ О Р Н О Й П РА К Т И К Е
Полученные нами средние значения иммуноглобулинов цервико-вагиналь- ного секрета у здоровых женщин не имели значительных отклонений от аналогичных показателей, указанных в литературе. Так, средние значения IgG составили 138±25 мкг/мл, IgM 5,9±0,2 мкг/мл, IgА 74,2±6,1 мкг/мл, секреторного IgA 174,2±36,3 мкг/мл (табл. 4).
При оценке состояния локального иммунитета у женщин с обострением хронического двустороннего сальпингоофорита перед началом терапии было установлено, что в обеих об-
следуемых группах уровень IgG был повышен: в 2,1 раза – в 1-й и в 2,6 раза
– во 2-й группе по сравнению с уровнем, зарегистрированным у здоровых женщин.
При обострении хронического сальпингоофорита концентрация основного иммуноглобулина секретов слизистых оболочек – секреторного IgA снижалась в 5–6 раз по сравнению со значениями в группе здоровых женщин. Скорее всего, угнетение продукции секреторного IgA в нашем исследовании было связано с длительно
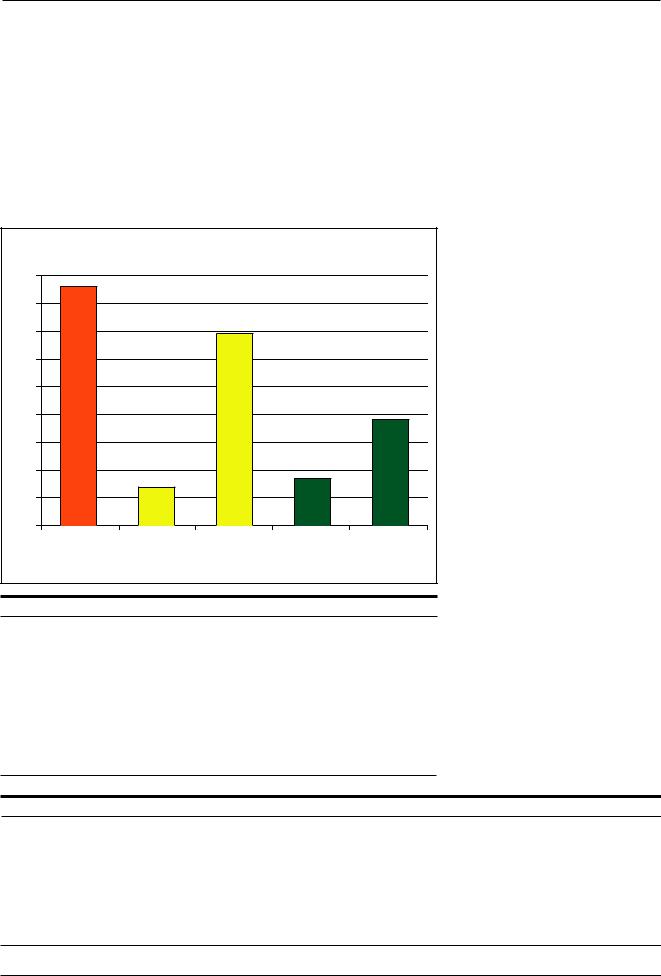
Динамика содержания секреторного IgA в секрете шейки матки. |
|
|||
мкг/мл |
|
|
|
|
180 |
|
|
|
|
160 |
|
|
|
|
140 |
|
* |
|
|
120 |
|
|
|
|
|
|
|
|
|
100 |
|
|
|
|
80 |
|
|
|
|
60 |
|
|
|
|
40 |
|
|
|
|
20 |
|
|
|
|
0 |
|
|
|
|
Здоровые |
Основная |
Основная |
Контрольная |
Контрольная |
|
группа |
группа |
группа |
группа |
|
до лечения |
после лечения |
до лечения |
после лечения |
Таблица 3. Динамика содержания иммуноглобулинов в сыворотке крови больных (M±m) |
||||
Группа |
Число пациенток |
|
иммуноглобулины, МЕ/мл |
|
|
|
|
|
|
|
|
IgG |
IgM |
IgA |
|
|
|
|
|
Здоровые |
30 |
135±25 |
192±12,8 |
125±20 |
Основная |
|
|
|
|
до лечения |
60 |
128±20 |
281±43* |
122±19 |
после лечения |
60 |
106±20 |
193±37** |
77±28 |
Контрольная |
|
|
|
|
до лечения |
40 |
125±26 |
300±25* |
126±20 |
после лечения |
40 |
109±19 |
211±70** |
111±34 |
|
|
|
|
|
*p<0,05 по сравнению со здоровыми обследованными. **p<0,05 по сравнению с показателем до лечения.
текущим хроническим воспалительным процессом.
На фоне лечения уровень секреторного IgA увеличивался. В 1-й группе отмечено увеличение концентрации секреторного IgA с 28±3,2 до 138±16,4 мкг/мл (р<0,05), во 2-й группе – с 34±4,8 до 76±10,2 мкг/мл (р<0,05). При этом уровень увеличения секреторного IgA в основной группе был существенно выше (р<0,05). Полученные данные позволяют считать эффективным применение Кипферона® в комплексном лечении хронического воспалительного процесса (см. рисунок).
Результаты исследования микрофлоры цервикального канала и влагалища свидетельствуют об эффективности лечения. Так, в основной группе после проведенной терапии с добавлением Кипферона® хламидии в цервикальном канале методами ПЦР и ПИФ-диагностики не выявлялись, а в контрольной группе их количество уменьшилось до 22,7%.
При изучении динамики изменения бактериологических показателей содержимого влагалища на фоне лечения было установлено, что после проведенного лечения в обследуемых группах произошли существенные изменения в составе микрофлоры влагалища. У больных, получавших помимо традиционной терапии Кипферон®, после лечения был выявлен значимый рост нормальной микрофлоры влагалища без применения эубиотиков. Нормализация уровня лактобактерий произошла у 58% пациенток, у 37% женщин их количество увеличилось до 104–106 KOE/мл. У пациенток 2-й группы уровень лактобактерий нормализовался только в 20% случаев, а повысился до 104–106 КОЕ/мл – у 10% женщин (р<0,05).
Установлено, что максимальный терапевтический эффект получен у пациенток 1-й группы: клиническое выздоровление при применении Кипферона® в комплексе с традиционной терапией составило 92,6% случаев, во 2-й группе данный показатель составил 78,9%, что было достоверно ниже (р<0,05).
Таким образом, результаты нашего исследования свидетельствуют о том, что у больных с обострением хронического двустороннего сальпингоофорита, ассоциированного с хлами-
Таблица 4. Содержание иммуноглобулина в секрете шейки матки (M±m)
Группа |
Число пациенток |
|
Иммуноглобулины, МЕ/мл |
|
|
|
|
|
|
|
|
|
|
IgG |
IgM |
IgA |
SIgA |
|
|
|
|
|
|
Здоровые |
30 |
140±25 |
6,3±0,2 |
73±5,9 |
172±32,5 |
Основная |
|
|
|
|
|
до лечения |
60 |
301±32* |
63±8* |
275±47* |
28±2,5* |
после лечения |
60 |
272±28 |
41±5,4** |
259±43 |
138±18*** |
Контрольная |
|
|
|
|
|
до лечения |
40 |
394±68* |
72±11,3* |
433±72* |
34±5* |
после лечения |
40 |
366±60 |
36±4,4** |
608±52** |
76±9** |
*p<0,05 по сравнению со здоровыми обследованными. **p<0,05 по сравнению с показателем до лечения. ***p<0,05 по сравнению с показателем в контрольной группе.
32 ГИНЕКОЛОГИЯ | ТОМ 12 | №1

И Н Ф Е К Ц И О Н Н О - В О С П А Л И Т Е Л Ь Н Ы Е З А Б О Л Е В А Н И Я В А М Б У Л АТ О Р Н О Й П РА К Т И К Е
дийной инфекцией, имеются выраженные нарушения как системного, так и локального иммунитета шейки матки. Включение в комплексную терапию этих пациентов иммунобиологического препарата Кипферон® позволяет получить хороший терапевтический эффект.
Литература 1. Антонова Л.В., Прозоровская К.Н., Семенова И.В.,
Шаткин А.А. Исследование иммунного статуса у больных острыми воспалительными заболеваниями придатков матки, ассоциированных с разными комбинациями микроорганизмов. Журн. микробиол. эпидемиол. иммунобиол. 1996; 1: 49–53.
2.Зулькарнеев Р.Ш. Лечение хламидиоза у беремен-
ных сочетанием рекомбинантного α2-интерфе- рона с КИП. Автореф. дис. ... канд. мед. наук. М., 1997.
3.Исаков В.А. и др. Терапия урогенитального хламидиоза (руководство для врачей). СПб.–Великий Новгород, 2004.
4.Баткаев Э.А., Липова Е.В. Урогенитальный хламидиоз. М., 2004.
5.Копанев Ю.А., Соколов А.Л., Кузьменко Л.Г. Эффективность и безопасность использования комплексного иммуноглобулинового препарата (КИП) для коррекции дисбактериозов кишечника и лечения острых кишечных инфекций у детей. Пробле-
мы инфекционных болезней. Сборник, посвященный 140-летию со дня рождения Г.Н.Габричевского. Ч. 2. 2000; с. 149–54.
6. Малышева З.В., Цветаева Т.Ю., Поспелова В.В., Ворошилина Н.Н. Микробные и иммуноглобулиновые
препараты в комплексной терапии воспалительных процессов женской половой сферы. Сборник научн. трудов МНИИЭМ им. Г.Н.Габричевского. М., 1996; 2: 138–41.
7.Цветаева Т.Ю., Малышева З.В., Послелова В.В. и др. КИП и формы его применения в терапии воспалительных заболеваний в гинекологии. Тезисы докладов Всероссийской научно-практической конференции «Дисбактериозы и зубиотики». Москва, 26–28 марта. М., 1996.
8.Шайков К.А. Состояние локального иммунитета шейки матки при воспалительных заболеваниях органов малого таза и методы его коррекции иммуномодулятором Кипферон. Автореф. дис. ... канд. мед. наук. М., 2005.
9.Bard E, Riethmuller D, Biichle S et al. Validation of a high sensitive immunoenzymatic assay to establish the origin of immunoglobulins in female genital secretions. J Immunoassay Immunochem 2002; 23 (2): 145–62.
О роли модуляции кислотности влагалищной жидкости в терапии
бактериального вагиноза
О.Л.Молчанов, Ю.Л.Тимошкова, В.Г.Абашин Кафедра акушерства и гинекологии им. А.Я.Крассовского Военно-медицинской академии
им. С.М.Кирова (зав. каф. – проф. В.Г.Абашин), Санкт-Петербург
Бактериальный вагиноз (БВ) стойко занимает одно из ведущих мест
в структуре инфекционно-воспали- тельных и дисбиотических заболеваний влагалища. Ежегодная отчетная статистика по данной проблеме высока и согласно ей не прослеживается тенденции к снижению показателей. Подобная динамика существует, несмотря на то что фармацевтическая промышленность оснастила врачей препаратами, действие которых более или менее универсально в отношении микроорганизмов, ассоциированных с БВ. В основном препараты имеют антибактериальную направленность, избирательно или поливалентно подавляя рост микроорганизмов. Другой реабилитационной составляющей терапевтических схем являются препараты пробиотического ряда, способствующие восстановлению резидентной ацидофильной микрофлоры влагалища. Возникает вопрос: почему проблема до настоящего времени не решена?
С позиций теории о «микроэкосистеме влагалища» микробный пейзаж определяется многими составляющими, такими как функциональная активность эпителия, состав влагалищной жидкости, факторы местного иммунитета, продукты микробного метаболизма.
Одним из ключевых звеньев патогенеза БВ является повышение рН влагалищной жидкости. Длительное время считалось и считается, что данный показатель определяется метаболической активностью резидентных штаммов лактобактерий. Тем не менее установлено, что влагалищный эпителий обладает, подобно эпителию почечных канальцев, карбоангидразной ак-
тивностью. Особенность данного |
рованных с БВ строгих анаэробных |
фермента заключается в его способ- |
микроорганизмов обладают цитоток- |
ности регулировать концентрацию |
сическим действием и нарушают регу- |
водородных ионов и осмолярность |
ляторную активность эпителия влага- |
влагалищной жидкости. |
лища. |
Доказано, что биогенные амины, ко- |
Возможно по этой причине исполь- |
роткоцепочечные жирные кислоты, |
зование микробных трансплантатов, |
специфические метаболиты ассоции- |
особенно при длительном течении за- |
Таблица 1. Степень выраженности аминового теста до лечения препаратом Вагинорм-С
Степень выраженности аминового теста |
Группа 1-я (n=15) |
Группа 2-я (n=15) |
|
|
|
1-я |
1 |
0 |
2-я |
13 |
0 |
3-я |
1 |
15 |
|
|
|
Таблица 2. Процент ключевых клеток до лечения препаратом Вагинорм-С
Процент ключевых клеток |
Группа 1-я (n=15) |
Группа 2-я (n=15) |
|
|
|
20–50 |
13 |
0 |
51–80 |
2 |
6 |
81–100 |
1 |
9 |
|
|
|
Таблица 3. Выраженность аминового теста после лечения препаратом Вагинорм-С (7–9-й день)
Степень выраженности показателя |
Группа 1-я (n=10) |
Группа 2-я (n=11) |
|
|
|
1-я |
8 |
7 |
2-я |
2 |
3 |
3-я |
0 |
1 |
|
|
|
Таблица 4. Процент ключевых клеток после лечения препаратом Вагинорм-С (7–9-й день)
Процент ключевых клеток |
Группа 1-я (n=10) |
Группа 2-я (n=11) |
|
|
|
0–19 |
8 |
8 |
20–50 |
2 |
2 |
51–80 |
0 |
1 |
81–100 |
0 |
0 |
|
|
|
ГИНЕКОЛОГИЯ | ТОМ 12 | №1 33

И Н Ф Е К Ц И О Н Н О - В О С П А Л И Т Е Л Ь Н Ы Е З А Б О Л Е В А Н И Я В А М Б У Л АТ О Р Н О Й П РА К Т И К Е
Рис. 1. Споры грибов (в центре) на фоне ключевых клеток.
Рис. 2. Больная К. Диагноз: БВ. До лечения.
Таблица 5. Выраженность аминового теста после лечения препаратом Вагинорм-С (21–30-й день)
Степень выраженности показателя |
Группа 1-я (n=6) |
Группа 2-я (n=9) |
|
|
|
1-я |
5 |
7 |
2-я |
1 |
2 |
3-я |
0 |
0 |
|
|
|
Таблица 6. Процент ключевых клеток после лечения препаратом Вагинорм-С (21–30-й день)
Процент ключевых клеток |
Группа 1-я (n=6) |
Группа 2-я (n=9) |
|
|
|
0–19 |
5 |
5 |
20–50 |
1 |
2 |
51–80 |
0 |
2 |
81–100 |
0 |
0 |
|
|
|
болевания, далеко не всегда достигает |
пользовании антибактериальных пре- |
желаемого результата – восстановле- |
паратов – производных 5-нитроими- |
ния пула нормальной микрофлоры. |
дазола или клиндамицина. Примеча- |
йТУ·ВММУТЪЛ ЪВ ‡ФЛЛ |
тельно, что к данным средствам чувст- |
вительны практически все ассоцииро- |
|
В настоящее время терапия БВ со- |
ванные с БВ микроорганизмы. Второй |
стоит из двух этапов. Первый заключа- |
этап подразумевает использование |
ется в местном или системном ис- |
трансплантации ацидофильных мик- |
роорганизмов – представителей нормальной микрофлоры влагалища.
Тем не менее известно, что уже через 1 мес после проведенного лечения до 30% пациенток отмечают рецидив БВ. В более отдаленный период эта цифра имеет стойкую тенденцию к увеличению.
Вероятно, это связано с тем, что не происходит нормализации таких важных показателей микроэкосистемы влагалища, как кислотность и осмолярность влагалищной жидкости.
Ранее для модуляции кислотности влагалищной жидкости использовали инстилляции растворов молочной кислоты. Однако недостатком данного метода является кратковременность воздействия и то, что с позиций теории ферментативного катализа продукты реакции тормозят активность ферментативных систем, действие которых направлено на их продукцию. С этих позиций очевидно, что использование молочной кислоты не будет стимулировать рост резидентных влагалищных лактобактерий.
LJ„ËÌÓ Ï-ë
В настоящее время арсенал средств терапии БВ пополнил препарат Ваги- норм-С. Влагалищные таблетки содержат аскорбиновую кислоту и моногидрат лактозы. Особенность препарата заключается в том, что он способен поддерживать физиологические значения рН влагалищной жидкости (3,8–4,2) в течение 24 ч. Лактоза является пищевым субстратом лактобацилл.
Ранее было установлено, что «ключевые клетки» – микробно-клеточные комплексы – при нормальных значениях кислотности влагалищного содержимого нестабильны. Освобождающаяся от ассоциированных с БВ рецепторная поверхность эпителиальных клеток становится доступной для ацидофильных микроорганизмов, адгезивность которых, напротив, в кислой среде повышается.
дОЛМЛ˜ВТНУВ ЛТТОВ‰У‚‡МЛВ
Цель исследования – изучить эффективность препарата Вагинорм-С при БВ.
Задача исследования – определение эффективности ретардной лекарственной формы Вагинорм-С в качестве монотерапевтического средства терапии БВ с позиций нормализации основных клинико-лабораторных показателей.
å‡Ú ˇÎ˚ Ë ÏÂÚÓ‰˚
Общая характеристика обследованных групп
Формирование обследуемых групп, сбор анамнеза, выяснение жалоб, клинической симптоматики проводились в амбулаторном отделении Кафедры акушерства и гинекологии им. А.Я.Крассовского Военно-медицин- ской академии им. С.М.Кирова, СанктПетербург.
34 ГИНЕКОЛОГИЯ | ТОМ 12 | №1

Под нашим наблюдением находились 30 небеременных женщин в возрасте от 19 до 37 лет, которым в результате обследования был поставлен диагноз «БВ». В исследование не включали женщин с диагностированной микстинфекцией.
Пациентки были объединены в две группы.
Градация проводилась на основании показателей рН влагалищной жидкости. В 1-й группе показатели кислотности соответствовали значениям 4,7–5,0; во 2-й – 5,3–6,1. Все пациентки 2-й группы предъявляли жалобы на характерные жидкие гомогенные выделения из влагалища; женщины, включенные в 1-ю группу, жалоб не предъявляли. Диагноз «БВ» был определен на основании результатов микроскопии влагалищного мазка.
Обе группы были сопоставимы по основным демографическим показателям. Асоциально-маргинальная категория граждан в исследование не включалась.
Пациенток обследовали в момент обращения в лечебное учреждение, в первые 3 дня после курса терапии и после очередной менструации (через 14–30 дней).
Клиническое и гинекологическое обследование пациенток проводили согласно стандартным схемам и методикам диагностики БВ.
Определение кислотности влагалища производили при помощи тест-полосок (SP pH Indicator Strips, Германия).
Микроскопическая диагностика осуществлялась путем исследования окрашенного 1% спиртовым раствором метиленового синего влагалищного мазка (Ув. 900). При обнаружении 20% и более ключевых клеток и характерного полиморфного коккобациллярного пейзажа выставлялся диагноз: БВ. Микроскопически споры и псевдомицелий грибов выявлены не были. Для диагностики скрытых инфекций использовался метод полимеразной цепной реакции.
Аминовый тест учитывался согласно степени выраженности.
кВБЫО¸Ъ‡Ъ˚ Л У·ТЫК‰ВМЛВ
В симптомокомплексе БВ ведущее место занимают патологические бели, которые имеют характерный запах гнилой рыбы. Важным является то, что органолептически этот запах не всегда определяется. Если во 2-й группе обследованных одной из основных жалоб – наличие неприятного запаха – было у всех больных, то в 1-й группе этот показатель в максимальной степени выраженности отмечался только у 1 пациентки. Для оптимизации диагностики используется аминовый тест – появление или усиление запаха после добавления к содержимому влагалища 10% раствора щелочи. Результаты исследования аминового теста представлены в табл. 1.
При микроскопии влагалищного мазка диагностическим признаком является наличие «ключевых клеток» – характерных комплексов, ассоциированных с БВ микроорганизмов и клеток эпителия. В 1-й группе диапазон показателя был от 23 до 86%; во 2-й – от 76 до 100%.
У пациенток 2-й группы в мазке отмечалось превалирование характерного для БВ микробного морфотипа. Следует отметить, что у пациенток 1-й группы в той или иной степени выраженности определялась и микрофлора, морфологически сходная с лактобактериями (табл. 2).
Важным этапом в микроскопической оценке влагалищного мазка является учет количества лейкоцитов. При классической форме БВ лейкореи нет, поскольку ассоциированные с БВ микроорганизмы входят в состав микробного пейзажа влагалища в норме. Развитие симптомокомплекса БВ определяется их гиперколонизацией. Причинами лейкоцитарной реакции при БВ являются эндоцервициты хламидийной и вирусной этиологии, хроническая трихомонадная инвазия, грибы, патогенные бактерии.
Диагностика вышеуказанных возбудителей важна. Определяется это тем, что при подавлении гиперколонизированных анаэробных микроорганизмов создаются условия для обострения латентных инфекций, возбудители которых получают доступ к источникам питания – гликогену эпителиальных клеток. На рис. 1 представлена микрофотография препарата, на которой видны споры грибов на фоне ключевых клеток.

П А Т О Л О Г И Я Б Е Р Е М Е Н Н О С Т И
|
|
|
|
Выраженным тест остался только у 1 |
|
|
Рис. 3. Больная К. Вторые сутки после курса лечения. Нормоценоз. |
|
пациентки 2-й группы. |
||
|
|
|
|
||
|
|
|
|
Микроскопическое исследование |
|
|
|
|
|
влагалищного мазка показало отсутст- |
|
|
|
|
|
вие признаков воспаления. В 80,0 и |
|
|
|
|
|
72,7% случаев соответственно группам |
|
|
|
|
|
результаты микроскопии были оцене- |
|
|
|
|
|
ны как нормоценоз или переходный |
|
|
|
|
|
тип биоценоза. У 2 пациенток 1-й |
|
|
|
|
|
группы и 3 пациенток 2-й группы ма- |
|
|
|
|
|
зок был оценен как соответствующий |
|
|
|
|
|
БВ, однако имела место положитель- |
|
|
|
|
|
ная динамика микробного морфоти- |
|
|
|
|
|
па. |
|
|
|
|
|
Микроскопический учет результа- |
|
|
|
|
|
тов лечения представлен на рис. 2 и 3. |
|
|
|
|
|
Проводилась |
катамнестическая |
|
|
|
|
оценка результатов лечения. К сожа- |
|
|
|
|
|
лению, по не зависящим от нас при- |
|
|
|
|
|
чинам на контрольное обследование |
|
|
|
|
|
явились не все пациентки. Результа- |
|
|
|
|
|
ты исследования представлены в |
|
|
|
|
|
табл. 5, 6. |
|
|
|
|
|
Из представленных в таблицах ре- |
|
|
|
|
|
зультатов видно, что и через 3–4 нед |
|
|
После обследования пациенткам в |
реакцией на использование именно |
после проведенного лечения сохраня- |
||
виде монотерапии вагинально назна- |
препарата Вагинорм-С. Подобные |
ются положительные результаты. Тем |
|||
чали препарат Вагинорм-С по 1 таб- |
проявления могут возникнуть при ис- |
не менее пациенткам с тенденцией к |
|||
летке 1 раз в день курсом 6 дней. Следу- |
пользовании лекарственных препара- |
рецидиву заболевания нами было ре- |
|||
ет отметить, что на 2–3-й день лечения |
тов других групп, это надо учитывать в |
комендовано повторное использова- |
|||
5 пациенток 1-й группы и 4 пациентки |
разработке терапевтической тактики. |
ние курса влагалищных таблеток Ва- |
|||
2-й группы отметили возникновение |
Все оставшиеся в исследовании |
гинорм-С. |
|
||
жжения во влагалище и характерные |
женщины 2-й группы отмечали поло- |
Ç˚‚Ó‰˚ |
|
||
творожистые выделения. При микро- |
жительную динамику с позиций ос- |
|
|||
скопическом исследовании были об- |
новных клинических симптомов. Пос- |
Препарат Вагинорм-С является эф- |
|||
наружены пседомицелий и споры гри- |
ле проведенной терапии проводилось |
фективным этиопатогенетическим |
|||
бов на фоне воспалительного типа |
исследование аминового теста и мик- |
лекарственным |
средством терапии |
||
мазка. Соответственно, в указанной |
роскопия влагалищных мазков. Ре- |
бактериального вагиноза. |
|||
группе больных исследуемый препа- |
зультаты исследования представлены |
Назначению препарата Вагинорм-С |
|||
рат отменялся, назначался курс анти- |
в табл. 3 и 4. |
должно предшествовать бактериоло- |
|||
микотиков, а пациентки исключались |
Из результатов, представленных в |
гическое обследование на грибы либо |
|||
из исследования. Надо отметить, что |
табл. 3, видно, что отмечается норма- |
профилактическое назначение сис- |
|||
манифестация кандидоза не является |
лизация показателей аминового теста. |
темных антимикотиков. |
|||
Патогенетическое обоснование тактики ведения отслойки хориона
и плаценты на ранних сроках
беременности
П.А.Кирющенков, Д.М.Белоусов, О.С.Александрина ФГУ Научный центр акушерства, гинекологии и перинатологии им. В.И.Кулакова Росмедтехнологий
(дир. – акад. РАМН, проф. Г.Т.Сухих), Москва
реди причин самопроизвольного |
нередко сочетающиеся с эндокрино- |
хориона представлена его гипопла- |
Спрерывания беременности, в осо- |
патиями, инфекционным фактором, |
зией, отставанием в созревании («об- |
бенности на ранних сроках, в послед- |
иммунологическими растройствами и |
лысении»), частичным или полным |
ние годы стали выделять так называе- |
нарушениями гемостаза как на сис- |
предлежанием. Частым признаком |
мый «маточный фактор», который мо- |
темном, так и на локальном уровне, |
является также образование гематом, |
жет быть представлен гипоплазией и |
приводят к неполноценности процес- |
которые в зависимости от локализа- |
«незрелостью эндометрия», наруше- |
сов имплантации и плацентации [1, 8]. |
ции подразделяют на 3 вида: субхо- |
ниями гемодинамики в сосудистом |
Клинико-ультразвуковая характе- |
риальные, субамниотические и крае- |
русле матки. Указанные изменения, |
ристика патологического развития |
вые [9]. |
36 ГИНЕКОЛОГИЯ | ТОМ 12 | №1

В общей популяции беременных частота выявления гематом составляет 3% [12].
Методом выбора диагностики при патологии хориона является ультразвуковое исследование с использованием допплерометрии [13, 15].
Субхориальные гематомы в среднем выявляются на 7 нед беременности. Прогноз для дальнейшего развития беременности зависит от сроков образования гематом (ранее 9 нед вероятность потери беременности в 12 раз выше, чем в более поздние сроки). К неблагоприятным факторам также относят размеры гематомы более 50 мл и возраст беременных старше 35 лет [7, 10, 11].
Субамниотические гематомы встречаются реже субхориальных и особенности течения беременности при данной патологии практически не описаны.
Наличие гематом сопровождается наружным кровотечением в 71% случаев, бессимптомным течением – в 29%. Если не происходит гибель эмбриона (плода), то в дальнейшем возможно развитие плацентарной недостаточности в 24% случаев, преждевременных родов – в 16–19% (из них 43% в сроки менее 34 нед), преэклампсии – в 8%, задержки развития плода – в 7%, диcтресс-синдрома у новорожденного – в 19%. Частота кесарева сечения у данного контингента беременных составляет 27% [12].
Следует отметить, что в литературе мало представлены ограниченные данные о патогенезе отслойки хориона на ранних сроках, недостаточно изучены особенности гемодинамики в матке и, соответственно, отсутствуют единые подходы к терапии.
Высокая частота акушерских и перинатальных осложнений при различных формах патологии хориона на ранних сроках диктует необходимость более глубокого изучения данной проблемы.
сВО¸ ЛТТОВ‰У‚‡МЛfl
На основании клинико-лабораторной и ультразвуковой оценки различных форм отслойки хориона и плаценты (на ранних сроках) разработать оптимальную профилактику осложнений течения беременности.
å‡Ú ˇÎ˚ Ë ÏÂÚÓ‰˚
Основную группу составили 50 беременных, у которых при ультразвуковом исследовании выявлена патология хориона в виде субхориальной гематомы (30 наблюдений) и субамниотической гематомы (20 наблюдений). В контрольную группу вошли 40 здоровых первобеременных женщин (средний возраст 26,5±0,5 года). Помимо оценки клинико-анам- нестических данных проводилось динамическое ультразвуковое исследование с использованием цифрового сканера Siemens SonoLine Elegra (Германия), снабженного мультичастотными датчиками с применением дуплексного режима сканирования. При ультразвуковом исследовании оценивались размеры эмбриона (плода), расположение и особенности строения хориона (плаценты) в соответствии со сроком беременности. При оценке гематом определялся их характер (субхориальные, субамниотические, краевые), объемные размеры, стадии развития. Допплерометрическую оценку состояния гемодинамики производили в миометрии в зонах отслойки и в интактных зонах. Оценивались показатели кровотока в маточных (Ma), аркуатных (Аа), радиальных (Ра), базальных артериях (Ба), а также хориальный кровоток. Для упрощения исследования учитывался индекс резистентности (RI). Допплерометрия проводилась при субхориальном и субамниотическом расположении гематом, при краевой отслойке проведение исследования представляло значительные трудности.
Наряду с ультразвуковым исследованием у женщин основной группы применялись бактериологические и вирусологические методы (бактериологический посев из цервикального канала, ПЦР-диагностика урогенитальных инфекций), гормональные (оценка характера и выраженности гиперандрогении), иммунологические (субпопуляционный состав лимфоцитов периферической крови, определение уровня антифосфолипидных антител, антител к хорионическому

П А Т О Л О Г И Я Б Е Р Е М Е Н Н О С Т И
Таблица 1. Динамика показателей кровотока в миометрии (RI) при субхориальных гематомах (n=30)
Артерии |
В зоне отслойки |
В интактной зоне |
Нормативные показатели |
||
|
|
|
|
|
|
|
до лечения |
после лечения |
до лечения |
после лечения |
|
|
|
|
|
|
|
Аркуатные |
0,75±0,06* |
0,62±0,03** |
0,64±0,05 |
0,62±0,04 |
0,60±0,02 |
Радиальные |
– |
0,77±0,07 |
0,46±0,04 |
0,54±0,04 |
0,56±0,01 |
Базальные |
– |
0,57±0,04 |
0,45±0,01 |
0,49±0,04 |
0,47±0,02 |
|
|
|
|
|
|
Примечание. *р<0,05 по сравнению с нормативным показателем; **р<0,005 по сравнению со значением до лечения.
Таблица 2. Динамика показателей кровотока в миометрии (RI) при субамниотических гематомах (n=20)
Артерии |
В зоне отслойки |
В интактной зоне |
Нормативные показатели |
||
|
|
|
|
|
|
|
до лечения |
после лечения |
до лечения |
после лечения |
|
|
|
|
|
|
|
Аркуатные |
0,64±0,05 |
0,67±0,03 |
0,60±0,05 |
0,57±0,03 |
0,60±0,02 |
Радиальные |
0,67±0,09 |
0,61±0,06 |
0,54±0,07 |
0,51±0,04 |
0,56±0,01 |
Базальные |
– |
– |
0,41±0,05 |
0,48±0,08 |
0,47±0,02 |
|
|
|
|
|
|
гонадотропину человека), молекуляр- |
сам HLA системы II класса была уста- |
вания гематом не было ни в одном слу- |
||
но-биологические (HLA система II |
новлена у 21% супружеских пар. |
чае, в 40% случаев гематомы находи- |
||
класса, полиморфизм генов компо- |
Таким образом, у беременных с раз- |
лись в стадии организации. |
||
нентов системы гемостаза), гемоста- |
личными формами отслойки хориона |
Сравнительный анализ ультразвуко- |
||
зиологические (оценка тромбофили- |
(плаценты) в I триместре наиболее час- |
вых параметров показал более позд- |
||
ческих состояний и синдрома ДВС). |
то выявлялись врожденные и приобре- |
нее |
возникновение субамниотиче- |
|
кВБЫО¸Ъ‡Ъ˚ Л У·ТЫК‰ВМЛВ |
тенные тромбофилические состояния. |
ских гематом по сравнению с субхо- |
||
Кроме того, обращает на себя внима- |
риальными на 3–6 нед (p<0,001). Объ- |
|||
Средний возраст беременных ос- |
ние повышенная активность киллер- |
ем субамниотических гематом в мо- |
||
новной группы составлял 31,5±0,9 го- |
ных клеток (CD56+16+), что наряду с |
мент их выявления и в конце лечения |
||
да. Возраст менархе – 13,4±0,4 года. |
совместимостью по 3 и более антиге- |
был значительно больше субхориаль- |
||
Менструальная функция: через |
нам HLA системы II класса могло играть |
ных (p<0,01). |
||
29,7±0,4 по 5,4±0,2 дня. Паритет жен- |
одну из главных ролей в нарушении |
При субхориальных гематомах ги- |
||
щин составлял от 1 до 4 беременно- |
процессов имплантации и плацента- |
поплазия хориона встречалась в 4 |
||
стей, при этом привычная потеря бе- |
ции. Неблагоприятным фактором так- |
раза чаще, чем при субамниотических |
||
ременности отмечалась в 30% наблю- |
же следует расценивать наличие гипе- |
(p<0,01). При субхориальных гемато- |
||
дений в сроки 7,1±0,6 нед. Роды в |
рандрогении. Кроме того, установлен- |
мах предлежание и низкое располо- |
||
анамнезе имелись у 18% женщин, из |
ное у каждой третьей беременной но- |
жение хориона отмечалось также ча- |
||
них перинатальные потери отмеча- |
сительство |
бактериально-вирусных |
ще, |
чем при субамниотических |
лись у 8%. |
инфекций могло свидетельствовать о |
(p>0,05). |
||
Из соматических заболеваний обра- |
наличии хронического эндометрита. |
При наличии субхориальных гема- |
||
щала на себя внимание высокая часто- |
Дифференцированная ретроспек- |
том до начала лечения усредненные |
||
та перенесенного хронического тон- |
тивная оценка показала, что в 80% слу- |
значения кровотока (RI) в маточных |
||
зиллита (47%), заболеваний мочевы- |
чаев субамниотических гематом выяв- |
артериях (Ма) составляли 0,84±0,02 |
||
водящих путей (20%), желудочно-ки- |
лялась патогенная бактериально-ви- |
(при норме 0,75±0,01), после лечения |
||
шечного тракта (20%), сердечно-сосу- |
русная флора, в то время как при нали- |
– уменьшились до 0,78±0,02 (p<0,05). |
||
дистой системы (13%). Отягощенный |
чии субхориальных гематом – только |
Как следует из данных табл. 1, в уча- |
||
аллергологический анамнез установ- |
в 10% случаев (p<0,001), что может |
стках матки, примыкающих к зоне от- |
||
лен у 30% обследованных женщин. |
свидетельствовать о различном пато- |
слойки, до лечения индекс резистент- |
||
Лабораторно-инструментальное |
генезе отслойки хориона (плаценты) |
ности (RI) в Аа достоверно превышал |
||
обследование, проведенное во время |
в I триместре. Среди выявленных ин- |
нормативные показатели, после про- |
||
беременности у женщин основной |
фекций преобладали гемолитический |
веденного лечения достоверно умень- |
||
группы, выявило высокую частоту сме- |
стрептококк В, энтерококк, эпидер- |
шился. До лечения в Rа кровоток опре- |
||
шанной бактериально-вирусной ин- |
мальный стафилококк, микоплазма, |
делялся только в 27% случаев, после ле- |
||
фекции (33%), гиперандрогении раз- |
уреаплазма, хламидии, вирус простого |
чения – в 67% (p<0,01). В Ба до лечения |
||
личного генеза (50%). При иммуноло- |
герпеса. |
|
кровоток не визуализировался ни в |
|
гическом обследовании выявлено по- |
Средние сроки выявления субхори- |
одном случае, после лечения опреде- |
||
вышение содержания естественных |
альных гематом составляли 8,3±0,4 |
лялся в 13% случаев. До лечения цвето- |
||
киллерных клеток с фенотипом |
нед, при этом в динамике наблюдения |
вые сигналы сосудов хориона не опре- |
||
CD56+16+ в периферической крови в |
объем гематом имел тенденцию к |
делялись ни в одном случае, после ле- |
||
63% наблюдений, антифосфолипид- |
уменьшению с 1,32±0,25 до 1,16±0,33 |
чения появились в 37% наблюдений. |
||
ных антител (60%), антител к хорио- |
см3. В конце лечения отсутствие визу- |
В интактных зонах миометрия до |
||
ническому гонадотропину человека |
ализации гематом было в 33% случаев, |
лечения хориальный кровоток ви- |
||
(33%). При исследовании показателей |
в стадии организации было 37% гема- |
зуализировался в 33% наблюде- |
||
системы гемостаза хроническая фор- |
том, в 30% наблюдений отмечался пе- |
ний, после лечения – в 87% (p<0,01). |
||
ма синдрома ДВС была установлена в |
реход субхориальных гематом в суб- |
В отличие от субхориальных при |
||
50% случаев. Гетеро- и гомозиготная |
амниотические. |
субамниотических гематомах в зоне |
||
формы мутации гена метилентетра- |
Средние сроки выявления субамни- |
отслойки кровоток в миометрии до и в |
||
гидро-фолатредуктазы (MTHFR) были |
отических |
гематом составляли |
конце лечения существенно не отли- |
|
обнаружены у 75% женщин, полимор- |
12,1±0,5 нед, при этом объем гематом |
чался от нормативов (табл. 2). До лече- |
||
физм генов ингибитора активатора |
в динамике имел тенденцию к умень- |
ния кровоток в базальных артериях не |
||
плазминогена -1 (PAI-1) – в 86% случа- |
шению с 17,7±6,0 до 10,0±3,7 см3. В |
определялся, после лечения – визуали- |
||
ев. Совместимость по 3 и более локу- |
конце наблюдения полного рассасы- |
зировался в 10% случаев. В интактной |
||
38 ГИНЕКОЛОГИЯ | ТОМ 12 | №1

П А Т О Л О Г И Я Б Е Р Е М Е Н Н О С Т И
зоне до лечения хориальный кровоток определялся в 35% наблюдений, после лечения – в 70%.
До начала лечения при субхориальных гематомах отсутствие визуализации кровотока в зоне отслойке на уровне радиальных и базальных артерий и повышение резистентности на уровне аркуатных артерий можно рассматривать как компенсаторную реакцию, препятствующую прогрессированию отслойки плаценты. В то же время повышение сосудистого сопротивления на уровне маточных артерий является неблагоприятным фактором развития плацентарной недостаточности [6]. В дальнейшем после
проведенной терапии отмечалась нормализация кровотока как в интактных зонах матки, так и в участках матки, прилегающих к зоне разрешающейся гематомы.
По мнению В.Е. Радзинского и соавт. [4], подобная динамика показателей кровотока создает благоприятный фон для инвазии трофобласта.
Полученные при динамическом ультразвуковом мониторинге данные послужили основанием для разработки оптимальной тактики ведения беременности при отслойки хориона (плаценты) с позиций профилактики плацентарной недостаточности. Представленные в литературе рекомендации в основном сводятся к использованию гестагенов, гемостатических препаратов, метаболической терапии. Противотромботические средства рекомендуется применять только после полного рассасывания гематомы [14, 16].
С учетом установленных форм патологии хориона в I триместре нами предлагается следующая схема терапии. Общепринятыми методами являются спазмолитическая, седативная терапия и профилактика плацентарной недостаточности. При гормональных и аутоиммунных нарушениях по показаниям используются глюкокортикоиды и гестагены. При совместимости по HLA системе II класса, высоком содержании CD56+16+ в периферической крови и гипоплазии хориона проводится лимфоцитоиммунотерапия (ЛИТ), внутривенное введение иммуноглобулина. Антибактериальная терапия в сочетании с внутривенным введением иммуноглобулина чаще применяется при наличии субамниотических гематом. При мутации гена MTHFR используется комбинация препаратов фолиевой кислоты и витаминов группы В.
Важным компонентом активной тактики ведения отслойки хориона (плаценты) на ранних сроках беременности является одновременное использование ингибиторов фибринолиза (транексамовая кислота – Транексам) и антиагрегантов. Наиболее
перспективным представляется использование дипиридамола (Курантил®, «Берлин-Хеми АГ»,
Германия), поскольку этот препарат оказывает мягкий и управляемый антиагрегантный эффект и не вызывает геморрагических осложнений. Курантил® также является ангиопротектором, снижает тонус артериол, повышает деформируемость эритроцитов, способствует развитию коллатералей [3]. Указанные эффекты дипиридамола подтверждаются данными ультразвуковой допплерометрии, полученными при выполнении данного исследования. Кроме того, ранее нами было показано, что даже 7–8-дневный курс препарата Курантил® оказывает стимулирующее влияние на эритропоэз у эмбриона и ангиогенез в ворсинах хориона при аутоиммунном невынашивании [2].
Нами предложен следующий алгоритм совместного использования препаратов Транексам и Курантил® при отслойки хориона (плаценты) на ранних сроках беременности. При наличии кровянистых выделений из половых путей применяется Транексам 5–10 мл на физиологическом растворе внутривенно капельно, после прекращения наружного кровотечения по 1 таблетке 3 раза в сутки до появления УЗ-признаков образования гематомы. После прекращения наруж-
ного кровотечения с целью нормализации кровообращения в матке применяется Курантил® в дозе 1 таблетка (25 мг) 3 раза в сутки в течение 2 нед. В случае продолжающегося кровотечения срок терапии увеличивается еще на 2 нед. Использование ацетилсалициловой кислоты при отслойке хориона (плаценты) неоправданно, поскольку при необходимости отмены препарата восстановление сосудистотромбоцитарного гемостаза происходит в течение 6–10 дней [5].
Анализ исходов беременности у женщин основной группы показал, что неразвивающаяся беременность в сроках 8–9 нед имела место в 4% наблюдений, своевременные роды произошли у 74% женщин, преждевременные в сроках 32–36 нед – у 22%. Путем кесарева сечения родоразрешены 32% женщин. С нормальными массо-рос- товыми показателями родились 94% новорожденных, с признаками задержки внутриутробного развития плода – 6%. В удовлетворительном состоянии родились 80% детей, в состоянии легкой гипоксии – 14%, гипоксии средней степени тяжести – 6%.
Таким образом, отслойка хориона (плаценты) в I триместре является одним из распространенных осложнений беременности, являющихся следствием различных эндотелиопатий, иммунологических, гемостазиологических, эндокринных нарушений. При субамниотических гематомах инфекционный фактор играет существенно бóльшую роль, чем при субхориальных. Гипоплазия хориона значи-
тельно чаще встречается при наличии субхориальных гематом и может свидетельствовать о нарушении процессов имплантации и плацентации. Субамниотические гематомы возникают на 3–6 нед позже субхориальных, имеют больший объем и их обратное развитие длительно.
Патологические изменения гемодинамики в матке более выражены при субхориальных гематомах, что требует использования наряду с гемостатической терапией средств, улучшающих микроциркуляцию (Курантил®).
Литература
1.Кирющенков П.А., Белоусов Д.М. Ультразвуковая оценка роли «маточного фактора» и особенности предгестационной подготовки женщин с привычным невынашиванием беременности I триместра. Пробл. берем. 2007; 13 (5): 19–25.
2.Милованов А.П., Сидельникова В.М., КирющенковП.А. и др. Морфометрия ворсин плаценты как критерий эффективности использования Курантила на ранних сроках беременности при аутоиммунном невынашивании. Вестн. Рос. ассоц. акуш.-гинек. 2000; 4: 21–4.
3.Сидельникова В.М., Кирющенков П.А., ХоджаеваЗ.С., Слукина Т.В. Патогенетическое обоснование использования Курантила в акушерстве. Акуш. и гинекол. 1999; 5: 52–4.
4.Ранние сроки беременности. Под ред. В.Е.Радзинского, А.А.Оразмурадова. М., 2005; с. 269–85.
5.Сидельникова В.М., Кирющенков П.А. Гемостаз и беременность. М., 2004; с. 179–87.
6.Стрижаков А.Н., Игнатко И.В. Потеря беременности. М., 2007; с. 145–6.
7.Bennet GL, Bromley B, Lieberman E, Benacerrof BR. Subchorionic hemorrhage in firsttrimester pregnancies: prediction of pregnancy outcome with sonography. Radiology 1996; 2000 (3): 803–6.
8.Hill JA, Choi BC. Maternal immunological aspects of pregnancy success and failure. Human implantation: recent advances and clinical aspects. Eds. C.Simon et al. J Reprod Fertil 2000; 55: 91–7.
9.Johns J, Hyett J, Jauniaux E. Obstetric outcome after threatened miscarriage with and without a haematoma on ultrasound. Obstet Gynecol 2003; 102 (3): 483–7.
10.Leite J, Ross AC, Jeanty P. Prognosis of very large first-trimester haematomas. J Ultrasound Med 2006; 25 (11): 1441–5.
11.Maso G, D’Ottavio G, De Seta F et al. Firsttrimester intrauterine hematoma and outcome of pregnancy. Obstet Gynecol 2005; 105: 339–44.
12.Nagy S, Bush M, Stone J et al. Clinical significance of subchorionic and retroplacental haematomas detected in the first trimester of pregnancy. Obstet Gynecol 2003; 102 (1): 94–100.
13.Ozkaya U, Ozkan S, Ozeren S, Corakci A. Doppler examination of uteroplacental circulation in early pregnancy: can it predict adverse outcome? J Clin Ultrasound 2007; 35 (7): 382–6.
14.Pelinescu-Onciul D. Subchorionic haemorrhage treatment with dydrogesterone. Gynecol Endocrinol 2007; 23 (Suppl. 1): 77–81.
15.Tamura H, Miwa I, Taniguchi K et al. Different changes in resistance index between uterine artery and uterine radial artery during early pregnancy. Hum Reprod 2008; 23 (2): 285–9.
16.Tower CL, Regan L. Intrauterine haematomas in a recurrent miscarriage population. Hum Reprod 2001; 16 (9): 2005–7.
ГИНЕКОЛОГИЯ | ТОМ 12 | №1 39

П А Т О Л О Г И Я Б Е Р Е М Е Н Н О С Т И
Профилактика репродуктивных потерь и осложнений гестации у пациенток с невынашиванием беременности
М.Ю.Скворцова, Н.М.Подзолкова Кафедра акушерства и гинекологии (зав. – проф. Н.М.Подзолкова)
ГОУ ДПО РМАПО Росздрава, Москва
Проблема репродуктивных потерь остается одной из наиболее акту-
альных в современном акушерстве [2, 6, 15, 22, 25, 30, 35].
Частота самопроизвольного прерывания беременности в России достаточно высока – от 15 до 23% всех зарегистрированных беременностей, при этом около 50% выкидышей приходится на долю привычного невынашивания беременности (ПНБ) [2, 12, 21, 25].
В мировой литературе в последние годы репродуктивные потери все чаще объединяют термином «синдром потери плода», который включает разные нозологии [2, 7, 17]. Под синдромом потери плода понимают:
•один и более самопроизвольных выкидыша при сроке беременности более 10 нед (включая и неразвивающуюся беременность);
•мертворождение;
•неонатальную смерть как осложнение преждевременных родов, тяжелого гестоза и/или плацентарной недостаточности;
•3 самопроизвольных выкидыша и более на преэмбрионической или ранней эмбрионической стадии (когда исключены анатомические, генетические и гормональные причины).
щЪЛУОУ„Лfl
Этиология ПНБ разнообразна. В настоящее время различают следующие ведущие причины привычной потери беременности: генетические, эндокринные, иммуногемореологические, инфекционные и анатомические (патология матки).
По обобщенным данным мировой литературы, среди причин ПНБ около 7% приходится на хромосомные аномалии. Существуют данные, согласно которым до 50% выкидышей на ранних сроках, 30% – во II триместре и 3% мертворождений (на более поздних сроках гестации) обусловлены хромосомными нарушениями [1, 5, 16, 18, 24, 28, 32, 38].
Эндокринные причины невынашивания беременности, по данным разных авторов, составляют 8–20%. Веду-
щими эндокринными факторами прерывания беременности являются гиперандрогения разного генеза, недостаточность лютеиновой фазы фертильного цикла, гиперпролактинемия и дисфункция щитовидной железы [1, 5, 15, 16, 18–20, 24, 32, 34].
Около 12–15% женщин с ПНБ имеют анатомические особенности опущения матки, которые в большинстве случаев сочетаются с нарушением ее функционального состояния (аномалии развития матки, генитальный инфантилизм, истмико-цервикаль- ная недостаточность, миома матки и внутриматочные синехии) [16, 24, 25, 34, 38].
Среди причин невынашивания беременности одно из ведущих мест занимают латентно и хронически протекающие воспалительно-инфекци- онные заболевания (хламидиоз, токсоплазмоз, микоплазменная, цитомегаловирусная и герпетическая инфекции и др.) [9, 13, 15, 19, 20, 24, 27, 34], а также нарушения рецепторной активности эндометрия [21, 25, 26] у пациенток с большим паритетом беременностей и внутриматочных вмешательств (в связи с наличием хронического эндометрита).
Иммунологические нарушения, лежащие в основе преимущественно ранних гестационных потерь, обусловлены аллоиммунными и аутоиммунными механизмами [1, 9, 15, 20, 24, 26, 28]. Однако в 20–40% случаев причины неудавшейся беременности остаются неизвестными [9, 15, 16, 19, 20, 34, 35, 36].
В последние годы при обсуждении генеза большинства акушерских осложнений особое внимание уделяют нарушениям в системе свертывания крови – генетически детерминированным, приобретенным и комбинированным формам тромбофилии [2, 3, 7, 10–12, 17, 23, 31, 33, 37]. При тромбофилии развивается системная эндотелиальная дисфункция, активируется провоспалительный ответ и формируется прокоагуляционный потенциал свертывающей системы крови. Все перечисленное является причиной нарушения процессов имплантации,
плацентации и роста плода [17, 22, 29, 30, 33, 37], что и обусловливает высокую частоту таких осложнений второй половины беременности, как гестоз и фетоплацентарная недостаточность.
ЕВ ВПВММУТЪ¸: МУ П‡О¸М‡fl Л УТОУКМВММ‡fl
Общепризнанно, что физиологическое течение беременности определяется многими факторами, в том числе:
•особенностями функционального состояния гипоталамо-гипофизарно- яичниковой системы и надпочечников в фертильном цикле (нормальное соотношение гонадотропных гормонов, регуляция селекции доминантного фолликула, состояние эндометрия в период «окна имплантации» и обеспечение адекватной адгезии и инвазии ранней бластоцисты);
•состоянием эндометрия (в фертильном цикле и на этапах ранней беременности), что обеспечивает нормальное формирование маточно-пла- центарной области и становление ма- точно-плацентарного кровотока (формирование которых в основном заканчивается к 17–18-й неделе беременности);
•физиологической иммуномодуляцией, поскольку известно, что в первые недели гестации осуществляется «иммунологический диалог» между организмом матери и продуктом зачатия (в период имплантации происходит локальная супрессия регуляторными цитокинами – интерлейкинами 10, 4, 5 и 6 – материнского организма антигенов главного комплекса гистосовместимости ранней бластоцисты);
•достаточной функциональной активностью желтого тела, которая в свою очередь способствует иммуномодулирующему эффекту посредством стимуляции выработки прогестерониндуцированного блокирующего фактора. Последний стимулирует выработку асимметричных антител («маскирующих» антигены эмбриона), угнетает иммунный ответ материнского
организма по Тh1-типу (снижается выработка цитотоксических цитокинов, превалирует образование регулятор-
40 ГИНЕКОЛОГИЯ | ТОМ 12 | №1
