
4 курс / Акушерство и гинекология / Akusherstvo_Aylamazyan_2015
.pdfВо время беременности не отмечается повышенного выпадения солей, которые могут служить исходным материалом для камнеобразования. Наоборот, беременность сопровождается повышением коллоидальной активности мочи, предотвращающей развитие мочекаменной болезни. При прогрессировании беременности коллоидальная активность мочи увеличивается. Благодаря этому камни не образуются, несмотря на наличие во время беременности всех основных факторов, способствующих литогении: стаз мочи в сочетании с инфекцией и изменениями в минеральном обмене.
Таким образом, МКБ обычно не возникает во время беременности, но ее клинические признаки могут стать отчетливо выраженными, если ранее заболевание протекало латентно. Этому может способствовать ускоренный рост уже имеющихся камней, благоприятные условия для перехода камня в мочеточник, легкость присоединения инфекции. Продукты воспаления при пиелонефрите (слизь, гной, эпителиальные клетки) участвуют в образовании ядра почечного камня, на который наслаиваются кристаллы. Связь МКБ с предшествующей беременностью, осложненной пиелонефритом, несомненна.
Течение МКБ при беременности имеет свои особенности. Расширение и атония лоханок и мочеточников предрасполагают к движению конкрементов в нижележащие отделы мочевого тракта, поэтому приступы почечной колики и гематурия наблюдаются чаще, чем до беременности. Перемещением камней объясняется большая частота диагностики МКБ при беременности. При нахождении камня в мочеточнике почечная колика выражена сильнее. Вероятность развития пиелонефрита чрезвычайно высока, причем, как правило, он развивается уже в I триместре беременности в отличие от некалькулезного гестационного пиелонефрита. Коралловидный нефролитиаз протекает малосимптомно, редко сопровождается почечными коликами, но отличается упорным хроническим пиелонефритом.
Поскольку уролитиаз очень часто осложняется присоединением инфекции, таким больным показаны все диагностические мероприятия, предпринимаемые при пиелонефрите. При отсутствии осложнений такие больные могут наблюдаться амбулаторно. Течение родов не представляет каких-либо особенностей, приступы почечной колики, как правило, снимаются спазмолитическими и наркотическими средствами. Большие камни мочевого пузыря могут привести к остановке родовой деятельности и абдоминальному родоразрешению, но это встречается крайне редко.
Диета больных МКБ зависит от характера нарушения минерального обмена. При мочекислом диатезе (выделение уратов с мочой) используют продукты, бедные пуринами. Пуриновые основания содержатся в мясе, мозгах, мясном бульоне. Следует отдать предпочтение молочно-растительной диете. Обильное питье снижает концентрацию уратов в моче. Фосфорнокислый диатез требует ограничения солей кальция. В этом случае ограничивают употребление молочных продуктов, зеленых овощей, картофеля, гороха, фасоли. Диета при щавелевокислом диатезе не должна содержать продуктов, способствующих образованию оксалатов. Из рациона исключают молоко, яйца, щавель, помидоры. Назначают продукты, подщелачивающие мочу: яблоки, арбузы. Возможно употребление отварного мяса и рыбы.
Медикаментозная терапия направлена на снятие болей спазмолитиками, спазмоанальгетиками и препаратами, избирательно расслабляющими мускулатуру мочеточников (цистенал♠, ависан♠). При отсутствии эффекта от спазмолитиков следует с осторожностью прибегать к наркотикам. Теплые ванны и грелки при беременности противопоказаны. Если спазмолитические и наркотические средства не купируют приступ почечной колики, следует провести катетеризацию мочеточника. Операция показана при анурии, вызванной обтурацией мочеточника и не поддающейся терапии, при септическом состоянии, обусловленном калькулезным пиелонефритом, при пионефрозе, при часто
291
повторяющихся приступах колик без тенденции к самопроизвольному отхождению камней.
Течение беременности и родов. Мочекаменная болезнь редко оказывает влияние на течение беременности, если не присоединяется инфекция. Самопроизвольные выкидыши происходят редко. Преждевременные роды имеют место у 15% беременных с уролитиазом. Перинатальная смертность выше, чем в популяции, и, скорее всего, связана с инфекционным началом. Роды протекают как обычно, через естественные родовые пути. При наличии больших камней в мочевом пузыре может встать вопрос о родоразрешении операцией кесарева сечения.
Хроническая болезнь почек (МКБ-10: N18.1-N18.5)
Хроническая болезнь почек (ХБП) - наднозологическое понятие, объединяющее всех больных с сохраняющимися в течение 3 и более месяцев признаками повреждения почек по данным лабораторных и инструментальных исследований и/или снижением их фильтрационной функции.
До недавнего времени единая общепринятая классификация хронической недостаточности почек отсутствовала. На территории России использовались различные классификации - Ратнера (по уровню креатинина), Тареева (по скорости клубочковой фильтрации - СКФ), Лопаткина (по осмолярности мочи, креатинину, мочевине), Рябова и Кучинского (комплексная).
В настоящее время общее признание получила концепция хронической болезни почек (ХБП), впервые предложенная на рассмотрение американскими нефрологами в 2002 году. По рекомендации ВОЗ в 2007 г. соответствующие изменения были внесены и в МКБ-10, в которой устаревший термин «хроническая почечная недостаточность» был заменен на термин «хроническая болезнь почек». Отличие классификации ХБП, в первую очередь, в том, что она шире понятия хронической почечной недостаточности (ХПН) и включает ранние стадии заболевания, когда имеются признаки повреждения почек, но сохранена фильтрационная функция. Кроме того, в отличие от старых классификаций ХПН, за основу взят только один показатель функции почек - скорость клубочковой фильтрации (креатинин и мочевина крови имеют теперь только вспомогательное значение), что значительно ее упрощает, делает удобной и более надежной, легко применимой врачами всех специальностей.
Критерии диагностики ХБП:
1) наличие любых маркеров повреждения почек:
а) клинико-лабораторных (в первую очередь, протеинурии/микроальбуминурии), подтвержденных при повторных исследованиях и сохраняющихся в течение не менее 3 мес;
б) необратимых структурных изменений почки, выявленных при лучевом исследовании или морфологическом исследовании почечного биоптата
и/или
2) снижение скорости клубочковой фильтрации до уровня <60 мл/мин на 1,73 м2, сохраняющееся в течение 3 мес и более.
Уровень СКФ в пределах 60-89 мл/мин на 1,73 м2 при отсутствии признаков почечного повреждения обозначается как «начальное снижение СКФ», диагноз ХБП не ставится. Таким пациентам рекомендуют контроль состояния почек не реже 1 раза в год и активную профилактику ХБП.
Стадии хронической болезни почек по МКБ-10:
292
N18.1 ХБП 1-й стадии, повреждение почек с нормальной или повышенной СКФ
(>90 мл/мин);
N18.2 ХБП 2-й стадии, повреждение почек с незначительно сниженной СКФ (60-89 мл/мин);
N18.3 ХБП 3-й стадии, повреждение почек с умеренно сниженной СКФ (30-59 мл/мин);
N18.4 ХБП 4-й стадии, повреждение почек с выраженным снижением СКФ (15-29 мл/мин);
N18.5 ХБП 5-й стадии, хроническая уремия, терминальная стадия заболевания почек (включая случаи ЗПТ - диализ и трансплантацию).
В данной классификации термин «почечная недостаточность» употребляется, когда речь идет о терминальной стадии хронического заболевания почек.
Значение СКФ <60 мл/мин (для диагностики ХБП) выбрано ввиду соответствия на этом этапе гибели более 50% нефронов. Существует достаточно близкое соответствие более ранних классификаций ХПН и классификации ХБП: ХПН I степени соответствует 3-й стадии ХБП (таких больных больше всего в популяции), ХПН II степени - 4-й стадии ХБП, ХПН III степени - 5-й стадии ХБП.
Хроническая болезнь почек занимает среди хронических неинфекционных болезней особое место, поскольку она широко распространена в популяции и составляет не менее 10%, а у отдельных категорий, например у больных инсулинозависимым сахарным диабетом, достигает 20% (для сравнения: хроническая сердечная недостаточность встречается у 1% населения).
К развитию ХБП может привести первичная патология почек: хронический или подострый гломерулонефрит (40% больных с ХБП), хронический пиелонефрит (32%), поликистоз и амилоидоз почек, лекарственный интерстициальный нефрит, туберкулез почек. Но самые распространенные в популяции заболевания почек - это вторичные нефропатии, когда ХБП развивается в результате вторичного поражения почек на фоне таких заболеваний, как сахарный диабет, гипертоническая болезнь, септический эндокардит, системные заболевания соединительной ткани, гиперкортицизм, гипернефрома, гемолитические анемии, гемобластозы (лейкозы).
Несмотря на многообразие этиологических факторов, большинство хронических заболеваний почек имеют единый механизм прогрессирования, а морфологические изменения в почках при почечной недостаточности однотипны и сводятся к преобладанию фибропластических процессов с замещением функционирующих нефронов соединительной тканью и сморщиванию почек.
У женщин с тяжелой ХПБ зачатие не происходит. При латентной стадии беременность обычно протекает как при 2-й степени риска. 4-я стадия ХПБ (II степень ХПН) соответствует 3-й степени риска для беременности и родов, а сама беременность способствует прогрессированию процесса, поэтому беременность в этой стадии противопоказана.
Принципы терапии беременных с ХБП. Обязательно применяется лечебноохранительный режим - ограничение нагрузки. Используется диета с ограничением белка (но не менее 80-100 г) наряду с достаточным введением аминокислот. Высокая калорийность обеспечивается за счет дополнительного введения жиров и углеводов (полиненасыщенные жирные кислоты), потребления значительного количества овощей и фруктов. Требуется ограничение соли - не более 5 г. При сохранной выделительной функции - количество выпиваемой жидкости существенно не ограничивается, до 2 л.
293
Медикаментозная терапия: внутривенные инфузии кристаллоидных растворов и растворов глюкозы♠, кальций, маннитол♠ (500 мл) или фуросемид для стимуляции диуреза. Гипотензивная терапия - допегит♠, клофелин♠, антагонисты кальция. При этом стремиться к снижению АД до нормальных цифр не нужно во избежание снижения почечного кровотока и ухудшения функции почек. Нельзя применять магнезиальную терапию, сердечные гликозиды, антикоагулянты. Антибактериальная терапия может применяться только в сниженных дозах.
При умеренно выраженной ХБП консервативная терапия может быть достаточно эффективной.
19.3. Беременность и анемии
МКБ-10: О99.0
Анемия (малокровие) - это клинико-гематологический синдром, характеризующийся снижением уровня гемоглобина или числа эритроцитов в крови из-за нарушения его продукции, повышенного разрушения, кровопотери или сочетания этих причин.
Анемия является частым осложнением беременности. При этом, несмотря на все многообразие форм малокровия, в 90% случаев диагностируется железодефицитная анемия (ЖДА). Существует зависимость между частотой выявления ЖДА беременных и уровнем социально-экономического развития. Так, по данным ВОЗ (2002), в развитых странах она встречается у 20-25% беременных, а в развивающихся - у 40-80%. Частота анемии у беременных, по данным Минздрава РФ, за последние 10 лет увеличилась в 6,3 раза.
Значение железа в организме велико. Железо является незаменимой составной частью гемоглобина, миоглобина, цитохромов, пероксидаз, ферментов желудочнокишечного тракта, клеток белой крови, переносчиков электронов по дыхательной цепи митохондрий. Железо участвует в синтезе структур костной ткани, играет значительную роль в снабжении клеток энергией, участвует в синтезе ДНК и в обеспечении функции иммунной системы.
В организме человека содержится 4000-4500 мг железа. Основная масса его сконцентрирована в гемоглобине (1500-3000 мг). От 500 до 1500 мг депонируется в печени, селезенке, костном мозге в виде ферритина и гемосидерина. На долю миоглобина и некоторых жизненно важных ферментов приходится не более 500 мг. Сывороточное (транспортное) железо в форме трансферрина, являющегося переносчиком железа, содержит 3-4 мг. Вне беременности суточный расход и, следовательно, потребности железа не превышают 2 мг.
Во время физиологически протекающей беременности потребность организма женщины в железе возрастает: 500 мг необходимо для усиления эритропоэза, 300 мг - на развитие фетоплацентарной системы и рост мышечного слоя матки, 190 мг - текущий расход железа, 230 мг - предполагаемые потери в родах. Таким образом, в целом за весь период беременности расходуется 1220 мг железа. Эта потребность восполняется за счет усиления процессов всасывания железа в кишечнике и мобилизации его из депо. Поступление железа за беременность с пищей составляет в среднем 760 мг, а недостающие 460 мг восполняются за счет запасов депо.
Однако у многих женщин механизмы, обеспечивающие повышенный расход железа, могут оказаться недостаточными по самым разным причинам:
294
1)несбалансированное питание, бедное железом, белками животного происхождения, витаминами (С, В6, В12, фолиевая кислота), микроэлементами;
2)нарушение всасывания железа при заболеваниях желудочно-кишечного тракта (гастрит, дуоденит, хронический энтерит и др.) и ранних токсикозах;
3)заболевания печени, при которых нарушаются процессы депонирования железа и/или продукции трансферрина;
4)потеря железа в результате повторяющихся кровотечений, не связанных с беременностью (язвенная болезнь желудка или двенадцатиперстной кишки, геморроидальные узлы, мочекаменная болезнь, носовые кровотечения и др.);
5)обильные менструальные кровопотери;
6)частые роды с длительным лактационным периодом;
7)повторные кровотечения при настоящей беременности, осложненной предлежанием плаценты;
8)многоплодная беременность.
С прогрессированием беременности изменения гомеостаза (иммунологические сдвиги и высокий уровень эстрадиола, угнетающие эритропоэз) способствуют переходу латентного дефицита железа в истинную железодефицитную анемию. Прогрессирующая анемия сопровождается развитием кислородного голодания, приводящего к функциональным (чаще) и органическим (реже) изменениям всех органов и тканей женщины. Формируется маточноплацентарная недостаточность и, как следствие ее, страдание плода.
На фоне анемии возникают многочисленные осложнения беременности и родов. Даже при скрытом дефиците железа у 59% женщин отмечается неблагоприятное течение беременности. При наличии анемии частота осложнений беременности крайне высока, возникают угроза прерывания беременности (20-42%), ранний токсикоз (29%), гестоз (40%), артериальная гипотензия (40%), преждевременная отслойка плаценты (25-35%), преждевременные роды (11-42%), плацентарная недостаточность, синдром задержки развития плода (25%). Наличие анемии может привести к возникновению преждевременного излития околоплодных вод (30%), слабости родовой деятельности (10-37%), преждевременной отслойке плаценты (10%), антенатальной и интранатальной гипоксии плода (35%). Анемия является фактором риска, оказывающим влияние на становление внешнего дыхания у новорожденных: до 29% новорожденных рождаются в состоянии асфиксии. Перинатальная смертность при анемии составляет от 4,5 до 20,7 ?.Врожденные аномалии развития плода имеют место в 17,8% случаев. Около 40% материнской смертности имеет связь с анемией. С анемией связаны атонические и гипотонические кровотечения в последовом и раннем послеродовом периоде (до 50%), ДВС-синдром и коагулопатические кровотечения, гнойно-септические заболевания в родах и послеродовом периоде (10-12%), гипогалактия (30-40%). Дефицит железа вызывает отставание в психосоматическом и умственном развитии в первые годы жизни ребенка.
Общепринятой классификации ЖДА не существует. По выраженности клинических проявлений условно выделяют следующие стадии развития железодефицитного состояния.
I стадия - потеря железа превышает его поступление, постепенное истощение запасов, всасывание в кишечнике компенсаторно увеличивается.
II стадия - латентный железодефицит. Истощение запасов в депо железа препятствует нормальному эритропоэзу, эриропоэз начинает снижаться.
295
III стадия - манифестный железодефицит, или железодефицитная анемия, со снижением цветового показателя и других индексов насыщения эритроцитов гемоглобином.
У беременных в зависимости от уровня гемоглобина (Hb) принято различать три степени тяжести анемии.
1-я степень - легкая: уровень гемоглобина ниже 110 до 100 г/л. 2-я степень - средней тяжести: от 99 до 90 г/л. 3-я степень - тяжелая: ниже 90 г/л.
Клинические проявления железодефицитной анемии многообразны по характеру и интенсивности. Часть из них объясняется количеством гемоглобина, а часть - дефицитом железосодержащих ферментов.
Первая группа симптомов ассоциируется с недостаточным обеспечением тканей кислородом. Женщин могут беспокоить слабость, быстрая утомляемость, сонливость днем и нарушение сна ночью, головокружение, обморочные состояния, сердцебиение, одышка. Вторая группа клинических признаков связана с дефицитом железа. К таким симптомам принадлежат изменения кожи, ногтей, волос, извращения вкуса и обоняния. Кожа у беременных становится сухой, ногти - ломкими, волосы - сухими и секущимися. Может появиться желание есть мел или глину, нюхать резко и даже неприятно пахнущие вещества.
Предположительный диагноз устанавливается на основании анамнеза (наличие предрасполагающих факторов) и на особенностях клинического течения заболевания (появление жалоб, свидетельствующих о кислородной недостаточности и дефиците железа). Для точной диагностики необходимы результаты лабораторных исследований.
Лабораторные признаки железодефицитной анемии:
1)уровень гемоглобина ниже 110 г/л;
2)количество эритроцитов менее 3,5 млн/л;
3)цветовой показатель менее 0,85;
4)гематокрит менее 0,33;
5)изменение морфологии эритроцитов (пойкилоцитоз, анизоцитоз);
6)микроцитоз (наличие эритроцитов средним объемом ниже 80 мкм3);
7)уровень сывороточного железа менее 12,5 мкмоль/л;
8)содержание ферритина менее 12 мкг/л;
9)средняя концентрация гемоглобина в эритроците менее 33%;
10)коэффициент насыщения трансферрина железом ниже 16%.
Гипохромная анемия (железодефицитная и анемия хронических воспалений) составляет до 85% всех анемий. Редко встречающиеся формы анемий при беременности - талассемия, сидеробластная анемия, анемия при свинцовых отравлениях. При талассемии или иной гемоглобинопатии требуются электрофоретический или хроматографический методы диагностики. В случае подтвержденной гемоглобинопатии (обычно гетерозиготной) следует выполнить диагностическое обследование партнера и, при наличии риска для плода, использовать инвазивную пренатальную диагностику. В редких случаях, сложных в диагностическом плане, приходится прибегать к стернальной пункции. Показания к ней определяют специалисты-гематологи.
«Золотым стандартом» диагностики гипохромной анемии является определение уровня ферритина. Определение ферритина в сыворотке крови используется для диагностики и мониторинга дефицита или избытка железа, дифференцированной диагностики анемий. Ферритин - растворимый в воде комплекс гидроокиси железа с
296
белком апоферритином. Он находится практически во всех тканях, но преимущественно в клетках печени, селезенки, костного мозга и ретикулоцитах. Ферритин является основным белком человека, депонирующим железо. Он содержит 20% общего количества железа в организме. Низкие значения ферритина - это первый показатель уменьшения запасов железа. Снижение уровня СФ во время беременности связано с расходом запасов материнского железа на нужды плодово-плацентарного комплекса. Вне беременности его уровень не должен быть менее 60-80 нг/мл, к середине беременности - не менее 30-40 нг/мл, а в III триместре - не менее 12 нг/мл. Крайне опасно снижение уровня ферритина менее 8 нг/мл.
Хронический или острый воспалительный процесс в организме исключает использование сывороточного ферритина как показателя оценки запасов железа. При наличии в организме воспалительного процесса определяемый уровень ферритина в сыворотке крови может быть «ложно нормальным» или «ложно повышенным», так как ферритин и белки острой фазы реагируют одинаково, т. е. ферритин также проявляет себя в качестве активного участника воспаления. По этой причине рекомендуют определять уровень С-реактивного белка параллельно с определением уровня ферритина. При анемии хронических воспалений информативны также параметры системы гемостаза, так как любой воспалительный процесс в организме инициирует активацию гемостатического потенциала и сопровождается повышением таких маркеров, как продукты деградации фибрина - Д-димер. Кроме того, фибриноген является не только прокоагулянтом, но и белком острой фазы воспаления, поэтому его концентрация при инфекционных процессах всегда повышается.
Лечение беременных, страдающих железодефицитной анемией, реализуется по двум направлениям:
1)обязательная адекватная коррекция дефицита железа;
2)терапия экстрагенитальных заболеваний и/или осложнений беременности при их
наличии.
Следует помнить, что ликвидировать дефицит железа в организме можно только назначением железосодержащих лекарственных средств. Известно, что при анемии всасывание железа в кишечнике активизируется, но максимальное количество железа, которое может поступить из пищи, составляет 2,5 мг/сут, в то время как из лекарственных препаратов может усвоиться в 15-20 раз больше, поэтому диета, богатая железом, белком
ивитаминами, служит только фоном для медикаментозного лечения. Из 2,5 мг железа, максимально всасываемого из пищи, 1/3 поступает в виде гема, из мясных продуктов. Гемовое железо дополнительно переносится гаптоглобином, поэтому его всасывание больше, чем из растительной пищи. Так, из мяса всасывается 6% железа, а из растительной пищи - 0,2%. Наибольшее количество железа содержится в свиной печени, в сердце, говядине, какао, яичном желтке. Современные железосодержащие поливитаминные комплексы, в которых железо присутствует в необходимой суточной дозировке, являются хорошими средствами профилактики железодефицита, но так же, как
идиета, не могут ликвидировать уже имеющуюся железодефицитную анемию.
Враспоряжении врача имеется большой выбор препаратов железа для перорального и парентерального использования.
Препараты железа для приема внутрь. Современные пероральные железосодержащие препараты отличаются удобством применения, хорошей переносимостью и достаточной эффективностью (табл. 19.5). В состав многих препаратов входят витамины (аскорбиновая и фолиевая кислоты, витамины группы В) и другие компоненты. Препараты двухвалентного железа всасываются с помощью
297
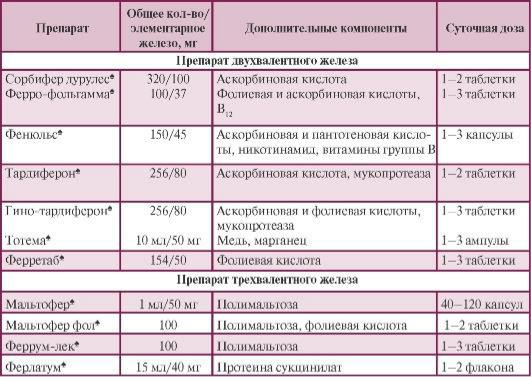
циркулирующего в крови дивалентного транспортера металлов; трехвалентное железо проникает диффузно.
Таблица 19.5. Препараты железа для приема внутрь
Для лечения латентного железодефицита (сниженный уровень ферритина при нормальном уровне гемоглобина) необходимо применять 50-100 мг элементарного железа в сутки, что может быть достигнуто при приеме 100 мг препарата трехвалентного железа или 150 мг препарата двухвалентного железа. При манифестном железодефиците, т. е. стадии ЖДА, суточная доза элементарного железа должна составлять 120-160 мг, что соответствует 300-350 мг препарата двухвалентного или 200 мг препарата трехвалентного железа. Терапия препаратами железа должна быть длительной. Увеличение содержания гемоглобина отмечается лишь к концу 3-й недели лечения. Нормализация всех показателей красной крови наступает только через 5-8 нед. При благоприятных клинических и лабораторных результатах через 2-3 мес лечения можно снизить дозу препарата вдвое и продолжить терапию еще на 2-3 мес.
При наличии у беременных заболеваний желудочно-кишечного тракта или при индивидуальной непереносимости препаратов, принимаемых внутрь, при медленном или недостаточном эффекте от пероральной терапии следует использовать парентеральный метод введения препаратов железа.
Показания к внутривенной ферротерапии при беременности: отсутствие ответа на прием железа внутрь (повышение уровня гемоглобина менее чем на 10 г/л через 14 дней лечения); несоблюдение назначенного лечения; непереносимость пероральных препаратов железа (побочные эффекты со стороны желудочно-кишечного тракта), тяжелая, запущенная или прогрессирующая анемия (уровень гемоглобина ниже 90 г/л), стремление быстро достичь эффекта (на поздних сроках беременности), при лечении и в ряде других случаев.
При гипохромной анемии на фоне хронических воспалений наиболее часто наблюдается низкая эффективность пероральной терапии железосодержащими препаратами. И в патогенезе развития анемии хронических воспалений, и в низкой эффективности ее пероральной ферротерапии большую роль играет белок гепсидин.
298
Железо может быть токсичным. Оно катализирует образование активных форм кислорода и в высоких концентрациях повреждает клетки. В связи с этим абсорбция железа находится в организме под жестким контролем. Гепсидин является гормоном, регулирующим содержание железа и ответственным за развитие анемий при хронических заболеваниях. Он продуцируется гепатоцитами и при этом относится к белкам острой фазы, участвующим в инфекционных и воспалительных процессах. Уровень гепсидина растет при инфекциях или воспалении и падает при гипоксии или анемии. Связь между воспалением/ инфекцией и продукцией гепсидина в печени осуществляется через выработку цитокинов, в первую очередь интерлейкина-6.
Кроме того, уровень гепсидина повышается при хронической болезни почек, что способствует развитию нефрогенной анемии и резистентности к стимуляторам эритропоэза.
Обходя действие гепсидина, внутривенная ферротерапия обеспечивает прямой транспорт железа к клеткам костного мозга. Внутривенное введение препаратов железа при анемии хронических воспалений обеспечивает:
1) достижение |
эффективной |
стимуляции |
эритропоэза: |
переключает |
|||
гипопролиферативный |
и |
неэффективный |
варианты |
эритропоэза |
на |
||
гиперпролиферативный; |
|
|
|
|
|
|
|
2)ускорение темпов прироста запасов железа;
3)преодоление блокады белком гепсидином трансмембранного транспорта ионов железа в энтероцитах.
Современные препараты железа для внутривенного применения - карбоксимальтозат железа (ферринжект♠), изомальтозат железа (монофер♠), сахарат железа (венофер♠) и декстран железа (космофер♠), которые представляют собой сферические железоуглеводные коллоиды (табл. 19.6). Эффективность и безопасность внутривенных препаратов железа зависят от их молекулярной массы, стабильности и состава. Стабильность такому комплексу придает углеводная оболочка, которая замедляет высвобождение железа и поддерживает образующиеся формы в коллоидной суспензии. Комплексы с низкой молекулярной массой, такие как глюконат железа (феррлецит♠), в настоящее время не используются, поскольку они менее стабильны и быстрее высвобождают в плазму железо, которое в свободном виде может катализировать образование реактивных форм кислорода, вызывающих перекисное окисление липидов и повреждение тканей. Препараты декстрана железа обладают большой молекулярной массой и высокой стабильностью, но характеризуются повышенным риском аллергических реакций, поэтому не показаны к применению в акушерстве.
Таблица 19.6. Препараты железа для внутривенного использования
|
|
|
Кол-во |
железа |
|
|
|
|
|
|
|
Препарат |
Форма железа |
|
(мг)/ |
|
Разовая доза и частота введения |
|
|||||
|
элементарного |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
железа в 1 мл |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Железа |
(III) |
|
|
2-3 раза в неделю внутривенно по 5- |
||||||
Венофер♠ |
гидроксид |
|
1 мл/20 мг |
|
|||||||
|
|
10 мл (100-200 мг) |
|
|
|
||||||
|
сахарозный комплекс |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
||||||
|
|
|
|
|
2 раза в неделю внутривенно по 10 |
||||||
Ферринжект♠ |
Железа |
(III) |
1 мл/50 мг |
|
мл |
(500 |
мг) |
в |
200 |
мл |
|
|
карбоксимальтозат |
|
|
изотонического |
раствора |
натрия |
|||||
|
|
|
|
|
хлорида или |
1 |
раз |
в |
неделю |
||
|
|
|
|
|
|
|
|
|
|
|
299 |
|
|
|
|
внутривенно 20 мл (1000 мг) в 250 |
|
|
|
|
мл изотонического раствора натрия |
|
|
|
|
хлорида |
|
|
|
|
|
|
Железа |
(III) |
|
2-3 раза в неделю внутривенно по 2- |
Космофер♠ |
гидроксид |
декстрана |
1 мл/50 мг |
4 мл (100-200 мг) или введение |
|
комплекс |
|
|
общей дозы железа за один прием |
|
|
|
|
|
|
|
|
|
2-3 раза в неделю внутривенно по 2 |
|
|
|
|
мл в 200 мл изотонического |
|
|
|
|
раствора натрия хлорида капельно |
Монофер♠ |
Железа |
(III) |
1 мл/100 мг |
(30 мин). |
|
||||
|
олигоизомальтозат |
|
1 раз в неделю (до 20 мг/кг) в 500 |
|
|
|
|
|
мл изотонического раствора натрия |
|
|
|
|
хлорида внутривенно капельно (60 |
|
|
|
|
мин) |
|
|
|
|
|
Препаратами выбора для внутривенной ферротерапии во время беременности и в послеродовом периоде являются венофер♠, ферринжект♠ и монофер♠. Ферринжект♠ и монофер♠, в отличие от сахарата железа, благодаря высокой молекулярной массе и низкой аллергенности, могут вводиться однократно, в высокой дозе.
Оценка эффективности внутривенной ферротерапии производится на 7-10-й день после однократной инфузии ферринжекта♠ или монофера♠ (или 3-5 инфузий венофера♠), при недостаточном повышении уровня гемоглобина курс можно повторить.
Однако следует помнить, что подходы к внутривенной терапии железодефицитной анемии (ЖДА) и анемии хронических воспалений (АХП) различны.
При ЖДА у беременных накануне родоразрешения и, особенно, у родильниц после кровопотери возможно введение однократной общей дозы ферринжекта♠или монофера♠, рассчитанной по формуле:
(Целевой уровень гемоглобина - Реальный уровень гемоглобина) х Масса тела х
0,24 + 500 мг.
При анемии хронических воспалений первостепенной задачей является снижение реакции воспаления. Железосодержащие препараты могут вводиться внутривенно только дробно, по 100-200 мг 2 раза в неделю. По необходимости добавляют препараты эритропоэтина.
При железодефицитной анемии II и III степени тяжести для стимуляции эритропоэза можно использовать подкожные инъекции рекомбинантного эритропоэтина - эпокрина♠. Известно, что эритропоэтин является одним из главных факторов, регулирующих эритропоэз. Насыщение организма беременной железом и в этой ситуации остается обязательным.
Профилактика железодефицитной анемии должна распространяться на всех беременных. На фоне рационального питания обязателен прием препаратов железа. По рекомендации ВОЗ, все женщины с самого начала беременности (не позднее 12-й недели и до родов) должны принимать 60 мг элементарного железа и не менее 400 мг фолиевой кислоты в сутки. Такие комплексные препараты - витрум пренатал♠, элевит пронаталь♠, железо плюс♠, пренатал оптима♠ - можно назначать курсами по 3 нед с перерывами на 3 нед.
300
