
ПРАКТИКУМ Гентех в мед ЛЕЧ 4 02 24
.pdf11
записывается легенда (данные о состоянии здоровья родственников, причинах и возрасте смерти и др.) и указывается дата составления этого документа.
Заболевания в родословной обозначают произвольно, чаще соответствующий символ полностью затушевывают; различные заболевания обозначаются разными символами. В некоторых случаях одним символом можно отметить несколько заболеваний.
После сбора анамнестических данных и оформления родословной необходимо приступить к клиническому обследования пробанда. Для этого проводят детальный осмотр, описывают фенотип (объективный статус), проводят дополнительные консультации специалистов и исследования и оценивают их результаты для проведения
синдромологического анализа и верификации диагноза.
МЕТОДИКА ГЕНЕАЛОГИЧЕСКОГО АНАЛИЗА
При анализе родословной исследователь может встретиться с генными и хромосомными заболеваниями, с болезнями, в развитии которых участвуют как генетические, так и средовые факторы, а также с «неизвестными» заболеваниями.
Генеалогический анализ при моногенных заболеваниях.
В настоящее время врачу приходится в большинстве случаев сталкиваться с уже известными моногенными заболеваниями, клинические особенности и тип наследования которых указаны во многих медицинских справочниках, хотя на практике врачу гораздо чаще приходится иметь дело с малыми семьями, он должен уметь ориентировочно определять тип наследования генных заболеваний, поскольку иногда от этого зависит правильно ли будет поставлен диагноз.
Этапы анализа родословной с моногенным заболеванием:
1)Определение типа наследования.
2)Определение генотипа индивидуумов.
3)Расчет величины генетического риска.
При аутосомно-доминантном типе наследования родословная имеет характерные признаки:
1.больными могут быть и мужчины, и женщины в равной степени, поскольку ген локализуется в аутосоме;
2.больные встречаются в каждом поколении;
3.каждый больной член семьи обычно имеет больного родителя;
4.вероятность рождения больного ребенка, если болен один из родителей, равна 50%;
5.у здоровых родителей дети будут здоровы.
При аутосомно-рецессивном типе наследования родословная имеет следующие отличительные признаки:
1.мужчины и женщины болеют одинаково часто;
2.заболевание в родословной встречается через поколения;
3.у здоровых родителей рождаются больные дети. Наиболее частый тип браков – это брак между гетерозиготными носителями (Аа х Аа), когда оба родителя здоровы, но у них могут быть дети с гомозиготным генотипом, поэтому у гетерозиготных носителей вероятность рождения больного ребенка равна 25%;
4.у больного родителя рождаются здоровые дети. В браке лица с рецессивной болезнью со здоровым человеком (обычно АА х аа) все дети будут здоровы;
5.болеют в основном сибсы, а не родители;
6. |
все дети |
больных родителей являются гетерозиготными носителями патологи- |
|
ческого гена; |
|
7. |
дети с АР заболеваниями часто рождаются в кровнородственных браках. |
|
|
Для |
Х-сцепленного рецессивного наследования характерно: |
1. |
болеют преимущественно лица мужского пола; |
|
12
2.больные мужчины наследуют патологический ген от матери, которая является здоровой носительницей этого аллеля;
3.сын никогда не наследует заболевание отца;
4.если больная женщина, ее отец обязательно болен, а мать – гетерозиготная носительница и болеют все ее сыновья;
5.в браке больных мужчин и здоровых гомозиготных женщин все дети будут здоровы, но у дочерей могут быть больные сыновья (с вероятностью 50%);
6.в браке здорового мужчины и гетерозиготной женщины вероятность рождения больного
сына составит 50%, а все девочки будут здоровыми.
Для Х-сцепленного доминантного наследования характерно:
1.Поражаются и мужчины, и женщины, но больных женщин в 2 раза больше, чем мужчин.
2.Больные женщины передают патологический аллель в среднем 50% сыновей и 50% дочерей.
3.Больной мужчина передает патологический аллель всем дочерям и не передает сыновьям, поскольку последние наследуют Y-хромосому.
4.В среднем мужчины (их генотип гемизиготный - XAY) болеют более тяжело, чем женщины (их генотип гетерозиготный -ХАХа ).
Митохондриальное наследование имеет следующие признаки:
1.болезнь передается только от матери.
2.больны и девочки, и мальчики.
3.больные отцы не передают болезнь ни дочерям, ни сыновьям.
Расчет риска при хромосомных болезнях.
При спорадических случаях числовых перестроек используются эмпирические данные.
При мозаицизме применяется следующая формула [Х:(2-Х)]·К, где Х – доля аномального клеточного клона, К – коэффициент элиминации несбалансированных зигот в эмбриогенезе.
При структурных перестройках эмпирические данные комбинируются с теоретическими расчетами.
Генеалогический анализ при мультифакториальных заболеваниях.
Анализ родословных мультифакториальных заболеваниях основан не на законах Менделя, так как их наследование полигенное, а на эмпирически полученных данных. Величина генетического риска мультифакториального заболевания зависит от следующих сведений клинико-генеалогического исследования:
1.От степени родства пробанда с больным(и) родственником(ами).
2.Числа больных родственников
3.От степени тяжести больного родственника, так как степень тяжести при мультифактори-
альных заболеваниях определяется суммарным действием нескольких генов.
4.От пола пробанда и больных родственников. Вероятность возникновения заболевания увеличивается в семье, в которой больной родственник относится к редко поражаемому полу.
Таблица 2
Величина генетического риска
0-5% |
низкий |
6-20% |
средний |
Более 20% |
высокий |
КОНТРОЛЬ ИСХОДНОГО УРОВНЯ ЗНАНИЙ
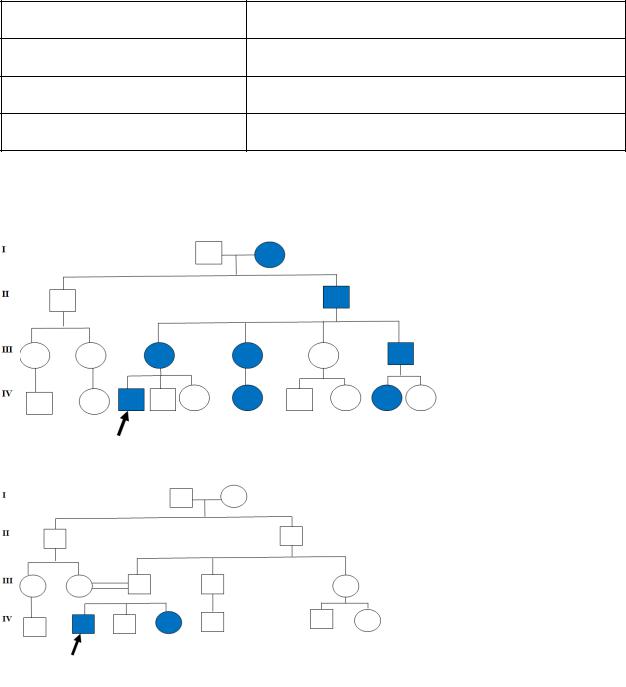
По предложенным родословным определить тип наследования заболевания, ответ обосновать.
13
ПРАКТИЧЕСКАЯ РАБОТА:
1.Разобрать цель и сущность клинико-генеалогического исследования, необходимость использования метода.
2.Методики расчета генетического риска при разных видах наследственной патологии Перенесите таблицу в тетрадь и заполните её.
Таблица 3
Методы расчета генетического риска при разных видах наследственной патологии
Генные болезни
- кровное родство супругов
Хромосомные синдромы
Мультифакториальная патология
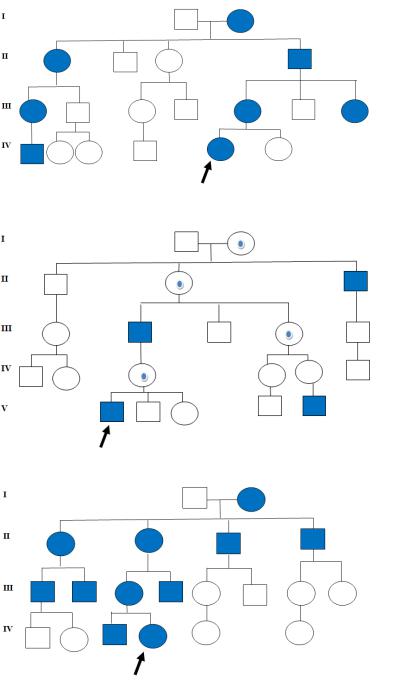
3.Провести анализ родословных с моногенным наследованием: определить тип наследования заболевания; генотипы пробанда и его родителей; определить генетический риск для сибса пробанда.
Родословная 1.
Родословная 2.
Родословная 3.
14
Родословная 4.
Родословная 5.
4.Провести анализ родословных пациентов с хромосомной патологией: определить генетический риск для сибса пробанда.
|
|
Таблица 4 |
Эмпирический риск при хромосомных болезнях (по С.И.Козловой, 2007) |
||
Трисомии 13, 18, 21 |
|
|
|
Возраст матери, годы |
Риск, % |
|
|
|
|
< 19 |
0,08 |
|
20-24 |
0,06 |
|
|
|
Суммарный популяционный риск в |
25-29 |
0,1 |
зависимости от возраста матери |
30-34 |
0,2 |
|
|
|
|
35-39 |
0,54 |
|
|
|
|
40-44 |
1,6 |
|
|
|
|
> 45 |
4,2 |

15
Трисомия 21 (синдром Дауна)
|
|
|
|
|
Повторный риск синдрома Дауна для сибсов пробанда в |
||||||||
|
|
|
|
|
|
|
зависимости от возраста матери |
||||||
|
Простая трисомная |
|
|
|
|
|
|
|
|
|
|
|
|
|
форма |
|
Возраст матери |
|
|
|
|
Риск |
|||||
|
|
|
|
До 35 лет |
|
|
|
|
1 % |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
Свыше 35 лет |
|
|
Удвоенный риск для данной возрастной группы |
|||||||
|
Транслокационная форма |
|
|
|
Риск для сибсов в спорадических случаях (при нормальном |
||||||||
|
|
|
|
|
кариотипе родителей) соответствует простой трисомии. |
||||||||
|
Риск для потомства |
|
|
Тип транслокации |
|
|
Пол носителя |
||||||
|
носителей семейных |
|
|
|
женщина |
|
|
мужчина |
|||||
|
|
|
|
|
|
|
|
|
|
||||
|
робертсоновских |
|
|
|
(21q22q) |
|
|
7% |
|
2% |
|
||
|
транслокаций (%) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(21q14q) |
|
|
10% |
|
2,4% |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(21q21q) |
|
|
100% |
|
100% |
|
||
|
Мозаицизм у родителей |
|
|
|
Риск = х / (2-х)*2, где х – доля аномального клеточного клона |
||||||||
|
Синдром Патау (трисомия 13) и Эдвардса (трисомия 18) |
||||||||||||
|
Простая трисомная форма и |
|
|
Риск для сибсов очень низкий (менее 1%) |
|||||||||
|
спорадическая транслокация |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||
|
Мозаицизм у родителей |
|
|
Риск = х/(2-х)*2, где х – доля аномального клеточного клона |
|||||||||
|
|
|
|
|
|
|
|
|
Повторный риск несбалансированных |
||||
|
|
|
|
|
|
|
|
|
хромосомных аномалий для сибсов |
||||
|
|
|
|
|
Тип транслокации |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
пол носителя |
|||
|
Семейные транслокации с |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
женщина |
|
|
мужчина |
||||
|
участием хромосомы 13 |
|
|
(13q14q) |
|
|
2% |
|
|
1% |
|
||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
(13q15q) |
|
|
2% |
|
1% |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
(13q13q) |
|
|
100% |
|
100% |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
(13q21q) |
|
|
10-15% |
|
|
<1% |
|
|
|
|
|
Структурные аномалии аутосом |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|||||
|
Риск для сибсов в спорадических случаях |
|
|
Очень низкий (менее 1%) |
|
||||||||
|
(при нормальном кариотипе родителей) |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
||||||
5.Разобрать принципы определения генетического риска при мультифакториальной патологии.
Таблица 5
Таблица эмпирического риска некоторых мультифакториальных заболеваний
Заболевание |
Дополнительные условия |
Риск, % |
|||
|
|
||||
для сибсов |
для потомства |
||||
|
|
|
|||
1 |
|
2 |
3 |
4 |
|
Анэнцефалия, |
после 1 |
больного |
2-5 |
|
|
черепно-мозговые грыжи |
после 2 |
больных |
10 |
|
|
|
после 3 |
больных |
15-20 |
|
|
1 |
2 |
3 |
4 |
||
Расщелина губы и/или нёба |
|
4 |
4 |
||
Расщелина нёба |
|
2 |
6-7 |
||
Атрезия пищевода |
|
<1 |
|
|
|
Атрезия и стенозы ануса и прямой кишки |
пробанд девочка |
<1 |
|
|
|
|
пробанд мальчик |
7-8 |
|
|
|
Пороки развития почек (аплазия, гипоплазия, дистопия, сращения) |
|
около 2 |
|
|
|
Гипоспадия |
|
10 – для братьев |
|
|
|
Эписпадия |
|
2 – для братьев |
|
|
|
Врождённый вывих бедра |
пробанд женщина |
1 – для братьев |
|
|
|
|
|
|
5 – для сестёр |
|
|
|
|
|
|
|
|
|
пробанд мужчина |
5 – для братьев |
|
|
|
|
|
|
7 – для сестёр |
|
|
Косолапость |
|
2 |
|
|
|
Множественный артрогриппоз спорадические случаи |
5 |
|
|
||
Множественные пороки развития неклассифицированного комплекса |
3 |
|
|
||
Детский церебральный паралич |
в спорадическихслучаяхпри |
2-3 |
|
|
|
|
исключении родовой трав- |
|
|
|
|
|
мы, моногенных синдромов |
|
|
|
|
Микрофтальм |
в спорадических случаях |
12 |
|
|
|
Колобома глаза |
в спорадических случаях |
10-20 |
|
|
|
Косоглазие |
|
10-15 |
|
|
|
Шизофрения |
если болен один из роди- |
|
|
10 |
|
|
если больны оба родителя |
|
|
40 |
|
|
спорадические случаи |
10 |
|
|
|
Аффективные психозы |
|
5-10 |
|
|
|
Глухота неясной этиологии |
спорадические случаи |
17 |
|
|
|
|
один из родителей глухой |
|
|
3-10 |
|
|
оба родителя глухие |
|
|
10-30 |
|
Аномалад Пьера-Робена (расщелина неба, микрогнатия, глоссоптоз) |
2-3 |
|
|
||
Язвенная болезнь желудка |
|
7,5 |
|
|
|
Язвенная болезньдвенадцатиперстнойкишки |
взрослая форма |
9 |
|
|
|
|
детская форма |
3 |
|
|
|
Псориаз |
|
16 |
20 |
||
Диффузный токсический зоб |
|
10 |
|
|
|
Злокачественные опухоли |
|
|
|
|
|
Прямой кишки |
|
|
5 |
|
|
Желудка |
|
|
5 |
|
|
Молочной железы |
|
|
6-7 |
|
|
Предстательной железы |
|
|
<1 |
|
|
Щитовидной железы |
|
|
<1 |
|
|
Тела матки |
|
|
6-7 |
|
|
Шейки матки |
|
|
<1 |
|
|
Аллергические заболевания |
|
|
|
|
|
Атопический дерматит |
|
|
16 |
|
|
Бронхиальная астма |
|
|
8-9 |
|
|
Системная красная волчанка |
|
|
2-10 |
|
|
Ревматоидный артрит |
|
|
5 |
|
|
6.Решить ситуационные задачи с использованием клинико-генеалогического метода.
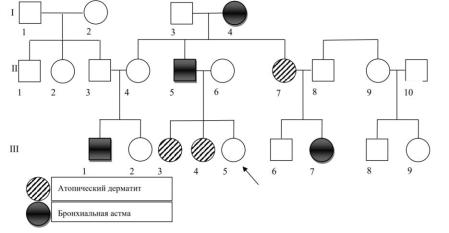
1.Оцените вероятность возникновения мульфакториального заболевания.
2.С помощью таблицы эмпирического риска развития мультифакториальных заболеваний и представленной родословной определите: риск какого заболевания (атопический дерматит или бронхиальная астма) может развиться у детей пробанда с большей вероятностью?
17
18
ЗАНЯТИЕ 2 Тема: Современные методы диагностики хромосомных болезней.
Цель занятия: углубить компетенции цитогенетического анализа. Понимать суть методик проведения цитогенетических исследований. Изучить основные способы окраски препаратов метафазных хромосом для анализа кариотипа. Изучить этапы приготовления, окраски, анализа препаратов метафазных хромосом на основе рутинной окраски. Изучить возможности использования рутинной окраски в исследовании кариотипа человека в норме и патологии.
Вопросы для самоподготовки:
1.Основы цитогенетического анализа.
2.Экспресс-методы определения полового хроматина.
3.Цитологические характеристики кариотипа (цитогенетическая номенклатура, аббревиатура, терминология).
4.Классификации хромосом человека.
5.Методика культивирования хромосом (этапы, методы окрашивания препаратов метафазных хромосом (рутинная, дифференциальная)
6.Флюоресцентная гибридизация in situ (FISH), основные этапы FISH-анализа.
7.Хромосомные патологии, выявляемые молекулярной цитогенетикой.
НЕОБХОДИМО ЗНАТЬ:
1.Методы цитогенетического анализа.
2.Методы экспресс-диагностики полового хроматина.
3.Денверскую классификация хромосом человека.
4.Парижскую номенклатуру хромосом.
5.Этапы приготовления препаратов метафазных хромосом.
6.Микроскопический анализ метафазных пластин, используемые в классической цитогенетике.
7.Анализ кариотипа в норме и патологии.
8.Возможности использования метода дифференциальной окраски метафазных хромосом для анализа кариотипа в норме и патологии.
9.Возможности использования флюоресцентной гибридизации in situ для анализа кариотипа в норме и патологии.
НЕОБХОДИМО УМЕТЬ:
1.Пользоваться цитогенетической терминологией.
2.Пользоваться учебной, научной, научно-популярной литературой, сетью Интернет.
НЕОБХОДИМО ВЛАДЕТЬ:
1.Интерпретировать заключения цитогенетического исследования в своей практической работе
2.Использовать результаты цитогенетического анализа в расчете повторного генетического риска.
ВНЕАУДИТОРНАЯ САМОСТОЯТЕЛЬНАЯ РАБОТА
1. Изучить цель и методику проведения классического кариотипирования (рис.1).

19
Рисунок 1
Алгоритм проведения кариотипирования
забор 1-2мл |
|
|
венозной крови |
хромосомный анализ (световая |
окрашивание |
|
микроскопия) |
|
культивирование лимфоцитов:
а) добавление в питательную среду |
|
|
распределение клеток |
|
|
|
|
|
путем раскапывания |
б) введение стимулятора митотического |
|
фиксация клеток |
||
деления лимфоцитов |
– |
|
|
(смесь 3/4 ледяной |
фитогемагглютинина |
(ФГА) |
|
|
уксусной кислоты и ¼ метанола) |
в) инкубация в течение 72 часов (t=37 C) |
центрифугирование (1500об/мин 5 мин) |
|||
г) введение колхицина(70час |
центрифугирование |
введение 4 мл |
||
культивирования) |
|
(1500об/мин 5 мин) |
гипотонического раствора |
|
2.Классификация хромосом человека. Изучить классификацию хромосом человека и краткую характеристику каждой группы.
Рисунок 2
Кариограмма нормального женского кариотипа

20
Группа А (1–3): большие метацентрические хромосомы. Хромосома 2 по морфологии более субметацентрическая.
Группа В (4–5): большие субметацентрические хромосомы.
Группа С (6–12): средние субметацентрические хромосомы. Самая многочисленная группа.
Группа D (13–15): средние акроцентрические хромосомы.
Группа E (16–18): малые субметацентрические хромосомы. Хромосома 16 по морфологии более метацентрическая.
Группа F (19–20): малые метацентрические хромосомы.
Группа G (21–22): малые акроцентрические хромосомы.
Половые хромосомы помещают в конце раскладки. Х-хромосома по морфологии средний субметацентрик (группа С); Y-хромосома малая акроцентрическая (группа G).
3.Изучить дифференциальную окраску хромосом при цитогенетическом исследовании (стандартное (рутинное) окрашивание, схематическое изображение рисунка сегментации и дифференциальное окрашивание хромосом при G, R, C-окраске).
Рисунок 3
Стандартное и дифференциальное окрашивание хромосом
1 |
2 |
3 |
4 |
5 |
------------------------- |
А---------------------------- |
-------------------------------------------------В |
-------------------------------------------------- |
|
6 |
7 |
8 |
9 |
10 |
11 |
12 |
--------------------------------------------------------------------------------- |
|
|
С---------------------------------------------------------------------------------- |
|
|
|
13 |
14 |
15 |
16 |
17 |
18 |
------------------------------------------ |
D----------------------------------- |
|
----------------------------------------E |
-------------------------------------- |
|
19 |
20 |
21 |
22 |
X |
Y |
------------------------- |
F--------------------- |
-----------------------G---------------------- |
|
|
|
4.Изучить цель и методику проведения метода флуоресцентной гибридизации in situ
(FISH).
Метод гибридизации in situ основан на способности ДНК или РНК образовывать устойчивые гибридные молекулы с ДНК / РНК - зондами непосредственно на препаратах фиксированных хромосом и интерфазных ядер. С помощью этого метода можно определить точное местоположение практически любой последовательности ДНК или РНК непосредственно в клетке, клеточном ядре или на хромосомах.
Для проведения гибридизации in situ пригодны цитологические или гистологические препараты клеток любых тканей или органов, приготовленные по стандартным методикам. В условиях клинической цитогенетической лаборатории используют препараты культивированных лимфоцитов периферической крови, клеток цитотрофобласта хорио-
