
соответствует потребностям клетки в энергии. Запасов АТФ в клетке не существует. Относительные концентрации АТФ/АДФ в тканях изменяются в узких пределах, в то время как потребление энергии клеткой, т.е. частота оборотов цикла АТФ — АДФ, может меняться в десятки раз.
Общее содержание АТФ в организме 30-50 г, но каждая молекула АТФ в клетке «живёт» меньше минуты. В сутки у человека синтезируется 40 — 60 кг АТФ и столько же распадается. Увеличение концентрации АДФ немедленно приводит к ускорению дыхания и фосфорилирования.
Транспорт АТФ и АДФ через мембраны митохондрий
В большинстве эукариотических клеток синтез основного количества АТФ происходит внутри митохондрии, а основные потребители АТФ расположены вне её. С другой стороны, в матриксе митохондрий должна поддерживаться достаточная концентрация АДФ. Эти заряженные молекулы не могут самостоятельно пройти через липидный слой мембран. Внутренняя мембрана непроницаема для заряженных и гидрофильных веществ, но в ней содержится определённое количество транспортёров, избирательно переносящих подобные молекулы из цитозоля в матрикс и из матрикса в цитозоль.
В мембране есть белок АТФ/АДФ-антипортер, осуществляющий перенос этих метаболитов через мембрану. Молекула АДФ поступает в митохондриальный матрикс только при условии выхода молекулы АТФ из матрикса:
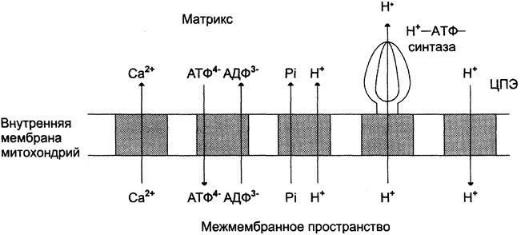
Схема трансмембранного переноса веществ за счёт энергии ∆μН:
потоки различных веществ (АТФ, АДФ, Н3РO4, Са2+) проходят через специфические транспортёры, при этом затрачивается энергия электрохимического потенциала мембраны.
Движущая сила такого обмена — мембранный потенциал переноса электронов по ЦПЭ. Расчёты показывают, что на транспорт АТФ и АДФ расходуется около четверти свободной энергии протонного потенциала. Другие транспортёры тоже
могут использовать энергию электрохимического градиента. Так переносится внутрь митохондрии неорганический фосфат, необходимый для синтеза АТФ. Непосредственным источником свободной энергии для транспорта Са2+ в матрикс также служит протонный потенциал, а не энергия АТФ.
Разобщение дыхания и фосфорилирования
Некоторые химические вещества (протонофоры) могут переносить протоны или другие ионы (ионофоры) из межмембранного пространства через мембрану в матрикс, минуя протонные каналы АТФ-синтазы. В результате этого исчезает электрохимический потенциал и прекращается синтез АТФ. Это явление называют
разобщением дыхания и фосфорилирования. В результате разобщения количество АТФ снижается, а АДФ увеличивается. В этом случае скорость окисления NАDН и ФАDН2 возрастает, возрастает и количество поглощённого кислорода, но энергия выделяется в виде теплоты, и коэффициент Р/О резко снижается. Как правило, разобщители — липофильные вещества, легко проходящие через липидный слой мембраны. Одно из таких веществ — 2,4-динитрофенол, легко переходящий из ионизированной формы в неионизированную, присоединяя протон в межмембранном пространстве и перенося его в матрикс:
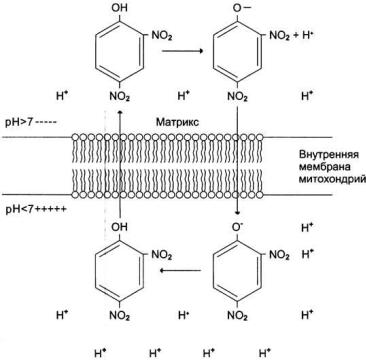
Механизм разобщения дыхания и фосфорилирования:
протонированная форма 2,4-динитрофенола переносит протоны через внутреннюю мембрану митохондрий и препятствует образованию протонного градиента.
Примерами разобщителей могут быть также некоторые лекарства, например, дикумарол — антикоагулянт или метаболиты, которые образуются в организме,
билирубин — продукт катаболизма гема , тироксин — гормон щитовидной железы. Все эти вещества проявляют разобщающее действие только при их высокой концентрации.
Терморегуляторная функция ЦПЭ
На синтез молекул АТФ расходуется примерно 40 — 45% всей энергии электронов, переносимых по ЦПЭ, приблизительно 25% тратится на работу по переносу веществ через мембрану. Остальная часть энергии рассеивается в виде теплоты и используется теплокровными животными на поддержание температуры тела. Кроме того, дополнительное образование теплоты может происходить при разобщении дыхания и фосфорилирования. Разобщение окислительного фосфорилирования может быть биологически полезным. Оно позволяет генерировать тепло для поддержания температуры тела у новорождённых, у зимнеспящих животных и у всех млекопитающих в процессе адаптации к холоду. У новорождённых, а также зимнеспящих животных существует особая ткань, специализирующаяся на теплопродукции посредством разобщения дыхания и фосфорилирования — бурый жир. Бурый жир содержит много митохондрий. В мембране митохондрий имеется большой избыток дыхательных ферментов по сравнению с АТФ-синтазой. Около 10% всех белков приходится на так называемый разобщающий белок (РБ-1) — термогенин. Бурый жир имеется у новорождённых, но его практически нет у взрослого человека. В последние годы появились факты, свидетельствующие о существовании в митохондриях разных органов и тканей млекопитающих разобщающих белков, похожих по своей структуре на РБ-1 бурой жировой ткани. По своей структуре термогенин близок к АТФ/АДФ-антипортеру, но не способен к транспорту нуклеотидов, хотя сохранил способность переносить анионы жирных кислот, служащих разобщителями.
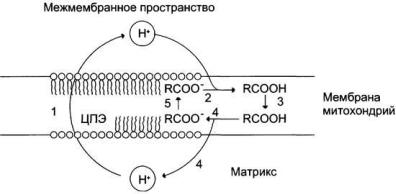
Механизм разобщающего действия жирных кислот:
1 — выкачивание протонов дыхательной цепью; 2 — протонирование аниона жирной кислоты; 3 — диффузия протонированной жирной кислоты к внутренней поверхности мембраны; 4 — диссоциация RСООН с образованием RСОO- и иона
Н+; 5 — перенос RСОOпосредством АТФ/АДФ-антипортера или разобщающего белка к наружной поверхности митохондриальной мембраны.
На внешней стороне мембраны анион жирной кислоты присоединяет протон и в таком виде пересекает мембрану; на внутренней стороне мембраны диссоциирует, отдавая протон в матрикс и тем самым снижает протонный градиент. Образующийся анион возвращается на наружную сторону мембраны с помощью АТФ/ АДФ-антипортера.
При охлаждении стимулируется освобождение норадреналина из окончаний симпатических нервов. В результате происходят активация липазы в жировой ткани и мобилизация жира из жировых депо. Образующиеся свободные жирные кислоты служат не только «топливом», но и важнейшим регулятором разобщения дыхания и фосфорилирования.

ОБЩИЙ ПУТЬ КАТАБОЛИЗМА
Углеводы, жирные кислоты и большинство аминокислот окисляются в конечном счёте через цикл лимонной кислоты до СО2 и Н2О. Прежде, чем эти вещества вовлекаются в заключительный этап катаболизма, их углеродный скелет превращается в двухуглеродный фрагмент в форме ацетил-КоА. Именно в этой форме большая часть «топливных» молекул включается в цикл лимонной кислоты.
Катаболизм основных пищевых веществ:
1 — 3 — пищеварение; 4 — 8 — специфические пути катаболизма; 9 — 10
— заключительный (общий путь) катаболизма; 11 — ЦПЭ; 12 — окислительное фосфорилирование.
Ацетил-КоА образуется в специфических реакциях катаболизма жирных кислот и некоторых аминокислот. Однако главным источником ацетил-КоА служит пировиноградная кислота, образующаяся в реакциях катаболизма глюкозы и некоторых аминокислот. Превращение пирувата в ацетил-КоА происходит при участии набора ферментов, структурно объединённых в пируватдегидрогеназный комплекс (ПДК). Ацетильный остаток — ацетил-КоА далее окисляется в цикле лимонной кислоты до СO2 и Н2O. В этих реакциях окисления принимают участие NAD-
и FAD-зависимые дегидрогеназы, поставляющие электроны и протоны в ЦПЭ, по которой они передаются на O2.
Окислительное декарбоксилирование пирувата
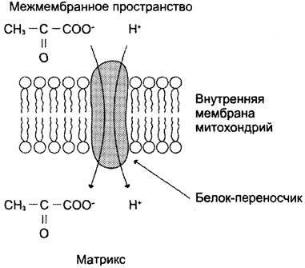
Окислительное декарбоксилированиепирувата происходит в матриксе митохондрий. Транспорт пирувата в митохондриальный матрикс через внутреннюю мембрану митохондрий осуществляется при участии специального белка-
переносчика по механизму симпорта с Н+:
Транспорт пирувата через митохондриальную мембрану
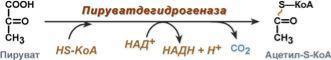
Пируватдегидрогеназный мульферментный комплекс
Процесс окислительного декарбоксилирования пирувата катализирует сложноорганизованный пируватдегидрогеназный комплекс (ПДК). В пируватдегидрогеназный комплекс (ПДК) входят 3 фермента: пируватдекарбоксилаза (Е1), дигидролипоилтрансацетилаза (Е2) и дигидролипоилдегидрогеназа (Е3), а также 5 коферментов: тиаминдифосфат (ТДФ), липоевая кислота, FAD, NAD+ и КоА. Кроме того, в состав комплекса входят регуляторные субъединицы: протеинкиназа и фосфопротеинфосфатаза
Суммарное уравнение окислительное декарбоксилирование пирувата:
Превращение пирувата в ацетил-КоА включает 5 стадий:
Стадия I. На этой стадии пируват соединяется с ТДФ в составе Е1 и
подвергается декарбоксилированию:
Пируват + Е1-ТДФ —>Гидроксиэтил-ТДФ + СО2
В результате этой реакции образуется производное ТДФ с гидроксиэтильной группой при тиазоловом кольце :
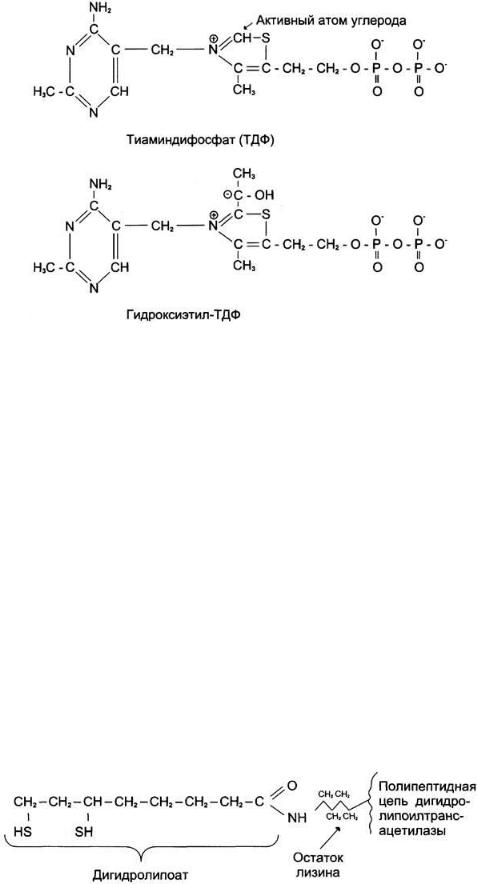
Стадия II. Дигидролипоилтрансацетилаза (Е2) катализирует перенос атома водорода и ацетильной группы от ТДФ на окисленную форму липоиллизиновых групп с образованием ацетилтииоэфира липоевой кислоты.
Стадия III. КоА взаимодействует с ацетильным производным Е2, в
результате чего образуются ацетил-КоА и полностью восстановленный липоильный остаток, простетическая группа Е2:
Липоевая кислота в составе дигидролипоилтрансацетилазы (Е2)
Стадия IV. Дигидролипоилдегидрогеназа (Е3) катализирует перенос атомов водорода от восстановленных липоильных групп на FAD — простетическую группу фермента Е3.
Стадия V. Восстановленный FADH2 передаёт водород на NAD+ с
образованием NADH.
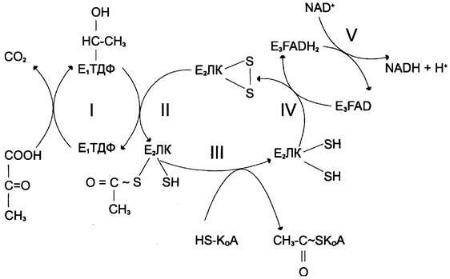
Последовательность реакций, катализируемых ПДК:
I — Е1 катализирует декарбоксилированиепирувата и перенос С2-фрагмента на ТДФ; II — Е2 катализирует окисление гидроксиэтильной группы и перенос С2-
фрагмента на липоевую кислоту (ЛК); III — ацетилированная дигидролипоилтрансацетилаза взаимодействует с КоА с образованием восстановленной формы пипоевой кислоты и ацетип-КоА; IV — окисленная форма трансацетипазы регенерируется при участии Е3; V — окисленная форма Е3регенерируется при участии NAD+.
Пируватдегидрогеназный комплекс характеризуется большим отрицательным окислительно-восстановительным потенциалом, который обеспечивает наряду с восстановлением кофермента (NADH) образование высокоэнергетической тиоэфирной связи в ацетил-КоА.
Структурное объединение 3 видов ферментов создаёт возможности для координации отдельных этапов сложной ферментативной реакции. Все промежуточные продукты реакции окислительного декарбоксилирования пирувата прочно связаны с комплексом, что увеличивает суммарную скорость процесса и сводит к минимуму побочные реакции.
Связь окислительного декарбоксилированияпирувата с ЦПЭ
Окислительное декарбоксилирование пирувата сопровождается
образованием NАDН, поставляющим электроны в дыхательную цепь и обеспечивающим синтез 3 молей АТФ на 1 моль пирувата путём окислительного фосфорилирования.
