
101
занимают энергетически более выгодные экваториальные положения. При этом у -аномера (составляет≈38%) полуацетальный гидроксил расположен на аксиальной, а у -аномера (составляет ≈62%) – экваториальной связи.
Уникальность -аномера глюкозы в том, что все объемные заместители находятся в экваториальном положении, это объясняет его выскую термодинамическую устойчивость.
УD-галактозы НО-группа при С-4 находится в аксиальном положении, соотношение - и -аномеров примерно такое же, как у глюкозы.
УD-маннозы НО-группа при С-2 занимает аксиальное положение и в
смеси таутомеров преобладает -аномер, т.к. у -аномера сближены орбитали с электронными парами трех атомов кислорода (циклического и гидроксильых групп при С-1 и С-2). Возникающее отталкивание электронов делает -аномер невыгодным. У -аномера гидроксильные группы при С-1 и С-2 более удалены друг от друга, поэтому он стабильнее.
Поскольку - и -аномеры являются диастереомерами, то их физические свойства, в частности оптическая активность, будут различны. У - аномера удельное вращение +112 , у -аномера + 19 . -D-глюкопираноза труднее растворяется в воде, чем -аномер, поэтому у свежеприготовленного раствора моносахарида наблюдается постепенное изменение удельного вращения пока не установится состояние динамического равновесия между аномерами; при этом удельное вращение установится постоянным +52.5 . Это явление изменения во времени угла вращения плоскости поляризованного луча называется мутаротацией.
12.1.3. Химические свойства моносахаридов.
Исходя из того, что моносахариды находятся в двух формах: открытой и циклической, в их молекулах можно выделить три реакционных центра:
–карбонильная группа (открытая форма),
–гликозидный гидроксил (циклическаяформа),
–спиртовые гидроксилы.
Реакции по карбонильной группе
Соединения, содержащие карбонильную группу, являются важнейшими субстратами биологического окисления и воостановления.
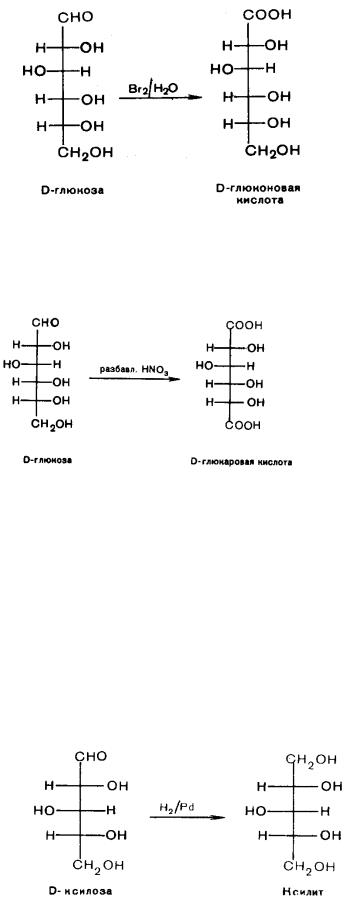
Реакции окисления. При окислении карбонильной группы (ее можно окислить даже таким слабым окислителем, как бромная вода) образуются
гликоновые кислоты (альдоновые кислоты).
102
С помощью более сильного окислителя (разбавленная азотная кислота) получают гликаровые кислоты, когда окислению подвергаются одновременно карбонильная и спиртовая группы. Гликаровые кислоты называют также сахарными.
Способность карбонильной группы к окислению используется в биохимических исследованиях для обнаружения глюкозы в биологических жидкостях. Альдозы в щелочной среде способны восстанавливать катионы металлов (серебра – реакция ―серебряного зеркала― или Толленса, меди – реакции Фелинга и Троммера, висмута – реакция Ниляндера и др.) Поскольку моносахариды в щелочной среде неустойчивы, то при их окислении образуется смесь продуктов.
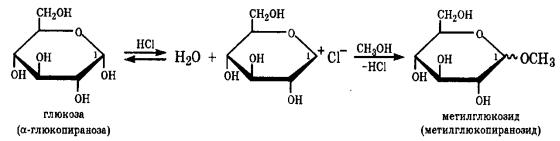
Восстановление. При восстановлении альдегидной или оксогруппы моносахаридов образуются многоатомные спирты (полиолы), называемые альдитами. Восстанавливают моносахариды водородом в присутствии металлических катализаторов (палладий, никель).
Шестиатомные спирты – глюцит (сорбит), дульцит и маннит –
получают при восстановлении соответственно глюкозы, галактозы и маннозы.
103
Это кристаллические вещества, легко растворимые в воде, обладают сладким вкусом, медленно всасываются в кровь из кишечника, поэтому в медицине ксилит и сорбит используют как заменители сахара при сахарном диабете.
Многоатомные спирты образуют сложные эфиры, имеющие практическое значение для медицины: D-глюцит-гексанитрат (нитросорбит) и D-маннит- гексанитрат применяют как сосудорасширяющие средства.
Электрофильно-нуклеофильные свойства лежат в основе кольчато-
цепной таутомерии моносахаридов. Образующиеся при этом циклические полуацетали содержат у аномерного атома углерода гликозидную гидроксильную группу, проявляющую (по сравнению с остальными) повышенную реакционную способность в реакциях с алкилирующими и ацилирующими реагентами. Гликозидная связь С-О легко расщепляется, и ее
аномерный атом углерода становится активным электрофилом. При взаимодействии моносахаридов с гидроксилили аминосодержащими соединениями в присутствии безводного НСl происходит активация электрофильного центра на аномерном атоме углерода и образуются циклические ацетали, называемые гликозидами (смесь - и -гликозидов). Если речь идет о смеси гликозидов, то с целью упрощения в формулах Хеуорса гликозидную связь обозначают волнистой линией.
Гликозиды, в отличие от простых эфиров, легко гидролизуются в кислой водной среде. Поскольку у гликозидов нет полуацетального гидроксила, они не способны к кольчато-цепной таутомерии, следовательно, восстанавливающими свойствами не обладают.
Как все ацетали, гликозиды устойчивы к гидролизу в щелочной среде. Более напряженные пятичленные гетероциклы фуранозидов расщепляются гидролитичеки быстрее шестичленных пиранозидов.
Молекулу гликозида формально можно представить состоящей из двух частей: углеводной, называемой гликоном и неуглеводной – агликона.
Однако в роли гидроксилсодержащих агликонов могут быть и моносахариды. Гликозиды, образованные с НО-содержащими агликонами, называют О- гликозидами, а с НN-содержащими соединениями – N-гликозидами (например, нуклеозиды).
Известны примеры S-гликозидов (тиогликозидов), например, содержащийся в горчице синигрин, при гидролизе которого образуется горчичное масло (действующее вещество горчичников).
104
Простые эфиры
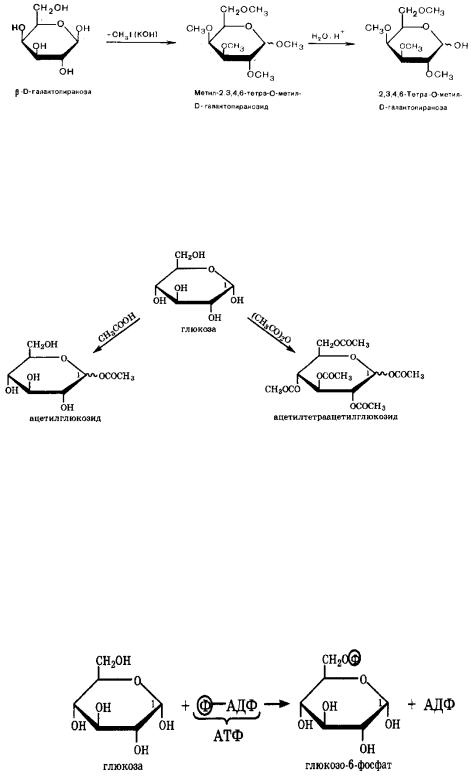
В гликозиде моносахарида остальные гидроксильные группы выступают как нуклеофильные центры и их атомы водорода замещаются при действии сильных ацилирующих реагентов с образованием полных простых эфиров. Одновременно в реакцию вступает и гликозидная гидроксильная группа, однако гликозидная связь в кислой среде легко подвергается гидролитическому расщеплению, а простые эфиры не гидролизуются:
Сложные эфиры
Моносахариды легко ацилируются ангидридами органических кислот, образуя сложные эфиры с участием всех гидроксильных групп, в то время как органическими кислотами ацилируется только гликозидный гидроксил.
Большое значение имеет образование эфиров неорганических кислот, в частности, эфиров фосфорной кислоты – фосфатов. Они содержатся во всех растительных и животных организмах и представляют собой метаболически активные формы моносахаридов. К ним прежде всего относятся фосфаты глюкозы и фруктозы. В живом организме под действием АТФ с участием фермента глюкокиназы происходит избирательное фосфорилирование глюкозы только по первичной гидроксильной группе у С-6 с образованием глюкозо-6- фосфата. Происходит нуклеофильное замещение у атома фосфора с образованием хорошо уходящей группы – АДФ:
105
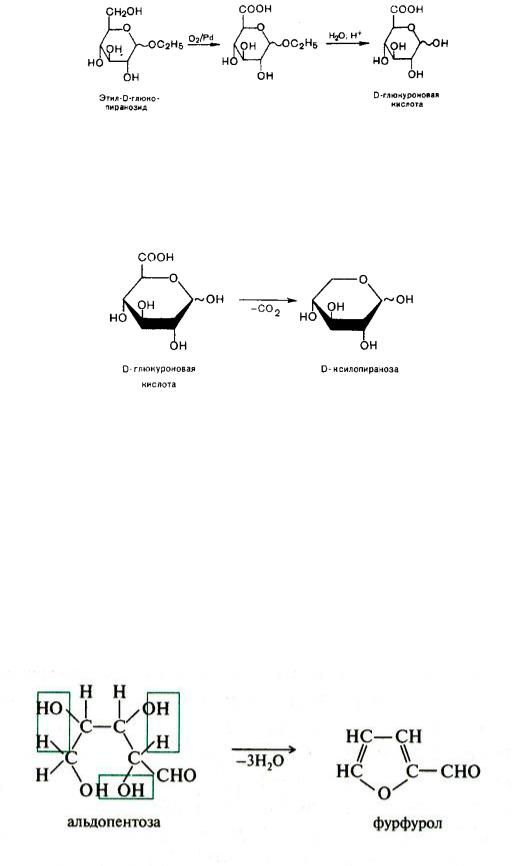
Окисление первичной спиртовой группы. При окислении первичноспиртовой группы моносахарида с защищенной альдегидной группой, например, в виде гликозида получаются гликуроновые (уроновые) кислоты:
Уроновые кислоты при нагревании их солей с металлами (никель, магний) подвергаются декарбоксилированию, при этом из гексуроновых кислот образуются пентозы. В организме в результате декарбоксилирования глюкуроновая кислота превращается в ксилозу
Уроновые кислоты играют важную биологическую роль: обезвреживают токсические продукты, образующиеся при распаде гема (билирубин), аминокислот (скатол, индол); являются структурными фрагментами гликозаминогликанов, которые входят в состав соединительной, хрящевой, костной тканей, дермы, фасций, связок.
Дегидратация моносахаридов
При нагревании с минеральными кислотами, например с серной кислотой, происходит дегидратация моносахаридов (отщепляется три молекулы воды), при этом из альдопентоз образуется фурфурол, а из альдогексоз – 5-гидроксиметилфурфурол:

106
12.1.4. Производные моносахаридов
В молекулах производных моносахаридов, встречающихся в природе, вместо одной или нескольких гидроксильных групп содержатся другие заместители: H, NH2, SH и др.
Дезоксисахара – моносахариды, в которых одна или несколько НО-групп заменены на Н. При гидролизе дезоксирибонуклеиновых кислот получают 2- дезоксирибозу, являющуюся производным рибозы, у которой при атоме С-2 нет гидроксильной группы.
В кристаллическом состоянии 2-дезоксирибоза существует в виде таутомеров - и -фураноз. В водных растворах 2-дезоксирибозы устанавливается динамическое равновесие между - и -аномерами и нециклическим таутомером.
Аминосахара (гликозамины) – моносахариды, содержащие вместо одной или нескольких НО-групп аминогруппу. В зависимости от положения аминогруппы различают 2-амино-, 4-амино-, 2,6-диаминосахара. В природе наиболее распространены 2-аминоглюкоза, 2-аминогалактоза и 2- аминоманноза. В животных организмах и растениях они встречаются в виде N- ацетилпроизводных, являющихся структурными компонентами гетерополисахаридов – гиалуроновой кислоты, гепарина, хондроитинсульфатов и др.

107
2-Аминоманноза является фрагментом N-ацетилнейраминовой кислоты, которая получается ферментативным путем в результате альдольной конденсации пировиноградной кислоты и N-ацетил –D-маннозамина:
Нейраминовые кислоты занимают концевое положение в углеводной цепи молекулы гликопротеинов и во многом определяют их свойства, маскируют антигенные детерминанты биополимера и придают ему отрицательный заряд, обеспечивают возможность их циркуляции в кровотоке и предотвращают захват клетками печени. Гликопротеины имеются почти во всех белковых фракциях крови .
N- и О-ацилированные производные нейраминовой кислоты называются сиаловыми кислотами. Ацилирование происходит, как правило, ацетильным СН3СОили гидроксиацетильным НОСН2СОрадикалами (остатками соответственно уксусной или гликолевой кислот). При ряде заболеваний уровень сиаловых кислот в крови повышается (пневмония, туберкулез, ревматизм, инфаркт и др.), что используется для диагностики. Изменение содержания сиаловых кислот на клеточной поверхности сопровождает такие процессы, как дифференцировка клеток и злокачественнон пе рерождение. Наличием избыточного количества сиаловых кислот на поверхности объясняют многие свойства опухолевых клеток.
Аскорбиновая кислота (витамин С) по структуре близка к моносахаридам. Это -лактон-2-оксо-L-гулоновой кислоты

108
Аскорбиновая кислота относится к водорастворимым витаминам, содержится в фруктах, особенно цитрусовых, ягодах (шиповник, черная смородина), овощах. При недостатке ее в организме развиваются различные заболевания, а в тяжелых случаях – цинга.
Аскорбиновая кислота обладает довольно сильными кислотными свойствами (рКа 4,2), обусловленными диссоциациацией одной из НО-групп ендиольного фрагмента. У нее также сильно выражены и восстановительные свойства, окисляясь, аскорбиновая кислота превращается в дегидроаскорбиновую кислоту:
В организме сопряженная пара аскорбиновая–дегидро-аскорбиновая кислота выполняет антиоксидантную роль, т.е. активно связывает свободнорадикальные окислительно-восстановительные процессы, интенсификация которых приводит к различным патологическим состояниям. Этим объясняется необходимость и высокая эффективность применения витамина С при многих заболеваниях.
12.2. Олигосахариды
Олигосахариды содержат от двух до двадцати моносахаридных остатков. Наибольшее значение имеют дисахариды, построенные из двух одинаковых или различных моносахаридных остатков, связанных О-гликозидной связью. Наиболее распространены: мальтоза, сахароза (свекловичный или тростниковый сахар), лактоза – молочный сахар и продукт неполного гидролиза клетчатки – целлобиоза. В зависимости от характера связывания моносахаридных остатков различают две группы дисахаридов: восстанавливающие (озидо-озы) и невосстанавливающие (озидо-озиды).
12.2.1. Восстанавливающие дисахариды
Моносахаридные остатки в них связаны за счет полуацетального гидроксила одного моносахарида и спиртового гидроксила (чаще в положениях С-4 или С-6) – другого. Поскольку у таких дисахаридов имеется свободный полуацетальный гидроксил, то они сохраняют способность к кольчато-цепной таутомерии, т.е. к образованию таутомера с карбонильной группой и, следовательно, могут быть восстановителями. Восстанавливающие дисахариды, согласно их строению, называют гликозид-гликозами. К ним относятся мальтоза, лактоза и целлобиоза. Моносахаридные звенья в
109
дисахаридах могут быть связаны друг с другом - или -гликозидной связью, в зависимости от конфигурации аномерного атома углерода.
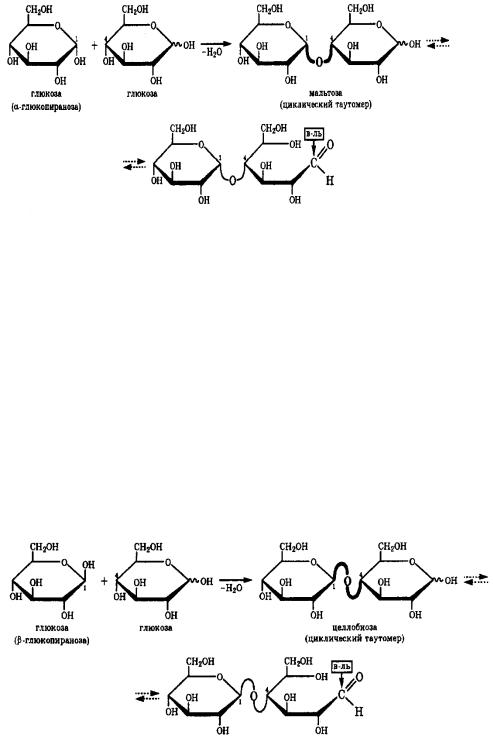
Мальтоза построена из двух молекул D-глюкозы, одна из которых в виде пиранозного таутомера за счет -гликозидного гидроксила связана с гидроксилом у С-4 второй молекулы глюкозы, т.е. остатки двух молекул D- глюкозы связаны (1 4)-гликозидной связью. Аномерный атом углерода второго остатка глюкозы с полуацетальной гидроксильной группой может иметь как -( -мальтоза), так и -конфигурацию ( -мальтоза)
Молекула глюкозы, поставляющая для образования гликозидной связи полуацетальный гидроксил, рассматривается как заместитель при С-4 второй молекулы глюкозы. В названии дисахарида ―первая‖ молекула приобретает суффикс –озил, а у ―второй― сохраняется суффикс –оза. Кроме того, в полном названии указываются конфигурации обоих аномерных атомов углерода, например, полное название -мальтозы: -D-глюкопиранозил-(1 4)- -D- глюко-пираноза.
Мальтоза, солодовый сахар (от лат. maltum-coлод) – основной продукт расщепления крахмала под действием фермента амилазы, содержащейся в слюне и соке поджелудочной железы. Мальтоза полностью усваивается организмом человека.
В целлобиозе, в отличие от мальтозы, в образовании гликозидной связи участвует -аномерный атом углерода, поэтому -(1 4)-гликозидная связь.
110
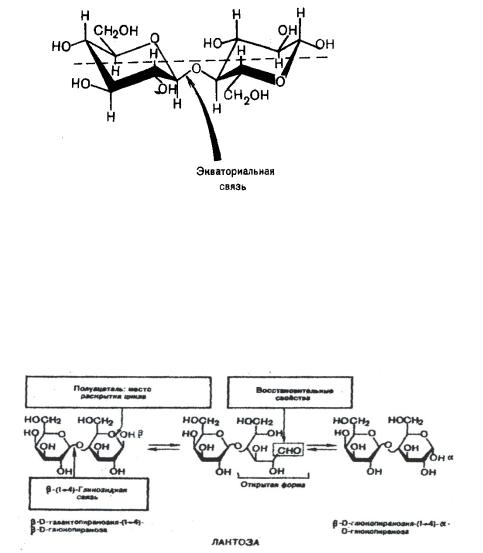
Целлобиоза является продуктом неполного гидролиза полисахарида целлюлозы (клетчатки), организмом человека не усваивается, так как в пищеварительном соке отсутствует фермент -гликозидаза, расщепляющий - гликозидную связь. -Гликозидная связь расположена экваториально в целлобиозе, что служит первопричиной линейного строения целлюлозы.
В молоке млекопитающих содержится дисахарид лактоза, в котором - гликозидный гидроксил D-галактозы связан со спиртовым гидроксилом у С-4
D-глюкозы -(1 4)гликозидной связью. Аналогично мальтозе, в
зависимости от конфигурации аномерного атома углерода D-глюкозы, может быть как - так и -лактоза.
Полуацеталь: место раскрытия |
|
Восстановительные |
цикла |
|
свойста |
|
|
|
Лактоза расщепляется в организме ферментом лактазой, но у некоторых людей из-за лактазной недостаточности (чаще генетически обусловленной) лактоза не усваивается, поэтому молоко должно быть исключено из их питания. Детей, страдающих лактазной недостаточностью, нельзя вскармливать молоком и искусственными молочными смесями.
Все восстанавливающие дисахариды в водных растворах мутаротируют и восстанавливают реактив Толленса до Ag, а реактив Фелинга и Троммера до Cu2O или до Cu. Для них, как и для моносахаридов, характерны реакции алкилирования и ацилирования в мягких условиях по полуацетальному гидроксилу с образованием соответствующих О-гликозидов.
