
893
.pdf
4.Михайлова, Л.А. Удобрения: виды, свойства, химический состав/ Л.А. Михайлова. – Пермь: Прокростъ, 2015. − 426 с.
5.Шеуджен, А.Х. Посевные качества семян риса при их обогащении цинком: сборник статей по материалам Международной конференции / А.Х. Шеуджен [и др.]. − 2018. − № 19. −
С. 106-118.
УДК 631.82:633.11
ВЛИЯНИЕ КОНЦЕНТРАЦИЙ АЗОМЕТИНА НА ПРОРОСТКИ ЯРОВОЙ ПШЕНИЦЫ
М.В. Землянникова – магистрант;
Н.М. Мудрых – научный руководитель, канд. с.-х. наук, доцент ФГБОУ ВО Пермский ГАТУ, г. Пермь, Россия
Аннотация. В данной работе установлено влияние различных концентраций тропилированного азометина на проростки яровой пшеницы. При замачивании семян на 1 час в растворах азометина и выращивании растений на песке было выявлено, что испытуемое вещество оказало неоднозначное влияние на ростки и корни.
Ключевые слова: тропилированный азометин, биометрические параметры, растворимый белок, пероксидазная активность, зерно, концентрации.
Азометины широко используются в органической и аналитической химии, а также применяются в качестве исходного сырья для производства антивирусных препаратов [5]. В последнее время немало работ посвящено производным 4-(7-циклогепта- 1,3,5-триенил)-анилина [1, 5, 8]. Интерес к тропилированным азометинам состоит в том, что на свободные места связей в гетероциклах можно внедрять катионы и анионы элементов питания, которые будут высвобождаться постепенно и обеспечивать растения ими в течение вегетации. Поэтому возникла необходимость исследовать тропилированный азометин на проростках пшеницы, так как он обладает такими свойствами, как: обеззараживает, стимулирует прорастание семян, обеспечивает растения элементами питания в течение всего периода вегетации.
Цель исследования – установить влияние концентраций азометина на проростки яровой пшеницы.
Исследуемое вещество разработано и получено с помощью восстановительного тропилирования на кафедре общей химии ФГБОУ ВО Пермского ГАТУ Т.А. Акентьевой [9]. Химическая формула азометина представлена на рисунке.
Рис. N-2-гидроксифенилметилен-41- (7-циклогепта-1,3,5-триенил)анилин (азометин)
291
Для установления оптимальной концентрации азометина проводили закладку модельного опыта с песчаной культурой. Растения выращивали в пластиковых сосудах объемом 150 мл3, вмещающих 120 г воздушно-сухой почвы. Перед посевом семена пшеницы замачивали на 1 час в исследуемом веществе. Культуру выращивали в течение 14 дней при температуре 20−25 ○C, полив проводили до влажности песка 60 % ПВ.
Опыт был проведён по данной схеме:
1.Контроль
2.1×10-5
3.1×10-4
4.1×10-3
5.1×10-2
Повторность вариантов в опыте шестикратная. Одновременно с уборкой растений определялись следующие показатели: высота растений, воздушно-сухая масса корней и ростков. Растения пшеницы убирали в соответствии с ИСО 11269-2 [4], ГОСТ Р 22030-2009 [3] и учебным пособием [2]. Далее объединенные пробы корней и проростков использовали для измерения следующих показателей: активность пероксидазы [6], содержание растворимого белка [7].
При обработке семян пшеницы азометином установлено, что на высоту растений вещество повлияло положительно при концентрации 0,001%, удлинение ростка по сравнению с контролем составило 3,02 см (при НСР05 = 0,88 см). При всех остальных изучаемых концентрациях вещество не повлияло на высоту растений, они не были математически доказаны.
На накопление воздушно-сухой массы в ростках пшеницы азометин не оказал влияние по сравнению с контролем при всех концентрациях (при НСР05 = 0,03 г). Причем максимальное уменьшение относительно контроля указанного показателя отмечено на варианте с концентрацией азометина 0,01 % и составило 0,19 г. На накопление воздушно-сухой массы в корнях пшеницы азометин повлиял положительно при концентрации 0,01 %, прибавка относительно контроля составила 0,20 г (при НСР05 = 0,06 г). На других концентрациях прибавки не наблюдается относительно контроля, максимальное уменьшение отмечено на варианте с концентрацией 0,00001 % и составило 0,24 г.
Замачивание семян на 1 час перед посевом повлияло на содержание растворимого белка в ростках пшеницы при изучении всех концентраций, прибавки относительно контроля составили 12,40−14,89 % (при НСР05 = 0,47 %). Максимальный эффект по сравнению с контролем отмечен на варианте 0,00001 %, прибавка составила 7,40 %. Положительный эффект наблюдается и на корнях пшеницы при всех концентрациях (при НСР05 = 0,21 %), прибавки относительно контроля составили 9,04−15,92 %. Наибольший эффект по сравнению с контролем наблюдается при концентрации 0,00001 %, прибавка составила 11,78 %.
Результаты исследований пероксидазной активности в ростках и корнях пшеницы показали, что наблюдается наибольшая положительная тенденция, при концентрациях 0,00001 и 0,0001 %, при концентрациях 0,001 и 0,01 % тенденция несколько ниже по сравнению с контролем.
На основании полученных результатов выяснено, что положительное математически доказанное действие азометина отмечено на высоту растений при концентрации 0,001 %. На массу ростков пшеницы концентрации азометина оказали математически доказанное ингибирующее влияние. На накопление воздушно-сухой массы корней от-
292
рицательно повлияла концентрация 0,00001 %, а концентрация 0,01 % приводила, наоборот, к увеличению массы корней. На содержания растворимого белка, азота и фосфора положительно повлияла концентрация 0,00001 %. Обработка семян исследуемым веществом в концентрации 0,01 % приводила к снижению содержания азота и фосфора в корнях и ростках пшеницы. Концентрация 0,0001 % положительно повлияла на содержание калия в ростках и корнях, отрицательное действие наблюдается на содержание азота и фосфора в ростках пшеницы.
Список литературы
1.Акентьева, Т.А. Производные 4-(7-циклогепта-1,3,5-триенил)анилина и оценка их биоло-гической активности/ Т.А. Акентьева, Н.М. Мудрых, А.Г. Фомина, Л.П. Юнникова // Бутлеровские сообщения. Тематический раздел: Биохимические исследования. Подраздел: Биотехнология – Казань, 2021 Т. 68, № 11. С. 156-160.
2.Белюченко И.С. Биомониторинг состояния окружающей среды: учебное пособие / под. ред. проф. И.С. Белюченко, проф. Е.В. Федоненко, проф. А.В. Смагина. – Краснодар: КубГАУ, 2014. – 153 с.
3.ГОСТ Р 22030-2009 Качество почвы. Биологические методы. Хроническая фитотоксичность в отношении высших растений. – М., Стандартинформ, 2010. −15 с.
4.ИСО 11269-2-2013 Качество почвы. Определение воздействия загрязняющих веществ на флору почвы. Часть 2. Воздействие загрязненной почвы на всхожесть и ранний рост высших растений 28 с.
5.Керемов А.Ф. Азометины на основе о-фенилендиамина // Вестник Дагестанского государственного университета. Серия 1. Естественные науки. – 2018. – Т. 33, вып. 4. – С. 102-105.
6.Князева, Т.В. Регуляторы роста растений в Краснодарском крае: монография // Т.В. Князева.- Краснодар: ЭДВИ, 2013. − 128 с.
7.Котляров, Д. В. Физиологически активные вещества в агротехнологиях: монография
/Д.В. Котляров, В.В. Котляров, Ю.П. Федулов. – Краснодар: КубГАУ, 2016. − 224 с.
8.Полюдова, Т.В. Оценка спектра антибактериальной активности тропилированных ариламинов/ Т.В. Полюдова, Т.А. Акентьева, Л.П. Юнникова //Актуальные вопросы экспериментальной микробиологии: теория, методология, практика, инноватика. Материалы Международной научно-практической конференции, посвященной 85-летию основания кафедры микробиологии, вирусологии, иммунологии и 100-летию со дня рождения профессора Людвиги Микртычевны Закарян. (Курск, 19 мая 2022). – Курск, 2022. − С. 172-176.
9.Юнникова, Л.П. Способ получения 4-(7-циклогепта-1,3,5-триенил)анилина и его гидрохлорида, проявляющих антимикробную активность/ Л.П. Юнникова, Т.А. Акентьева, Г.А.
Александрова, Г.Н. Никонов // Патент на изобретение RU 2568641 C2, 20.11.2015. Заявка № 2013158271/04 от 26.12.2013.
УДК 632.15:504.054
ЭКОЛОГИЧЕСКАЯ ОЦЕНКА ЗАГРЯЗНЕНИЯ СРЕДЫ МИКРОПЛАСТИКОМ
М.Р. Зюзина, Д.А. Ярославцева – студенты 2-го курса;
С.В. Лихачев – научный руководитель, канд. с.-х. наук, доцент ФГБОУ ВО Пермский ГАТУ, г. Пермь, Россия.
Аннотация. Рассмотрена проблема загрязнения окружающей среды микропластиком, особенности его распространения и влияния на окружающую среду. Сделан
293
вывод о степени изученности данной проблемы, даны рекомендации по дальнейшему ее изучению.
Ключевые слова: микропластик, загрязнитель, окружающая среда, распространение микропластика, экологическая оценка.
На сегодняшний день пластик является одним из наиболее востребо-ванных материалов и используется практически во всех сферах жизнедеятельности человека. До недавнего времени считалось, что пластиковые отходы создают только неблагоприятный эстетический эффект. Однако после того, как пластик попадает в окружающую среду, под действием механического и химического воздействия он разрушается, образуя огромное количеств частиц – микропластик.
Проблема заключается в том, что эти частицы несут в себе потенциальную угрозу экосистемам. При этом первые сообщения об обнаружении микропластика относятся к началу прошлого века, но проблема загрязнения им экосистем начала изучаться сравнительно недавно и слабо освещена в отечественной литературе.
Микропластик – это не особый вид пластика, а его частицы разнообразной формы, различного происхождения и химического состава, размером менее 5 мм. Эти фрагменты попадают в экосистемы из множества источников, включая косметику, синтетическую одежду и промышленные процессы, связанные с полимерами. Также они образуются при разрушении более крупных пластиковых частиц, которыми в большей степени являются полиэтиленовые отходы, но главными источниками являются автомобильные шины и синтетика. [1,4]. Определенную опасность могут представлять композитные материалы на основе полимерных материалов [5]. Имея малые размеры и плотность, близкую к плотности воды, микропластик распространяется в основном посредством сточных, грунтовых вод, рек, морских течений, трансграничного переноса. Распространен он повсеместно, его обнаружили даже на полюсах и в Марианской впадине. Он проник во все среды: водную, воздушную, почвенную и даже организменную. Его обнаружили в биоматериалах человека, животных и растений. Исследователи предполагают, что количество микропластика в Мировом океане может превысить количество планктона в скором времени [2]. Но точных данных о том, сколько микропластика присутствует в той или иной биосистеме нет.
Если рассматривать пластик как отход то в основном 3-й и 4-й класс опасности для окружающей природной среды [6].
Учитывая такие масштабы распространения, микропластик признали новым загрязнителем окружающей среды, потенциально опасным для экосистем. Известно, что он переносит опасные микроорганизмы, для которых он стал субстратом, в экосистемы, а также токсичные химические вещества, сорбируя их из окружающей среды. Помимо этого микропластик сам является смесью из опасных химических веществ [5]. Особую опасность представляют проглоченные частицы микропластика, они могут физически повредить органы, вызывать непроходимость и разрыв кишечника, также выделять в организм вещества, которые несут потенциальную угрозу для его систем [3]. Единственная польза, которую дает микропластик экосистеме, это то, что он является средством для расселения простейших. Исследований по влиянию микропластика на среду и организмы сравнительно мало, поэтому оговорить однозначно о последствиях попадания этих частиц в экосистемы пока невозможно.
На данный момент разработаны три метода обнаружения и анализа микропластика: спектроскопия, термический анализ и микроскопия [6]. Наиболее эффективной
294
является спектроскопия, она позволяет определять количество частиц в пробе, тип полимера обнаруженных частиц, их размеры и форму. А примеси в частицах полимера, которые несут главную опасность, можно определить только с помощью термического анализа (таблица).
|
|
|
|
Таблица |
|
Методы обнаружения и анализа микропластика |
|
||
|
|
|
|
|
Параметр |
Спектроскопия |
Термический анализ |
|
Микроскопия |
|
|
|
|
|
Тип полимера |
+ |
+ |
|
- |
|
|
|
|
|
Форма |
+ |
- |
|
+ |
|
|
|
|
|
Размер |
+ |
- |
|
+ |
|
|
|
|
|
Кол-во частиц |
+ |
- |
|
+ |
|
|
|
|
|
Примеси |
- |
+ |
|
- |
|
|
|
|
|
Данные методы подходят только для обнаружения микропластика в небольших образцах, а количественная оценка частиц пластика в масштабах целой экосистемы на данный момент затруднительна.
На основе результатов исследования проблемы микропластика, были разработаны некоторые рекомендации по борьбе с загрязнением окружающей среды частицами полимеров:
1)идентификация и количественная оценка источников поступления;
2)сокращение производства полимерных изделий;
3)переработка пластиковых отходов;
4)сокращение использования продуктов, содержащих микропластик; 5) использование методов отчистки воды и почвы от этих частиц, таких как
фильтрация или центрифугирование.
Таким образом, микропластик признан новым загрязнителем окружающей среды во всем мире, он проник даже в самые отдаленные уголки нашей планеты, но человечество еще не до конца понимает, какой ущерб он может нанести, так как, учитывая размеры, его обнаружение встречает трудности. Безусловно, необходимы дальнейшие исследования по данной проблеме, ведь она слабо изучена в виду недостатка данных о количественном содержании микропластика в среде, также не создано единых, эффективных и наиболее экономически выгодных методов идентификации и извлечения частиц пластика из окружающей среды. Необходимо проведение исследований о количественном содержании микропластика в экосистеме, о том, какое влияние он оказывает на организмы людей и животных. После сбора недостающих данных, человечество сможет разработать эффективную стратегию по борьбе с этим загрязнителем.
Список литературы
1.Бутовский, Р.О. Проблема загрязнения окружающей среды микропластиком/ Р.О. Бутовский /Университет XXI века: научное измерение. − Т.: Тульский ГПУ им. Л.Н. Толстого,
2020. − С. 200-202.
2.Казмирук, В. Д. Микропластик в окружающей среде: нарастающая проблема планетарного масштаба/ В. Д. Казмирук. − М.: Ленанд, 2020. − 432 с.
3.Ольхова, С.Е. Пластик, который мы едим, 2019 [Электронный ресурс] / С.Е. Ольхова // Успехи науки. − 2021. − № 7(3). URL : https://www/science/org/ (дата обращения: 20.11.2022).
4.Симонова А.В., Стожко Н.Ю. Проблема загрязнения окружающей среды микропластиком / ФГБОУ ВО «УрГЭУ», 2019. С. 278-280.
295
5.Мартынова, А.А. Эколого-токсикометрическая характеристика эпоксиуретанового композита на основе алюминийсодержащего отхода [Электронный ресурс] / А.А. Мартынова, С.В. Лихачев // Естественные и технические науки. − 2021. − № 6 (157). − С. 60-63. URL : https://www.elibrary.ru/item.asp?id=46367408 (дата обращения: 20.11.2022).
6.Федеральный классификационный каталог отходов [Электронный ресурс] URL : https://rpn.gov.ru/fkko/(дата обращения 14.11.22).
7.Setting the facts straight on plastics, 2019. URL : https://www.weforum.org/agenda/2019/10/plastics-what-are-they-explainer (дата обращения 14.11.22).
УДК 547-386:543.422.3
ИССЛЕДОВАНИЕ РЕАКЦИИ КОМПЛЕКСООБРАЗОВАНИЯ N-НОНАИЛ-N'-(2-НАФТИЛСУЛЬФОНИЛ)ГИДРАЗИНА С ИОНАМИ КОБАЛЬТА (II) В АММИАЧНОЙ СРЕДЕ
Р.В. Иванов – лицеист 10-го класса1; Ю.Б. Ельчищева научный руководитель, канд. хим. наук, доцент2,
П.Т. Павлов научный руководитель, канд. хим. наук, доцент2
1Лицей ПГНИУ, г. Пермь, Россия;
2ПГНИУ, г. Пермь, Россия
Исследована реакция N-нонаил-N'-(2-нафтилсульфонил)гидразина (НСГ) с ионами Co(II) в аммиачных средах экстракционно-спектрофотометрическим методом. Зарегистрированы спектры поглощения НСГ и его комплекса с ионами Co(II). Определены оптимальные условия комплексообразования НСГ с ионами Co(II) pH образования комплекса; время экстракции; количество реагента, необходимое для количественного связывания ионов Co(II). В оптимальных условиях построен градуировочный график для определения ионов Co(II). Закон Бугера-Ламберта-Бера соблюдается в интервале от 0,06 до 0,35 мг Co(II) в 25 мл раствора. Средний молярный коэффициент светопоглощения составляет 11311 см2/моль.
Ключевые слова: ацилсульфонилгидразины; комплексообразование; органические лиганды; экстракционно-спектрофотометрическое определение; цветные металлы.
Поиск органических комплексообразующих реагентов актуальная задача в процессах концентрирования ионов металлов (экстракция, флотация, сорбция), которые имеют важное значение для обогащения руд цветных металлов, переработки техногенных отходов, очистки сточных вод и других технологических процессов. Ацилсульфонилгидразины (АСГ), содержащие гидразидную группу, способны образовывать прочные комплексы с ионами цветных металлов [1]. Изучены физико-химические свойства и процессы комплексообразования N-(ацил, арил)-N'-(2-нафтилсульфонил)гидразинов общей формулой RC(O)NHNHSO2C10H7, где R = С5H11; С12H25, C4H9CH(C2H5); C14H29 и
С6H5(OH) с ионами цветных металлов в аммиачных средах [2]. Исследованные реагенты зарекомендовали себя, как хорошие осадители и собиратели ионов цветных металлов [3, 4]. Представляло интерес исследовать комплексообразующие свойства N- нонаил-N'-(2-нафтилсульфонил)гидразина (НСГ) с ионами Co(II) в качестве нового представителя нафтильного ряда.
296

Исследуемый реагент можно представить следующей формулой:
O |
O |
CH3 |
|
|
|
S |
NH NH |
|
O
(1)
Реактивы и приборы. В исследовании использовали стандартный 1,0·10-2 моль/л этанольный раствор НСГ, растворы аммиака с концентрацией 2,0 и 6,0 моль/л, 1,0·10-2 моль/л раствор CoSO4, растворители: хлороформ, этиловый спирт.
Для проведения экстракционно-спектрофотометрического исследования использовали спектрофотометр СФ-2000 (ОКБ-Спектр, Санкт-Петербург). При изучении влияния кислотности на процесс комплексообразования НСГ с ионами Co(II) значения рН растворов измеряли на рН-метре АНИОН 4100 (Инфраспак-Аналит, Новосибирск) с комбинированным электродом ЭСК-10603/7.
Методика исследования реакции комплексообразования НСГ с ионами Co ( ) в аммиачных средах
В мерную колбу вместимостью 25,00 мл помещали 2,50 мл 1,0·10-2 моль/л раствора соли Co( ), затем добавляли необходимое количество 2,0 моль/л раствора аммиака до образования аммиаката, вносили 5,00 мл 1,0·10-2 моль/л НСГ, доводили до метки дистиллированной водой и тщательно перемешивали. В результате реакции комплексообразования НСГ с ионами Co(II) образуется осадок светло-розового цвета, что свидетельствует об образовании комплексного соединения. Содержимое мерной колбы количественно переносили в делительную воронку емкостью 50 мл, добавляли 5,0 мл хлороформа. Органический слой окрашивается в розовый цвет. Время экстракции 5 минут. После расслаивания фаз экстракт помещали в кварцевую кювету толщиной 0,3 см. Регистрировали спектр поглощения НСГ и его комплекса с ионами Co(II) на фоне холостого опыта на спектрофотометре СФ-2000 (рис. 1). Из спектров поглощения следует, что максимальная длина волны составляет 305 нм. Контрастность спектрофотометрической реакции составляет 55 нм.
Рис. 1. Спектры поглощения НСГ и его комплекса с ионами Co(II)
297
Результаты и обсуждение. Природу образующего комплексного соединения ионов Co( ) с НСГ доказывали экстракцией комплекса в органическую фазу (хлороформ). Для этого окрашенный комплекс количественно переносили в делительную воронку и экстрагировали в 5,0 мл хлороформа. Время экстракционного равновесия составило 5 минут. После расслаивания (в случае плохого расслаивания добавляли NaCl на кончике шпателя) проводили реэкстракцию: добавляли к органической фазе 5,0 мл 1 моль/л раствора H2SO4. Содержание ионов Co( ) в водной и органической фазах определяли комплексонометрическим титрованием в присутствии ацетатного буферного раствора (рН ~ 5) и 0,1% индикатора ксиленолового оранжевого. Степень извлечения (Е,% около 99,9%) подтверждает образование комплексного соединения ионов Co( ) с НСГ.
Оптимальные условия реакции комплексообразования НСГ с ионами
Co(II). Для установления оптимального времени экстракции образующийся комплекс экстрагировали в течение 2, 5, 10 минут. После расслаивания фаз измеряли оптическую плотность экстракта на фоне холостого опыта при оптимальной длине волны 305 нм. Максимальная оптическая плотность наблюдается при экстракции в течение 5 минут.
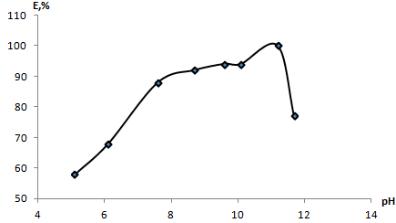
Изучение влияния кислотности на процесс комплексообразования НСГ с ионами Co( ) проводили по вышеизложенной методике в варианте «экстракцияреэкстракция». После расслаивания определяли степень извлечения ионов Co(II) (Е,%), а в рафинате замеряли pH раствора. Зависимость комплексообразования НСГ с ионами Co( ) от рНравн представлена на рис. 2. Из рисунка видно, что оптимальный интервал рН комплексообразования составляет от 7,6 до 11,2.
Для изучения влияния количества реагента на комплексообразование ионов Co(II) c НСГ в колбу объемом 25,0 мл помещали 2,5 мл 1·10-2 моль/л раствора соли Co(II), затем добавляли определенное количество раствора аммиака с концентрацией 2 моль/л для образования водорастворимого аммиачного комплекса (рН ~ 7,6 ÷ 11,2). Вносили расчетное количество 1,0∙10-2 моль/л раствора НСГ в этиловом спирте, создавая соотношения [Co(II)]:[НСГ] = 1:0,5; 1:1; 1:1,5; 1:2; 1:2,5, доводили до метки дистиллированной водой и перемешивали. Затем экстрагировали комплекс в 5 мл хлороформа. После расслаивания измеряли оптическую плотность экстракта при оптимальной длине волны в кварцевой кювете толщиной 0,3 см.
Рис. 2. Зависимость степени извлечения (Е,%) ионов Co(II) HСГ
от рН раствора; Сисх(HСГ)= Сисх(Co(II))= 1,0∙10–2 моль/л, аммиачная среда
298

По результатам исследования построена зависимость оптической плотности от количества НСГ (рис. 3). Оптимальный объем реагента составляет 2,5 мл. Анализируя кривую насыщения можно сделать вывод, что молярное соотношение [Сo(II)]:[НСГ] = 1:2.
Рис. 3. Влияние количества НСГ на |
Рис. 4. Градуировочный график для оп- |
комплексообразование с Co(II) |
ределения Co(II) c НСГ |
В выбранных оптимальных условиях построен градуировочный график для определения ионов Co(II) с НСГ (рис. 4). Закон Бугера-Ламберта-Бера выполняется в интервале от 0,06 до 0,35 мг Co(II) в 25 мл раствора. Средний молярный коэффициент светопоглощения составляет 11311 см2/моль.
Заключение. В ходе проведенных исследований реакции комплексообразования ионов Co(II) с N-нонаил-N'-(2-нафтилсульфонил)гидразином в аммиачной среде экс- тракционно-спектрофотометрическим методом была доказана возможность использования реагента в процессах концентрирования ионов цветных металлов.
Список литературы
1.Мачхошвили, Р.И. Координационные соединения металлов с гидразинами: диc. ...
доктора хим. наук / Р.И. Мачхошвили. − Москва: ИОНХ, 1983. − 457 c.
2.Ельчищева, Ю.Б. Физико-химические и комплексообразующие свойства N-ацил-N'- (2-нафтилсульфонил)гидразинов / Ю.Б. Ельчищева, Л.Р. Сунгатуллина, Е.Д. Армянинова, Н.А. Шахторин, П.Т. Павлов, А.С. Максимов // Вестник Пермского университета. Серия «Химия». 2017. − Т. 7, вып. 2. − С. 194-208.
3.Ельчищева Ю.Б. N-(2-гидроксибензоил)-N'-(2-нафтилсульфонил)гидразин - как реагент для осаждения ионов цветных металлов из аммиачных растворов / Ю.Б. Ельчищева, А.С. Максимов, А.В. Андрова, В.Р. Дробинина // Вестник Пермского университета. Серия «Химия».
−2018. − Т. 8, вып. 2. − С. 131-144.
4.Ельчищева Ю.Б., Шалагинова П.А., Максимов А.С. Физико-химические и поверхно-
стно-активные свойства N-тридеканоил-N-(2-нафтилсульфонил)гидразина // Вода: химия и экология. − 2019. − № 7-9. − С. 116–122.
УДК 631.412(470.53)
ХАРАКТЕРИСТИКА СЕРЫХ ЛЕСНЫХ ПОЧВ КУНГУРСКОГО МУНИЦИПАЛЬНОГО ОКРУГА ПЕРМСКОГО КРАЯ
К.А. Исаева – студент 3-го курса; Е.С. Лобанова – научный руководитель, канд. биол. наук, доцент
ФГБОУ ВО Пермский ГАТУ, г. Пермь, Россия
299
Аннотация. Серые лесные почвы Кунгурского муниципального округа Пермского края характеризуются низким и средним содержанием гумуса, удовлетворительными физико-химическими свойствами, от среднекислой до близкой к нейтральной реакцией среды.
Ключевые слова: строение профиля, морфологические и физико-химические свойства, гумус.
В почвенном покрове Кунгурского муниципального округа Пермского края встречаются серые лесные почвы, обладающие по сравнению с дерново-подзолистыми почвами, более высоким природным плодородием. Однако темпы роста производства продукции растениеводства и животноводства на них невысокие. В связи с этим важным является изучение свойств серых лесных почв, их режимов, процессов почвообразования для повышения их плодородия [1].
Цель работы – дать характеристику серых лесных почв Кунгурского муниципального округа Пермского края.
Объектами исследования являлись светло-серые лесные и серая лесная почвы расположенные в д. Снегири (разр. 23, 35) и на окраине города Кунгур Кунгурского муниципального округа (разр.29, 39): светло-серая среднемощная тяжелосуглинистая на лессовидных суглинках (разрез 23), серая лесная среднемощная тяжелосуглинистая на лессовидных суглинках (разрез 35), светло-серая среднемощная тяжелосуглинистая на лессовидных суглинках (разрез 29), светло-серая лесная среднемощная среднесуглинистая на делювии почва (разрез 39).
Серые лесные почвы образуются в результате развития таких почвообразовательных процессов как гумусообразование, оподзоливание и лессиваж. В результате они имеют следующий профиль и морфологические свойства.
Разрез 35. Почва серая мощная тяжелосуглинистая на лессовидных суглинках. Залежь.
Гор. Ад (0-4 см) – дернина.
Гор. А1 (4-38 см) – гумусовый, влажноватый, серый, тяжелосуглинистый, комко- вато-зернистый, уплотнен, тонкопористый, тонкотрещиноватый, копролиты, червоточины, наличие единичной гальки (2 см), наличие множества корней, переход к следующему горизонту плавный по структуре.
Гор. А1А2 (38-52 см) – гумусово-элювиальный, влажноватый, темно-серый, мелкозернистый, наличие затеков гумуса, наличие множества корней, переход к следующему горизонту по цвету резкий.
Гор. В1 (52-72 см) – иллювиальный, влажный, бурый, ореховатый, плотный, тонкопористый, наличие множества корней, переход к следующему горизонту по структуре и гранулометрическому составу.
Гор. В2 (72-96 см) – иллювиальный, влажный, бурый, крупноореховатый, плотный, наличие множества корней, переход к следующему горизонту постепенный по структуре.
Гор. ВС (96-122 см) – влажный, коричневато-бурый, ореховато-комковатый, плотный, переход постепенный.
Гор. С (122 и ниже) – влажный, коричневато-бурый, бесструктурный, плотный. Разрез 29. Почва: светло-серая лесная среднемощная тяжелосуглинистая на лес-
совидных суглинках. Залежь. Глубина – 125 см. Гор. Ад (0-2 см) – дернина.
300
