
Глава 19. Мембранное разделение
19.1. Общие сведения. Классификация методов мембранного разделения
Мембранное разделение – процесс разделения газовых или жидких смесей с помощью мембран. Мембраны – полупроницаемые перегородки, избирательно пропускающие компоненты газовых или жидких смесей.
Р ассмотрим
процесс мембранного разделения на
примере бинарного раствора компонентаВ
в растворителе
А.
Пусть растворитель проходит сквозь
мембрану лучше, чем растворенное
вещество. Тогда после контакта с мембраной
исходная смесь разделится на два
продукта: концентрат
(ретант),
обогащенный растворенным веществом В
и фильтрат
(пермеат),
с меньшей
концентрацией компонента В
по сравнению с исходной смесью (рис.
19.1.).
ассмотрим
процесс мембранного разделения на
примере бинарного раствора компонентаВ
в растворителе
А.
Пусть растворитель проходит сквозь
мембрану лучше, чем растворенное
вещество. Тогда после контакта с мембраной
исходная смесь разделится на два
продукта: концентрат
(ретант),
обогащенный растворенным веществом В
и фильтрат
(пермеат),
с меньшей
концентрацией компонента В
по сравнению с исходной смесью (рис.
19.1.).
Рис. 19.1. Схема
процесса мембранного разделения:![]()
![]() массовые расходы и
массовые расходы и![]()
![]() массовые доли компонентаВ
в исходной смеси, концентрате и фильтрате;
массовые доли компонентаВ
в исходной смеси, концентрате и фильтрате;
![]()
Для представленной схемы процесса мембранного разделения можно записать уравнения материального баланса по смеси в целом и компоненту В соответственно:
![]() (19.1.)
(19.1.) ![]() (19.2)
(19.2)
Процесс мембранного разделения может характеризоваться селективностью и проницаемостью j. Селективность определяется долей растворенного компонента В, не прошедшего сквозь мембрану
![]() .
(19.3.)
.
(19.3.)
Если мембрана
совершенно не пропускает компонент В,
то
![]()
![]()
![]() достигается полное разделение (компонентВ
отсутствует в фильтрате). Если же мембрана
одинаковым образом пропускает оба
компонента А
и В,
то ее селективность
достигается полное разделение (компонентВ
отсутствует в фильтрате). Если же мембрана
одинаковым образом пропускает оба
компонента А
и В,
то ее селективность
![]() ,
,![]() разделение полностью отсутствует.
разделение полностью отсутствует.
Проницаемость (удельная производительность, поток массы) – масса фильтрата, проходящая через единицу поверхности мембраны за единицу времени
![]() ,
(кг/м2с).
(19.4.)
,
(кг/м2с).
(19.4.)
Классифицировать методы мембранного разделения можно по различным признакам. Так, в зависимости от природы движущей силы их можно подразделить на:
баромембранные (движущей силой является градиент давления
 );
);диффузионно-мембранные (движущей силой являются градиенты химических потенциалов
 );
);электромембранные (движущей силой наряду с градиентами химических потенциалов является градиент электрического потенциала
 )
)
Баромембранное разделение осуществляется за счет разности давлений по обе стороны мембраны. В зависимости от размера задерживаемых мембраной частиц баромембранные процессы подразделяют на:
а) обратный осмос (10-4 – 10-3 мкм);
б)
ультрафильтрацию
(10-3 –
2![]() 10-2
мкм);
10-2
мкм);
в)
микрофильтрацию
(2![]() 10-2
– 10мкм).
10-2
– 10мкм).
Обратный осмос.
В основе
этого процесса разделения лежит явление
осмоса
– самопроизвольного перехода растворителя
через мембрану в раствор. Перепад
давлений, который устанавливается при
этом между раствором и растворителем
по достижении равновесия, называется
осмотическим
давлением
![]() (рис. 19.2.)
(рис. 19.2.)
Р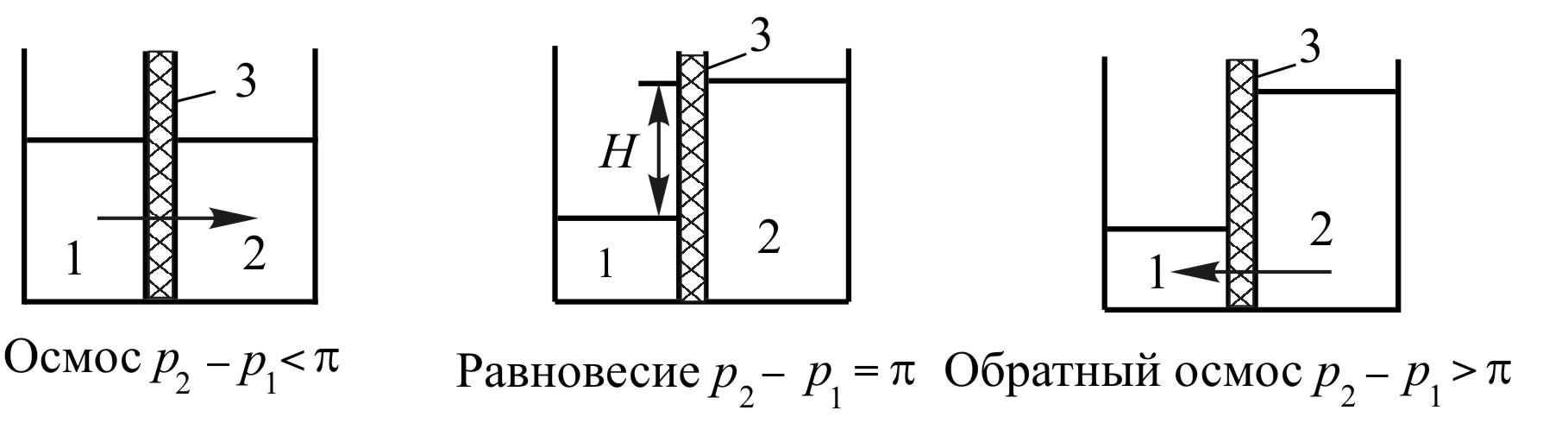 ис.
19.2. Схематическое изображение переноса
растворителя и состояние равновесия в
сосуде, разделенном мембраной3:
1
– расположение растворителя, 2
– расположение раствора;
р1
и р2
–
давления
жидкости в соответствующих частях
сосуда на одинаковом расстоянии от
днища,
ис.
19.2. Схематическое изображение переноса
растворителя и состояние равновесия в
сосуде, разделенном мембраной3:
1
– расположение растворителя, 2
– расположение раствора;
р1
и р2
–
давления
жидкости в соответствующих частях
сосуда на одинаковом расстоянии от
днища,
![]() –
осмотическое давление.
–
осмотическое давление.
Для
проведения процесса обратного осмоса
необходимо создать перепад давлений
между раствором и растворителем,
превышающий осмотическое давление. Это
приведет к переносу растворителя из
раствора и увеличению концентрации
раствора (рис. 19.2.) Обратный осмос
применяется, в основном, для разделения
растворов электролитов. При этом
осмотическое давление может составлять
десятки и сотни атмосфер, а рабочее
давление в аппарате и того больше. Так,
для морской воды
![]() =25
атм, а рабочее давление при ее опреснении
составляет примерно 60 атм.
=25
атм, а рабочее давление при ее опреснении
составляет примерно 60 атм.
Ультрафильтрация применяется для отделения высокомолекулярных соединений от низкомолекулярных, при этом проходят сквозь мембрану лишь последние. Осмотическое давление в таких растворах невелико и рабочие давления не превышают, как правило, десяти атмосфер.
Микрофильтрация служит для концентрирования растворов крупных коллоидных частиц. Этот процесс является промежуточным между ультрафильтрацией и обычным фильтрованием. Следует иметь в виду, что в отличие от фильтрования при мембранном разделении образуется концентрат в виде раствора, а не осадок.
Достоинствами баромембранных процессов разделения являются малые энергозатраты ввиду отсутствия фазовых превращений (мембранное опреснение воды требует в 10-15 раз меньше энергозатрат, чем дистилляция); низкие температуры, позволяющие разделять термически нестойкие соединения. К их недостаткам относятся высокие рабочие давления (особенно для обратного осмоса), а также падение селективности и проницаемости при увеличении концентрации растворов, обусловленное концентрационной поляризацией – увеличение концентрации растворенного вещества у поверхности мембраны. Для снижения концентрационной поляризации можно применить турбулизацию потока, перемешивание, вибрацию, что приводит к выравниванию концентраций.
Диффузионно-мембранное разделение осуществляется за счет различной скорости диффузии компонентов смеси через мембраны. Компоненты должны обладать различными коэффициентами диффузии, следовательно, отличающимися молекулярными массами и потенциалами взаимодействия (смотри 1.3.1. и П.3.2.). Диффузионно-мембранные процессы используют при испарении через мембрану (исходный раствор и концентрат жидкости, а фильтрат – пар); для разделения жидких растворов – диализ (исходный раствор и оба продукта жидкости), а также для разделения газовых смесей. Диффузионно-мембранные процессы могут применяться для разделения азеотропных и близкокипящих смесей.
Электромембранные процессы применяют для разделения ионосодержащих растворов (электродиализ). Их движущей силой является совокупность градиентов химического и электрического потенциалов. Выражение для потока компонента i в отличие от (1.16.) будет иметь вид:
![]() ,
(19.5.)
,
(19.5.)
где
ezi
–
заряд иона,
![]() – потенциал электрического поля.
– потенциал электрического поля.
