
9958
.pdf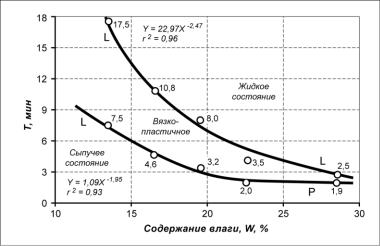
100
гетерогенных систем, состоящих из трех фаз — зернистого материала, воды,
воздуха, — пределов пластичности, называемых иногда в литературе пределами Аттерберга, которые представлены на рисунке 5.2.
Они характеризируются содержанием воды в критических точках, опре-
деляющих границы между жидким, вязко-пластичным и сыпучим состояниями системы. Верхний предел LL соответствует такому значению влажности (W), при котором слой воды между частицами достаточно велик, чтобы при слабом механическом воздействии молекулярные силы сцепления перестали удерживать их вблизи друг друга, при этом система превращается в суспензию.
Рисунок 5.5 — Определение пределов пластичности, по Аттербергу:
Условные обозначения: LL – верхний предел пластичности;
LP – нижний предел пластичности
Нижний предел LP характеризует состояние сиcтемы, при котором сорбированная вода содержится в достаточном количестве для перемещения при механическом воздействии на поверхность с образованием зеркала. Этот процесс определяет то минимальное содержание влаги, при котором все свободное пространство между частицами заполнено водой и система из трехкомпонентной превращается в двухкомпонентную.
Пределы Аттерберга определялись по следующей методике: верхний — по минимальному содержанию влаги в фосфогипсе, при котором еще можно скатать сырую массу в валики диаметром 0,5 см, так, чтобы они не разрывались; нижний — в желоб укладывался слой сырой массы фосфогипса и
101
в нем делался вырез V-образной формы длиной 1 см. Сечение должно быть закрыто по всей длине после 25 встряхиваний. Удаление воздуха и смачивание частиц приводит к появлению капиллярных сил сцепления, а также и электростатических сил адгезии, для которых воздух является диэлектриком.
Максимальная средняя плотность фосфогипса колебалась в пределах от 1,70 до
1,85 г/см3. Она характерна для точек, находящихся в непосредственной близости к нижнему пределу пластичности. Нужно отметить, что область вязко-пластичного состояния кислого фосфогипса значительно уже и расположена внутри полосы нейтрализованного фосфогипса.
Исходя из приведенных выше результатов и учитывая влияние других факторов, оптимальная влажность фосфогипса принята в интервале 15−20 %.
Во всех последующих экспериментах влажность фосфогипса при активации находилась в этих пределах.
Пределы пластичности Аттерберга дают качественную характеристику системы, и они очень удобны при варьировании влажности в широком диапазоне.
Количественную оценку пластической прочности и лучшую воспроизводимость результатов мы получили при использовании конического пластометра конструкции МГУ. Пластическая прочность определялась по формуле
Rпл = K1K2 · Р/h2 , |
(5.4) |
где К1 и К2 — константы прибора; Р — нагрузка, кг; h — глубина |
|
погружения конуса, в сантиметрах. |
|
Зависимость пластической прочности |
Rпл от продолжительности |
обработки на бегунах и влажности фосфогипса приведена на рисунках 5.3 и 5.4.
Активация влажного фосфогипса проведена на бегунах,
продолжительность ее изменялась. Полученные результаты хорошо
102
согласуются с результатами определений удельной поверхности и пределов пластичности, по Аттербергу.
После первоначального увеличения дисперсности и после перехода системы из трехкомпонентной в двухкомпонентную изменение пластической прочности небольшое и в основном связано с поверхностными явлениями.
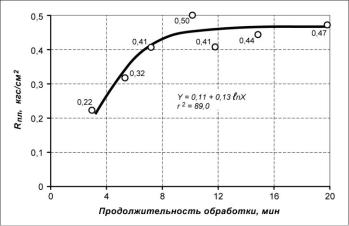
Рисунок 5.6 — Зависимость пластической прочности фосфогипса от
продолжительности его обработки на бегунах
Повышение рН жидкой фазы фосфогипса с 3−4 до 11−12 происходит практически сразу после добавления извести.
Из полученных результатов можно сделать два вывода: нейтрализация примесей, которые находятся в жидкой фазе, происходит интенсивно и заканчивается в течение 1−2 мин, нейтрализация примесей, которые сосредоточены по плоскостям спайности, в воздушных пузырьках, раковинах и пустотах агрегатов, происходит на два порядка медленнее в диффузионной области. Замедление вызвано также и образованием «маточных» фосфатов как на поверхности кристаллов фосфогипса, так и на поверхности частиц извести.

103
Рисунок 5.7 — Зависимость пластической
прочности фосфогипса от его влажности при обработке
Механическое истирание массы фосфогипса в бегунах ускоряет процессы нейтрализации как за счет сдирания пленок, так и путем вывода примесей при разрушении агрегатов и искусственном старении кристаллов.
Обычно места концентрации примесей представляют собой ослабленные зоны, где происходит разрушение кристаллов. Ускорение нейтрализации с увеличением добавки СаО связано с ростом поверхности взаимодействия.
Определено также влияние извести на прочность искусственного камня после МХА.
Образцы 5×5×5 см изготовлены из активированного фосфогипса с последующей сушкой при температуре (45−50 °С). Обработка фосфогипса проведена на лабораторных бегунах в течении 5 мин. Результаты испытаний приведены на рисунке 5.5.
Рисунок 5.8 — Влияние продолжительности обработки на прочность образцов из фосфогипса после сушки
104
Результаты исследования активированных проб, отобранных из скважин,
приведены в Приложении 2.
Проведенные исследования показали, что механохимическая активация позволяет осуществить процессы переработки фосфогипса:
—осуществить нейтрализацию кислоты в жидкой фазе;
—получить пластичную смесь, пригодную для формования изделий способом литья;
—приготовить искусственный камень и строительные изделия без обжига фосфогипса.
На основании этих исследований предложена и разработана технология
производства безобжиговых изделий из фосфогипса. Технологическая схема
включает операции подачи влажного фосфогипса из накопителя, добавление
извести в количестве 3−5 % массы сухого отхода, обработку на бегунах в
течении 5−7 мин, формование изделий путем виброобработки и сушки при
температуре теплоносителя 110−120 °С (на входе в сушильную камеру) и
50−60 °С на выходе.
По предложенной технологии изготовлена опытная партия плит межкомнатных перегородок со средней плотностью 1300−1400 кг/м3.
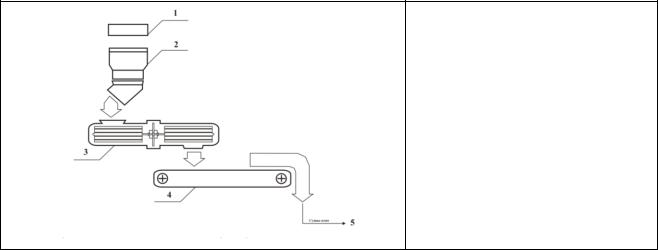
Рисунок 5.9 – Технологическая схема переработки фосфогипса:
1 – дозатор;
2 – бункер хранения;
3 – бегуны;
4 – установка виброформования; 5 – сушка плит
Прочность при сжатии изменялась в пределах от 4,0 до 7,4 МПа (сухие
образцы).
105
Технология позволяет изготавливать гранулы из фосфогипса для цементной промышленности.
Механохимическая активация позволяет также использовать фосфогипс для устройства оснований под дорожные покрытия с уплотнением моторными катками.
Технология позволяет получить конкурентоспособную продукцию, т. к.
отсутствует энергоемкая операция обжига фосфогипса.
6 ОТХОД, ОБРАЗУЮЩИЙСЯ ПРИ ОЧИСТКЕ ВОДЫ НА ТЭЦ
Процессы образования шлама
Подготовка воды на электростанциях с паротурбинными установками является ответственной задачей, так как от качества ее в значительной мере зависит надежность и экономичность эксплуатации оборудования. Чтобы исключить отложения в котлоагрегатах высокого и сверхвысокого давления и в турбинах на ТЭЦ, поступающая в котлоагрегаты вода подвергается пред-
варительной очистке, а затем глубокому обессоливанию на ионитовых фильтрах. На первой предварительной стадии очистки воды образуется остаток,
содержащий твердые частицы (шлам химводоподготовки).
Процессы обработки воды на предочистке включают в себя осветление воды и частичное её умягчение, а также снижение рН.
Осветление происходит при удалении из воды грубодисперсных и коллоидных примесей. Осветление осуществляется методом коагуляции. Для снижения рН воды и частичного ее умягчения применяется известкование.
Известкование обычно сочетают с коагуляцией. Эти методы обработки воды называются осаждением, т. к. твердые вещества удаляются в виде осадка,
образование которого достигается введением в обрабатываемую воду специальных реагентов.
106
В процессе коагуляции происходит укрупнение коллоидных частиц,
завершающееся выпадением вещества в осадок. В качестве коагулянта используют железный купорос FeSO4 7H2O. В результате реакции гидролиза
FeSO4 + 2Н2O ↔ Fe(OH)2↓ + H2SO4
и последующего окисления гидроксида железа растворённым в воде кислородом образуется малорастворимый в воде гидроксид железа:
4Fe(OH)2 + О2 + 2Н2О 4Fe(OH)3 .
В смеси различных коллоидных и грубодисперсных веществ достаточно,
чтобы частицы одного вещества оказались неустойчивыми и вся система начала коагулировать. В воде при её химической обработке таким неустойчивым компонентом является Fe(OH)3, образующийся в результате гидролиза коагулянта.
Процессы коагуляции проводятся совместно с известкованием, поэтому реакция образования гидроксида железа реализуется по схеме:
4FeSO4 + 4Са(ОН)2 + О2 +2Н2O 4Fe(OH)3 + 4СаSO4 .
Интенсивность процессов коагуляции и полнота их завершения зависят от следующих факторов:
а) рН жидкой фазы, в которой протекает процесс: сернокислое железо
FeSO4 коагулирует эффективно только при высоких значениях рН (8–10), что является причиной применения его для коагуляции совместно с известкованием;
б) температуры воды: наиболее эффективно процессы коагуляции протекают при температуре 30−40 С;
в) дозы коагулянта: для успешного протекания процессов коагуляции необходимо вводить коагулянт в строго определенном количестве (доза
107
коагулянта). Обычно доза коагулянта составляет 0,6 мэкв/л и увеличивается в период паводка до 1,0 мэкв/л;
г) длительности процесса и интенсивности перемешивания воды и раствора коагулянта.
Известкование воды
Известкование производится с целью изменения рН жидкой фазы и удаления из неё свободной углекислоты.
При известковании воды протекают следующие процессы.
Прежде всего из воды удаляется СО2 и образуется труднорастворимый,
выпадающий в осадок углекислый кальций (СаСО3):
СО2 + Са(ОН)2 СаСО3 + Н2О.
При введении извести в количестве большем, чем это необходимо для связывания свободной углекислоты, в воде повышается содержание гидроксильных ионов (ОН)-,что приводит к переходу гидрокарбонатов (НСО3-)
в карбонаты (СО2-3):
Са2+ + 2НСО3- + Са2+ + 2ОН- ↔СаСО3↓ + Н2О + СО2
Mg2+ + 2НСО3- + Са2+ + 4ОН- ↔ СаСО3↓ + Mg(OH)2↓ + 2H2О
Ионы магния (Мg2+), взаимодействуя с гидроксильными ионами, выде-
ляются в осадок в виде труднорастворимого гидроксида магния (Мg(ОН)2):
Мg2+ + 2ОН- Мg(ОН)2
Образующиеся в процессе известкования воды карбонат кальция (СаСО3)
и гидроксид магния Мg(ОН)2 выпадают в виде осадка (шлама), происходит снижение рН воды.
108
Процессы выпадения этих соединений в осадок состоят из первоначального образования высокодисперсных частиц СаСО3 и Мg(ОН)2 и
последующего укрупнения их в агрегаты. Первая стадия процесса идет с достаточно большой скоростью, вторая — протекает относительно медленно и при неправильном ведении режима обработки воды может привести к
выпадению указанных соединений вне осветлителя (в баках и трубопроводах, а
также на фильтрах).
На процессы известкования в целом большое влияние оказывают рН исходной воды, температура и некоторые коллоидные вещества.
Коллоидные вещества (глинистые вещества, коллоидные поликремневые кислоты) при высоком их содержании в исходной воде сильно замедляют процессы кристаллизации СаСО3 и Мg(ОН)2. Поэтому в период паводка, когда коллоидных частиц в воде особенно много, может наблюдаться замедление процессов обработки воды и понижение ее качества.
При эксплуатации осветлителя подачу известкового молока регулируют по величине рН (10,1–10,3).
При известковании и коагуляции кроме указанных процессов происходит частичное удаление поликремневых кислот, концентрация которых снижается на 30−40 %.
Таким образом, с предочистки (механические фильтры и осветлители)
сбрасываются нетоксичные осадки — карбонат кальция, гидроксиды железа и магния, поликремневые кислоты, органические вещества, глинистые частицы.
Образующийся шлам, хранящийся в отвале, создает проблемы экологического и экономического характера. В сутки на ТЭЦ образуется до 15 т
шлама.
Учитывая, что на долю тепловых электростанций в бывшем СССР
приходилось около 77 % вырабатываемой электроэнергии, масштабы
109
образующихся отходов являются достаточными для промышленной их переработки.
Объем и состав осадка, образуемого при химводоподготовке на ТЭЦ,
определяются технологией очистки, типом и концентрацией химических реагентов, качеством очищаемой воды.
Наибольшее распространение получила технология физико-химической очистки воды, в которой широко используются коагулянты [(Al2(SO4)3],
Fe(OH)3, FeSO4) и флокулянты (полиакриламид, активная поликремневая кислота), а также осадитель — гашеная известь.
В заводской практике химводоочистки не придается значение качеству извести и часто используется строительная известь, в которой содержание МgО
колеблется в пределах от 7 до 40 %.
Помимо типа и качества применяемых реагентов при химводоподготовке воды существенное влияние также оказывает состав исходной воды.
Важнейшими показателями качества воды для использования в теплоэнергетике являются концентрации грубодисперсных веществ,
растворенных примесей (ионный состав), коррозионно-активных газов, ионов водорода; а также технологические показатели, в которые входят сухой и прокаленный осадок, окисляемость, жесткость, щелочность, кремнесодержание,
удельная электропроводность и т. д. В данной работе исследовались шламы ТЭЦ Нижегородской области, которые образуются при использовании воды рек Волги и Оки.
По существующей классификации, природная вода этих рек относится по содержанию солей к пресной воде средней минерализации, по значению общей жесткости (Жо) — к воде с повышенной жесткостью, по содержанию соответствующих анионов — к гидрокарбонатному классу, по степени загрязнения органическими веществами, характеризующейся величиной окисляемости, — к группе повышенной окисляемости. Содержание пылеватых
