
8128
.pdf20
гия является функцией состояния.
Теплотой или теплообменом называют передачу энергии, происходящую под воздействием хаотического, т.е. теплового движения микрочастиц. Количе-
ство Q передаваемой при этом энергии также называют теплотой.
Теплообмен обусловлен наличием разности температур между телами и может происходить как при непосредственном контакте тел, так и путем излу-
чения телом электромагнитных волн, поглощаемых затем другим телом.
В результате теплообмена внутренняя энергия более нагретого тела (не подпитываемого другой энергией) уменьшается на количество передаваемой теплоты, а внутренняя энергия менее нагретого тела (не передающего свою энергию другим телам) возрастает на ту же величину.
Теплота есть микроформа передачи энергии между телами. Как и работа,
теплота проявляется только в процессе энергообмена и, следовательно, являет-
ся функцией этого процесса. Поэтому количество передаваемой теплоты зави-
сит от характера процесса энергообмена.
Энергия, как таковая, является функцией состояния тела, может быть за-
пасена (аккумулирована) телом и храниться в нем неограниченное время.
В отличие от энергии, работа и теплота не могут быть запасены "впрок" и
существуют только во время протекания процесса энергообмена (подобно то-
му, как свет электролампы существует лишь при протекании через нее элек-
трического тока и мгновенно исчезает после прекращения последнего).
По своей сути работа и теплота не являются видами энергии, они оп-
ределяют лишь количество энергии, передаваемой между телами в форме рабо-
ты или теплообмена соответственно.
Следует подчеркнуть, что работа и теплота являются неравноценными формами передачи энергии. Работа может быть непосредственно направлена на пополнение запаса любого вида энергии (например, потенциальной энергии тя-
жести, электрической, магнитной и т.д.). Теплота же непосредственно, т.е. без промежуточного преобразования в работу, может быть использована для попол-
нения запаса только внутренней энергии тела. Неравноценность теплоты и рабо-
21
ты в указанном смысле является следствием второго закона термодинамики, за-
прещающего некомпенсированный непрерывный переход теплоты в работу.
2.1.2. Эксергия и энергия
Второй закон термодинамики вносит ограничения на полноту пре-
вращения энергии из одного вида в другой. Согласно этому закону имеется три группы энергии. В первую группу входят энергии, способность которых к пре-
образованию неограничена. К ним относятся механическая, электрическая, хи-
мическая энергии, каждая из которых может быть полностью, без остатка пре-
образована в любой другой вид. Ко второй группе относятся энергии, преобра-
зуемые из одного вида в другой в ограниченном количестве. Такими являются внутренняя энергия и энергия, передаваемая в форме теплоты. Последняя,
например, не может быть полностью преобразована в механическую энергию в непрерывном процессе и частично обязательно должна быть передана окружа-
ющей среде также в форме теплоты.
К третьей группе относят энергии, полностью непереводимые в другие виды. Такой является энергия окружающею среды, а также энергия, передавае-
мая в форме работы вытеснения против давления окружающей среды.
Все неограниченно превратимые формы энергии называют эксергией.
Термин «эксергия» предложил в 1953 г. немецкий ученый З. Рант.
Эксергией является также та часть ограниченно превратимой энергии, ко-
торая может быть преобразована в другие виды энергии.
Непереводимые в эксергию виды энергии называют анергией. Анергией является также та часть ограниченно превратимой энергии, которая не может быть преобразована в другие виды энергии.
Таким образом, в общем случае энергию W можно представить в виде суммы эксергии Е и анергии А:
W E A , |
(2.4) |
причем как первое, так и второе слагаемые правой части уравнения могут быть равны нулю. Так, для полностью превратимых энергий первой группы анергия
22
равна нулю, а для полностью непревратимых энергий третьей группы нулю равна эксергия.
Введение понятия эксергии позволило более глубоко оценивать эф-
фективность различных теплоэнергетических устройств.
2.2. Термодинамическая система
Термодинамическое исследование начинают с выделения части про-
странства, подлежащей изучению. Выделенную часть пространства называют термодинамической системой. Следовательно, объектом изучения в термоди-
намике является термодинамическая система. Все что находится вне системы,
называют окружающей или внешней средой. Из окружающей среды также мо-
жет быть выделена другая система.
Термодинамическая система может включать в себя одно или несколько тел, или являться рабочим телом теплосиловой установки.
В некоторых случаях в систему включают частично или полностью окру-
жающую среду. Такую систему называют расширенной.
Воображаемую или материальную поверхность, отделяющую систему от окружающей среды, называют границей системы или контрольной по-
верхностью. Границы системы могут быть проницаемы или непроницаемы для потоков вещества и энергии.
Закрытой называют систему, границы которой непроницаемы для потока вещества. Поэтому закрытая система содержит постоянное количество веще-
ства, хотя объем ее может изменяться, если границы системы подвижны. При-
мером такой системы является газ, содержащийся в цилиндре с подвижным поршнем (рис. 2.1). Перемещением поршня можно изменять границы и объем газа в системе, сохраняя постоянной массу газа.
Открытой называют систему, границы которой проницаемы для потока вещества. Примером открытой системы служит теплообменник с потоками ве-
ществ А и Б (рис. 2.2).
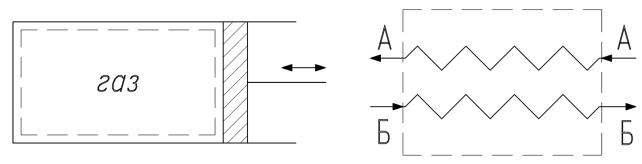
23
Рис. 2.1. Закрытая система:
- - - - границы системы
Рис 2.2. Открытая система:
- - - - границы системы
Изолированной называют систему, границы которой непроницаемы для потоков и вещества, и энергии. Очевидно, что любая изолированная система является закрытой, в то время как закрытая система может быть неизолирован-
ной. Система может быть изолирована частично или полностью. Систему, в ко-
торой исключен энергообмен с окружающей средой в форме теплоты, называ-
ют термически изолированной или адиабатной. В такой системе возможен энергообмен с окружающей средой в форме работы.
Систему, в которой исключен энергообмен с окружающей средой в фор-
ме работы, называют механически изолированной. В такой системе возможен энергообмен с окружающей средой в форме теплоты. В полностью изолиро-
ванной системе исключен энергообмен в обеих формах.
Систему называют гомогенной, если ее химический состав и физические свойства в пределах границ системы одинаковы. Свойством гомогенности об-
ладают также смеси различных веществ, если состав смеси во всей системе одинаков. Каждую гомогенную область системы называют фазой. Следова-
тельно, гомогенная система состоит из одной фазы.
Гетерогенной называют систему, состоящую из нескольких (двух и бо-
лее) фаз. Например, жидкая вода и водяной пар, находящиеся в сосуде, образу-
ют двухфазную гетерогенную систему.
24
2.2.1. Состояние системы
Состояние системы есть форма ее существования. Состояние термоди-
намической системы определяется характером ее взаимодействия с окружаю-
щей средой. Если система достаточно долго изолирована от окружающей сре-
ды, то в результате непрерывного взаимодействия микрочастиц внутри системы с течением времени прекращается видимый макроскопический обмен энергией и веществом между различными частями системы. При этом любые одноимен-
ные физические характеристики во всех точках системы выравниваются по ве-
личине. Такую систему называют равновесной. Иными словами, равновесной является такая система, во всех точках которой одноименные макропара-
метры равны по величине.
Равновесное состояние является наиболее вероятным и может сохра-
няться сколь угодно долго при условии полной изоляции системы от ок-
ружающей среды. Самопроизвольно выйти из равновесного состояния такая система не может.
Приведенные выше положения определяют содержание первого по-
стулата термодинамики. Согласно статистической физике смысл термоди-
намического равновесия заключается в том, что у всякой изолированной систе-
мы существует такое определенное и единственное макроскопическое состоя-
ние, которое чаще всего создается непрерывно движущимися частицами. Это есть наиболее вероятное состояние, в которое и переходит изолированная си-
стема с течением времени.
Следовательно, первый постулат не является абсолютным, а выражает лишь наиболее вероятное поведение системы. Никогда не прекращающееся движение микрочастиц системы приводит к ее спонтанным отклонениям
(флуктуациям) от равновесного состояния. Относительные спонтанные откло-
нения макроскопической системы от равновесия при прочих равных условиях тем меньше, чем больше частиц в системе. Так как термодинамические систе-
мы состоят из очень большого числа частиц, то флуктуациями в большинстве случаев можно пренебречь, что и делается в термодинамике.
25
Согласно первому постулату, термодинамика не рассматривает системы,
для которых равновесное состояние невозможно (системы, процессы в которых не могут завершиться наступлением равновесия, например, из-за ограниченно-
го числа микрочастиц), а также явления, сопровождающиеся большими само-
произвольными отклонениями системы от равновесного состояния.
В случае неравенства хотя бы одного макропараметра в каких-либо точ-
ках системы, последнюю называют неравновесной. Неравновесность возникает при взаимодействии системы с окружающей средой. Например, при нагревании воздуха в помещении отопительным прибором появляется разность температур непосредственно возле поверхности прибора и на удалении от него. В этом случае воздух образует термически неравновесную систему.
Наличие разности давлений в объеме системы определяет ее механи-
ческую неравновесность. Однако, если градиент давления является результатом действия гравитационного поля (например, градиент давления по высоте атмо-
сферы земли или по глубине воды в море), систему условно считают механиче-
ски равновесной, поскольку градиент гравитационного давления не создает дви-
жение и не может быть, поэтому, использован для получения полезной работы.
Различают состояния устойчивого, неустойчивого и относительно ус-
тойчивого равновесия.
Устойчивое равновесие (стабильное состояние) характерно тем, что, если внешним воздействием вывести из него систему, после снятия этого воздей-
ствия система сама возвратится в исходное состояние.
Система, находящаяся в неустойчивом равновесии (лабильное со-
стояние), после выхода из этого состояния и снятия внешнего воздействия не возвращается в исходное состояние, а переходит в состояние устойчивого рав-
новесия. Вывести систему из лабильного состояния можно даже слабым внеш-
ним воздействием.
Относительно устойчивое равновесие (метастабильное состояние) может быть нарушено только при достаточно сильном внешнем воздействии, после сня-
тия которого такая система переходит в состояние устойчивого равновесия. При
26
слабом воздействии метастабильное состояние нарушается, однако после снятия слабого воздействия система возвращается в исходное метастабильное состояние.
Понятие равновесного состояния играет в термодинамике важную роль.
Методами классической термодинамики могут быть аналитически описаны и графически изображены только равновесные системы.
2.2.2. Термодинамические параметры состояния
Для определения конкретных физических условий существования (состо-
яния) равновесной термодинамической системы используют макроскопические
(т.е. относящиеся ко всей системе в целом) величины, называемые термодина-
мическими параметрами состояния.
Важнейшим свойством любого термодинамического параметра является независимость его величины от характера пути, по которому система пришла в данное состояние. Следовательно, термодинамические параметры являются функциями состояния системы.
Термодинамические параметры разделяют на внешние и внутренние.
Внешними называют параметры, величина которых зависит от положения не входящих в систему внешних тел, относящихся к окружающей среде. Внеш-
ними параметрами являются, например, объем системы при фиксированном положении ее границ, определяемых расположением внешних тел; напряжен-
ность силового поля, зависящая от положения источников поля зарядов и то-
ков, находящихся за пределами рассматриваемой системы, и т.д. Следователь-
но, внешние параметры являются функциями координат внешних тел.
Внутренними называют параметры, определяемые совокупным дви-
жением и распределением в пространстве входящих в систему микрочастиц.
Внутренними параметрами являются, например, давление в системе с фиксиро-
ванными границами, энергия, поляризованность, намагниченность и др., так как их величины зависят от движения и положения микрочастиц системы и входящих в них зарядов.
Так как пространственное расположение микрочастиц в системе зависит от
27
расположения внешних тел, то, следовательно, внутренние параметры определя-
ются положением и движением микрочастиц и значением внешних параметров.
Необходимо отметить, что в зависимости от условий существования си-
стемы один и тот же параметр может быть как внешним, так и внутренним.
Так, если в качестве термодинамической системы рассматривается газ, распо-
ложенный в сосуде с фиксированными стенками (газовом баллоне), то объем газа, равный объему сосуда, является внешним параметром, а давление – внут-
ренним параметром, т.к. зависит от координат и импульсов молекул газа. Если же газ находится в цилиндре с подвижным поршнем под постоянным давлени-
ем, то давление будет внешним параметром, определяемым действием внешних сил, а объем – внутренним, т.к. зависит в этом случае от положения и движения молекул газа.
Следует иметь в виду, что давление и объем не могут одновременно быть внутренними или внешними параметрами: если первый из них внутренний, то второй внешний, и наоборот.
Внутренние параметры разделяют на интенсивные и экстенсивные. Ин-
тенсивными называют параметры, не зависящие от количества вещества, нахо-
дящегося в термодинамической системе. Такими величинами являются давле-
ние и температура. Действительно, если находящийся в баллоне сжатый газ разделить перегородкой на две части, то величины давления и температуры в каждой части газа сохранятся прежними.
Экстенсивными (или аддитивными) называют параметры, зависящие от количества вещества. Экстенсивными являются энергия, энтальпия и др. пара-
метры. В предыдущем примере после разделения газа на две части энергия и эн-
тальпия каждой части газа окажутся меньше, чем у всего газа до его разделения.
Величина экстенсивного параметра сложной системы, состоящей из не-
скольких частей, может быть представлена как сумма величин одноименных параметров всех частей системы.
Экстенсивные параметры неудобны для использования, поскольку для одной и той же системы они могут иметь различную величину в зависимости от
28
количества вещества, находящегося в системе. Поэтому такие параметры при-
меняют в удельной форме, отнесенными к единице количества вещества, чаще всего к 1 кг. Представленные в удельной форме экстенсивные параметры пере-
стают зависеть от количества вещества и приобретают свойства интенсивных величин. Внешние параметры состояния всегда являются интенсивными.
В технической термодинамике наиболее важное значение имеют сле-
дующие параметры: объем, давление, температура, внутренняя энергия, эн-
тальпия, энтропия.
Объем, давление и температуру называют термическими или основными
параметрами, поскольку в совокупности они определяют тепловое состояние тела и могут быть непосредственно измерены с помощью соответствующих приборов.
Остальные три величины (внутреннюю энергию, энтальпию, энтропию)
называют калорическими параметрами или функциями состояния. Эти величи-
ны характеризуют энергетическое состояние системы. Они не могут быть непо-
средственно измерены и определяются расчетным путем через известные ос-
новные параметры.
Рассмотрим подробнее основные параметры, способы и единицы их из-
мерения.
Полный объем V системы выражают в м3. Объем определяют по ха-
рактерным размерам тела с помощью соответствующих аналитических со-
отношений. Объем твердого тела можно определить также погружением по-
следнего в жидкость. Объем вытесненной при этом жидкости равен объему по-
груженного в нее тела.
Объемные расходы газов и жидкостей (для открытых систем) измеряют с помощью приборов – расходомеров, изучаемых в специальных дисциплинах.
Выше было показано, что в зависимости от вида системы объем может быть как внешним, так и внутренним параметром. Полный объем системы с фиксированными границами является внешним и поэтому, интенсивным пара-
метром. Действительно, объем газа в стальном баллоне не зависит от массы
29
находящегося в нем газа. В данном случае величина объема газа, рассматривае-
мого как отдельная термодинамическая система, определяется только формой и расположением стенок баллона, являющихся для этой системы внешним телом.
Объем системы с подвижными границами является внутренним, экс-
тенсивным параметром. Например, объем воздуха в эластичном воздушном шарике зависит, при прочих равных условиях, от массы этого воздуха.
Поэтому в качестве термодинамического параметра обычно используют удельный объем ν, получаемый делением полного объема V системы на ее мас-
су М:
v |
V |
,м3 / кг. |
(2.5) |
|
M |
||||
|
|
|
Таким образом, удельный объем можно определить как объем единицы массы (1 кг) вещества.
Иногда вместо удельного объема используют обратную ему величину ρ,
называемую плотностью вещества:
ρ |
l |
|
M |
,кг/ м3 . |
(2.6) |
|
v |
V |
|||||
|
|
|
|
Плотность является массой единицы объема (1 м3) вещества.
Давление р представляет собой силу, действующую по направлению нор-
мали на единичную площадку некоторой поверхности, находящейся в системе.
Как показано выше, в зависимости от вида системы давление может быть или внутренним, или внешним параметром. Однако во всех случаях оно являет-
ся интенсивной величиной.
Давление идеального газа определяется основным уравнением молеку-
лярно-кинетической теории
p |
2 |
|
mw2 |
|
||
|
n |
|
, |
(2.7) |
||
3 |
2 |
|||||
|
|
|
|
|||
где п – число молекул в единице объема;
т – масса молекулы;
w – среднеквадратичная скорость поступательного движения молекул.
