
- •Лекция 10 спирты и фенолы
- •1. Одноатомные спирты
- •1.1. Классификация, номенклатура, изомерия.
- •1.2. Способы получения
- •1.2.1. Из алкенов
- •1.2.2. Из галогенопроизводных.
- •1.2.3. Синтез спиртов с использованием реактива Гриньяра.
- •1.2.4. Восстановление карбонильных соединений.
- •1.3. Физические свойства
- •1.4. Химические свойства
- •1.4.1. Реакции с разрывом связи о-н Кислотно-основные свойства
- •1.4.1.1. Этерификация кислотами
- •1.4.2.1.Реакции с галогеноводородами
- •1.4.2.2. Реакции с галогенидами фосфора и серы
- •1.4.3. Окисление
- •1.4.4. Восстановление
- •2. Многоатомные спитры
- •2.1. Классификация, номенклатура, изомерия.
- •2.2. Способы получения.
- •2.3. Физические и химические свойства
- •2.3.1. Образование солей с металлами
- •2.3.2. Образование сложных эфиров
- •2.3.3. Дегидратация
- •3.2. Физические свойства
- •3.3. Химические свойства
1.4.1.1. Этерификация кислотами

Образование уксусноэтилового эфира:

1.4.1.4. Реакции с галогеналканами.
Спирты являются слабыми нуклеофилами поэтому практически не реагируют с галогеналканами. Исключение составляют аллил и бензилгалогениды и некоторые третичные галогенпроизводные. Реакции протекают по механизму SN1.
Алкоксид-анионы являются сильными нуклеофилами и основаниями, поэтому способны реагировать с галоидными алкилами по механизму SN2:

1.4.2. Реакции с разрывом связи С-О
1.4.2.1. Этерификация минеральными кислотами
Спирты взаимодействуют с минеральными и органическими кислотами с образованием соответствующих сложных эфиров и воды:
![]()


Эфиры неорганических кислот получаются при взаимодействии спиртов и хлорангидридов неорганических кислот:
1.4.3. Дегидратация
При действии на спирты водоотнимающих средств происходит межмолекулярное и внутримолекулярное отщепление воды. Водоотнимающими веществами являются кислоты: серная, фосфорная, щавелевая, беннзолсульфокислота; оксиды металлов: оксид алюминия, оксид тория.
При межмолекулярной дегидратации образуются простые эфиры. Механизм реакции включает две стадии. На первой стадии образуется сложный эфир, который на второй стадии вступает в реакцию нуклеофильного замещения со второй молекулой спирта:

В случае внутримолекулярной дегидратации спиртов, протекающей при более высокой температуре, от сложного эфира минеральной кислоты отщепляется кислота с образованием непредельного соединения. В этом случае на второй стадии протекает реакция элиминирования:

При этом водород отщепляется в соответствии с правилом Зайцева, с образованием наиболее алкилированного олефина.
Эта закономерность в сочетании с правилом Марковникова дает возможность переходить от одних спиртов к другим. Например, от изобутилового к третичному бутиловому спирту:

1.4.2.1.Реакции с галогеноводородами
Спирты реагируют с галогеноводородами с образованием галогеналканов и воды. Третичные спирты вступают в реакцию легче, чем вторичные, а вторичные легче, чем первичные. Реакция спиртов с галогеноводородами является обратимой. Гидроксил плохо уходящая группа. Обладает низкой поляризуемостью. Для повышения поляризуемости, соответственно, для более легкого разрыва связи С-О действуют кислотами, что приводит к образованию оксониевого иона и легкому отщеплению воды, либо к образованию сложного эфира и также легкому отщеплению кислотного остатка.
Реакцию проводят пропуская газообразный галогеноводород в спирт, или нагревая спирты с концентрированными растворами галогеноводородных кислот. Бромалканы получают нагреванием спиртов (кроме третичных) с бромидом калия или натрия в присутствии серной кислоты:

1.4.2.2. Реакции с галогенидами фосфора и серы
Эти реакции являются лучшими методами получения галогенопроизводных из спиртов. Протекают быстро, с высокими выходами, без побочных процессов:
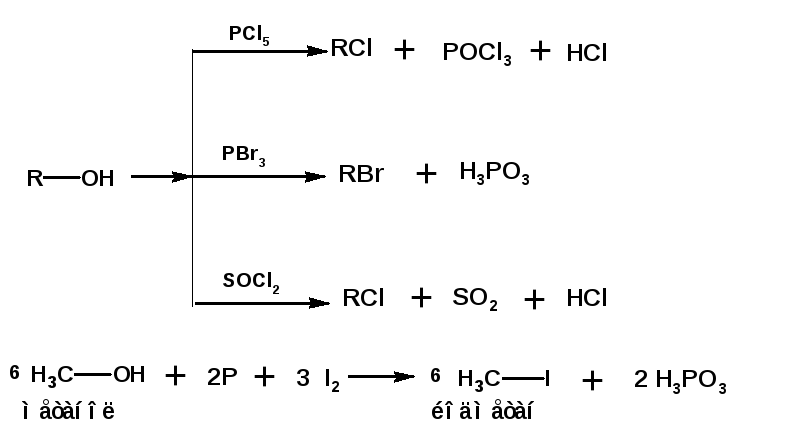
1.4.3. Окисление
В качестве окислителей спиртов могут быть использованы: хромовый ангидрид, хромовая кислота, перманганат калия, двуокись марганца и т.д. Во всех случаях первичные спирты дают альдегиды, а вторичные – кетоны. Кроме того, при пропускании паров первичного или вторичного спирта над медным катализатором при 3000С протекает реакция дегидрогенизации (дегидрирования) спиртов. Также из первичных спиртов получаются альдегиды, а из вторичных – кетоны:

Третичные спирты окисляются трудно, при этом происходит разрыв углерод-углеродных связей и образуется смесь кислот и кетонов.
