
книги / Основы технологии металлургического производства чугуна, стали, алюминия, меди, титана и магния
..pdf
3. ПРОИЗВОДСТВО АЛЮМИНИЯ
Алюминий − второй после железа металл современной техники. Наиболее важное свойство алюминия, определяющее его широкое применение, − это плотность, равная 2,7 г/см3 (т. е. алюминий почти в 3 раза легче железа), а также хорошая электрическая проводимость, составляющая 65 % электрической проводимости меди. Кроме того, алюминий имеет высокую теплопроводность и теплоемкость, химически стоек против органических кислот и хорошо сопротивляется воздействию азотной кислоты. Он очень быстро окисляется на воздухе, покрываясь тонкой пленкой оксида, которая, в отличие от оксида железа, не пропускает кислород в толщу металла, делая его стойким против коррозии. Его кристаллическая решетка − куб с центрированными гранями с параметром а = 0,404 нм. Никаких аллотропических превращений у алюминия не обнаружено.
Температура плавления алюминия составляет 660 °С, температура кипения – около 2500 °С. Механические свойства алюминия невысоки. Предел прочности при разрыве составляет 90…180 МПа, НВ 20…40; он имеет высокую пластичность, что дает возможность прокатывать его в очень тонкие листы. Однако чистый алюминий трудно обрабатывается резанием, а также имеет значительную линейную усадку (1,8 %). Для устранения этих отрицательных свойств в алюминий вводят различные добавки, поэтому широко распространены сплавы алюминия.
Алюминиевая промышленность − сложное производство. Для получения алюминия недостаточно иметь только алюминиевую руду; требуется еще другой вид сырья − плавиковый шпат для полу-
41
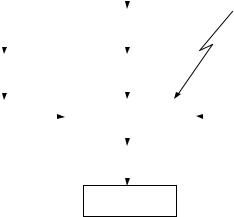
чения криолита и других фтористых солей, необходимых в производстве алюминия. Нужны также чистые углеродистые материалы для получения анодной массы и других электродных изделий, без которых невозможно электролитическое производство алюминия. Нельзя его осуществить и без большого расхода электрической энергии (рис. 11).
|
|
|
|
|
|
|
|
Руды алюминия |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Плавиковый |
|
|
|
|
Производство |
|
|
|
|
|
|||
|
шпат |
|
|
|
|
глинозема |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Технологическая |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Производство фтор |
|
|
|
Чистая окись |
|
|
|
|
электроэнергия |
|||||
|
солей и криолита |
|
|
|
алюминия |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Чистый |
|
|
|
Электролитическое |
|
|
|
Угольные аноды |
|||||
|
криолит |
|
|
|
|
получение алюминия |
|
|
|
или анодная |
||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
масса |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рафинирование |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Сортовой
алюминий
Рис. 11. Общая схема получения алюминия
Таким образом, современное производство алюминия складывается из четырех самостоятельных процессов: производства глинозема, получения криолита, электродного производства и электролитического получения алюминия.
3.1. Алюминиевые руды
Алюминий − наиболее распространенный металл в земной коре (8,8 %); в чистом виде он не встречается, зато много минералов, содержащих алюминий. По данным акад. А. Е. Ферсмана, их боль-
42
ше 250, но алюминиевыми рудами для получения алюминия служат бокситы.
Бокситы − сложная горная порода, которая содержит алюминий в виде гидрооксидов. Лучшие бокситы содержат примерно 60 % А12О3. Кроме того, в бокситах всегда присутствуют оксиды железа, кремнезем в виде кварца, а также карбонат кальция, оксиды титана и др. Качество бокситов определяется количеством оксидов алюминия и содержанием кремнезема − вредной примеси, затрудняющей получение алюминия.
Другая руда, которую используют для производства алюминия в нашей стране, − нефелин. Этот минерал можно представить фор-
мулой Na(К)2О А12О3 2SiO2.
К перспективным рудам алюминия относятся также кианиты − А12О3SiO2, каолины, или глины, содержащие алюминий в виде А12О3 2SiO2 2Н2O. Лучшие сорта глин содержат до 39 % А13О3.
3.2. Производство глинозема
Как видно из схемы на рис.11, для производства алюминия сначала необходимо получить чистый оксид алюминия, глинозем − Al2O3. Современная алюминиевая промышленность использует для этого несколько способов, выбор которых зависит от вида и состава руды.
Рассмотрим один из щелочных способов получения оксидов алюминия − спекание. Боксит и известняк дробят и как мокрую шихту, тонко размалывают в шаровых мельницах, а затем направляют в трубчатые, медленно вращающиеся печи, имеющие длину 80…150 м и диаметр 2,5…5 м (рис. 12). Полученную жидкую пульпу подают в холодный конец печи, где она встречается с отходящими печными газами, имеющими температуру 300…400 °С. В результате влага испаряется, высохшая шихта перемещается в горя-
43
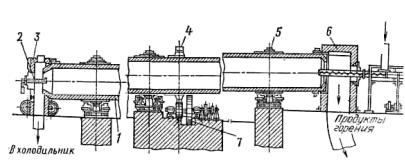
чую зону, температура в которой достигает 1200…1250 °С. По мере нагрева в шихте протекают сложные химические процессы, в результате которых оксид алюминия соединяется с содой и образуется алюминат натрия, растворимый в воде.
|
|
|
|
4 |
|
5 |
|
6 |
2 |
|
3 |
|
|
|
|||
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Загрузка
|
|
|
|
|
|
Продукты |
|
|
|
|
|
|
|
горения |
|
|
|
1 |
|
|
|||
|
|
|
7 |
||||
|
|
|
|
|
|||
В холодильник |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
Рис. 12. Трубчатая вращающаяся печь: 1 − труба; 2 − форсунка; 3 − разгрузочная головка; 4 − венцовая шестерня; 5 − опорные бандажи;
6 − загрузочная головка; 7 − редуктор
Полученный спек охлаждают, дробят и подвергают выщелачиванию, сущность которого заключается в воздействии на спек слабых растворов соды. В результате выщелачивания из спека в раствор переходит алюминат натрия (Na2О А12О3 или NaА1O2), а нерастворившаяся часть, называемая шламом, отбрасывается. После очистки от кремния и фильтрации чистый алюминатный раствор подвергают карбонизации. Назначение этой операции − выделение из раствора гидрооксида алюминия, не загрязненного другими веществами; ее проводят в цилиндрических баках с мешалкой, в которых углекислый газ (обычно очищенные печные газы) продувают через раствор. Под действием СО2 алюминатный раствор разлагается, из него выпадает белый осадок − гидрат окиси алюминия, который отделяют от раствора соды фильтрацией:
Na2O А12О3 + СО2 + 3Н2О = Na2СО3 + А12О3 3Н2О.
44
Оставшийся оборотный раствор соды после добавления в него некоторого количества свежей соды возвращается на подготовку шихты для очередного спекания, а гидрат окиси алюминия прокаливается в трубчатых вращающихся печах (аналогичных печам спекания) при температуре 1200 °С; в результате получается безводный негигроскопичный глинозем, вполне пригодный для получения алюминия электролизом.
3.3. Электролитическое производство алюминия
Алюминий получают электролизом расплавленных солей, т. е. путем пропускания постоянного электрического тока через расплавленный криолит, в котором растворен глинозем. Сущность этого процесса можно понять, рассмотрев рис. 13.
|
|
|
|
|
|
6 |
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|||||||||
|
|
в |
г |
|
|
|
|
|
б |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
||||||||||
а |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|||||
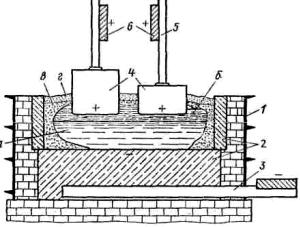
Рис. 13. Схема электролизера для получения алюминия
Электролизер состоит из прочного сварного корпуса 1, футерованного внутри угольными блоками 2, в подовую часть которого
45
с помощью шин 3 подведен отрицательный полюс источника тока. Над корпусом подвешен угольный анод 4, к которому с помощью шин 5 и 6 подведен положительный полюс. Если в электролизер залить расплав, и при температуре 1000 °С в этот расплав опустить анод, и пропускать через расплав постоянный ток большой силы и необходимого напряжения, то через определенное время на дне электролизера можно обнаружить расплавленный алюминий а. Он собирается под слоем расплавленного электролита б, состоящего из криолита Na3А1F6, в котором обычно растворено 1…8 % глинозема. Электролит поддерживается в расплавленном состоянии только за счет теплоты, выделяющейся при прохождении через него постоянного электрического тока, поэтому часть электролита всегда настывает на холодных стенках и образует твердую застывшую корку в, на которую сверху насыпают порошкообразный оксид алюминия г.
Расплавленный криолит диссоциирует по следующей схеме:
Na3А1F6 = Nа+ + А1F63−.
Комплексный ион А1F63−, видимо, может диссоциировать и дальше вплоть до ионов алюминия и фтора.
Глинозем, растворенный в расплавленном криолите, тоже диссоциирует на ионы. Диссоциацию глинозема можно представить в виде следующей схемы:
А12О3 = 2А13+ + 3О2−.
Все эти ионы принимают участие при прохождении тока через электролит, но не все из них разряжаются на электродах. На катоде в первую очередь разряжаются ионы А13+, так как в электролите нет других, более электроположительных ионов (а ионы натрия имеют более отрицательный потенциал), в результате чего на дне ванны образуется слой металлического алюминия. На аноде преимущественно разряжаются ионы кислорода, который немедленно окисляет угольный анод, образуя СО и СО2.
46
Наиболее широко применяют электролизеры с силой тока, превышающей 120 кА, с верхним подводом тока к самообжигающимся анодам (см рис. 10) и с несколькими (12…30 шт.) обожженными анодами (см. рис. 13). Получение алюминия в электролизере осуществляется непрерывно в течение двух-трех лет; при этом выполняют следующие основные операции: наблюдение за составом электролита, обеспечение своевременной загрузки глинозема и извлечения алюминия, наблюдение за напряжением на ванне, а также обслуживание, восстановление расходуемой анодной системы.
Как видно, процесс электролиза сводится к разряду ионов А13+ и О2−, из которых состоит непрерывно расходуемый глинозем. Криолит не подвергается непосредственному электролизу и расходуется мало, однако из-за его физических потерь (испарения, выплескивания и т. д.), а также взаимодействия его отдельных составляющих с примесями глинозема и футеровкой электролизера приходится систематически следить за его уровнем в ванне, равным 18…25 см, и химическим составом. Некоторые заводы вводят в
электролит небольшие добавки СаF2 и МgР2 для снижения температуры плавления электролита на несколько десятков градусов.
Когда в электролите остается мало глинозема (менее 1 %), возникает анодный эффект. Внешне он проявляется быстрым скачком напряжения на электролизере от обычных 4…4,7 В до 30…50 В: около анода появляются электрические дуги, электролит начинает перегреваться и бурлить. Для ликвидации анодного эффекта пробивают корку электролита и, перемешивая, растворяют в нем глинозем (очередная порция которого всегда заранее насыпается на корку электролита).
После растворения глинозема в электролите анодный эффект обычно прекращается и напряжение становится нормальным. Допустимо возникновение на электролизере одного-двух анодных эффектов в сутки.
47
Алюминий извлекают из электролизера, пробивая корку электролита и опуская на дно футерованную огнеупором стальную трубку, через которую алюминий откачивают в вакуумный ковш. Извлечение металла проводят не чаще одного раза в сутки.
По мере извлечения алюминия постепенно опускают анод и тщательно регулируют напряжение и межполюсное расстояние электролизера. Поскольку нижняя часть анода сгорает, и он постепенно опускается, необходимо заменять сгоревший анод новым, не допуская расплавления металлических частей токоподводящей системы, или наращивать верхнюю часть. В кожух самообжигающегося анода систематически загружают анодную массу, которая постепенно коксуется на горячем конусе анода за счет теплоты, выделяющейся из ванны. Токоподводящие стальные штыри постепенно опускаются с анодом, во избежание их расплавления и загрязнения алюминия железом в очередной последовательности их выдергивают из тела анода и поднимают на более высокий уровень, а в образовавшуюся полость затекает анодная масса и затем коксуется.
На получение 1т первичного алюминия электролизом расходуется примерно 14…17 МВт·ч электроэнергии и почти 2 т глинозема.
Извлеченный из электролизеров алюминий для очистки от неметаллических включений отстаиванием направляют в большие электропечи сопротивления САН, из которых затем осуществляют его полунепрерывную или непрерывную разливку в калиброванные заготовки для производства проволоки и листа. Эти же печи применяют для получения многих сплавов на алюминиевой основе. Алюминий предварительно хлорируют газовой смесью хлора и нейтрального газа 10…15 мин при температуре 750 °С в ковше для удаления главным образом, неметаллических включений (частичек угля, глинозема, фтористых солей и т. д.).
В современных стандартах первичный алюминий делится на три группы: алюминий особой чистоты (марка А999), высокой чис-
48
тоты и технической чистоты. Предусмотрено восемь марок, допускающих содержание примесей 0,15…1 %, причем название марки указывает на ее чистоту. Так, марка технической чистоты А8 обозначает, что в металле должно быть 99,8 % А1, а в марке высокой чистоты А99 − соответственно 99,99 % А1. В электролизных ваннах получают алюминий технической чистоты. Для получения алюминия более высокой чистоты требуется его дополнительное рафинирование.
3.4. Рафинирование алюминия
Наиболее широко применяют электролитическое рафинирование трехслойным методом, осуществляемое в расплавленной среде.
Сущность процесса электролитического рафинирования по трехслойному методу сводится к следующему. На дно электролитической ванны помещают расплавленный анодный сплав из алюми- ния-сырца с 25 % Сu плотностью 3,5 г/см3 и подводят к нему положительный полюс. Над анодным сплавом заливают электролит, состоящий из криолита Na3AlF6 и хлористого бария BaCl2, плотностью 2,7 г/см3. Если через анодный сплав и электролит пропускать постоянный электрический ток, то через некоторое время на катоде, находящемся наверху ванны, начнется выделение чистого алюминия (плотность которого в этих условиях 2,4 г/см3) и образование третьего жидкого слоя. В процессе содержание алюминия в анодном сплаве постепенно уменьшается, а количество чистого алюминия на катоде увеличивается.
Этот процесс теоретически аналогичен электролитическому рафинированию меди и отличается тем, что протекает не в водном растворе, а в расплавленных солях, и не с твердыми, а с жидкими электродами. Суммарно процесс можно представить с помощью уравнения на аноде:
49
[А1ж]− Зе = Аl+3; А13+ + Зе = [Аl ж ]
Впервом случае: ионы алюминия образуются и переходят в электролит; во втором − выделяется и накапливается слой жидкого алюминия, который выполняет роль катода.
Более электроположительные, чем алюминий примеси не могут перейти из анода в электролит до тех пор, пока в анодном сплаве имеется значительное количество алюминия. Примеси более электроотрицательные, чем алюминий, переходят из анода в электролит, но не могут выделяться на катоде до тех пор, пока концентрация ионов алюминия в электролите имеет значительную величину, так как потенциал выделения этих примесей выше, чем у алюминия.
Ванодный сплав периодически добавляют алюминий-сырец через специальный карман, а накапливающийся на катоде чистый алюминий отчерпывают из ванны.
Ванодном слое и электролите постепенно накапливаются примеси, и при значительном повышении их концентрации возникает опасность выделения примесей на катоде. Во избежание загрязнения катодного алюминия часть анодного сплава и электролита периодически меняют.
Высота слоя анодного сплава в ванне 200…250 мм, электроли-
та − 120…150 мм. Слой электролита такой толщины обеспечивает, при прохождении тока, необходимую температуру 760…800 °С. Слой металла на катоде дожжен быть толщиной около 100 мм. Во избежание окисления катодного металла его засыпают сверху тонким слоем порошкообразного электролита. Напряжение на ванне выдерживают в пределах 6…7 В, сила тока равна 40…50 кА. При этом может быть получен алюминий чистотой до 99,99 %. Рафинирование с помощью метода обходится очень дорого, поэтому при-
50
