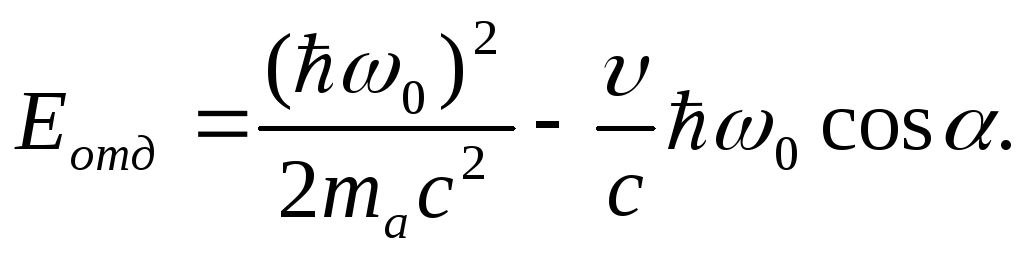Лекция 11
8.1. Линейчатые спектры атомов с одним
валентным электроном
Атомы щелочных металлов имеют один внешний электрон и заполненные внутренние оболочки. Этот внешний электрон движется в электрическом поле атомного остатка, т.е. ядра и заполненных электронных оболочек.
Если n(главное квантовое число) велико, то электрон движется далеко от атомного остатка и находится в центральном поле одного заряда (равного заряду +е). В этом случае спектральные термы атома подобны спектральным термам атома водорода.
Если же электрон подходит близко к атомному остатку, то он своим полем поляризует атомный остаток и движется в электрическом поле, образованном точечным зарядом и диполем.
Спектральные термы щелочных атомов выражаются формулой:
![]()
где R– постоянная
Ридберга, n–
главное квантовое число,σ–
поправка, зависящая от орбитального
квантового числа
![]() .
Таким образом, у щелочных металлов
энергия валентного электрона зависит
не только от главного квантового числа,
но и от орбитального квантового числа
.
Таким образом, у щелочных металлов
энергия валентного электрона зависит
не только от главного квантового числа,
но и от орбитального квантового числа
![]() ,
поэтому при одном и том жеnэнергетические уровни дляs,p,d,f и т.д. состояний
валентного электрона будут различны.
,
поэтому при одном и том жеnэнергетические уровни дляs,p,d,f и т.д. состояний
валентного электрона будут различны.
В ионах щелочных металлов реализуются
не все возможные электронные переходы,
а лишь разрешенные, которые удовлетворяют
правилу отбора Δ![]() =
±1, где Δ
=
±1, где Δ![]() – разность значений орбитальных
квантовых чисел, соответствующих двум
состояниям валентного электрона.
– разность значений орбитальных
квантовых чисел, соответствующих двум
состояниям валентного электрона.
В спектрах испускания щелочных металлов наблюдается главная серия, которая возникает при переходах оптического, т.е. валентного, электрона из различных возбужденных p– состояний в основные, невозбужденныеs– состояния. При переходе электрона в ближайшееs– состояние изp– состояния спектральная линия главной серии имеет максимальную интенсивность. Например, дляLiэта линия соответствует переходу 2р→ 2s. Для всех линий главной серии энергия переходов определяется выражением:
![]()
где m= 2, 3, 4, …
Здесь σsиσр- поправки, соответствующие конечномуsи начальномурсостояниям электрона (ридберговские поправки).
Кроме главной серии (наблюдаемой и при излучении, и при поглощении) наблюдаются также резкая, диффузная и основная серии. Резкая серия имеет резкие линии, диффузная – размытые.
Для натрия спектральные серии могут быть представлены переходами:
резкая серия
![]() ,n= 4, 5, …
,n= 4, 5, …
главная серия
![]() ,n= 3, 4, …
,n= 3, 4, …
диффузная серия
![]() ,n= 3, 4, …
,n= 3, 4, …
основная серия
![]() ,n= 4, 5, …
,n= 4, 5, …
Исследования оптических спектров ионов щелочных металлов показали, что момент импульса атомного остатка равен нулю, т.е. момент импульса атома щелочного металла равен моменту его валентного электрона. При возбуждении атома щелочного металла и при испускании им света изменяется только состояние валентного электрона.
8.2. Ширина спектральных линий
Из возбужденного состояния атом может спонтанно перейти в более низкое энергетическое состояние. Время τ, за которое число атомов, находящихся в данном возбужденном состоянии, уменьшается вераз, называется временем жизни возбужденного состояния. Эта величина ~ 10-8– 10-9с. Возможность спонтанных переходов указывает на то, что возбужденные состояния нельзя рассматривать как строго стационарные. Поэтому и энергия возбужденного состояния не является точно определенной, а возбужденный энергетический уровень имеет конечную ширинуГ. Согласно соотношению неопределенности Гейзенберга:
![]()
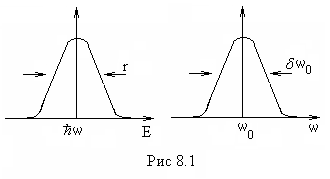
Основное же состояние атома стационарно, из него невозможен спонтанный переход в другие состояния. Поэтому энергия основного состояния определяется вполне точно. Из-за конечной ширины возбужденных уровней энергия испускаемых атомами фотонов имеет разброс, а испускаемая спектральной линией имеет конечную ширину (рис.8.1):
![]()
При τ ~10-8с![]() = 108 c-1,δλ~ 10-4 Å,
= 108 c-1,δλ~ 10-4 Å,![]() и δλ – естественная ширина спектральных
линий.
и δλ – естественная ширина спектральных
линий.
Тепловое движение излучающих атомов приводит к доплеровскому расширению спектральных линий.
Рассмотрим процесс испускания фотона
атомом. Пусть в момент испускания фотона
атом обладает импульсом
![]() и энергией поступательного движения
и энергией поступательного движения![]() ,
гдеma– масса атома. Фотон уносит с собой
импульс
,
гдеma– масса атома. Фотон уносит с собой
импульс
![]() ,
равный по модулю
,
равный по модулю![]() .
При этом импульс атома изменяется и
становится равным
.
При этом импульс атома изменяется и
становится равным![]() .
Таким образом, должна измениться и
энергия поступательного движения
атомов. Атом получает энергию отдачи:
.
Таким образом, должна измениться и
энергия поступательного движения
атомов. Атом получает энергию отдачи:
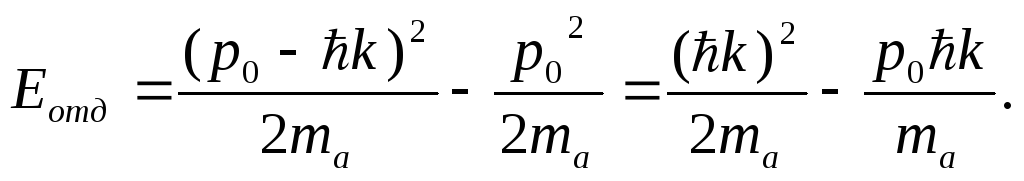
Подставим
![]() .
Учтем, что скорость атома до излучения
.
Учтем, что скорость атома до излучения![]() .
Имеем:
.
Имеем:
![]() (8.1)
(8.1)
где α – угол между векторами
![]() и
и![]() (угол
между направлением движения атома и
направлением, в котором испускается
фотон).
(угол
между направлением движения атома и
направлением, в котором испускается
фотон).
Пусть
![]() – убыль внутренней энергии атома за
счет перехода электрона с уровняnна уровеньm. Закон
сохранения энергии примет вид:
– убыль внутренней энергии атома за
счет перехода электрона с уровняnна уровеньm. Закон
сохранения энергии примет вид:
![]()
Если бы атомы при излучении не имели
отдачи, они испускали бы фотоны частотами
![]() и
и
![]() .
.
Энергия отдачи составляет для видимого
света ~ 10-11![]() .
Поэтому в формуле (8.1)
.
Поэтому в формуле (8.1)![]() можно заменить на
можно заменить на![]() ,
скорость
,
скорость![]() есть средняя скорость теплового движения
молекул. Тогда:
есть средняя скорость теплового движения
молекул. Тогда: