
теплоэнергетика
.pdfнятом до упоров положении снять груз, то, чтобы поршень опустился, нужно охладить содержащийся в цилиндре газ, т.е. отвести часть теплоты. Таким образом, для совершения цикла нужно иметь два источника теплоты. Горячий – для подвода тепла, холодный – для отвода тепла. Если мы в верхнем положении поршня снимем груз, то совершенная работа, которая заключалась в том, чтобы поднять этот груз, будет полезной работой. Отношение полезной работы к затраченной теплоте Q1 называется коэффициентом полезного действия:
|
L |
. |
(4.3) |
|
|||
|
Q1 |
|
|
Тепловые двигатели, в которых происходит процесс преобразования теплоты в механическую энергию, обычно разделяются на две группы в зависимости от применяемого метода преобразования. В одних используется потенциальная энергия рабочего тела (пара или газа), его давление на поршень. В других используется кинетическая энергия движущейся с большей скоростью струи пара или газа. Двигатели первой группы называют поршневыми, а двигатели второй группы – турбинными. К поршневым двигателям относятся паровые машины и двигатели внутреннего сгорания. Турбины могут быть паровыми и газовыми. Часто в качестве рабочего тела в тепловых двигателях используется водяной пар.
Второй закон термодинамики. Исходя из первого закона термодинамики допустимо считать, что любой мыслимый процесс, который не противоречит закону сохранения энергии, принципиально возможен и мог бы происходить в природе. Однако наблюдения привели к выводу, что теплота сама собой переходит лишь от тела с более высокой температуры к телу с более низкой температурой, но никогда наоборот; некомпенсированный переход теплоты от тела с меньшей температурой к телу с большей температурой невозможен. Это есть одна из формулировок второго закона.
В термодинамике используют еще один параметр состояния рабочего тела – энтропию, устанавливающую связь между количеством теплоты и температурой. Поясним этот параметр, исходя из следующих соображений.
Уравнение первого закона термодинамики можно записать в виде
dq = du + pdυ = du + dl. |
(4.4) |
51
В этом уравнении dq не является полным дифференциалом, поскольку в правую часть уравнения входит член dl, не являющийся полным дифференциалом, так как работа является не параметром состояния газа, а функцией процесса. Известно, что всякий двучлен можно представить в виде полного дифференциала, если его умножить на так называемый интегрирующий множитель.
При умножении на интегрирующий множитель 1/Т(где Т – абсолютная температура) приведенное выше уравнение примет вид
dq |
|
du |
|
dl |
. |
(4.5) |
T |
T |
|
||||
|
|
T |
|
|||
Уравнение (4.5) можно представить в несколько ином виде, а именно:
dq /T = СvdT/T + Rd / . |
(4.6) |
Выражение (4.5) говорит о том, что dq/T представляет собой полный дифференциал некоторой функции S (т.е. dq /T = ds),являющейся параметром состояния газа, поскольку она зависит только от двух параметров состояния (Т и) и поэтому не зависит от того, каким путем газ из одного состояния перешел в другое. Этот параметр состояния в общем случае называют энтропией, обозначают буквой S и измеряют в Дж/кг К.
Следовательно, можно записать:
dq /T= ds, а dq = T ds.
Полное количество теплоты в термодинамическом процессе можно определить как
2 |
|
q= T ds |
.(4.7) |
1 |
|
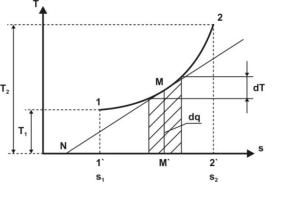
Этот интеграл можно вычислить, если известна функциональная зависимость между температурой и энтропией. Пользуясь этой зависимостью, в координатах Т, s (рис 4.2) строят кривые, отображающие те или иные термодинамические процессы.
Величину S можно рассчитать по известным значениям температуры Т, давления р и удельного объёма для любого состояния, и она также будет характеризовать состояние тела.
52
dS |
dQ |
|
dU |
|
pd |
. |
(4.8) |
T |
T |
T |
|
||||
Удобство этого нового параметра состояния заключается в том, что если изображать графически зависимость между температурой и энтропией (рис 4.2) при соответствующих давлениях, то получается график изменения параметров состояния рабочего тела, например водяного пара, в процессе подвода или отвода
теплоты. |
|
|
|
|
Энтропию |
|
|
||
нельзя |
измерить, |
|
||
ее смысл затруд- |
|
|||
нительно |
проде- |
|
||
монстрировать |
с |
|
||
помощью |
нагляд- |
|
||
ных пособий, |
но |
|
||
можно |
понять |
по |
|
|
следующим |
ин- |
|
||
терпретациям: |
|
|
||
1) Энтропия – |
|
|||
мера |
|
ценности |
Рис. 4.2. Тепловая T, s - диаграмма |
|
теплоты, |
ее рабо- |
|
||
тоспособности и технологической эффективности.
2) Энтропия – мера потери работы вследствие необратимости реальных процессов. Чем более необратим процесс в изолированной системе, тем больше возрастает энтропия и тем большая доля энергии не превращается в работу, а рассеивается в окружающую среду.
4.3. Цикл Карно
При громадном количестве топлива, расходуемого на получение механической энергии, очень важно повысить термический КПД двигателей. Но необходимо знать и тот предел, к которому нужно стремиться, т.к. попытки достичь невозможного бесполезны. Ответ на этот вопрос дал французский инженер Сади Карно (1796 – 1832). Он показал, как должен строиться цикл изменения состояния рабочего тела, чтобы для заданных условий работы двигателя термический КПД имел наибольшее значение. Этот цикл получил название цикла Карно (рис. 4.3).
Идеальный обратимый цикл Карно состоит из двух изотерм и двух адиабат. Подвод и отвод теплоты осуществляются при постоянной температуре от источников с бесконечной теплоёмко-
53

стью. В процессе изотермического расширения А-В рабочее тело получает теплоту q1, в процессе В-С происходит адиабатное расширение рабочего тела до температуры Т2. В процессе изотермического сжатия С-D рабочее тело отдает теплоту q2 теплоприемнику. Замыкается цикл адиабатой сжатия D-А с повышением температуры ра-
бочего тела от Т2 до Т1. Полезная работа цикла ,
численно равная площади прямоугольника, изображающего цикл в Т, s - диаграмме (рис. 4.3), определяется как разность подведенной q1 и отведенной q2 теплоты. Таким образом, при осуществлении цикла Карно не вся теплота q1 источника превращается в ра-
боту, а только часть её (q1– q2), другая же часть q2 отдается охладителю и не может быть использована ни для получения работы, ни для нагревательных целей, то есть является тепловым отбросом кругового процесса.
Тогда термический КПД цикла Карно может быть определен по выражению
к |
|
|
q1 q2 |
1 |
q2 |
1 |
T2 S |
1 |
T2 |
. |
(4.9) |
|
|
|
T1 S |
|
|||||||
t |
q1 |
|
q1 |
|
q1 |
|
|
T1 |
|
||
|
|
|
|
|
|
||||||
Теорема Карно: Термический коэффициент полезного действия цикла Карно зависит только от абсолютных температур источника тепла и холодильника и не зависит от свойств рабочего тела.
Чем больше разность температур, то есть чем больше температура горячего источника теплоты и меньше температура «холодильника», тем выше КПД цикла Карно. Термический КПД всех других циклов в данном интервале температур T1 и T2 не может быть больше КПД цикла Карно.
При равенстве температур T1 и T2 термический КПД цикла Карно равен нулю, что указывает на невозможность превращения теплоты в работу, если рабочее тело находится в тепловом равновесии с окружающей средой.
54
4.4. Водяной пари его применение в качестве рабочего тела
Чтобы составить представление о процессе получения пара из воды и возможности совершения этим паром работы с наибольшим аффектом, предварительно ознакомимся с основными свойствами водяного пара.
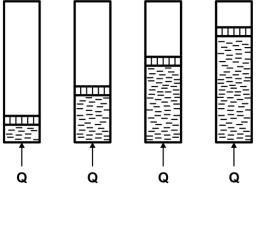
Если взять 1 кг воды при °0С, поместить его в цилиндрический сосуд (рис. 4.4, позиция 1), плотно закрытый сверху подвижной крышкой (поршнем), и нагревать воду так, чтобы давление в сосуде оставалось все время постоянным и равным одной абсолютной атмосфере (0,0981 МПа),то при прогревании воды до 100°С (точнее до 99,1°С) объем ее незначительно увеличивается (позиция 2), и вода начинает закипать.
При дальнейшем нагревании при постоянном давлении вода постепенно начинает превращаться в пар. Объем под поршнем увеличивается (позиция 3), но температура всё время остается постоянной. С момента закипания воды до превращения всей
воды в пар (позиция |
|
|
|
|
||||
4), т.е. в процессе |
|
|
|
|
||||
парообразования |
|
|
|
|
||||
затрачено |
будет |
|
|
|
|
|||
теплоты в 5,4 |
раза |
|
|
|
|
|||
больше, |
чем |
до |
|
|
|
|
||
начала |
кипения, |
|
|
|
|
|||
объем же получен- |
|
|
|
|
||||
ного |
пара |
будет в |
|
|
|
|
||
несколько сотен раз |
|
|
|
|
||||
больше объема во- |
|
|
|
|
||||
ды. |
Полученный в |
|
|
|
|
|||
таком виде пар но- |
|
|
|
|
||||
сит название сухого |
1 |
2 |
3 |
4 |
||||
насыщенного. |
За- |
|||||||
|
|
|
|
|||||
траченное |
на |
полу- |
Рис. 4.4. Процесс подвода теплоты к воде и |
|||||
|
|
|
|
|||||
чение пара из кипя- |
|
водяному пару |
|
|||||
щей |
воды |
тепло |
|
|
|
|
||
называют скрытой теплотой парообразования. Теплота называется скрытой потому, что при этом не замечается повышения температуры. Ее постоянство при парообразовании объясняется тем, что тепло идет, с одной стороны, на преодоление сил сцепления при превращении жидкости в парообразное состояние, с другой – на работу расширения, связанную с увеличением объема.
55
Обратный процесс, т.е. превращение пара в воду, называется конденсацией. Он происходит при постоянном давлении с отдачей теплоты и также при постоянной температуре с резким уменьшением объема.
Количество теплоты, которое необходимо сообщить воде или пару при постоянном давлении, начиная с 00 С до рассматриваемого состояния, называется энтальпией.
Описанный процесс парообразования происходил при постоянном давлении, следовательно, мы получили при каждом состоянии соответствующую энтальпию, а именно: в начале кипения энтальпию жидкости h , равную в данном случае около 419 кДж/кг воды.
h = h + r = 2 680 кДж/кг.
Если продолжать сообщать теплоту полученному пару при неизменном давлении, то температура начнет уже повышаться, плотность падать и объем возрастать.
В настоящее время энергетика, благодаря достижениям металлургии, имеет дело с очень высокими параметрами пара – давлением 14 – 24 МПа, температурой до 540 – 550°С, поэтому уже при первом знакомстве с теплоэнергетикой следует знать некоторые характерные особенности поведения водяного пара.
Так, если нагревать воду при давлении 10 МПа, то темпера-
тура |
кипения |
будет |
уже 310°С, |
а энтальпия жидкости |
1408 |
кДж/кг. |
Зато на |
испарение |
будет затрачено лишь |
1316 кДж/кг, т.е. меньше, чем при атмосферном давлении примерно в 1,5 раза.
При давлении, равном 22,1 МПа, для начала закипания нужно будет сообщить теплоты еще больше, а именно 2045 кДж/кг, т.е. почти в 5 раз больше, чем при Р = 0,1 МПа, а на парообразование потребуется всего лишь 102 кДж/кг, причем объем увеличится всего в 1,4 раза, т.е. плотность пара мало отличается от плотности жидкости, из которой он получается.
При Р = 22,115 МПа и температуре t= 374,12°С энтальпия жидкости h = 2095 кДж/кг, r = 0. Такое состояние называется критическим. Т, s - диаграмма для водяного пара приведена на рис.4.5. Пограничные линии х= 0 и х= 1 сходятся в критической точке К, где свойства пара и воды неразличимы. Пограничными линиями диаграммы являются линии х = 0 и кривая АВК, каждая точка которой соответствует состоянию кипящей воды, и х = 1, кривая КСЕ, соответствующая состоянию сухого насыщенного пара. Параметр х, называемый степенью сухости пара, показы-
56
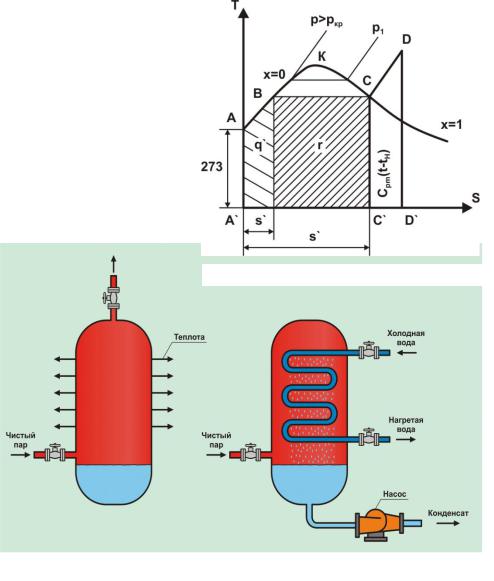
вает, сколько по массе в паре находится сухого насыщенного пара и капель воды.
Левее и выше линии х = 0 параметры среды соответствуют воде, нагретой до температуры кипения, правее и выше линии х = 1 – пере-
гретому |
пару, |
а |
между |
линиями |
|
х = 0 |
и х = 1 |
– |
влажному пару. Образовавший-
ся в сосуде водяной пар может при
Рис.4.5. Т, s - диаграмма для водяного пара
1
2
а
тепловую |
энер- |
Рис.4.6. Процесс конденсации водяного пара в |
гию через |
стенки |
теплообменниках |
сосуда окружающей его холодной воде. При этом давление пара
57
над зеркалом воды в сосуде будет уменьшаться и всегда совпадать с давлением насыщения, соответствующим температуре образующейся жидкости.
Пар превращается в воду потому, что от него отбирается теплота конденсации, равная теплоте парообразования r. В результате конденсации пара на дне сосуда образуется конденсат, а над зеркалом конденсата – насыщенный водяной пар. Чем сильнее будет охлажден пар в сосуде, тем больше образуется конденсата на его дне и тем более низкое давление будет получено в сосуде.
В процессе конденсации пара в сосуде может быть получено давление существенно ниже атмосферного, т. е. вакуум. На рис.4.6 показана принципиальная схема установки для непрерывной конденсации постоянно поступающего пара. Если в сосуде установить змеевик, по которому пропускать относительно холодную воду, то пар, поступающий в сосуд, будет встречать на своем пути холодную поверхность змеевика и конденсироваться на ней.
Для удаления образующегося конденсата применяется насос, благодаря чему происходит непрерывная конденсация поступающего пара, а внутри сосуда поддерживается давление, соответствующее температуре образующегося конденсата. На описанном принципе основана работа конденсаторов, сетевых и регенеративных подогревателей и многих других теплообменных аппаратов, применяемых в энергетике.
Таким образом, процесс превращения пара в жидкость, осуществляющийся при отнятии от него тепла и являющийся процессом, обратным парообразованию, называется конденсацией. Этот процесс, так же как и парообразование, происходит при постоянной температуре, если давление постоянно.
Контрольные вопросы
1. Кем и в каком году было опубликовано первое термодинамическое исследование работы паровых машин?
2. Укажите основные параметры состояния рабочего тела и единицы измерения их.
3. Определите, какому давлению в МПа соответствует давление 735,6 мм рт. ст.
4. Приведите основное уравнение идеального газа.
5. Дайте определение внутренней энергии тела.
58
6. Объясните сущность первого закона термодинамики и напишите его математическое выражение.
7. Какова сущность второго закона термодинамики? Дайте некоторые формулировки этого закона.
7. Покажите на Т, s - диаграмме цикл Карно.
8. По какому выражению можно определить термический КПД цикла Карно?
9. Покажите на Т, s - диаграмме характерные области и линии для воды и водяного пара.
10. Покажите на Т, s - диаграмме площадки, соответствующие теплоте, затрачиваемой на подогрев воды, парообразование и на перегрев пара.
11. Что такое температура насыщения для пара? Какой основной параметр её определяет?
12. Пар находится в состоянии насыщения. Как изменится состояние пара при его охлаждении или нагреве?
13. Назовите температуру и давление для критической точки для воды и водяного пара.
14. Какому состоянию пара и воды соответствует параметр х, называемый степенью сухости пара?
20.Назовите точку на Т, s - диаграмме воды и водяного пара,
вкоторой сходятся пограничные линии х = 0 и х = 1.
59
Раздел 5.Основы теории теплообмена
5.1. Общие положения
Теория теплообмена изучает способы теплообмена и распределения тепловой энергии. С теплообменом связано большое количество самых разнообразных явлений. Теплообменом сопровождаются производственные процессы, а также множество явлений, наблюдаемых в природе. Процессами теплообмена мы часто пользуемся в быту. Человеческое тело имеет отличную от окружающей среды температуру, и потому оно непрерывно участвует в процессе теплообмена.
В топке парового котла сжигается топливо, а выделяющаяся при этом теплота передается воде и пару. Чем больше теплоты от газов будет передано воде и пару, тем меньше потребуется топлива для получения необходимого количества пара, тем экономичнее будет котельный агрегат.
Основной процесс в паровой турбине – расширение парав каналах турбинных решеток. Использование специального теплообменника – конденсатора, установленного на выходе паровой турбины, позволяет увеличить количество теплоты, превращенной в полезную работу в турбине. Внутри трубок конденсатора течет холодная вода, а выходящий из турбины пар, соприкасаясь с холодными поверхностями труб, конденсируется, т.е. превращается в воду. Даже в электрическом генераторе использование процессов теплообмена приносит большую пользу. Охлаждение обмоток генератора позволяет увеличить надежность работы и уменьшить его вес и размеры.
5.2. Теплопроводность. Закон Фурье
Количество теплоты, которое проходит через тело путем теплопроводности, зависит от способности материала тела пропускать тепло, от разности температур на поверхностях тела и от его размеров и формы. Количество теплоты, передаваемое теплопроводностью через тело, пропорционально разности температур на его поверхностях.
Способность материала стенки пропускать тепло путем теплопроводности можно оценить по тепловому потоку, который пройдет через один квадратный метр поверхности стенки при разности температур в один градус.
В 1822 г., изучая явление теплопроводности в твёрдых телах, французский физик Жозеф Фурье установил, что количество
60
