
- •Эи.Лпр4 – Электрохимические преобразователи
- •Зависимость электропроводности растворов от концентрации.
- •Зависимость электропроводности растворов от температуры.
- •Электродные и граничные потенциалы.
- •Электролиз и поляризация.
- •Электролитические резистивные преобразователи
- •Гальванические измерительные преобразователи
Гальванические измерительные преобразователи
Наиболее распространенными разновидностями гальванических измерительных преобразователей являются преобразователи рН- метров, применяемые для измерения активности водородных ионов, по которой можно определить состав и свойства растворов, и гальванические источники э. д. е., в частности нормальные элементы, используемые в качестве мер э. д. с.
Принцип действия гальванических преобразователей рН-метров основан на зависимости э. д. с. гальванической цепи от концентрации ионов в электролите и окислительно-восстановительных процессов, происходящих на электродах.
Наиболее точным и универсальным методом измерения рН является электрометрический метод, т. е. определение электродных потенциалов различных электродов, помещаемых в исследуемый раствор, содержащий водородные ионы. Следовательно, гальванические преобразователи, являющиеся датчиками рН-метров, в качестве естественной входной величины имеют значение концентрации водородных ионов, выражаемое в единицах рН, а в качестве выходной величины — гальваническое напряжение, равное разности электродных потенциалов.
Так как практически измерить потенциал одного электрода невозможно, то гальванический преобразователь всегда состоит из двух полуэлементов: измерительного электрода, помещаемого в исследуемый раствор, и вспомогательного полуэлемента, электродный потенциал которого должен оставаться постоянным.
Устройство водородного электрода показано на рис. 4-9.
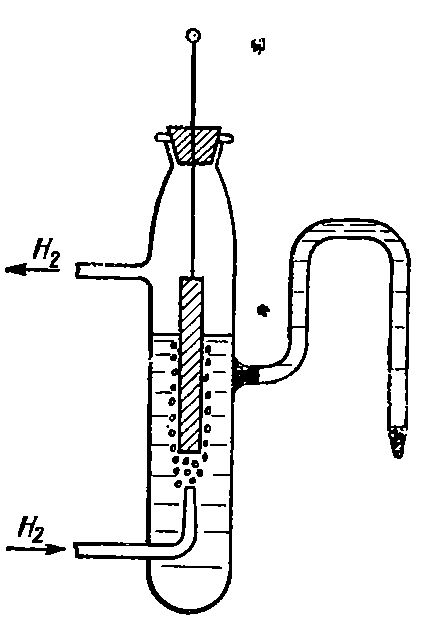
Рис.4-9
Пластинка из черненой платины с выводом частично погружается в раствор, содержащий ионы водорода Н+. Через раствор непрерывно пропускается чистый водород, поступающий при атмосферном давлении. При этом на электроде происходит реакция
Н2=2Н+ + 2е.
Платина электрода в реакции не участвует и является лишь проводником электронов и носителем водорода, который хорошо адсорбируется на поверхности черненой платины.
Вспомогательные полуэлементы. В гальванических преобразователях используются каломельный, хлорсеребряный, бромсеребряный и другие вспомогательные полуэлементы.
Каломельный полуэлемент показан на рис. 4-10.

Рис.4-10
Потенциал Е0 нормального каломельного полуэлемента относительно потенциала нормального водородного полуэлемента при температурах 15, 18, 20, 25 и 30° С соответственно составляет 0,2852; 0,2845, 0,2840, 0,2828 и 0,2816 В.
Гальванический преобразователь, состоящий из водородного электрода, помещенного в исследуемый раствор, и нормального каломельного полуэлемента, будет при 18 °С развивать э. д. с.
![]()
Хлорсеребряный полуэлемент представляет собой платиновую проволоку, покрытую слоем хлористого серебра и погруженную в раствор НС1. Нормальный потенциал хлорсеребряного полуэлемента равен 0,222 В при 25° С. Достоинствами хлорсеребряных полуэлементов являются простота и компактность конструкции, хорошая воспроизводимость потенциала электрода, возможность применения при температурах до 150—250° С, а также в условиях тряски и вибраций [100].
Измерительные электроды гальванических преобразователей. В качестве измерительных электродов, кроме водородного, применяются хингидронный электрод, сурьмяный электрод и получивший наибольшее распространение стеклянный электрод.
Хингидронный электрод образуется путем помещения в контролируемый раствор платинового электрода и добавления в раствор небольшого количества хингидрона С6Н402-С6Н4(0Н)2. Такой электрод является аналогом водородного электрода, получающего водород из равновесной окислительно-восстановительной системы хинонгидрохинон, благодаря чему отпадает необходимость непрерывно подавать в контролируемый раствор газообразный водород. Э. д. с. хингидронно-каломельного преобразователя при 18 °С равна Е = 0,457—0,058 рН. Хингидронный электрод дает хорошие результаты в кислых и слабых щелочных растворах (рН < 9).
Сурьмяный электрод представляет собой литой сурьмяный стержень, опускаемый непосредственно в испытуемый раствор. Для того чтобы можно было применять этот электрод в растворах, окисляющих, разъедающих или покрывающих электрод продуктами разложения электролита, его необходимо подвергать непрерывной механической очистке.
Сурьмяный электрод используют при не очень высоких требованиях к точности измерения для анализа растворов с рН = 2 ч- 12.
Стеклянный электрод представляет собой шаровую тонкостенную колбочку (мембрану), выдуваемую на конце трубки из специальных сортов стекла. Толщина стенки колбочки равна 0,05—0,1 мм. Колбочка заполняется контрольным раствором (нормальным или децинормальным) какой-либо соли или кислоты и погружается в исследуемый раствор, концентрацию которого надо измерить.
Опыт показывает, что на границе стекло — раствор появляется определенный потенциал, зависящий от активности водородных ионов раствора, в который погружен стеклянный электрод. Иначе говоря, стеклянный электрод ведет себя, как водородный электрод. При этом безразлично, какая поверхность колбочки будет использована — внутренняя или внешняя; обе поверхности нужно рассматривать как водородные электроды, один из которых в практических измерениях должен иметь постоянный потенциал. Промежуточный слой стекла между обеими поверхностями является, по существу, проводником, соединяющим оба электрода.
Гальванический преобразователь со стеклянным электродом обычно состоит из стеклянного электрода и двух вспомогательных полуэлементов, которые используются для снятия потенциала с внутренней и внешней поверхностей стеклянного электрода. Во вспомогательном полуэлементе для снятия потенциала с внутренней поверхности чаще всего используется хлорсеребряный микроэлектрод, который встраивается внутрь стеклянного электрода.
Схема устройства гальванического преобразователя со стеклянным электродом показана на рис. 4-11.

Рис.4-11
Стеклянный электрод 1 и каломельный полуэлемент 3 помещаются в исследуемый раствор. Внутрь стеклянного электрода, заполненного образцовым раствором с известным значением рН, например 0,1 и раствором НС1, вставлен вспомогательный хлорсеребряный электрод 2.
Э. д. с. на выводах преобразователя является алгебраической суммой потенциалов хлорсеребряного полуэлемента, внутренней и наружной поверхности стеклянного электрода и потенциала каломельного полуэлемента.
При изменении рН исследуемого раствора изменяется только потенциал наружной поверхности электрода, который зависит от активности водородных ионов в растворе. Все же остальные составляющие э. д. с. остаются неизменными (при постоянной температуре) поэтому, измеряя э. д. с. на выводах преобразователя со стеклянным электродом, можно определить рН исследуемого раствора.
Стеклянный электрод может применяться для измерения рН большинства растворов и поэтому получил наиболее широкое применение. Принцип действия стеклянного электрода основан на процессе ионного обмена. При помещении стеклянного электрода в раствор щелочные ионы стекла (Na или Li) переходят в раствор, а их места занимают более подвижные ионы водорода из раствора. В результате этого поверхностный слой стекла оказывается насыщенным водородными ионами, и стеклянный электрод приобретает свойства водородного электрода.
Характерной особенностью гальванических преобразователей со стеклянными электродами является их большое внутреннее сопротивление, так как в него входит сопротивление стеклянной мембраны. В зависимости от химического состава и толщины стеклянного электрода его сопротивление составляет 0,5—1000 МОм.
Другой особенностью стеклянного электрода является наличие потенциала асимметрии, который проявляется в том, что при помещении внутрь и снаружи электрода одинаковых растворов на выводах гальванического преобразователя со стеклянным электродом возникает э. д. е., которая может достигать 10—20 мВ. Потенциал асимметрии тем больше, чем толще стенка электрода и чем выше его сопротивление. После изготовления стеклянный электрод необходимо вымачивать в 0,1 н растворе НС1 в течение нескольких- суток, что снижает и стабилизирует его потенциал асимметрии. Кроме того, вымачивание способствует уменьшению инерционности стеклянного электрода. Постоянные времени стеклянных электродов лежат в пределах 1—10 с. Время установления потенциала увеличивается с понижением температуры, с уменьшением скорости протекания раствора и при загрязнении электродов.
Точность воспроизведения стеклянным электродом водородной функции и стабильность этой функции во времени сильно зависят от сорта стекла. Хорошими электродными свойствами обладают литиевые силикатные стекла. Повышение процентного содержания Si02 расширяет температурный диапазон применения стеклянных электродов. В настоящее время разработаны стеклянные электроды, которые можно использовать при повышенных температурах — до 150 °С.
