
БИОХИМИЯ ПЕЧЕНИ
.doc
БИОХИМИЯ ПЕЧЕНИ.
Печень как никакой другой орган отличается разнообразием ферментов и метаболических превращений. в организме нет путей метаболизма, которые прямо или косвенно не контролировались бы печенью. Центральное место, которое занимает печень в обмене веществ, определяется в 1-ую очередь тем, что в нее по воротной вене попадает бóльшая часть веществ, всосавшихся в кишечнике (за исключением липидов, транспорт которых в основном осуществляется через лимфатическую систему), поэтому печень выступает в роли первичного регулятора содержания многих жизненно важных компонентов крови. Это орган - альтруист, так как: 1) обеспечивает другие ткани различными веществами, необходимыми для их функционирования; 2) защищает эти ткани от токсинов, как экзогенных, так и эндогенных.
химический состав печени: вода - 70%, белки (в основном глобулины) - 20%, липиды (таг, фл, хс) - 5%, гликоген - 5% (150-200 г). содержание fe, cu, mn, ni и некоторых других элементов в печени больше, чем в других тканях.
Биохимические функции печени: 1) регуляторно-гомеостатическая; 2) мочевинообразовательная; 3) желчеобразовательная; 4 экскреторная; 5 обезвреживающая.
регуляторно-гомеостатическая функция реализуется через участие в обмене питательных веществ
а. углеводный обмен. печень обеспечивает постоянство уровня глюкозы в крови при повышении глюкозы крови например после приема пищи активируется глюкокиназа образуется глюкозо-6-фосфат который активно используется в гликолизе пфц в синтезе гликогена при снижении глюкозы крови например при голодании сначала быстро активируется гликогенолиз позже более медленно - глюконеогенез в основном из аминокислот а также из лактата образующегося в мышцах свободная нефосфорилированная) глюкоза выходит в кровь и используется разными тканями в первую очередь нервной.
в печени осуществляется превращение фруктозы и галактозы:
 фруктозо-6-фосфат
гликолиз
фруктозо-6-фосфат
гликолиз

 гк адф
гк адф
атф
фруктоза

 атф
дигидроксиацетонфосфат
атф
дигидроксиацетонфосфат
ф рукто-
адф
фр-1-ф
рукто-
адф
фр-1-ф
к иназа
фр-1-фосфат альдолаза
иназа
фр-1-фосфат альдолаза

триокиназа


 глицеральдегид
гл-д-3-ф
гликолиз
глицеральдегид
гл-д-3-ф
гликолиз
атф адф
галактозо-1-фосфат
галактокиназа уридилтрансфераза
г


 алактоза
гал-1-ф
гл-1-ф
алактоза
гал-1-ф
гл-1-ф
атф адф удф-глюкоза удф-галактоза
удф-галактоза либо участвует в синтезе сложных углеводов (гликолипидов, гликопротеинов), либо под действием эпимеразы превращается в удф-глюкозу. удф-глюкоза может участвовать в синтезе как гликогена, так и гликолипидов и гликопротеинов.
б. липидный обмен
-
образующиеся в печени желчные кислоты нужны для переваривания и всасывания липидов (эмульгация жиров активация панкреатической липазы транспорт длинноцепочечных жирных кислот
-
происходит синтез жирных кислот таг преимущественно из глюкозы см. схему или из жирных кислот поступающих с кровью фл сфинголипидов хс и его эфиров причем холестерина синтезируется больше чем поступает с пищей. скорость синтеза фл определяется лимитируется количеством липотропных факторов; регуляция синтеза холестерина и его метаболизм - см. лекцию.
-
печень распределяет липиды по тканям посредством образования и секреции лпвп -лп и лпонп пре--лп т.к. помимо липидов здесь синтезируется белковая часть лп - апо а апо в и др. Т.о. в норме синтезируемые ТаГ не накапливаются в печени а в составе лпонп транспортируются по крови в жировую ткань для хранения.
-
в печени происходит распад таг, окисление жк синтез кетоновых тел являющихся энергетическими субстратами для внепеченочных тканей.
в. обмен белков
i. синтез белков. из 80-100 г белков синтезируемых в организме человека половина образуется в печени. в гепатоцитах образуются специфические белки плазмы крови 1) все альбумины 13-18 гсут 75-90 -глобулинов 50 -глобулинов а в купферовских клетках - -глобулины; 2) белки свертывающей и антисвертывающей систем крови например фибриноген протромбин проконвертин проакцелерин 3) транспортные белки: трансферрин церулоплазмин транскортин ретинолсвязывающих белок кальциферолсвязывающий белок тироксинсвязывающий глобулин тестостерон-эстрадиол-связывающий глобулин, нр транскобаламины i и ii и т.д. т.е. белки участвующие в переносе минеральных веществ витаминов гормонов нв билирубина и т.д. 4) ферменты функционирующие в плазме холинэстераза лхат печеночная липаза и др.
ii обмен аминокислот активно протекают как их собственный синтез так и использование аминокислот в синтезе других веществ креатина холина глутатиона никотиновой кислоты пуринов пиримидинов порфиринов и т.д. Аминокислоты активно переаминируются дезаминируются декарборсилируются их углеродные скелеты либо используются в синтезе глюкозы например, кетоновых тел, либо сгорают с выделением энергии. при голодании печень первой расщепляет свои резервные белки для снабжения аминокислотами других тканей.
Пурины распадаются до мочевой кислоты. образующийся при дезаминировании nh3 обезвреживается путем синтеза из него мочевины; важность этого процесса обусловила выделение специальной мочевинообразовательной функции печени.
г. участие печени в обмене витаминов:
- синтез транспортных белков;
-
депонирование витаминов, в основном жирорастворимых (например, витаминов а, к, е), и некоторых водорастворимых (вит. в1, в9, в12, с, н);
-
синтез никотиновой кислоты из триптофана;
-
синтез витаминных коферментов (тдф, над, надф, метилкобаламина и дезоксиаденозилкобаламина и др.);
-
метаболизм витамина d (образование 25-гидроксикальциферолов).
д. участие печени в водно-минеральном обмене:
- синтез специальных транспортных белков;
-
способна задерживать na, k, cl, ca, h2o и выделять их в кровь;
-
депонирует микроэлементы (fe, cu, и др.) и участвует в распределении их по другим тканям с помощью транспортных белков.
е. участие печени в метаболизме гормонов:
-
синтез транспортных белков для некоторых из них;
-
инактивация гормонов: пептидные гормоны расщепляются протеиназами. инактивация инсулина включает сначала разрыв дисульфидного межцепочечного мостика, а потом - гидролиз а- и в-цепей, причем в печени разрушается 80% инсулина при однократном прохождении крови через нее. адреналин и норадреналин: дезаминирование моноаминооксидазой, метилирование по он-группам, конъюгация с серной и глюкуроновой кислотами, после чего продукты катаболизма выводятся в основном с мочой. стероидные гормоны: в основном инактивируются микросомальными гидроксилазами и выводятся в форме конъюгатов с глюкуроновой и серной кислотами. тироксин: путем переаминирования превращается в кетопроизводное или конъюгирует по фенольной группе с глюкуроновой и серной кислотами.
желчеобразовательная и экскреторная функции. Гепатоциты активно секретируют желчь, примерно 500-700 мл (10 мл/кг) в сутки. основные компоненты желчи: н2о, желчные кислоты, холестерин и его эфиры, сжк, фл, пигменты (билирубинглюкурониды), муцин, минеральные вещества (k, na, ca, cl), некоторые ферменты (например, щелочная фосфатаза), неактивные продукты обмена гормонов и витаминов, чужеродные вещества. пузырная желчь является более концентрированной, чем печеночная. хс нерастворим в воде, поэтому в желчи он образует мицеллы с желчными кислотами и фх и благодаря этому не выпадает в осадок. Нормальное соотношение основных компонентов мицеллы: 5% хс, 15% фх, 80% солей желчных кислот. при недостатке желчных кислот – холестериновые камни.
Т. о., с желчью выводятся из организма не только хс, желчные кислоты и пигменты, но и многие лекарства, токсины, различные неорганические вещества (медь, цинк, ртуть).
обезвреживающая функция. печень - основной орган, где обезвреживаются как собственные метаболиты, так и чужеродные вещества (ксенобиотики). обезвреживание обычно включает две фазы: 1) модификации и 2) конъюгации. в результате модификации в структуре вещества появляются функциональные группы (он-, nh2 -, cooh-, sh- и некоторые др.), которые, во-первых, повышают растворимость вещества и, во-вторых, позволяют ему вступить во вторую фазу - конъюгации, т.е. ферментативного присоединения к этим группам какого-либо вещества. превращения ксенобиотиков в печени происходят как в эпс (= микросомах), так и вне микросом (гиалаплазма, лизосомы, пероксисомы, мх).
главная роль в фазе модификации принадлежит микросомальным гидроксилазам (=монооксигеназам). в мембранах эпс находится монооксигеназная цепь окисления. источником электронов и протонов является надфн2, образующийся в
2ē



 h
о2
h
о2
 rh
rh
s
 надфн2
фп2
р450
надфн2
фп2
р450
roh

 h
h

 2h+
2h+
h2o
2h+
2h+
h2o
пфц. с надфн2 электроны и протоны поступают на флавопротеид (фп2),
коферментом которого является фад. с фп2 электроны транспортируются на цитохром р450, а протоны - в окружающую среду. цитохром р450 - основной компонент микросомальной системы окисления - переносит электроны на о2 и таким образом активирует его, а уже активированный кислород использует для окисления вещества (rh) и образования воды. два протона для образования воды берутся из среды.
Общая реакция микросомального окисления:
r h
+ o2
+ надфн2
roh
+ h2o
+ надф+
h
+ o2
+ надфн2
roh
+ h2o
+ надф+
Например:
о
c h3-ch2oh
+ надфн2
+ о2
сн3с-н
+ надф+
+ 2н2о
h3-ch2oh
+ надфн2
+ о2
сн3с-н
+ надф+
+ 2н2о
этанол ацетальдегид
Монооксигеназная цепь микросом служит универсальной биологической системой окисления любых неполярных соединений. неполярных, т.к. цитохром р450 находится в липидном слое мембран. эндогенные субстраты микросомального окисления - стероидные гормоны и холестерин (из холестерина при этом могут образоваться желчные кислоты); экзогенные субстраты - лекарства и токсины.
основные типы реакций, осуществляемых микросомальными цепями печени (3):
1) окисление ксенобиотиков:



 он
он
 + о2
+ надфн2
+ н2о
+ надф+
+ о2
+ надфн2
+ н2о
+ надф+
бензол фенол
2) окисление природных субстратов:
-
- окисление жирных кислот (см. лекцию),
-
гидроксилирование различных стероидов, а также простагландинов;
3) восстановление ксенобиотиков. Оно идет на уровне не цитохрома р450 , а фп2, с которого водород поступает на субстрат.
монооксигеназная цепь окисляет очень много различных веществ, делая их при этом более полярными. растворимость их в воде повышается, они легче вступают в другие реакции и выводятся из организма.
внемикросомальные превращения веществ:
- в митохондриях - окислительное дезаминирование биогенных аминов;
-
в цитоплазме - окисление алифатических спиртов алькогольдегидрогеназой в альдегиды, которые окисляются альдегиддегидрогеназой в органические кислоты;
-
в пероксисомах возможно окисление этанола каталазой:
каталаза о
 ch3-ch2oh
+ н2о2
сн3с-н
+ 2н2о
ch3-ch2oh
+ н2о2
сн3с-н
+ 2н2о
этанол ацетальдегид
-
в лизосомах осуществляется гидролиз эфирных связей эстеразами (псевдохолинэстераза, фдэ-зы, сульфатазы и др.).
Фаза конъюгации нужна для образования нетоксичных, легковыводимых продуктов метаболизма. Конъюгация может быть:
а) глюкуронидная - самая частая. источник глюкуроновой кислоты - удф-гк. Этому виду конъюгации подвергаются, например, билирубин, стероидные гормоны, витамин д, а также ксенобиотики, имеющие он-, nh2-, cooh-, sh- группы. фермент – удф- глюкуронилтрансфераза.
б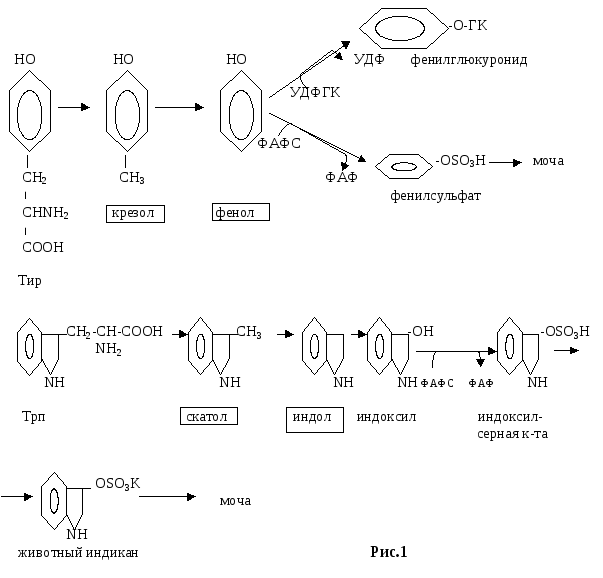 )
сульфатная. источник
серной кислоты - 3-фосфоаденозин-5-фосфосульфат
= фафс (стр.
453). ей
подвергаются вещества, являющиеся, как
правило, циклическими и имеющие свободные
он-, nh2
-группы.
фермент -
арилсульфотрансфераза.
Например, стероиды, иодтиронины,
токоферолы, нафтохиноны, а также продукты
гниения белков, образующиеся в кишечнике
под действием ферментов микрофлоры:
индол, скатол, фенолы. В
печени эти вещества обезвреживаются:
гидроксилируются (если нет Он-группы)
и конъюгируют с глюкуроновой или серной
кислотами (рис.1).
)
сульфатная. источник
серной кислоты - 3-фосфоаденозин-5-фосфосульфат
= фафс (стр.
453). ей
подвергаются вещества, являющиеся, как
правило, циклическими и имеющие свободные
он-, nh2
-группы.
фермент -
арилсульфотрансфераза.
Например, стероиды, иодтиронины,
токоферолы, нафтохиноны, а также продукты
гниения белков, образующиеся в кишечнике
под действием ферментов микрофлоры:
индол, скатол, фенолы. В
печени эти вещества обезвреживаются:
гидроксилируются (если нет Он-группы)
и конъюгируют с глюкуроновой или серной
кислотами (рис.1).
в )
ацетильная.
источник ацетильной группы -
ацетил-коа.
ей подвергаются вещества со свободной
nh2-группой.
n-ацетилирование
моносахаров с образованием
n-ацетилглюкозамина,
n-ацетилгалактозамина,
нейраминовой кислоты - необходимая
реакция в синтезе гетерополисахаридов.
кроме
того, с помощью n-ацетилирования
могут обезвреживаться некоторые
биогенные амины (серотонин, гистамин и
др.).
среди ксенобиотиков
ацетилированию подвергаются, например,
сульфаниламиды, гидразиды изоникотиновой
кислоты, производные анилина (рис.2).
)
ацетильная.
источник ацетильной группы -
ацетил-коа.
ей подвергаются вещества со свободной
nh2-группой.
n-ацетилирование
моносахаров с образованием
n-ацетилглюкозамина,
n-ацетилгалактозамина,
нейраминовой кислоты - необходимая
реакция в синтезе гетерополисахаридов.
кроме
того, с помощью n-ацетилирования
могут обезвреживаться некоторые
биогенные амины (серотонин, гистамин и
др.).
среди ксенобиотиков
ацетилированию подвергаются, например,
сульфаниламиды, гидразиды изоникотиновой
кислоты, производные анилина (рис.2).
лекарство инактивируется, поэтому для определения эффективной дозы следует расчитывать ацетилирующую способность организма (см. практическую работу);
г) метильная. источник метильной группы - s-аденозил-метионин. метилируется много природных веществ, а к ксенобиотикам сн3-группа присоединяется по он-, sh-, nh2- группам или по азоту в гетероцикле. Пример: пиридин, тиоурацил, никотиновая кислота и др.;
д) тиосульфатная. источник тиосульфатной группы - серосодержащие аминокислоты. используется для ферментного обезвреживания цианидов, т.к. образующийся тиоцианат менее токсичен;
е) глициновая. Ей подвергаются циклические карбоновые кислоты. например, образуются гликохолевая, гликодезоксихолевая кислоты, а также глициновый конъюгат бензойной кислоты - гиппуровая кислота;
ж) глутаминовая - очень редко.
Т.о., в ходе модификации и конъюгации вещество становится более гидрофильным и, как правило, менее токсичным, легче выводится из организма. некоторые лекарства способны индуцировать ферменты микросомального окисления и конъюгации, например, фенобарбитал, что, с одной стороны, снижает эффективность самого лекарства, т.к. оно быстрее инактивируется, а с другой стороны, повышает обезвреживающую способность печени, например, конъюгацию билирубина, что используют при желтухе новорожденных.
