
Хирургия / 103
.rtfХроническая ишемическая болезнь сердца
Атеросклеротическое поражение венечных артерий является прогрессирующим заболеванием. На ранней стадии развития липиды инкорпорируются в интиме, образуя атеросклеротические бляшки, окруженные фиброзной тканью. Это сопровождается постепенным сужением и уменьшением просвета коронарных артерий, а следовательно, и снижением кровоснабжения миокарда. В ряде случаев фиброзная ткань содержит отложения кальция. В более поздней стадии наступает разрыв ткани над бляшкой, изъязвление ее. Над поврежденной бляшкой образуется тромбоцитарный сгусток, дающий начало тромбу, дальнейшему уменьшению просвета артерий, инфаркту миокарда. По мере сужения венечных артерий наступает несоответствие между потребностью миокарда в кислороде и возможностями его доставки. В связи с этим возникают приступы стенокардии.
По статистическим данным, около одной трети населения умирает от атеросклеротического заболевания коронарных артерий. В начале ишемической болезни сердца преобладает спазм венечных артерий, сопровождающийся ишемическими болями при физической нагрузке (стенокардия напряжения) или в покое (стенокардия покоя). В последующем очень часто возникает инфаркт миокарда.
Атеросклеротическое поражение венечных артерий может быть ограниченным или диффузным. Обтурация их просвета приводит к очаговой ишемии миокарда, которая может быть обратимой или необратимой (инфаркт миокарда). Важнейшим симптомом ишемии являются загрудинные боли, стенокардия.
Клиническая картина и диагностика. Больных беспокоят приступы загрудинных болей, которые прекращаются после приема нитроглицерина; нарушение ритма, приступы сердцебиения. Клинические проявления весьма вариабельны. Согласно классификации Нью-Йоркской сердечной ассоциации (NYHA), тяжесть загрудинных болей и течения хронической ишемической болезни сердца подразделяют на четыре класса. I класс — отчетливых симптомов болезни нет; П класс — появление стенокардии после тяжелой физической нагрузки; III класс — появление стенокардии после легкой физической нагрузки; IV класс — стенокардия в покое. Пациенты, отнесенные к I—II классу, не испытывают тяжких приступов стенокардии, болезнь не мешает им вести нормальный образ жизни (стабильная стенокардия). В случае нарастания класса болезни в течение короткого периода времени имеется основание говорить о прогрессирующей стенокардии, которая существенно ухудшает прогноз. В поздней стадии ишемия возникает в покое и становится рефрактерной к применяемому медикаментозному лечению (нестабильная стенокардия). Прогноз при этой стадии болезни существенно ухудшается, возникает опасность инфаркта или внезапной смерти. У значительной части больных болезнь развивается не по приведенным классам, а может сразу проявиться инфарктом или внезапной смертью. Иногда наблюдается бессимптомная ишемия миокарда, тогда болезнь распознается только в поздней стадии.
Важную информацию дает электрокардиограмма, полученная в покое и при дозированной физической нагрузке на велоэргометре. Анализ электрокардиограммы позволяет определить выраженность и локализацию (очаги) ишемии миокарда, степень нарушения проводимости, характер аритмии.
Большое значение имеет цветное ультразвуковое допплерографическое и эхокардиографическое исследование. Оно позволяет определить изменения сократительной способности миокарда. По характеру движений стенок желудочков сердца можно выявить очаг и распространенность ишемии миокарда по зонам гипокинезии, акинезии или дискинезии в зоне, снабжаемой суженной ветвью венечной артерии. Замедление скорости движения стенок желудочка при сокращении миокарда называют гипокинезией, отсутствие движения стенки желудочка — акинезией. При аневризме сердца в момент сокращения непораженного миокарда рубцово-измененный участок выпячивается (дискинезия). Эхокардиографическое исследование позволяет определить систолический, конечно-диастолический и остаточный объемы левого желудочка, фракции выброса, минутный объем и сердечный индекс и другие показатели гемодинамики. Наиболее точную информацию о состоянии коронарного кровообращения дает магнитно-резонасная томография.
Для уточнения степени и локализации сужения венечных артерий, состояния периферического и коллатерального кровообращения в сердечной мышце производят селективную коронарографию, в том числе кинорентгенографию. Это важно для определения локализации и протяженности сужения перед и во время операции.
Радионуклидные исследования позволяют уточнить обширность очага поражения миокарда по степени накопления нуклида в миокарде.
Прогрессирующее сегментарное сужение венечных артерий неизбежно приводит к инфаркту миокарда. Судьба больного зависит от обширности и локализации инфаркта, степени нарушения функции сердца и внутренних органов.
Лечение. Хирургическое лечение показано при стенозе главного ствола левой коронарной артерии на 75%, при стенозе 2—3 ветвей артерии и клинических проявлениях по III—IV классу NYHA, снижении фракции выброса левого желудочка менее 50%.
Неотложным показанием к операции реваскуляризации миокарда является нестабильная "предынфарктная ангина", не поддающаяся консервативному лечению, а также резко выраженный стеноз левой венечной артерии, стеноз проксимального участка передней межжелудочковой ветви левой венечной артерии, так как закупорка их сопровождается обширным инфарктом миокарда. При стабильной стенокардии, поддающейся медикаментозному лечению, операцию производят в плановом порядке. Результатом операции является восстановление коронарного кровообращения, у 80—90% больных после операции исчезают явления стенокардии, резко снижается опасность возникновения инфаркта миокарда.
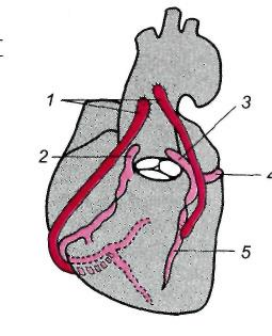
Рис. 17.6. Аортокоронарное шунтирование.
1 — аортокоронарное шунтирование веной; 2 — правая коронарная ар терия; 3 — левая коронарная артерия; 4 — огибающая ветвь (ramus cir cumflexus); 5 — межжелудочковая ветвь (ramus interventricularus).
Основным способом хирургического лечения атеросклеротических поражений венечных артерий является аортокоронарное шунтирование (bypass — байпас). Операция заключается в создании одного или нескольких анастомозов между восходящей аортой и венечной артерией и ее ветвями дистальнее места окклюзии (рис. 17.6). В качестве шунта используют участок вены голени (v. saphena magna). В 1964 г. В. И. Колесов впервые сделал анастомоз между внутренней грудной и коронарной артерией ниже ее сужения (коронарно-маммарный анастомоз). Эта операция при определенных показаниях производится в ряде учреждений. В настоящее время мобилизованные участки артерий (a. thoracica in-terna, a. epigastrica и др.) нередко используются для ангиопластики. По ряду показателей ангиопластика с применением артерии превосходит аортокоронарное шунтирование с применением сегмента вены. Предпосылками для успешной реваскуляризации миокарда являются: 1) стеноз венечных артерий (50% и более) при хорошей проходимости их периферических отделов; 2) достаточный диаметр (не менее 1 мм) периферического участка венечных артерий; 3) сохранение сократительной способности миокарда ("живой" миокард) листальнее стеноза артерий.
В последние годы с развитием эндоваскулярной рентгенохирургии для лечения сужений венечных сосудов стали применять их дилатацию с помощью специальных зондов с баллонами, которые вводят в просвет артерии. Наполняя баллон контрастным веществом, добиваются растяжения суженного сегмента просвета артерии и восстановления ее проходимости. Достигнутый при дилатации успех можно закрепить установкой стента.
Выбор метода операции зависит от характера поражения коронарных артерий и состояния пациента по NYHA классу. Делаются попытки разрушения атеросклеротической бляшки лучом лазера. При развитии у больного предынфарктного состояния вследствие тромбоза суженной венечной артерии для обнаружения локализации тромба выполняют экстренную коронарографию. Затем в венечную артерию к месту ее закупорки вводят через катетер стрептокиназу. Таким путем добиваются реканализации венечной артерии, уменьшения зоны ишемии. Впоследствии выполняют аортокоронарное шунтирование в плановом порядке.
17.8. Постинфарктная аневризма сердца
Аневризма в большинстве случаев развивается после обширного транс-мурального инфаркта миокарда, сопровождающегося некрозом мышечной ткани и замещением ее рубцовой. Редко причиной аневризмы может быть врожденный дефект развития или травма. Различают также ложные аневризмы, возникающие после ранее перенесенных операций или бактериального эндокардита. Аневризма сердца развивается у 10—15% больных, перенесших инфаркт миокарда, в большинстве случаев в первые 6 мес, а иногда уже через несколько недель. Остается неизвестным, почему у одних пациентов постинфарктная аневризма развивается, а у других нет. Аневризмы преимущественно локализуются в верхушке левого желудочка (85%) или на передней его стенке (15%), возникают на месте рубцовой ткани, разросшейся в зоне бывшего некроза миокарда. В этих случаях в функциональном отношении левый желудочек как бы состоит из сокращающегося и аневриз-матического (несокращающегося) сегментов. Между ними располагаются "ворота" аневризмы. Во время систолы кровь из сокращающегося сегмента желудочка поступает в восходящую аорту и частично в аневризматический мешок (парадоксальный кровоток). В связи с этим фракция выброса и минутный объем сердца снижаются, что может привести к недостаточности кровообращения. В аневризматическом мешке нередко находятся пристеночные тромбы. Отрыв кусочков тромба (эмболы) вызывает тромбоэмболи-ческие осложнения. В раннем периоде формирования аневризмы, когда некротизированный участок миокарда еще не замещен плотной соединительной тканью, возможны разрыв стенки аневризмы и тампонада сердца излившейся в полость перикарда кровью.
Клиническая картина и диагностика. Больных беспокоят боли в области сердца, загрудинные боли, одышка, перебои. В анамнезе у ряда больных имеются данные о перенесенном инфаркте миокарда и длительно существующей коронарной недостаточности.
При осмотре и пальпации иногда определяют прекордиальную парадоксальную пульсацию в четвертом межреберье слева от грудины, отдельно от верхушечного толчка; нередко выслушивают систолический шум, связанный с изменениями папиллярной мышцы, пролабированием створки левого предсердно-желудочкового клапана в левое предсердие и возникновением недостаточности самого клапана. На электрокардиограмме выявляют характерные признаки аневризмы сердца: комплекс QS или QR, стойкий подъем интервала S— Т и отрицательный зубец Г в грудных отведениях. При рентгенологическом исследовании отмечают изменение конфигурации тени сердца за счет мешковидного выпячивания.
При эхокардиографии четко определяется локализация аневризмы, ее размеры, наличие тромботических масс в полости аневризмы. Это исследование позволяет определить изменения гемодинамических показателей — фракцию выброса, конечно-систолический и конечно-диастолический объем левого желудочка, другие показатели гемодинамики.
Селективная коронарография позволяет уточнить локализацию стеноза или окклюзии венечной артерии, оценить изменения сосудистого русла дистальнее места окклюзии. Левосторонняя вентрикулография дает возможность точно установить величину аневризмы, локализацию, изменения миокарда вследствие патологического процесса, оценить в целом сократительную способность оставшейся части миокарда левого желудочка.
В течение первых 2—3 лет после образования аневризмы при естественном течении болезни больные умирают. Наиболее часто причинами смерти являются повторный инфаркт миокарда, эмболия различных артерий и сердечная недостаточность. Показаниями к операции являются опасность разрыва или прикрытая перфорация аневризмы, рецидивирующие тромбоэмболии и желудочковая тахикардия.
Лечение. Операция заключается в иссечении стенки аневризм, удалении пристеночных тромбов, ушивании образовавшегося дефекта. При стенозирующем процессе в венечных артериях одномоментно выполняют аортоко-ронарное шунтирование. При инфаркте, захватывающем папиллярную мышцу, с развитием недостаточности левого предсердно-желудочкового клапана показано протезирование клапана.
