
органика для медиков
.pdf
К алкилсерному эфиру добавляется второй моль этанола и поднимают температуру до 140°С. К этилсерному эфиру можно добавить другой спирт и получить смешанный эфир.
CH3CH2-O-SO3H CH3OH CH3CH2-OCH3 + H2SO4
Кроме концентрированной серной кислоты в качестве водоотнимающего агента используют Al2O3 при 300°С.
IV. Внутримолекулярная дегидратация
В результате внутримолекулярной дегидратации из спиртов образуются алкены.
Из первичных спиртов - под действием к.H2SO4/ 180°; Al2O3/375°.
Из вторичных спиртов - под действием H3PO4/ t°, KHSO4/ t°; Al2O3/350°;
ThO2/300°.
Из третичных спиртов под действием р.H2SO4/ t°; KHSO4/ t°; ZnO/t°.
Пример реакции
|
β |
α |
|
H2SO4k |
CH3CH=CH2 |
+ H2O |
|
|
|
|
|
|
|
|
||||||||||
CH3CH2-CH2-O-H |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
1800C |
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
пропен |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Механизм Е1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
HOSO3H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
CH3CH2-CH2-O-H |
CH |
CH |
CH |
-O-SO |
H |
|
|
|
|
CH3- |
CH-CH2 |
|
CH3CH=CH2 |
||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|||||||||||||||||||||
|
|
|
|
-H2O |
|
3 |
2 |
2 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
-OSO3H |
|
|
|
|
|
|
-H |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Все типы спиртов дегидратируются по механизму Е1. Реализация мономолекулярного механизма отщепления для первичных спиртов связана с высокой температурой реакции и нестабильностью промежуточного сложного эфира.
|
|
CH3 |
|
|
|
|
|
|
|
β |
|
α |
OH |
15% H2SO4 |
CH3-C=CH2 |
|
E1 |
||
|
CH2-C |
|
+ H2O |
||||||
|
|
|
t0 |
|
|||||
|
|||||||||
|
|
|
|
|
|
|
|
||
H CH3 |
|
|
|
CH3 |
|
|
|||
|
|
|
|
|
|
|
2-метилпропен, |
|
|
|
|
|
|
|
|
|
изобутен |
|
|
Реакция согласуется с правилом Зайцева. Первичные спирты дегидратируются в наиболее жестких условиях.
92

V. Окисление и дегидрирование спиртов
При окислении и дегидрировании первичных и вторичных спиртов образуются альдегиды и кетоны соответственно. Третичные спирты окисляются с расщеплением углерод-углеродных связей, дегидрированию не подвергаются.
Окисление |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
Окислители для первичных |
|
|
и вторичных |
спиртов: |
K2Cr2O7/H2SO4; |
|||||||||||||||||||||||||||||||
Na2Cr2O7/H2SO4; CrO3/CH3COOH; KMnO4/OH− при нагревании. При |
|||||||||||||||||||||||||||||||||||||
использовании KMnO4/OH− |
из первичных спиртов образуются альдегиды, |
||||||||||||||||||||||||||||||||||||
которые окисляются до карбоновых кислот. |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
Примеры реакций |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
O |
|||||||
|
|
|
|
|
|
|
|
|
[O] |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
CH CH -CH-O-H |
|
|
|
|
|
|
|
|
|
|
|
[CH -CH |
- |
CH-O- H] |
|
|
|
|
|
CH CH C |
H |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
3 |
2 α |
K2Cr2O7/H+,t0 |
3 |
2 |
|
|
|
|
|
|
|
|
-H2O |
3 |
2 |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
геминальный |
|
пропаналь |
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
диол (неустойчивый) |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
CH |
CH -CH -O-H |
|
|
[O] |
|
|
CH3CH2C |
O |
|
|
|
|
|
|
|
CH CH C |
O |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
3 |
2 |
|
2 |
|
KMnO4/OH |
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
3 |
2 |
OH |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пропановая |
||||||||||||
|
|
|
|
|
|
|
|
|
|
t0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислота |
|
||||||||
OH |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
H |
[O] |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
CH3-C |
|
|
|
|
|
|
|
|
|
|
CH3-C-O H |
|
|
|
|
|
|
|
|
|
CH3- |
C |
-CH3 |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
KMnO4/OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-H O |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
t0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
O |
|
ацетон |
|
|
|||||||||||
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Третичные спирты окисляются K2Cr2O7/H2SO4; Na2Cr2O7/H2SO4 при нагревании до смеси карбоновых кислот и кетонов через образование алкенов. С помощью этой реакции можно установить строение третичного спирта.
Пример и схема реакции
|
CH3 |
|
|
|
|
|
CH3 |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
β α β' |
K2Cr2O7/H+,t0 |
|
CH2=C-CH2-CH3 + CH3-C=CH-CH3 |
|
|
||||||||
|
|
|
|||||||||||
CH3-C-CH2-CH3 |
|
|
|
|
|
|
|||||||
|
-H2O |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
2-метилбутанол-2 |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
CO2 |
+ CH3-C-CH2-CH3 + |
CH3-C-CH3 |
+ CH3COOH |
||||||||
|
|
||||||||||||
|
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
|
|
бутанон |
|
|
|
пропанон, |
этановая, |
||||
|
|
|
|
|
|
|
|
|
ацетон |
уксусная кислота |
|||
93

Многоатомные спирты
Атόмность – количество гидроксильных групп в спирте. Диолы (гликоли) содержат две гидроксильных группы.
|
CH2- |
CH2 |
CH3- |
CH- |
CH-CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
OH OH |
|
OH OH |
||
этандиол |
бутандиол-2,3 |
||||
этиленгликоль (тривиальное) |
эритрит (тривиальное) |
||||
Поскольку в эритрите два асимметрических атома углерода С , то возможно существование четырех оптических изомеров, т.е. двух пар энантиомеров. По взаимному расположению гидроксильных групп (или галогенов, аминогрупп) относительно вертикали различают две конфигурации. В трео-конфигурации заместители (одинаковые или разные) находятся по разные стороны вертикали (в данном случае ОН-группы). В эритроконфигурации заместители находятся по одну сторону вертикали.
Для эритрита описывается пара энантиомеров в трео-конфигурации и, так называемая, оптически неактивная мезо-форма. Отсутствие пары энантиомеров эритро-конфигурации связано с наличием оси симметрии в этом стереоизомере. Симметричность строения стереоизомера приводит к исчезновению оптической активности, для эритрита имеется набор из трех:
|
|
|
CH3 |
|
|
|
|
|
|
CH3 |
|
HO |
|
|
|
|
H |
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||
H |
|
|
|
OH |
|
OH |
|
|
|
H |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
CH3 |
|||
2(R), 3(R) бутандиол-2,3 2(S), 3(S) бутандиол-2,3
пара энантиомеров трео-конфигурация
CH3
H OH
H OH
CH3
2(R), 3(S) бутандиол-2,3
мезо-форма (оптически неактивна) эритро -конфигурация
Если диол несимметричен, то он описывается полным набором стереоизомеров.
1 2 3 4 5 |
2n = 4 изомера |
||
CH3- |
CH- |
CH-CH2-CH3 |
|
|
|
|
|
|
|
|
|
|
OH OH |
|
|
94

|
1 |
CH3 |
|
|
|
|
|
CH3 |
|
|
|
CH3 |
|
|
|
|
|
CH3 |
|
|
|||
HO |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
H |
|
H |
|
|
|
OH |
H |
|
|
|
|
OH |
|
HO |
|
|
H |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
H |
|
OH |
|
OH |
|
|
|
|
H |
H |
|
|
|
OH |
|
HO |
|
|
|
H |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
4 |
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
CH2CH3 |
|
|
|
|
CH2CH3 |
|
|
|
CH CH |
|
|
|
CH |
CH |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
2 |
3 |
|
|
|
2 |
|
3 |
||||
2(R),3(R) пентандиол-2,3 |
|
2(S), 3(S) пентандиол-2,3 |
2(S), 3(R)пентандиол-2,3 |
|
2(R),3(S)пентандиол-2,3 |
||||||||||||||||||
|
|
|
трео-конфигурация |
|
|
|
|
|
|
|
|
эритро -конфигурация |
|
||||||||||
Триолы (глицериновые)
CH |
2 |
|
|
CH |
CH2 |
пропантриол-1,2,3 |
|
||||||
|
|
|
|
|||
|
|
|
|
|
|
гдицерин |
|
OH |
|
OH |
OH |
|
|
Методы получения
Для диолов
1.Гидроксилирование алкенов (см. тему “Алкены”).
2.Гидролиз оксидов алкенов.
|
|
|
CH2-CH2 |
|
H3O |
|
|
CH2-CH2 |
этандиол-1,2 |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
O |
|
|
|
|
|
|
|
этиленгликоль |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
OH OH |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Получение глицерина |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
Cl2 |
|
|
|
|
HOH |
|
|
Cl |
+ H |
O |
||||
|
CH -CH=CH |
2 |
|
|
|
|
CH2-CH=CH2 |
|
|
|
|
CH2-CH=CH2 |
2 |
2 |
|
||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
3 |
|
|
4000C |
|
|
|
|
CaCO3 |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
-HCl |
Cl |
|
-HCl |
OH |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
3-хлорпропен, |
3-пропенол, |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
хлористый аллил |
аллиловыйспирт |
|
|
|||||||||
|
|
|
CH -CH-CH |
|
|
CH2-CH-CH2 |
HOH |
CH |
-CH-CH |
||||||||||||
|
|
|
|
2 |
2 |
|
+ |
|
|
|
|
|
|
|
|
2 |
|
|
2 |
||
|
|
|
|
|
|
|
|
|
|
OH Cl OH |
-HCl |
|
|
||||||||
|
|
|
OH OH Cl |
|
|
OH OH OH |
|||||||||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
1-хлорпропандиол-2,3 2-хлорпропандиол-1,3 |
|
пропантриол-1,2,3, |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
глицерин |
|
||
95

Реакционная способность
1. Слабые ОН-кислоты, но более сильные, чем одноатомные спирты (сказывается бόльшее количество гидроксильных групп и их взаимное влияние друг на друга).
рКа |
этиленгликоля |
14,18 |
рКа |
глицерина |
13,99 |
рКа |
метанола |
16,0 |
Гликоли и глицерины образуют алкоголяты, аналогично одноатомным спиртам. Отличительным свойством многоатόмных спиртов является образование соединений типа хелатов (от греч. сhélé - клешня) с ионами тяжелых металлов. С Cu(ОН)2 образуется раствор синего цвета (качественная реакция).
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
||||
|
|
|
|
|
|
H2C |
|
O |
|
|
|
|
|
|
CH2 |
|||||||||
H C |
|
OH |
|
|
|
|
O |
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|||||||||||||||||||||
2 |
|
|
|
|
|
|
Cu(OH)2 |
|
|
|
|
|
|
Cu |
|
|
|
|
|
|
|
|
||
2 HC |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
HC |
|
|
|
|
|
O |
O |
|
|
|
CH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH H |
HO |
|
|
|
|
|
||||
H C |
|
|
OH |
|
|
|
H2C |
|
|
CH2 |
||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
||||||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
глицерат меди |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
2. Образование сложных эфиров
Реакция протекает с избытком реагентов.
H2C |
|
OH |
3 HO-NO2 |
|
H2C |
|
|
ONO2 |
+ 3H2O |
||||||||||||
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ONO2 |
||||||
HC |
|
|
|
|
OH |
|
HC |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
H SO |
4 |
k.,t0C |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
||
H2C |
|
|
OH |
|
|
|
|
|
|
H2C |
|
ONO2 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
тринитрат глицерина, |
|||||||||
нитроглицерин
Образование сложных эфиров глицерина и высших карбоновых кислот будет описано в теме “Жиры и масла”.
3. Реакция с HCl, HBr
HO |
|
CH -CH |
2 |
|
OH |
HCl |
HO |
|
CH -CH |
2 |
|
Cl |
PCl5 |
|
Cl |
|
CH -CH |
2 |
|
Cl + POCl |
+ HCl |
2 |
|
|
|
|
2 |
|
|
|
|
|
2 |
3 |
|
||||||||
|
|
|
|
|
|
|
|
2-хлорэтанол |
|
1,2-дихлорэтан |
|
||||||||||
96

|
CH2- |
CH- |
CH2 |
2 HBr |
1 |
2 |
3 |
1 |
2 |
3 |
||||||
|
CH |
-CH-CH |
CH |
-CH-CH |
||||||||||||
|
|
|
|
|
|
2 |
|
|
|
2 |
|
2 |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH OH OH |
|
|
OH |
Br |
Br |
Br |
OH Br |
||||||||
|
|
|
|
2,3-дибромпропанол-1 |
1,3-дибромпропанол-2 |
|||||||||||
4. Дегидратация
|
|
|
|
ZnCl2 |
CH3-C |
O |
+ H2O |
|
HO |
|
CH2-CH2 |
OH |
H |
||||
|
t0C |
|
||||||
|
|
|
|
этаналь |
|
|||
|
|
|
|
|
|
|
|
|
|
CH2- |
CH- |
CH2 |
KHSO4 |
SO |
|
β α |
O |
|
|
или k. H |
4 |
|||||||
|
|
|
|
2 |
|
|
CH2=CH-C |
+ 2H2O |
|
|
|
|
|
t0C |
|
|
|
||
|
|
|
|
|
|
|
|
H |
|
OH OH OH |
|
|
|
пропеналь |
|||||
перегонка |
|
||||||||
|
|
|
|
|
акролеин (тривиальное) |
||||
|
|
|
|
|
|
|
|
||
α,β−непредельный альдегид
5. Окисление
а)
|
|
|
|
|
|
p. HNO3 |
O |
C-C |
O |
этандиаль, |
|||
|
|
|
|
|
|
|
|
|
H |
|
H |
глиоксаль |
|
|
|
|
|
|
|
|
|
|
|
|
|||
HO |
|
CH2-CH2 |
|
OH |
H2O2 |
|
|
O |
|
оксиэтаналь, |
|||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
H2C-C |
|
гликолевый альдегид |
||
|
|
|
|
|
|
Fe+3 |
|
||||||
|
|
|
|
|
|
|
|
H |
|
|
|||
|
|
|
|
|
|
|
|
|
HO |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
k. HNO3 |
O |
C-C |
O формилметановая кислота, |
||||
|
|
|
|
|
|
H |
OH |
глиоксиловая кислота |
|||||
|
|
|
|
|
|
|
|
|
|
|
|||
б) Периодатное окисление – применяется для установления строения полиолов с вицинальным расположением гидроксильных групп.
C C |
HIO4 |
C |
O + O C |
+ HIO3 |
|
OH  OH
OH
Примеры реакций
|
HIO4 |
O |
|
O |
|
CH3-CH2CH-CH-CH3 |
CH3-CH2-C |
+ CH3-C |
H + HIO3 |
||
|
|||||
|
|
H |
этаналь |
|
|
OH OH |
|
пропаналь |
|
97
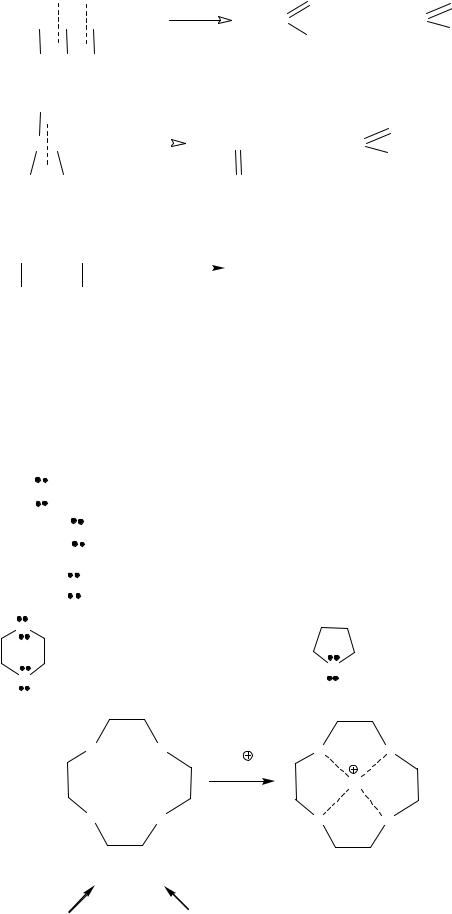
|
|
HIO4 |
|
O |
|
O |
|
|
CH |
-CH-CH-CH-CH |
H-C |
+ |
2 CH3-C |
+ HIO3 |
|||
H |
||||||||
|
||||||||
3 |
3 |
|
|
OH |
|
|
||
|
|
|
|
|
|
|
||
|
OH OH OH |
|
метановая кислота |
этановаякислота |
||||
|
CH3 |
|
|
|
|
|
|
|
|
||
CH -C-CH-CH |
HIO4 |
CH3-C-CH3 |
+ CH |
-C |
O |
+ HIO |
|||||
|
|
H |
|||||||||
3 |
3 |
|
|
|
|
3 |
|
3 |
|||
|
OH |
OH |
|
|
|
O |
этаналь |
|
|
||
|
|
|
|
|
|
пропанон |
|
|
|||
R- |
CH-CH2- |
CH-CH2-R HIO4 |
нет реакции |
|
|
|
|||||
|
OH |
|
OH |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||
ПРОСТЫЕ ЭФИРЫ
Соединения, в которых алкильные группы связаны через атом кислорода называются простыми эфирами.
Примеры соединений
CH3-O-CH3 |
|
метоксиметан, диметиловый эфир |
||||
CH -CH -O-CH -CH |
|
этоксиэтан, диэтиловый эфир , |
||||
3 2 |
2 |
3 |
серный эфир, медицинский эфир |
|||
CH3-CH2-O-CH3 |
|
метоксиэтан, метилэтиловый эфир |
||||
O |
|
|
|
4 |
|
3 |
|
диоксан |
|
|
5 |
O |
2 2,3,4,5-тетрагидрофуран (ТГФ) |
O |
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
циклические простые эфиры |
|
|
|||
|
|
|
|
|||
|
O |
O |
M |
O |
|
O |
|
|
|
|
|
M |
|
|
|
|
|
|
|
|
|
O |
O |
|
O |
|
O |
краун-эфир
12-краун-4
количество атомов |
количество атомов |
углерода и кислорода |
кислорода |
98

Краун-эфиры (от англ. crown - корона) образуют комплексы с солями щелочных металлов за счёт неподелённой пары электронов кислорода. Применяются в качестве катализаторов в ряде органических реакций. Связывая катион, краун-эфиры существенно увеличивают нуклеофильность реагента.
Пример реакции
н-C8H17Br + K |
|
|
|
|
|
|
18-краун-6 |
н-C8H17F + KBr |
|
|
|
|
F |
||||||
|
|
|
|
бензол |
|
||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
(растворитель) 92% |
||
SN2, Nu F 
Методы получения эфиров
1.Из первичных спиртов – под действием к.H2SO4/ 180°; Al2O3/300° (см. тему “Спирты”).
2.Алкоголиз третичных спиртов (см. тему “Спирты”).
3.Реакция Вильямсона
|
|
|
|
|
|
|
|
CH3CH2OH |
|
CH -CH |
2 |
-ONa |
+ CH |
-CH |
-Br |
(растворитель)CH3-CH2-O-CH2-CH3 + NaBr |
|||
3 |
|
3 |
2 |
|
SN2 |
этоксиэтан, |
|||
|
|
|
|
|
|
|
|
|
диэтиловый эфир |
|
|
|
|
|
|
|
|
|
|
|
|
|
SN2 |
CH3ONa/CH3OH (растворитель) |
|||||
|
|
|
CH3-CH2-O-CH3 |
|
|
||||
|
|
|
метоксиэтан, |
|
|
||||
|
|
метилэтиловый эфир |
|
|
|||||
CH |
3 |
|
|
|
(CH3)3COH |
CH3 |
|||
|
|
|
|
|
|||||
CH -C-ONa |
+ CH |
-I(растворитель)CH3-C-O-CH3 + NaBr |
|||||||
3 |
|
|
3 |
|
|
SN1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
2-метил-2-метоксипропан, |
|
|
|
|
|
|
|
|
|
метил-трет-бутиловый эфир |
|
4. Присоединение спиртов к алкенам |
|
||||||||
|
|
|
−δ +δ |
|
|
|
|||
+δ |
|
−δCH3O←Η |
|
|
|
||||
CH3→CH=CH2 |
|
|
|
CH3-CH-O-CH3 |
AdE |
||||
HBF4 |
|
||||||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
2-метоксипропан, |
|
|||
|
|
|
метилизопропиловый эфир |
||||||
99
Реакционная способность
Простые эфиры являются нуклеофилами и основаниями за счет НПЭ атома кислорода. Атомы водорода в α-положении простых эфиров являются подвижными за счёт смещения электронной плотности к атому кислорода.
|
|
|
|
|
|
|
|
|
α |
α/ |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
R-CH→O←CH2-R |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
1. Оснόвные свойства |
|
|
|
+δ |
−δ |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
BF3 |
|
|
|
HCl(газ) |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
Cl |
||||||||||||||||||
C2H5-O-C2H5 |
|
|
C2H5-O-C2H5 |
|
|
C2H5-O-C2H5 |
|||||||||||||||
|
|
|
|
||||||||||||||||||
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
BF3 |
|
|
|
|
|
H |
|
|
|
|||||||||||
эфират трехфтористого бора |
|
|
|
|
|
хлорид диэтилоксония |
|||||||||||||||
(устойчивое соединение,используется вкачестве донора BF3)
Аналогично идут реакции с другими минеральными кислотами и кислотами Льюиса.
2. Расщепление простых эфиров (с помощью k.HI и k.HBr)
|
HI |
|
a) CH3-O-CH3 |
|
CH3OH + HI |
|
||
|
t ° |
|
Механизм SN2
I - нуклеофил
|
|
|
+δ −δ |
|
|
H |
H |
|
a) |
CH3-O-CH3 |
H−I |
+δ |
I |
I.........C.......O-CH3 |
CH3I + CH3OH |
||
-I |
CH -O-CH |
3 |
||||||
|
|
|
3 |
H H |
|
|
||
|
субстрат |
|
|
H |
|
|
||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
хорошая уходящая |
|
|
|
|
|
|
|
|
группа |
|
|
|
|
|
+δ |
+δ/ |
|
HBr |
CH3Br + CH3CH2OH |
|
||
б) CH3→O←CH2←CH3 |
|
|
||||||
+δ >+δ/
100

В случае метилалкилэфиров всегда образуются бромистые и йодистые метилы. Атака нуклеофила идет на атом углерода, имеющий наибольший дефицит электронной плотности (в данном случае в метильной группе).
3. Реакции простых эфиров по связи Сα-Н
а) Окисление
Простые эфиры при стоянии на свету образуют взрывоопасные пероксиды.
α |
α/ |
O2 |
CH3-CH-O-CH-CH3 |
||
CH3-CH2-O←CH-CH3 |
|||||
hν |
|||||
|
|
|
OOH OOH |
||
|
|
|
|
||
|
H |
|
|||
|
|
|
|||
Механизм (SR)
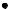 O-O
O-O  CH3-CH2-O−CH2-CH3 -OOH
CH3-CH2-O−CH2-CH3 -OOH
H
CH3-CH2-O−CH-CH3
O-O
O-O
CH3-CH2-O-CH-CH3
в этом свободном радикале наблюдается делокализация НПЭ и неспаренного электрона, за счет чего достигается его стабилизация
C2H5-O-C2H5 CH3-CH2-O-CH-CH3 + CH3-CH2-O−CH-CH3
O-OH
и т.д.
б) Хлорирование
Хлорирование происходит на свету по α-С-атому.
α |
Cl2 |
CH3- |
|
CH-O−CH2-CH3 |
|
||
CH3- |
CH→O←CH2-CH3 |
|
C |
|
SR |
||
hυ, 200 |
|
||||||
|
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
H |
|
|
Cl |
|
|||
|
|
|
|
1-хлор-1-этоксиэтан, |
|
||
α-хлордиэтиловый эфир
Эти производные простых эфиров легко вступают в реакции замещения и дегидрогалогенирования, их реакционная способность выше, чем у хлористого трет-бутила. Ниже приведены примеры реакций нуклеофильного замещения и элиминирования для 1-хлор-1-этоксиэтана.
101
