
- •Назначение стартерных акб
- •Устройство свинцо́во-кисло́тного аккумуля́тора
- •Основные типы аккумуля́торов
- •Основные технические характеристики аккумуляторов
- •Маркировка аккумуляторных батарей
- •Аккумуляторы российского производства
- •Акб европейского производства
- •Аккумуляторы американского производства
- •Батареи азиатского производства
- •Маркировка дата выпуска аккумуляторов у разных производителей
- •Практическая часть.
Федеральное агентство железнодорожного транспорта
Федеральное государственное бюджетное образовательное учреждение высшего образования
ПЕТЕРБУРГСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ПУТЕЙ СООБЩЕНИЯ ИМПЕРАТОРА АЛЕКСАНДРА I
Кафедра «Наземные транспортно-технологические комплексы»
Лабораторная работа № 15
«Аккумуляторные батареи»
дисциплина
«Конструкция и эксплуатационные свойства ТиТТМО»
Выполнил
Студент группы АСБ-016
Федотов Георгий
Санкт-Петербург
2021
Цель работы: Изучить аккумуляторные батареи транспортных средств.
Для этого необходимо решить следующие задачи:
1. Изучить общие теоретические сведения
2. Изучить основные типы АКБ
3. Изучить основные технические характеристики АКБ
4. Изучить маркировку АКБ
5. Написание выводов по работе
Общие теоретические сведения
Химическим источником тока называется устройство, в котором за счет протекания пространственно разделенных окислительно-восстановительных химических реакций их свободная энергия преобразуется в электрическую.
По характеру работы эти источники делятся на две группы:
● первичные химические источники тока или гальванические элементы;
● вторичные источники или электрические аккумуляторы.
Первичные источники допускают только однократное использование, так как вещества, образующиеся при их разряде, не могут быть превращены в исходные активные материалы. Полностью разряженный гальванический элемент, как правило, к дальнейшей работе непригоден — он является необратимым источником энергии.
Вторичные химические источники тока являются обратимыми источниками энергии — после как угодно глубокого разряда их работоспособность можно полностью восстановить путем заряда. Для этого через вторичный источник достаточно пропустить электрический ток в направлении, обратном тому, в котором он протекал при разряде. В процессе заряда образовавшиеся при разряде вещества, превратятся в первоначальные активные материалы. Так происходит многократное превращение свободной энергии химического источника тока в электрическую энергию (разряд аккумулятора) и обратное превращение электрической энергии в свободную энергию химического источника тока (заряд аккумулятора). Т. е. Электри́ческий аккумуля́тор относится как раз, ко вторичным химическим источникам тока.
Автомобильный аккумулятор (точнее — автомобильная аккумуляторная батарея [сокр. автомобильная АКБ]) — тип электрической аккумуляторной батареи, применяемый на автомобильном или мототранспорте. Используется в качестве вспомогательного источника электроэнергии в бортовой сети при неработающем двигателе и для запуска двигателя. Их также называют еще стартерными.
На электротранспорте является не вспомогательным источником энергии, а основным. Такие аккумуляторы принято называть тяговыми.
Назначение стартерных акб
Основная функция батареи — надежный пуск двигателя. Другая функция — энергетический буфер при работающем двигателе. Ведь наряду с традиционными видами потребителей, появилось множество дополнительных сервисных устройств, улучшающих комфорт водителя и безопасность движения. Батарея компенсирует дефицит энергии при движении по городскому циклу с частыми и длительными остановками, когда генератор не всегда может обеспечить отдачу мощности, необходимую для полного обеспечения всех включенных потребителей. Третья рабочая функция — энергоснабжение при выключенном двигателе. Однако длительное использование электроприборов во время стоянки с неработающим двигателем (или двигателем, работающем на холостом ходу), приводит к глубокому разряду батареи и резкому снижению ее стартерных характеристик.
Батарея предназначена еще и для аварийного электропитания. При отказе генератора, выпрямителя, регулятора напряжения или при обрыве ремня генератора она должна обеспечить работу всех потребителей, необходимых для безопасного движения до ближайшей СТО.
Итак, стартерные батареи должны удовлетворять следующим основным требованиям:
● обеспечивать нужный для работы стартера разрядный ток, то есть обладать малым внутренним сопротивлением для минимальных внутренних потерь напряжения внутри батареи;
● обеспечивать необходимое количество попыток пуска двигателя с установленной продолжительностью, то есть иметь необходимый запас энергии стартерного разряда; ● иметь достаточно большую мощность и энергию при минимально возможных размерах и массе;
● обладать запасом энергии для питания потребителей при неработающем двигателе или в аварийной ситуации (резервная емкость);
● сохранять необходимое для работы стартера напряжение при понижении температуры в заданных пределах (ток холодной прокрутки);
● сохранять в течение длительного времени работоспособность при повышенной (до 70 °С) температуре окружающей среды;
● принимать заряд для восстановления емкости, израсходованной на пуск двигателя и питание других потребителей, от генератора при работающем двигателе (прием заряда);
● не требовать специальной подготовки пользователей, обслуживания в процессе эксплуатации;
● иметь высокую механическую прочность, соответствующую условиям эксплуатации;
● сохранять указанные рабочие характеристики продолжительное время в процессе эксплуатации (срок службы);
● обладать незначительным саморазрядом;
● иметь невысокую стоимость.
Устройство свинцо́во-кисло́тного аккумуля́тора
Стандартный свинцо́во-кисло́тный аккумулятор – это шесть маленьких аккумуляторов, заключенных в один корпус. Шесть отсеков объединены в едином корпусе. Часто их называют банками. Каждая банка дает напряжение в 2,1В – 2,2В. Шесть банок соединены последовательно толстыми свинцовыми перемычками, что в итоге дает напряжение в 12,6В – 13,2В.
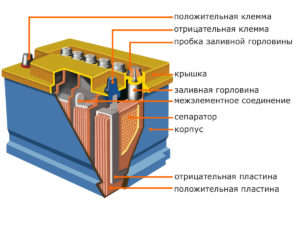
Рис.1. Свинцово-кислотный аккумулятор
Автомобильный аккумулятор состоит из следующих основных элементов:
пластиковый корпус;
крышка;
отрицательные пластины (электроды);
положительные пластины;
перемычки, соединяющие отсеки;
жидкий электролит;
сепараторы;
положительный и отрицательный вывод (клеммы);
заливные пробки.
Корпус и крышка выполнены из пластика, который нейтрален к кислоте. В каждой банке находятся свинцовые пластины – электроды.
Отрицательная пластина из губчатого свинца (Pb) называется катод, положительная пластина пористая с диоксидом свинца (PbO2) – анод. Чтобы батарея разряжалась не так быстро, используется не чистый свинец, а с применением разных присадок. Ранее добавляли 5% сурьмы, но процесс сульфатации все равно проходил быстро. В современных жидкостных аккумуляторах добавлен кальций. Он значительно снижает процесс сульфатации и повышает емкость АКБ до 70%. Если говорить про гелевые или AGM аккумуляторы, то в них применяется только чистый свинец. Это позволяет повысить мощность и отдаваемый пусковой ток до 1000-1300А.
В каждой банке залит электролит. Это смесь серной кислоты и дистиллированной воды, в соотношении 35:65. Плотность электролита находится в пределах 1,23-1,31 г/см3. Чем она выше, тем батарея более устойчива к морозам.
В простых жидкостных аккумуляторах между пластинами находится сепаратор. От слова “separate” – разделять. Обычно сепараторы изготавливаются из нейтрального пластика. Эти пластины разделяют положительные и отрицательные электроды от замыкания. Материалом для сепараторов служит ревертекс или эбонит. Также эти элементы иногда называют диэлектрической прослойкой.
В более современных необслуживаемых аккумуляторах в качестве сепараторов применяется микроволокно. Этот высокотехнологичный материал удерживает электролит внутри и не дает ему вытекать и испаряться. Пластины завернуты в микроволокно как в конверте и плотно прижаты друг к другу.
Клеммы аккумулятора также изготавливаются из свинца. К ним присоединяются контакты. На обслуживаемых аккумуляторах на корпусе располагаются заливные пробки. Их количество равно количеству банок. Они служат для заливки дистиллированной воды в случае необходимости.
Принцип работы
Между пластинами и электролитом непрерывно происходит электрохимическая реакция. При разряде химическая энергия преобразовывается в электрическую, а при заряде, наоборот, – электрическая в химическую. Когда аккумулятор подключен к потребителям энергии, то происходит его разрядка.
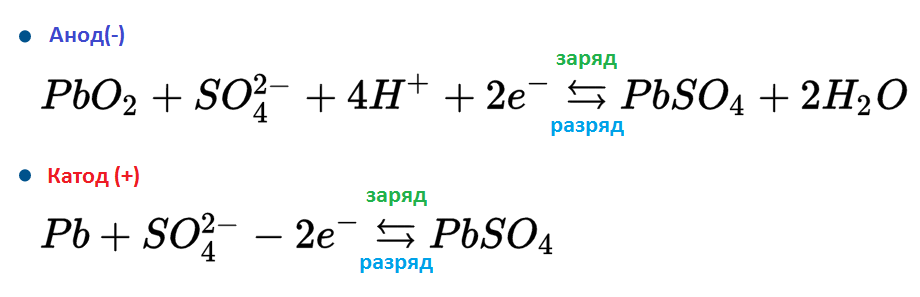
Рис. 2. Химическая формула реакции
Происходит следующий процесс. На катоде идет восстановление диоксида свинца. Свинец на аноде окисляется. Серная кислота вступает в реакцию с металлами на обеих пластинах. При этой реакции образуется сульфат свинца. Процесс называется сульфатацией. Из серной кислоты выделяется водород, который затем вступает в реакцию с кислородом из положительно заряженной пластины. Образуется вода, а серная кислота расходуется. Плотность электролита понижается. Процесс реакции показан на картинке.
При зарядке весь процесс происходит в обратном порядке. Серная кислота восстанавливается. Вновь образуется диоксид свинца и серная кислота. При полной зарядке плотность электролита должна быть в пределах 1,29 гр/см3. Это значение показывает уровень содержания серной кислоты на один кубический сантиметр электролита.
Таким образом, работа батареи основана на циклах заряд-разряд. Если допустить глубокий разряд, процесс может быть необратимым. Останется только вода и сульфат свинца. Поэтому нужно всегда следить за уровнем заряда.
