
- •1.Общие вопросы
- •1.Цикл Кребса, его биологическая роль
- •2.Метаболизм пвк в клетке.
- •3.Метаболизм Ацетил-Коа в клетке
- •2.Биохимия белков
- •4.Классификация белков. Характеристика важнейших представителей простых белков
- •5.Современное представление о биосинтезе белков и их регуляции.
- •6.Понятие о нативном и денатурированном белке. Виды денатурации, практическое использование
- •7.Физико-химические свойства белков.
- •8.Структура и функции сложных белков
- •9.Переваривание и всасывание белков в жкт. Судьба всосавшихся аминокислот
- •2.Механизм активации пепсина
- •1. Активация панкреатических ферментов
- •2. Специфичность действия протеаз
- •11. Синтез и биологическая роль креатинина
- •12. Окисление аминокислот в тканях. Прямое и непрямое дезаминирование
- •13. Аминокислоты как источники биологически активных веществ: гистамин, гамк, серотонин, адреналин
- •14.Гликолиз и его биологическая роль
- •17.Роль "ключевых" ферментов в углеводном обмене.
- •18. Регуляция концентрации глюкозы крови.
- •19.Пентозный путь окисления глюкозы и его биологическая роль.
- •20. Биохимические механизмы возникновения гипогликемий.
- •21.Глюконеогенез и его биологическая роль.
- •5. Фосфоенол пируват превращается в глюкозу
- •22. Синтез и распад гликогена.
- •23. Переваривание и всасывание углеводов в жкт.
- •28.Внутриклеточный липолиз.Окисление глицерина до co2 и h2o
- •29. Окисление жирных кислот в клетке.
- •30. Метаболизм кетоновых тел.
- •31) Перекисное окисление липидов (пол). Про- и антиоксидантные системы организма.
- •32) Уровни организации структуры ферментов. Мультиферментные системы.
- •33) Множественные формы ферментов. Изоферменты и их клинико-диагностическое значение.
- •34) Классификация и номенклатура ферментов. Единицы измерения ферментативной активности.
- •36) Регуляция активности ферментов.
- •37) Активаторы и ингибиторы ферментов.
- •39) Химическая природа и функциональные участки молекул ферментов.
- •40) Структура и биологическая роль днк и рнк.
- •41. Распад нуклеиновых кислот в тканях. Метаболизм мочевой кислоты.
- •42. Пути биосинтеза пуриновых и пиримидиновых оснований.
- •43. Современное представление о биологическом окислении. Типы биологического окисления.
- •44. Микросомальное окисление.
- •45.Окислительное фосфорилирование. Теория сопряжения. Влияние ядов на тканевое дыхание и окислительное фосфорилирование
- •46. Оксидазный путь биологического окисления. Субстраты, ферменты и коферменты биологического окисления.
- •47. Строение хромопртеинов .Важнейшие представители и их био. Роль.
- •49.Распад гемоглобина. Основные продукты распада, место их образования и пути выведения.
- •9. Биохимия витаминов.
- •51. Классификация витаминов, общие свойства .Суточная потребность и групповая характристика витаминов.
- •53. Строение, функции и биологическая роль витамина d в организме .Гипо-и гипервитаминоз.
- •54. Структура, функции и биологическая роль витамина к.Понятие об антивитаминах.
- •55. Витамины ,фолиевая кислота и никотиновая кислота, химическая природа , коферментные функции ,влияние на обмен веществ , пищевые источники.
- •56. Структура, коферментные функции и биологическая роль антидерматитных витаминов в6,н,пантотеновой кислоты.
- •Биохимия гормонов и биологически активных веществ
- •57.Роль посредников в гормональной регуляции обмена веществ.
- •1.Передача гормональных сигналов через мембранные рецепторы
- •2. Передача сигналов через внутриклеточные рецепторы
- •3.Передача сигналов через рецепторы, сопряжённые с ионными каналами
- •58.Гормоны гипоталамуса и гипофиза, их строение и механизм действия.
- •2. Кортиколиберин
- •3. Гонадолиберин
- •4. Соматолиберин
- •5.Соматостатин
- •1. Гормон роста, пролактин
- •2.Тиреотропин, лютеинизирующий гормон и фолликулостимулирующий гормон
- •3.Группа гормонов,образующихся из проопиомеланокортина
- •4. Гормоны задней доли гипофиза
- •59. Гормоны коркового вещества надпочечников.
- •1. Синтез и секреция катехоламинов
- •2. Механизм действия и биологическая роль катехоламинов
- •3. Патология мозгового вещества надпочечников
- •2. Биологические функции инсулина
- •3. Механизм действия инсулина
- •2. Передача сигналов через внутриклеточные рецепторы
- •1. Регуляция секреции фсг и лг
- •2. Механизм действия и эффекты фсг и лг
- •1. Синтез андрогенов
- •2. Регуляция синтеза и секреции андрогенов
- •3. Мишени для андрогенов
- •4. Эффекты андрогенов
- •1. Образование эстрогенов
- •2.Регуляция секреции эстрогенов
- •3.Механизм действия и биологические эффекты эстрогенов
- •4. Образование прогестерона
- •5. Биологические эффекты прогестерона
- •64. Современные представления о механизме действия гормонов белковой природы.
- •65.Метаболизм арахидоновой кислоты:простагландины,тромбоксаны,простациклины,лейкотриены.
- •66.Гормоны щитовидной железы и их влияние на обмен веществ.
- •1. Биосинтез йодтиронинов
- •2. Регуляция синтеза и секреции йодтиронинов
- •3. Механизм действия и биологические функции йодтиронинов
- •4. Заболевания щитовидной железы
- •67. Роль цикла трикарбоновых кислот во взаимосвязи обмена белков, липидов, углеводов.
- •69. Роль важнейших макроэргических соединений в обмене веществ.
- •70. Дыхательная функция крови. Основные типы гипоксий.
- •72. Нарушения кислотно-основного состояния и клинико-биохимические показатели кос.
- •73. Роль почек и легких в поддержании кислотно-основного равновесия.
- •74. Электролитный состав плазмы крови.
- •88. Обезвреживающая функция печень. Механизмы конъюгации.
- •89. Тесты лабораторной диагностики при заболеваниях печени
- •90.Белки соединительной ткани: строение,биологическая роль.Особенности метаболизма соединительной ткани.
- •91.Особенности состава и метаболизма нервной ткани.Роль медиаторов в возникновении и проведении нервных импульсов.
- •3.Синтез гормонов(эритропоэтин,кальцитриол)
- •95.Сосудисто-тромбоцитарный гемостаз,компоненты и их функции.
- •96.Плазменно-коагуляционный гемостаз .Компоненты и их функции.
- •97.Система антикоагулянтов. Основные эндогенные антикоагулянты и их функции.
- •98.Система фибринолиза .Компоненты и их функции в системе гемостаза
31) Перекисное окисление липидов (пол). Про- и антиоксидантные системы организма.
Реакции перекисного окисления липидов (ПОЛ) являются свободнорадикальными и постоянно происходят в организме. Свободнорадикальное окисление нарушает структуру многих молекул. В белках окисляются некоторые аминокислоты. В результате разрушается структура белков, между ними образуются ковалент-ные "сшивки", всё это активирует протеолитические ферменты в клетке, гидролизующие повреждённые белки. Активные формы кислорода легко нарушают и структуру ДНК. Неспецифическое связывание Fe2+ молекулой ДНК облегчает образование гидроксильных радикалов, которые разрушают структуру азотистых оснований. Но наиболее подвержены действию активных форм кислорода жирные кислоты, содержащие двойные связи, расположенные через СН2-группу. Именно от этой СН2-группы свободный радикал (инициатор окисления) легко отнимает электрон, превращая липид, содержащий эту кислоту, в свободный радикал.
ПОЛ - цепные реакции, обеспечивающие расширенное воспроизводство свободных радикалов, частиц, имеющих неспаренный электрон, которые инициируют дальнейшее распространение перекисного окисления.
Стадии перекисного окисления липидов:
1) Инициация: образование свободного радикала (L•)
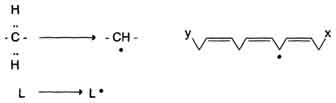
Инициирует реакцию чаще всего гидроксильный радикал, отнимающий водород от СН2-групп полиеновой кислоты, что приводит к образованию липидного радикала.
2) Развитие цепи:
L • + О2 → LOO • LOO• + LH → LOOM + LR•
Развитие цепи происходит при присоединении О2, в результате чего образуется липопе-роксирадикал LOO• или пероксид липида LOOH.
ПОЛ представляет собой свободнорадикальные цепные реакции, т.е. каждый образовавшийся радикал инициирует образование нескольких других.
3) Разрушение структуры липидов
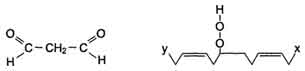
Конечные продукты перекисного окисления полиеновых кислот - малоновый диальдегид и гидропероксид кислоты.
4) Обрыв цепи - взаимодействие радикалов между собой:
LOO• + L• → LOOH + LH L• + vit E → LH + vit E• vit E• + L• → LH + vit Еокисл.
Развитие цепи может останавливаться при взаимодействии свободных радикалов между собой или при взаимодействии с различными антиоксидантами, например, витамином Е, который отдаёт электроны, превращаясь при этом в стабильную окисленную форму.
Ферменты антиоксидантного действия:
К ферментам, защищающим клетки от действия активных форм кислорода, относят супероксиддисмутазу, каталазу и глутатионпероксидазу; Наиболее активны эти ферменты в печени, надпочечниках и почках, где содержание митохондрий, цитохрома Р450 и пероксисом особенно велико. Супероксиддисмутаза (СОД) превращает супероксидные анионы в пероксид водорода:
2![]() +
2H+ →
H2O2 +
O2
+
2H+ →
H2O2 +
O2
Пероксид водорода, который может инициировать образование самой активной формы ОН•, разрушается ферментом каталазой:
2Н2О2 → 2 Н2О + О2.
Каталаза находится в основном в пероксисомах, где образуется наибольшее количество пероксида водорода, а также в лейкоцитах, где она защищает клетки от последствий «респираторного взрыва».
Глутатионпероксидаза - важнейший фермент, обеспечивающий инактивацию активных форм кислорода, так как он разрушает и пероксид водорода и гидропероксиды липидов. Он катализирует восстановление пероксидов с помощью трипептида глутатиона (γ-глутамилцистеинилглицин). Сульфгидрильная группа глутатиона (GSH) служит донором электронов и, окисляясь, образует дисульфидную форму глутатиона, в которой 2 молекулы глутатиона связаны через дисульфидную группу.
Н2О2 + 2 GSH → 2 Н2О + G-S-S-G.
Витамины, обладающие антиоксидантным действием: - Витамин Е отдаёт атом водорода свободному радикалу пероксида липида (ROO•), восстанавливая его до гидропероксида (ROOH) и таким образом останавливает развитие ПОЛ. - Витамин С (аскорбиновая кислота) также является антиоксидантом и участвует с помощью двух различных механизмов в ингибировании ПОЛ. - β-Каротин, предшественник витамина А, также обладает антиоксидантаьш действием и ингибирует ПОЛ.
