
Разное / обмен углеоводов
.pdf
Большая часть углеводов, поступивших с пищей, переносится по воротной вене в виде глюкозы в печень и мышцы, где из нее синтезируется гликоген.
Схема синтеза гликогена
глюкоза
АТФ
Е1 |
расход энергии |
АДФ
I этап
глюкозо–6–фосфат
Е2
II этап
глюкозо–1–фосфат |
|
|
|
Е3 |
УТФ |
АДФ |
|
РР пирофосфат |
|||
|
|
||
УДФ–глюкоза |
|
расход энергии |
|
|
Н3РО4 Н3РО4 |
|
Праймер гликогена [С6(Н2О)5] n |
Е4 |
АТФ
УДФ
гликоген [С6(Н2О)5] n+1
. |
(α–1,4– гликозидные связи) |
|
|
Удлинение и ветвление |
|
|
Е5 |
|
|
молекулы гликогена |
|
|
α–1,6– гликозидные связи |
|
|
|
Покажите на схеме место и механизм действия перечисленных ферментов:
–гексокиназы – Е1;
–фосфоглюкомутазы – Е2;
–гексозо–1–фосфат–уридилтрансферазы – Е3 (УДФ-глюкопирофосфорилаза);
–гликогенсинтазы – Е4;
–гликогенветвящего фермента – Е5.
Какие гормоны стимулируют (инсулин), а какие ингибируют (глюкагон, адреналин) синтез гликогена?
Молекула гликогена (содержит около 50000 остатков глюкозы) синтезируется наиболее быстро в печени, в наибольшем количестве в скелетных мышцах;
Биологическая роль этого процесса – депонирование глюкозы, как наиболее легко мобилизруемого депо энергии (в печени содержание гликогена может достигать 5% и в скелетных мышцах ≈1%). Общее содержание гликогена в организме человека может составить 450 г.
Гликоген мало растворим в воде и поэтому его накопление мало отражается на осматическом давлении в клетке.
11
Ветвление гликогена (≈ 10 остатков глюкозы в одной «ветке») позволяет многим молекулам энзимов прикрепляться к каждой «ветке» и осуществлять быстрее синтез (гликогенсинтетаза) или распад (фосфорилаза) гликогена
Мобилизация гликогена (гликогенолиз - фосфоролиз).
–Биологический смысл каскада химических реакций гликогенолиза (фосфоролиза).
(напоминает цепную реакцию, когда 1 молекула гормона способна активировать огромное количество молекул фосфорилаз), быстро мобилизировать гликоген и повысить в крови содержание глюкозы.
–Чем отличается мобилизация гликогена в печени и скеклетных мышцах?
–Наличие глюкозо–6–фосфатазы (Е2) в печени стимулирут образование глюкозы и выделение ее в кровь.
–Отсутствие глюкозо–6–фосфатазы (Е2) в мышцах – усиление гликолиза.
–Какие гормоны активируют (глюкагон, адреналин) и ингибируют (инсулин) распад гликогена, (инсулин-глюкогоновый индекс)?
–Чем отличается распад гликогена в желудочно–кишечном тракте от его распада в тканях (гидролиз–фосфоролиз)?
Регуляция активности гликогенсинтетазы и фосфорилазы осуществляется путем фосфорилирования и дефосфорилирования, при этом их активность изменяется прямо противоположным (+/-)образом (реципроктно).
Каскадный механизм реакций мобилизации гликогена
12

13

14

Гликолиз (схема)
Гликолиз — это последовательность ферментативных реакций, проходящих через стадию превращения глюкозы в пируват с образованием АТФ.
Аэробный гликолиз — при наличии в клетке кислорода.
Анаэробный гликолиз — при дефиците в клетке кислорода.
Гликогенолиз — это распад гликогена с образованием глюкозы и ее дальнейший катаболизм с образованием лактата, а при наличии кислорода СО2, Н2О и АТФ.
I э т а п
6 и 11 – реакции гликолитической оксидоредукции
?
?
?
стадия а
Субстратное
фосфорилирование
Субстратноебстадия фосфорилирование
2
15

16

Особенности I этапа катаболизма глюкозы и биологический смысл реакций стадии а и б
Объясните и покажите на схеме:
пусковые ферменты в печени (глюкокиназа) и в мышцах (гексокиназа)
их Кm и биологическое значение (см. ферменты)
образование глюкозо – 6 – фосфата как ловушки для глюкозы (выход глюкозо – 6 – фосфата из клетки через мембрану - невозможен)
—ключевые (регуляторные) ферменты дихотомического пути распада (Е3, Е10)
—расход АТФ: реакции 1, 3
—образование АТФ:
в анаэробных условиях реакции 7, 10 (реакции субстратного фосфорилирования)
в аэробных условиях реакции 7, 10 (реакции субстратного фосфорилирования) и окисление НАДН2 (из реакции 6) в цепи биологического окисления
—регуляция скорости I этапа путем изменения активности ферментов: Е2 (ФФК), Е10 (ПК)
активаторы ферментов - АМФ, АДФ
ингибиторы ферментов – АТФ, НАДН
—необратимые реакции стадии (а) – 1,3 и (б) – 10 гликолиза, назовите их ферменты
—сходство и различие в реакциях I этапа анаэробного и аэробного путей окисления глюкозы (варианты окисления НАДН2 образуемого в реакции 6):
в анаэробных условиях: реакции гликолитической оксидоредукции (Е6 и Е11).
|
|
|
|
|
|
|
ОН |
|
|
|
|
|
|
|
|
|
ОН |
|
|
|
|
|
|
|
Н3РО4 |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Н2С |
|
|
|
|
|||||
Н2С |
|
|
|
|
|
О Р = О |
|||||||||||
|
О Р = О |
|
Е6 |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
ОН |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ОН |
|
|
Н С |
|
ОН |
|||||
Н С |
|
ОН |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
О |
ОН |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
С |
|||||
|
|
С |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
О ~ Р = О |
||||
Н |
О |
|
НАД |
НАДН2 |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
ОН
2
НАД НАДН2
Е11 (ЛДГ) — фермент заключительной реакции анаэробного гликолиза
коферменты (НАД, НАДН2)
изоферменты ЛДГ (локализация в тканях, активность)
регуляция активности (ретроингибирование)
Биологическая роль анаэробного гликолиза и гликогенолиза (производство АТФ без участия О2; рассчитайте баланс энергии, используя реакции субстратного фосфорилирования).
17

в аэробных условиях: челночные механизмы транспорта протонов от НАДH2 в митохондрии в цепь биологического окисления, что приведет к синтез АТФ путем окислительного фосфорилирования:
Глицерофосфатный челночный механизм переноса и окисления цитозольного НАДН2 в митохондриальном матриксе скелетных мышцах и ткани мозга.
Цитозоль
глюкоза
гликолиз
|
митохондриальная |
|
Матрикс |
|||||
|
|
мембрана |
|
митохондрий |
||||
Глицерол-3-фосфат |
|
|
Глицерол-3-фосфат |
|||||
|
|
|||||||
НАД+ |
Цитоплазматическая |
|
|
|
Митохондриальная |
ФАД |
||
НАДН2 |
|
|
|
|
ФАДН2 |
|||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Цепь |
|
|
|
|
|
|
|
биологического |
||
|
|
|
|
|
|
окисления |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 АТФ |
|
|
|
|
|
|
|
|
|
|
Диоксиацетонфосфат  Диоксиацетонфосфат
Диоксиацетонфосфат
Обратите внимание:
1. В клетках каких органов действует глицеролфосфатный челночный механизм (в клетках скелетных мышц и мозга)?
2.Если функционирует глицеролфосфатный челночный механизм, то сколько молекул АТФ может образоваться при окислении цитозольной молекулы НАДH2 (2 молекулы АТФ, почему)?
18

Малатаспартатный- челночный механизм для переноса цитозольного НАДН2 в митохондриальный матрикс
(в клетках печени, почек и сердца)
|
Внутренняя |
Матрикс |
Цитозоль |
митохондриальная |
митохондрии |
|
мембрана |
|
гликолиз |
Малат |
|
Малат |
|
|||
Цитоплазматическая малатдегидрогеназа |
|
Митохондриальная малатдегидрогеназа |
глюкоза
НАД+ 
 НАД
НАД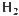
Оксалоацетат





 Оксалоацетат
Оксалоацетат
аспартат
COOH |
|
в цитоплазме |
|
COOH |
|
| |
|
| |
|||
|
НАД |
НАД |
|||
C = О |
|
|
H – C – H |
||
|
|
|
|
||
| |
|
|
|
| |
|
|
|
|
|||
|
|
|
|
|
|
H – C – H |
|
|
|
H – C – H |
|
| |
|
HАДН2 |
НАД |
| |
|
|
в митохондрии |
||||
COOH |
|
|
COOH |
||
|
|
|
|
||
НАД+
НАД
Цепь биологического окисления
3 АТФ
Обратите внимание:
-в клетках каких органов действует малат-аспартатная челночная система переноса водорода (миокард, почки)
-в какой форме оксалоацетат возвращается из митохондрии в цитозоль (аспартат)
-если функционирует малат – аспартатный челночный механизм, объясните почему 3 молекулы АТФ может образоваться при окислении НАДH.
—Эффект Пастера: подавление гликолиза дыханием (переключение анаэробного пути на
аэробный в присутствии О2)
19

20
