
3 курс / Фармакология / Нейротропные средства
.pdf
Побочные эффекты могут быть связаны с ганглиоблокирующим действием (гипотензия), освобождением гистамина (гипотензия и бронхоспазм), угнетением сердечного выброса (гипотензия), с блокированием М-холинорецепторов сердца - тахикардия, угнетением нейронального захвата катехоламинов - тахикардия и гипертензия, с угнетением ацетилхолинэстеразы может быть связано повышение активности секреторных желез.
Антагонисты миорелаксантов
Для безопасного применения миорелаксантов необходимы эффективные антагонисты. В настоящее время известны и широко используются только антагонисты недеполяризующих миорелаксантов.
Антагонисты недеполяризующих миорелаксантов представлены двумя группами:
1.Средства препятстствующие гидролизу эндогенного ацетилхолина - антихолинэстеразные средства: прозерин, галантамин, пиридостигмин, эдрофоний;
2.Средства, способствующие освобождению ацетилхолина из окончаний двигательных нервов: пимадин (4- аминопиридин).
Таким образом, принцип действия обеих групп антагонистов заключается в повышении концентрации медиатора ацетилхолина в синаптической щели, конкурирующего с миорелаксантами за холинорецептор, что и способствует восстановлению нервно-мышечной передачи.
Антагонистический эффект антихолинэстеразных средств зависит от адекватной работы пресинаптического механизма высвобождения ацетилхолина. Высвобождение ацетилхолина может тормозиться целым рядом факторов, включая высокое содержание внеклеточного Mg++ или низкий уровень внеклеточного Ca++, например, при действии некоторых антибиотиков (аминогликозидов, полимиксинов) или токсина A ботулизма.
Пимадин усиливает вызванное высвобождение ацетилхолина путем блокирования каналов для K+ в окончаниях двигательных нервов. Это приводит к открыванию каналов для Na+ и таким образом способствует поступлению Ca++ в нервные окончания, что облегчает Ca++-зависимое высвобождение ацетилхолина.
53

Глава
5
АДРЕНЕРГИЧЕСКИЙ СИНАПС
Передача возбуждения с постганглионарных нервных волокон симпатической нервной системы на эффекторные клетки осуществляется с помощью адреноподобных веществ - нордреналина и дофамина. Эти вещества являются медиаторами и во многих отделах ЦНС. Адреналин на периферии рассматривается, как гормон мозгового слоя надпочечников, а в ЦНС он может выступать и как истинный медиатор, наряду норадреналином и дофамином. В последнее время на роль медиатора в центральной нервной системе претендует еще одно веще-
ство - фенилэтиламин.
Поскольку все эти вещества - адреналин, норадреналин и дофамин относятся, относятся к производным пирокатехина или катехоламинам, синапсы, где они служат в качестве медиатора можно обозначить и как катехоламинергические.
Историческая справка
Изучение адренергических структур имеет достаточно длительную историю. Адреналин был впервые обнаружен в экстрактах надпочечников в
1895 г.
Позже обнаружилось, что надпочечники выделяют также и норадреналин. Оба вещества продуцируются хромаффинными клетками надпочечников. Основываясь на функциональном единстве симпатоадреналовой системы, что находит свое выражение в поразительном сходстве действия гормона адреналина с эффектом раздражения симпатических нервов, Elliott (1905)
высказал предположение об участии веществ, близких к адреналину, в реализации влияний симпатических нервов.
54
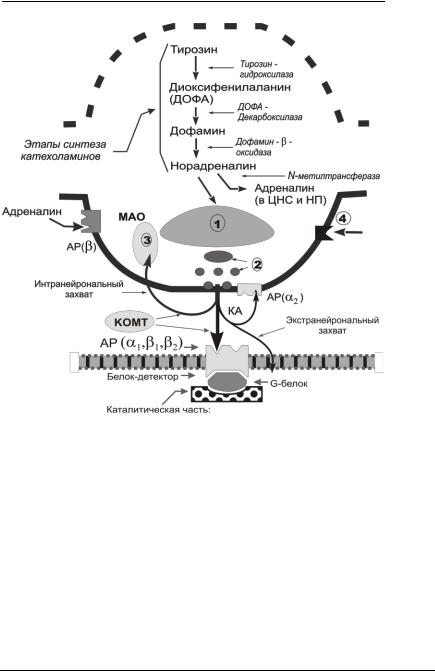
Рисунок 5. Схема строения адренегического синапса.
СтФ - стабильная фракция; ЛФ - лабильная фракция; СвФ - Свободная фракция; МАО - моноаминооксидаза; КОМТ - катехол-О-метилтрансфераза; КА - катехоламины (норадреналин); G - белок-коннектор
1 - обратный интранейрональный захват; 2 - экстранейрональный захват
В 1946 г. Von Euler обнаружил, что нейромедиатор, выделяющийся из адренергических терминалей является норадреналин, который, освобождаясь под действием приходящих нервных импульсов, возбуждает специфические адренорецепторы на мембране постсинаптической эффекторной клетки или постсинаптического нейрона.
55

Строение адренергического синапса.
Адренергический синапс (Рисунок 5), как и любой другой синапс, по существу является нейрохимической преобразующей системой, трансформирующей электрическую энергию нервного импульса в химические процессы, приводящие к возбуждению или торможению иннервируемой клетки.
Центральным процессом, обеспечивающим изменение функции иннервируемой клетки, является взаимодействие медиатора с участком постсинаптической мембрана, способной рецептировать медиатор адренергических нервов.
На периферии адренергические волока, подходя к эффектору, разветвляются на тонкую сеть волокон с варикозными расширениями, которые собственно и участвуют в образовании синаптических контактов с эффекторными клетками в качестве пресинаптических структур. Варикозные утолщения содержат везикула, в которых и находится медиатор. Анатомическое представление адренергического синапса в ЦНС более многообразно.
Синтез катехоламинов.
Предшественником катехоламинов является тирозин, а сам тирозин образуется в печени путем окисления фенилаланина при участии фермента фенилаланингидроксилазы.
Под влиянием растворимого фермента тирозиноксидазы (TO) из тирозина образуется диоксифенилаланин (ДОФА). Эта реакция является лимитирующим звеном в цепи синтеза медиатора, так как фермент тирозин-3-гидроксилаза может быть ингибирован одним из конечных продуктов: норадреналином, дофамином или адреналином.
Реакция декарбоксилирования ДОФА в дофамин происходит также в цитоплазме и, в данном случае, не лимитирует синтез нейромедиатора. Дофамина накапливается в везикулярных депо, где может гидроксилироваться в -положении ферментом дофамин- -гидроксилазой с образованием норадреналина, который также накапливается в везикулах (Рисунок 5.).
Вмозговом веществе надпочечников и в некоторых нейронах ЦНС осуществляется дополнительная стадия синтеза, катализируемая ферментом фенилэтаноламин-N-метилтрансферазой.
Врезультате N-метилирования образуется адреналин.
56
Однако в ЦНС имеются области, богатые фенилэтаноламин- N-метилтрансферазой, и в которых адреналин выполняет роль нейромедиатора. Некоторые из этих областей, например, гипоталамус и ядро одиночного пути, участвуют в регуляции артериального давления.
Скорость синтеза медиатора зависит как от общего уровня норадреналина, так и от его содержания в различных депо.
Депонирование.
Существенным звеном в функционировании катехоламинергического синапса является депонирование медиатора. Различают два (стабильный или лабильный) или три (резервный, лабильный и свободный) фонда или депо катехоламинов в терминалях:
1.Резервный (стабильный, прочно связанный в виде комплексного соединения с АТФ и специфическим белком хромгранином) локализуется в “крупных” гранулярных синаптических везикулах. Здесь сосредоточено основное количество медиатора в виде тройного комплекса амин-АТФ-белок (Рисунок 5. СтФ)
2.Лабильный (мобильный) фонд составляет около 1520% локализуется в малых гранулах и представляет собой активную форму медиатора, участвующую в проведении нервного импульса (Рисунок 5.ЛФ).
3.Свободный фонд, находящийся в цитоплазме (около 5% от общего количества), состоит в основном из обратно захваченного из синаптической щели норадреналина (Рисунок 5. СвФ)
Все три фонда находятся между собой в динамическом равновесном состоянии. Регуляция этого процесса происходит при участии ионов Mg++ и Ca++, Ca-Mg-зависимой АТФ-азы и фермента МАО. МАО локализуется в митохондриях нейронов и эффекторных клеток. В связи с этим, данный фермент принимает участие в инактиировании только внутриклеточных аминов.
Адренергические рецепторы.
Адренергические, или точнее катехоламинергические, рецепторы - это включенные в мембрану макромолекулы преимущественно белковой природы (протеолипиды или нуклеопротеиды), с генетически предопределенной структу-
57

рой активного центра, способные за счет функциональных групп последнего обратимо взаимодействовать с катехоламинами и их изостерами так, что возникает цепь энзимо- и электрохимических процессов, приводящих к изменению функции клетки (активация цАМФ, раскрытие ионного канала)
Ф а р м а к о л о г и ч е с к а я д и ф ф е р е н ц и а ц и я а д р е н е р г и - ч е с к и х р е ц е п т о р о в .
Dale (1906) первым пришел к заключению о существовании разных типов адренорецепторов. В последствии Ahlquist (1948, 1966) развил эту идею, выделив - и -адрено- рецепторы.
Адренорецепторы делят в настоящее время на две большие группы - и -рецепторы, возбуждение которых сопровождается различными физиологическими эффектами.
В свою очередь они делятся на 1- и 2-рецепторы и на 1- и 2-адренорецепторы. Такое деление основано как на неодинаковой чувствительности отдельных органов и тканей к различным фармакологическим агентам, оказывающим агонистическое или антагонистическое действие на адренорецепторы, так и на различиях в организации и функционировании различных типов и подтипов рецепторов, что установлено сравнительно недавно.
- и -адренорецепторы могут быть представлены как трансмембранная регуляторная и сигнальная система, пронизывающая бислойную липидную мембрану и состоящую, по крайней мере, из трех принципиальных компонентов: детек-
тирующего устройства рецептора, воспринимающего агонист, сопрягающей системы или белка-коннектора - G-белок,
осуществляющего процесс сопряжения активированного ре-
цептора с третьей субъединицей - каталитическим компонентом.
Адренорецептор, как и холинорецептор, имеет собственные активные центры, посредство которых он и реагирует с функ- ционально-активными группами катехоламинов. Анионный центр рецептора электростатически взаимодействует с катионной головкой NH-группы молекулы катехоламина. Гидроксильные группировки ароматического ядра катехоламинов образуют водородные связи с рецептором.
58

Некоторые типы адренорецепторов могут тормозить процессы гидролиза фосфатидилинозитола и связанные с этим события.
Эти и другие внутриклеточные процессы приводят к реализации соответствующего физиологического эффекта.
Таблица 2. Локализация и функции -адренорецепторов.
Типы |
|
|
|
ре- |
Локализация |
Результат активации |
|
цеп- |
|||
|
|
||
торов |
|
|
|
|
|
|
|
|
|
|
|
1 |
Гладкая мускулатура кр. сосудов |
Констрикция |
|
|
почек, кожи, сл. оболочек и мезен- |
|
|
|
териальных сосудов; предальвео- |
|
|
|
лярный жом, гл. муск. уретры, |
|
|
|
матки, волос. Фолликулы, сфинк- |
|
|
|
теры ЖКТ. |
|
|
|
|
|
|
1 |
Миокард |
Увел. сердечных со- |
|
|
|
кращений. |
|
|
|
|
|
1 |
Селезенка |
Сокр. капсулы |
|
|
|
|
|
1 |
Радиальная мышца глаза |
Сокращение |
|
|
|
|
|
1 |
Печень |
Увел. гликолиза |
|
|
|
|
|
1 |
ЦНС |
Повыш. локомоции |
|
|
|
|
|
2 |
Окончания адренергических воло- |
Снижение высво- |
|
|
кон |
бождения катехола- |
|
|
|
минов. |
|
|
|
|
|
2 |
Кровеносные сосуды (внесинапти- |
Сужение |
|
|
чески) |
|
|
|
|
|
|
2 |
Адренергические нейроны в ЦНС |
Успокоение, аналь- |
|
|
|
гезия, угнетение |
|
|
|
структур регуляции |
|
|
|
сосудистого тонуса |
|
|
|
|
|
2 |
Жировая ткань |
Угнетение липолиза |
|
|
|
|
|
2 |
Островки поджелудочной железы |
Снижение выделе- |
|
|
|
ния инсулина. |
|
|
|
|
59

-адренорецепторы
В настоящее время выделяют два основных типа - адроенорецепторов: 1- и 2- адренорецепторы, отличающиеся между собой как по локализации, так и по особенностям действия (Таблица 2).
Предполагается, что 1-АР связаны с системой фосфатидилинозитола, активируют процесс его гидролиза и образование активных вторичных мессенджеров: инозитола трифосфата и диацилглицерина. В результате этого происходит открытие рецепторных Са++ каналов и повышение концентрации кальция внутри клетки.
2-АР, наоборот тормозят системы фосфатидилинозитола и аденилатциклазы и тормозят процессы активации внутриклеточного метаболизма, связанные с этими системами.
-адренорецепторы
-адренорецпторы, как и -, не являются гомогенной популяцией. Деление на 1- и 2-адренорецепторы первоначально было осуществлено на основании фармакологического анализа и применительно к периферическим структурам. В дальнейшем были сделаны успешные попытки идентификации подтипов -рецепторов в структурах мозга (Таблица 3).
Установлено строение и различия основных подтипов - рецепторов. 2-АР представляется как димер, состоящий из двух идентичных субъединиц, каждая из которых содержит, содержит место связывания для лиганда (медиатора). 1-АР - мономер, весьма сходен с одной субъединицей 2 АР. Высказана гипотеза, что нейротрансмитерный белок-детектор развивается из одного общего предшественника и 2 рецепторы образовались из 1 посредством дупликации генов.
Оба типа -адренорецепторов сопряжены с системой аденилатциклазы. Однако в зависимости от сущности белкаконнектора может наблюдаться активация АД-циклазы (белок
-Gs) или торможение и угнетение образования цАМФ (белок
-Gi)
Количественное соотношение в тканях и органах - и - рецепторов различно. Наглядным примером этого служит эксперимент по извращению гипертензивного эффекта адреналина на фоне адреноблокаторов.
60

Таблица 3. Локализация и функции -адренорецепторов.
Типы |
Локализация |
Результат активации |
|
|
|
|
|
|
1 |
Синусовый узел |
Повышение возбудимо- |
|
|
сти, учащение сокра- |
|
|
щений сердца. |
|
|
|
1 |
Миокард |
Увеличение силы сер- |
|
|
дечных сокращений. |
|
|
|
1 |
Атриовентрикулярный узел |
Увеличение проводи- |
|
|
мости. |
|
|
|
1 |
Пучок и ножки Гисса |
Увеличение автоматиз- |
|
|
ма |
|
|
|
1 |
Печень и скелетные мышцы |
Увеличение гликогенеза |
|
|
|
2 |
Окончания адренергических |
Увеличение высвобож- |
|
волокон (пресинаптические ре- |
дения катехоламинов. |
|
цепторы) |
|
|
|
|
2 |
Окончания холинергических |
Увеличение высвобож- |
|
волокон (пресинаптические ре- |
дения ацетилхолина. |
|
цепторы) |
|
|
|
|
2 |
Миометрий |
Снижение сократитель- |
|
|
ной активности |
|
|
|
2 |
Артериолы скелетных мышц, |
Релаксация |
|
гл. мускулатура бронхов, ЖКТ. |
|
|
|
|
2 |
Иммунокомтентные клетки |
Торможение медиато- |
|
|
ров аллергии |
|
|
|
2 |
Островки поджелудочной же- |
Ув. выделения инсули- |
|
лезы |
на. |
|
|
|
1,2 |
Жировая ткань |
Усиление липолиза |
|
|
|
|
Юкста-гломерулярный ком- |
Ув. освобождения ре- |
|
плекс |
нина |
|
|
|
61

Выделение медиатора и роль пресинаптич е- ских рецепторов.
В основе физиологического механизма выделения катехоламинов в ответ на поступление нервного импульса является кальцийзависимый экзоцитоз.
Под влиянием поступающих по аксону нервных импульсов происходит деполяризация пресинаптических мембран и изменение прохождения через них ионов.
Увеличивается поступление ионов Ca++ из экстрацеллюлярного пространства внутрь терминалей, что способствует продвижению синаптических пузырьков по направлению к синаптической щели и выброс квантов медиатора.
Повышение в среде ионов Ca++ усиливает эффект выделения медиатора. При этом ионы Ca++ играют роль фактора, ускоряющего расщепление комплекса амин-АТФ-белок и стимулирует сокращение микрофиламентов. В результате этого содержимое везикул извергается в синаптическую щель.
Выброс медиатора может происходить также под влиянием симпатомиметических аминов, таких как тирамин. В этом случае освобождение происходит путем вытеснения медиатора из везикулярных депо без экзоцитоза. Этот процесс не является кальцийзависимым.
Пресинаптические рецепторы.
Langer et al. в 1971 году впервые показали существование пресинаптических тормозных -адренорецепторов на норадренергических нервных терминалях и указали на их модулирующую роль в освобождении норадреналина.
Эти пресинаптические -адренорецепторы (Рисунок 5. ) регулируют освобождение норадреналина посредством включения механизма отрицательной обратной связи при участии самого медиатора. Следовательно, как только норадреналин, освобождаемый при нервном возбуждении, достигает некой пороговой концентрации в синаптической щели, он активирует пресинаптические -адренорецепторы, запускающие механизм обратной связи, ингибирующей дальнейшее выделение нейромедиатора. Это происходит за счет торможения кальциевого механизма высвобождения медиатора.
62
