
3 курс / Фармакология / Alyautdin_Farmakologia_bolshaya_sinyaya_kniga
.pdfГлава 27. Средства, влияющие на гемостаз и тромбообразование |
563 |
лебранда (адгезия тромбоцитов). Это вывызывает активацию тромбоцитов (рис. 27.1). В результате сами тромбоциты становятся источниками биологически активных веществ, стимулирующих агрегацию, таких как тромбоксан A2, АДФ, серотонин, которые высвобождаются в кровоток. Тромбин, который образуется локально в процессе свертывания крови, также индуцирует агрегацию тромбоцитов. Кроме того, индукторами агрегации являются катехоламины, фактор активации тромбоцитов и некоторые другие эндогенные вещества.
Агрегации тромбоцитов препятствуют простациклин и эндотелиальный релаксирующий фактор, которые образуются клетками эндотелия сосудов и высвобождаются в кровоток. При повреждении эндотелиальных клеток синтез этих веществ снижается, и на таком фоне доминирует действие веществ, стимулирующих агрегацию. В результате тромбоциты объединяются в агрегаты, из которых формируется тромбоцитарный тромб.
Тромбоцитарный тромб становится более прочным благодаря нитям фибрина, который образуется в процессе свертывания крови. Основные участники этого процесса — белки плазмы крови, называемые факторами свертывания крови.
Плазменные факторы свертывания синтезируются в печени и циркулируют в крови в неактивной форме. При повреждении сосудистой стенки происходит быстрая активация фактора VII при участии тканевого фактора — трансмембранного белка, который синтезируется гладкомышечными клетками и фибробластами субэндотелиального слоя и в норме с кровью не контактирует. Экспрессия тканевого фактора на поверхности этих клеток при повреждении эндотелия значительно ускоряет активацию фактора VII (превращение его в каталитически активный фактор VIIa)
вприсутствии ионов Са2+. Кроме того, тканевой фактор высвобождается
вкровоток при разрыве атеросклеротических бляшек и экспрессируется на поверхности моноцитов при воспалении, что также может инициировать образование тромбов.
Фактор VIIa (в присутствии тканевого фактора) вызывает последовательную активацию факторов свертывания крови IX и X в сложной аутокаталитической системе, называемой каскадом свертывания крови. Для активации фактора X под действием фактора IX и для дальнейшего функционирования фактора Xa необходимы факторы VIIIa и Va соответственно, выполняющие роль рецепторов на поверхности активиро-
ванных тромбоцитов. При связывании с этими белками каталитическое действие факторов IX и X ускоряется в 109 раз. В результате под действием фактора Xa из протромбина (фактора II) образуется тромбин (фактор IIа), который превращает циркулирующий в крови растворимый белок

Рис. 27.1. Адгезия и агрегация тромбоцитов при повреждении сосудистой стенки: ЭК — эндотелиальная клетка; ФВ — фактор фон Виллебранда; ТхА2 — тромбоксан А2; ПГI2 — простациклин; NO — эндотелиальный релаксирующий фактор; GP — гликопротеины; GPIIb/IIIa — гликопротеины IIb/IlIa (Из: Katzung B.G. Basic and Clinical Pharmacology. — NY, 2001, с изм.)
564
фармакология Частная .II Часть
Глава 27. Средства, влияющие на гемостаз и тромбообразование |
565 |
фибриноген (фактор I) в нерастворимый фибрин (см. рис. 27). Фибрин полимеризуется и, заполняя пространство между тромбоцитами, укрепляет тромбоцитарный тромб. Фибриновые нити пронизывают тромб, образуя сеть, которая задерживает циркулирующие в крови эритроциты. Происходит формирование красного тромба.
Свертыванию крови противодействуют вещества, которые являются естественными ингибиторами активации факторов свертывания крови.
Активации фактора Х под действием фактора VIIa препятствует ингибитор пути тканевого фактора, экспрессируемый эндотелиальными клетками и обнаруженный также в липопротеиновой фракции плазмы крови. При связывании этого ингибитора с фактором Хa образуется бинарный комплекс, инактивирующий фактор VIIa.
Ингибитор тромбина и некоторых других активированных факторов свертывания (Хa, IХa ХIa, ХIIa) — антитромбин III, циркулирующий
вплазме крови белок, который действует в комплексе с гепарином или гепариноподобными веществами (такими как гепаран сульфат), присутствующими на поверхности неповрежденных эндотелиальных клеток. Эти вещества в 1 000 раз ускоряют инактивацию факторов свертывания крови под действием антитромбина III.
Ингибитор факторов VIIIa и Va — активированный протеин C. Этот белок синтезируется в печени при участии витамина K, циркулирует в крови
внеактивной форме и активируется под действием комплекса тромбин– тромбомодулин на поверхности неповрежденных эндотелиальных клеток. Активация протеина C увеличивается при чрезмерном образовании тромбина. Активированный протеин С совместно со своим кофактором
протеином S (оба белка содержат остатки глутаминовых кислот, способствующих их связыванию с Са2+) вызывает деградацию факторов VIIIa и Va, таким образом угнетая образование тромбина.
При локальном образовании тромбов в месте повреждения сосудистой стенки вышеназванные ингибиторы способствуют поддержанию крови
вжидком состоянии, препятствуя росту тромба внутри сосуда. Агрегация тромбоцитов и свертывание крови взаимосвязаны. Преоб-
ладание того или иного процесса в механизме тромбообразования зависит от калибра сосуда и скорости кровотока. Агрегация тромбоцитов имеет большее значение для формирования тромбов при высокой скорости кровотока, т.е. в артериях. В венозных сосудах, где скорость кровотока невелика, преобладает процесс свертывания крови.
Последующая судьба тромба зависит от активности фибринолитической системы. Если эта система функционирует нормально, происходит постепенное растворение фибрина (фибринолиз) при участии фермента
566 |
Часть II. Частная фармакология |
плазмина, образующегося из неактивного предшественника (плазминогена) под влиянием активаторов. Действию плазмина препятствуют циркулирующие в крови антиплазмины. Активаторы плазминогена нейтрализуются специфическими ингибиторами.
Нарушение процессов агрегации тромбоцитов и свертывания крови и/или повышение активности фибринолитической системы могут привести к кровоточивости, а чрезмерная активация этих процессов или угнетение фибринолиза — к возникновению внутрисосудистых тромбов (тромбозу). В результате тромбоза артериальных сосудов уменьшается приток крови к тканям, развивается их ишемия и, как следствие ишемии, — гибель клеток (некроз). Тромбозы могут быть причиной таких тяжелых осложнений, как инфаркт миокарда (тромбоз коронарных артерий), ишемический инсульт (тромбоз сосудов мозга) и др. Венозные тромбозы могут быть причиной эмболии легочной артерии.
Для предупреждения тромбозов используют вещества, которые ингибируют агрегацию тромбоцитов и свертывание крови, таким образом препятствуя образованию тромбов. При тромбозах используют также вещества, вызывающие лизис тромбов, — тромболитические (фибринолитические) средства.
Для остановки кровотечений применяют средства, повышающие свертываемость крови, и средства, угнетающие фибринолиз. Выбор тех или иных средств зависит от причины возникновения кровотечения.
Практическое значение имеют следующие группы средств, влияющих на тромбообразование.
●Средства, снижающие агрегацию тромбоцитов (антиаг реганты).
●Средства, влияющие на свертывание крови:
—средства, понижающие свертывание крови (антикоагулянты);
—средства, повышающие свертывание крови (гемостатики).
●Средства, влияющие на фибринолиз:
—фибринолитические (тромболитические) средства;
—антифибринолитические средства (ингибиторы фибринолиза).
27.1. СРЕДСТВА, СНИЖАЮЩИЕ АГРЕГАЦИЮ ТРОМБОЦИТОВ (АНТИАГРЕГАНТЫ)
Тромбоциты — небольшие по размеру форменные элементы крови дисковидной формы, образуются как фрагменты мегакариоцитов костного мозга. Тромбоциты циркулируют в крови в течение 6–12 дней, а затем захватываются тканевыми макрофагами.
Глава 27. Средства, влияющие на гемостаз и тромбообразование |
567 |
Эндотелий сосудов оказывает влияние на функциональную активность тромбоцитов. Эндотелиальные клетки выделяют в кровоток простациклин (простагландин I2) и эндотелиальный релаксирующий фактор, который идентифицируют с оксидом азота — NO. Эти вещества препятствуют агрегации тромбоцитов. Кроме того, эндотелиальные клетки секретируют вещества, уменьшающие свертывание крови и способствующие лизису тромба. Все это обеспечивает антитромбогенные свойства неповрежденного эндотелия сосудов.
При повреждении эндотелия сосудов, которое может быть вызвано различными факторами (механическая травма, инфекции, атеросклеротические изменения сосудистой стенки, повышение АД и др.), антитромбогенные свойства эндотелия снижаются, и это создает условия для формирования тромба. Нарушается синтез простациклина и эндотелиального релаксирующего фактора, что облегчает контакт тромбоцитов с поврежденной поверхностью эндотелия. Тромбоциты скапливаются
вместе повреждения и взаимодействуют с субэндотелием сосудов непосредственно или через фактор фон Виллебранда, который секретируется активированными тромбоцитами и поврежденными эндотелиальными клетками. Тромбоциты связываются с коллагеном и другими белками субэндотелия непосредственно или через фактор фон Виллебранда при участии специфических гликопротеинов, локализованных в тромбоцитарных мембранах: гликопротеин Ib связывается с фактором фон Виллебранда, а гликопротеин Ia — с коллагеном (см. рис. 27.1).
Воздействие коллагена (а также тромбина, который в небольших количествах образуется локально уже на начальном этапе тромбообразования)
на тромбоциты вызывает изменение их состояния — активацию, которая связана с повышением внутриклеточной концентрации Са2+. В процессе активации тромбоциты меняют свою форму: из дисковидных они становятся уплощенными с множеством отростков — псевдоподий, в результате увеличивается площадь тромбоцитов и облегчается их контакт с поврежденной поверхностью сосуда.
При активации тромбоциты высвобождают различные биологически активные вещества, которые в неактивированных тромбоцитах находятся
вгранулах (α-гранулы, плотные гранулы). Плотные гранулы — хранилище веществ, стимулирующих агрегацию тромбоцитов: АДФ и серотонина. Высвобождаемый в кровоток АДФ стимулирует специфические (пуринергические) рецепторы, локализованные в мембране тромбоцитов. Через рецеп-
торы, связанные с Gi-белками (Р2Y12-пуринергические рецепторы), АДФ вызывает угнетение аденилатциклазы и снижение уровня цАМФ, что приводит к повышению уровня Са2 в цитоплазме тромбоцитов (рис. 27.2).

568 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Часть II. Частная фармакология |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 27.2. Механизмы действия антиагрегантов (ацетилсалициловой кислоты, тиклопидина, клопидогрела и эпопростенола): ЭК — эндотелиальная клетка; ФЛ — фосфолипиды клеточных мембран; АК — арахидоновая кислота; ФЛА2 — фосфолипаза А2; ЦОГ — циклооксигеназа; ТС — тромбоксансинтетаза; ПС — простациклинсинтетаза; ПГG2/H2 — циклические эндопероксиды; ТхА2 — тромбоксан А2; ПГI2 — простациклин; АЦ — аденилатциклаза; ФЛС — фосфолипаза С; IP3 — инозитол-1, 4, 5-трифосфат
Кроме того, при активации тромбоцитов повышается активность фосфолипазы А2 тромбоцитарных мембран — фермента, участвующего в образовании арахидоновой кислоты из мембранных фосфолипидов. В тромбоцитах из арахидоновой кислоты под влиянием циклооксиге- назы-1 сначала синтезируются циклические эндопероксиды (простагландины G2/Н2), а из них при участии тромбоксансинтетазы образуется тромбоксан А2 — активный стимулятор агрегации тромбоцитов и вазоконстриктор. После высвобождения в кровоток тромбоксан А2 стимулирует тромбоксановые рецепторы на мембране тромбоцитов. В результате такого взаимодействия через связанные с этими рецепторами Сq-белки активируется фосфолипаза C и увеличивается образование инозитол- 1,4,5-трифосфата (IP3), который вызывает высвобождение Са2+ из внутриклеточного депо тромбоцитов (роль кальциевого депо в тромбоцитах выполняет система плотных микротрубочек). Это приводит к увеличению цитоплазматической концентрации Са2+ (см. рис. 27.2). Таким же образом тромбоксан А2 вызывает повышение концентрации Са2+ в гладкомышечных клетках сосудов, что приводит к вазоконстрикции.

Глава 27. Средства, влияющие на гемостаз и тромбообразование |
569 |
АДФ и тромбоксан А2, повышая уровень Са2+ в цитоплазме тромбоцитов, вызывают изменение конформации гликопротеинов IIb/IIIa тромбоцитарных мембран, в результате чего они приобретают способность связывать фибриноген. Одна молекула фибриногена имеет два участка связывания для гликопротеинов IIb/IIIa и таким образом может объединить между собой два тромбоцита (рис. 27.3). Объединение многих тромбоцитов фибриногеновыми мостиками приводит к образованию тромбоцитарных агрегатов, формирующих тромб.
Рис. 27.3. Механизм агрегации тромбоцитов и антиагрегантное действие блокаторов гликопротеинов IIb/IIIa: ТхА2 — тромбоксан А2; Ф — фибриноген; + — изменение конформации гликопротеинов IIb/IIIa
Противоположным образом на агрегацию тромбоцитов влияет простациклин (простагландин I2). Как и тромбоксан, простациклин образуется из циклических эндопероксидов, но под действием другого фермента — простациклинсинтетазы. Простациклин синтезируется эндотелиальными клетками и высвобождается в кровоток, где стимулирует простациклиновые рецепторы в мембране тромбоцитов и связанную с ними через Gs-белок аденилатциклазу. В результате в тромбоцитах повышается уровень цАМФ и снижается концентрация цитоплазматического Са2+ (см. рис. 27.2). Это препятствует изменению конформации гликопротеинов IIb/IIIa, и они утрачивают способность связывать фибриноген. Таким образом, простациклин предупреждает агрегацию тромбоцитов. Под действием простациклина снижается концентрация Са2+ в гладкомышечных клетках сосудов, и сосуды расширяются.
Можно выделить следующую последовательность основных событий, приводящих к агрегации тромбоцитов (рис. 27.4).

570 |
Часть II. Частная фармакология |
Адгезия тромбоцитов
Активация тромбоцитов
Синтез и выделение |
|
Выделение АДФ |
тромбоксана А2 |
|
|
|
|
Стимуляция рецепторов на мембране тромбоцитов
Повышение уровня Са2+ в цитоплазме тромбоцитов
Изменение конформации гликопротеинов IIb/IIIa мембран тромбоцитов
Связывание гликопротеинов IIb/IIIa тромбоцитов с фибриногеном
Агрегация тромбоцитов
Рис. 27.4. Механизм агрегации тромбоцитов (схема)
Основная направленность действия антиагрегантов, применяемых в настоящее время в клинической практике, связана с устранением действия тромбоксана А2 и АДФ, а также с блокадой гликопротеинов IIb/ IIIa мембран тромбоцитов. Используют также вещества иного механизма действия, которые повышают концентрацию цАМФ в тромбоцитах и, следовательно, снижают в них концентрацию Са2+.
Выделяют следующие группы средств, снижающих агрегацию тромбоцитов.
●Средства, устраняющие действие тромбоксана A2:
—ингибиторы циклооксигеназы: ацетилсалициловая кислота;
—ингибиторы циклооксигеназы и тромбоксансинтетазы: индобуфен.
Глава 27. Средства, влияющие на гемостаз и тромбообразование |
571 |
●Средства, стимулирующие простациклиновые рецепторы (повышают концентрацию цАМФ в тромбоцитах): эпопростенол.
●Средства, препятствующие действию АДФ на тромбоциты:
—тиклопидин;
—клопидогрел;
—прасугрел;
—тикагрелор;
—кангрелор.
●Средства, ингибирующие фосфодиэстеразу тромбоцитов (повышают концентрацию цАМФ в тромбоцитах):
—дипиридамол;
—пентоксифиллин.
●Средства, блокирующие гликопротеины IIb/IIIa мембран тромбоцитов:
—моноклональные антитела: абциксимаб;
—синтетические блокаторы гликопротеинов IIb/IIIa: эптифибатид; тирофибан.
27.1.1. Средства, ингибирующие синтез тромбоксана A2
Для устранения действия тромбоксана А2 на тромбоциты применяют ингибиторы его синтеза из арахидоновой кислоты. С этой целью можно использовать ЛВ, ингибирующие циклооксигеназу и/или тромбоксансинтетазу. Кроме того, изучаются возможности применения блокаторов тромбоксановых рецепторов.
Из числа ЛВ, устраняющих действие тромбоксана А2 на агрегацию тромбоцитов, в основном используют ацетилсалициловую кислоту.
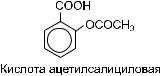
Ацетилсалициловая кислота (аспирин♠) — известное противовоспалительное, анальгетическое и жаропонижающее средство. В настоящее время широко применяется в качестве антиагреганта (рис. 27.5). Антиагрегантное действие ацетилсалициловой кислоты связывают с ее ингибирующим влиянием на активность циклооксигеназы-1 в тромбоцитах, в результате чего нарушается синтез тромбоксана A2.
Ацетилсалициловая кислота необра- |
|
тимо ингибирует циклооксигеназу (вы- |
|
зывает необратимое ацетилирование этого |
|
фермента), нарушая образование из арахи- |
|
доновой кислоты циклических эндоперок- |
|
сидов — предшественников тромбоксана |
|
A2 и простагландинов. Поэтому под дей- |
Рис. 27.5. Химическая структура |
ствием ацетилсалициловой кислоты |
ацетилсалициловой кислоты |
572 |
Часть II. Частная фармакология |
уменьшается не только синтез тромбоксана A2 в тромбоцитах, но и синтез простациклина в эндотелиальных клетках сосудов (см. рис. 27.2). Однако путем подбора соответствующих доз и режима применения можно добиться преимущественного действия ацетилсалициловой кислоты на синтез тромбоксана A2. Это связано с существенными различиями между тромбоцитами и эндотелиальными клетками.
Тромбоциты — это фрагменты мегакариоцитов костного мозга, не имеющие ядра и, следовательно, не способные синтезировать белки,
втом числе циклооксигеназу. Поэтому необратимое ингибирование этого
фермента ацетилсалициловой кислотой нарушает синтез тромбоксана A2 на протяжении всей жизни тромбоцита, т.е. в течение 7–10 дней. Однако вследствие образования новых тромбоцитов, содержащих активную ци-
клооксигеназу, синтез тромбоксана A2 восстанавливается быстрее (приблизительно через 2 сут). По этой причине для достижения стабильного эффекта препарата (для стабильного снижения уровня тромбоксана
втромбоцитах) его рекомендуют назначать 1 раз в сутки.
Вто же время в клетках эндотелия сосудов (где из арахидоновой кислоты образуется простациклин) происходит ресинтез циклооксигеназы,
иактивность этого фермента восстанавливается уже через несколько часов после приема ацетилсалициловой кислоты. При таких условиях назначение препарата 1 раз в сутки не приводит к существенному снижению синтеза простациклина.
Кроме того, ацетилсалициловая кислота приблизительно на 30% подвергается пресистемному метаболизму (деацетилированию) в печени, поэтому ее концентрация в системном кровотоке ниже, чем в портальной крови. В результате на тромбоциты в портальном кровотоке ацетилсалициловая кислота действует в более высоких концентрациях, чем на эндотелиальные клетки сосудов системного кровотока. Поэтому для подавле-
ния синтеза тромбоксана A2 в тромбоцитах необходимы меньшие дозы ацетилсалициловой кислоты, чем для подавления синтеза простациклина
вклетках эндотелия. По этим причинам при увеличении дозы и кратности назначения ацетилсалициловой кислоты ее угнетающее действие на синтез простациклина становится более выраженным, что может привести к уменьшению антиагрегантного эффекта. В связи с указанными особенностями ацетилсалициловую кислоту в качестве антиагреганта рекомендуют назначать в небольших дозах (в среднем 100 мг) 1 раз в сутки.
Вкачестве антиагреганта ацетилсалициловую кислоту используют: ●при нестабильной стенокардии; ●для профилактики инфаркта миокарда, ишемического инсульта
итромбозов периферических сосудов;
