
- •Мужской пол
- •Острый инфаркт миокарда
- •156. Эмфизема легких: определение, виды, механизмы развития, патологическая анатомия, исходы, осложнения, клиническое значение.
- •158. Интерстициальные болезни легких: определение, этиология, патогенез, морфогенез, классификация, патологическая анатомия, осложнения, клиническое значение.
- •159. Саркоидоз легких: определение, этиология, патогенез, макро- и микроскопические изменения в легких, осложнения, исходы.
- •160. Рак легкого: классификация, локализация, морфологическая характеристика, особенности метастазирования, осложнения, причины смерти больных.
- •161. Злокачественная гипертония
- •162. Крупозная пневмония
- •163. Острые воспалительные заболевания лёгких или острые пневмонии
- •164. Хронические воспалительные заболевания лёгких
- •165. Редкие формы пневмонии
126. Ревматические болезни: определение понятия, классификация, общая характеристика. Стадии дезорганизации соединительной ткани.
Ревматические болезни (РБ) объединяют группу страданий, при которых происходит системное поражение соединительной ткани с вовлечением в про- цесс сосудов, особенно микроциркуляторного русла. При данных заболева- ниях развивается иммунное воспаление в связи с нарушенным гомеостазом. В эту группу входят: ревматизм, болезнь Бехтерева (спондилоартрит), ревма- тоидный артрит, системная красная волчанка, системная склеродермия, узел- ковый периартериит, дерматомиозит, сухой синдром Шегрена.
Общими признаками, объединяющими КБ в одну группу, являются:
• наличие хронической очаговой инфекции;
• выраженные нарушения иммунологического гомеостаза;
• генерализованные васкулиты,
• хроническое волнообразное течение;
• системная прогрессирующая дезорганизация соединительной ткани.
Роль хронической инфекции в возникновении КБ общеизвестна. Так b‐гемолитический стрептококк группы А является причиной воз‐никновения ревматизма. Диплострептококк и микоплазма рассматриваются как причина развития ревматоидного артрита. Вирусы кори, краснухи, парагриппа, Эп- штейна–Барр могут быть причинами развития различных коллагеновых за- болеваний. Для возникновения заболеваний необходимы условия реализа- ции инфекции: наследственная предрасположенность, наследственная ано- малия коллагена в волокнах соединительной ткани, сходство антигенов ми- кроорганизмов с антигенами тканей человека (молекулярная мимикрия). Выраженное нарушение иммунологического гомеостаза проявляется ре- акциями гиперчувствительности, чаще всего III типа, когда антигены ми- кроорганизмов с антителами образуют токсические иммунные комплексы, а также аутологичные антигены и аутоантитела образуют иммунные ком- плексы, которые повреждают различные ткани и стенки сосудов. Из этого следует, что процессы аутоиммунизации при коллагенозах являются веду- щим звеном патогенеза. Реакция гиперчувствительности замедленного типа чаще представлена клеточным цитолизом, который может быть очаговым (формирование гранулем) и диффузным.
Системная прогрессирующая деструкция соединительной ткани прояв- ляется в виде системной прогрессирующей деструкции коллагеновых воло- кон и складывается из следующих фаз: мукоидного и фибриноидного на- бухания, воспалительных клеточных реакций, склероза и васкулитов. Для этих болезней характерна вся сумма перечисленных процессов, причем наи- более ярким признаком считается сочетание в каждом случае заболевания свежих дистрофических изменений соединительной ткани и более старых процессов в виде организации и склероза. Хроническое и волнообразное течение характеризуется чередованием обострений и ремиссий. В зависимости от поражения тех или иных орга- нов, определяют вид ревматического заболевания, например, при ревматиз- ме страдает преимущественно сердце, при ревматоидном артрите – суставы,
при системной красной волчанке – сердце, почки и другие органы, при си- стемной склеродермии – кожа, почки, при дерматомиозите – мышцы и кожа, но полиорганность поражения характерна для всех коллагенозов.
127. Ревматизм: определение, клинико-морфологические формы, патологоанатомические изменения в сердце, суставах, коже, нервной системе.
Ревматизм (болезнь Сокольского–Буйо) – инфекционно‐аллергическое заболевание, характеризующееся системным поражением соединительной ткани преимущественно сердца и сосудов, волнообразным течением с пора- жением висцеральных органов.
Этиология. Заболевание возникает у предрасположенных лиц, главным образом, молодого возраста (7–15 лет) после воспалительного процесса в глотке (ангины), вызванного b‐гемолитическим стрептококком группы А. Большое значение в возникновении болезни имеют генетические факто- ры и возраст. В патогенезе основными звеньями являются:
• сенсибилизация организма в результате перенесенной инфекции;
• образование под влиянием антигенной общности стрептококка
• с тканевыми антигенами аутоантител и клона сенсибилизированных лимфоцитов;
• развитие реакций ГЗТ и ГНТ с преимущественным поражением сосудов микроциркуляторного русла и соединительной ткани сердца.
Патологическая анатомия. Наиболее характерные изменения при ревматизме развиваются в сердце и сосудах.
При ревматизме в сенсибилизированном организме возникает сложный иммунологический ответ на возбудитель. Следует отметить, что на антиге- ны стрептококка развивается перекрестный с антигенами кардиомиоцитов иммунный ответ, поэтому образующиеся в организме антитела направлены не только на антигены стрептококка, но и против миоцитов сердца. Неко- торые ферменты стрептококка разрушают окружающую миоциты соедини- тельную ткань, в результате чего образуются антитела, направленные про- тив соединительной ткани. Морфогенез. Структурную основу ревматизма составляет системная прогрессирующая дезорганизация соединительной ткани с её набуханием, развитием гранулем и склероза. Мукоидное набухание является поверхностной и обратимой фазой дезор- ганизации соединительной ткани и характеризуется метахромазией (извра- щенным цветом) при окраске толуидиновым синим, отёком и разволокнени- ем, в основе которого лежит деполимеризация основного вещества с накопле- нием кислых гликозаминогликанов. Среди клеточных элементов встречаются лаброциты, мукогенные клетки, отдельные лимфоциты и гистиоциты. Фибриноидное набухание (набухание и некроз) представляет собой фазу глубокой и необратимой дезорганизации, сопровождающейся гомогенизацией коллагеновых волокон и пропитыванием их белками плазмы, в том числе фи- брином, и заканчивающейся гибелью соединительной ткани, проявляющейся в изменении состава её основного вещества и деструкции волокнистых эле- ментов с последующими за ними воспалительными клеточными реакциями. 23
Клеточные воспалительные реакции выражаются образованием специфи- ческой ревматической гранулемы, описанной Ашоффом и детально изученной Талалаевым. Формирование гранулёмы начинается с момента фибриноидных изменений. Гранулема состоит из аморфного вещества, по периферии которо- го частоколом располагаются макрофагальные клетки с базофильной цитоплаз- мой и гиперхромными ядрами. Такие макрофаги принимают активное участие в рассасывании фибриноида, обладают высокой фагоцитарной активностью. Ревматические гранулемы, состоящие из таких крупных макрофагов, обозначают как «цветущие», или «зрелые». В дальнейшем клетки гранулёмы вытягиваются, среди них появляются фибробласты, фибриноидные массы в центре узелка почти исчезают, такие узелки называют «увядающими гранулемами». На последнем этапе в рев- матической гранулеме преобладают фибробласты, между которыми появ- ляются аргирофильные, а затем и коллагеновые волокна, узелок сморщива- ется и приобретает характер «рубцующейся гранулемы». Склероз является заключительной стадией ревматического поражения соединительной ткани, носит системный характер, но наиболее выражен в оболочках сердца, стен- ках сосудов и серозных оболочках. Продолжительность всех фаз поражения соединительной ткани состав- ляет 4–6 месяцев. Различают четыре клинико‐анатомические формы ревматизма: полиар- тритическую, церебральную, кардиоваскулярную, нодозную. Полиартритическая форма характеризуется припуханием, краснотой и болью в области крупных суставов. В полости сустава появляется серозно‐ фибринозный экссудат. Синовиальная оболочка полнокровна, наблюдаются васкулиты, соединительная ткань подвергается мукоидному набуханию. Де- формации суставов обычно не развиваются. Церебральная форма (малая хорея) ревматизма клинически проявляется гиперкинезами. Основным морфологическим субстратом являются фибри- ноидное набухание и склероз мелких сосудов головного мозга с очагами кро- воизлияний, что приводит к гипоксии и дистрофическим изменениям нейро- нов и нервных волокон. При кардио‐васкулярной форме ревматизма поражаются все оболочки сердца (эндокард, миокард и перикард) и сосуды микроциркуляторного рус- ла. Ревматический эндокардит – встречается чаще других форм. По локали- зации различают клапанный, хордальный и пристеночный эндокардит. Наи- более чаще поражаются митральный или аортальный клапан. Выделяют че- тыре вида ревматического клапанного эндокардита: 1) острый диффузный эндокардит, или вальвулит Талалаева, характери- зуется мукоидным и фибриноидным набуханием, отёком и полнокровием капилляров створок клапанов; 24
2) острый бородавчатый эндокардит вследствие деструкции эндотелия (к ранее указанным изменениям добавляется тромбообразование); 3) фибропластичекий эндокардит характеризуется организацией и скле- розом створок; 4) возвратно‐бородавчатый эндокардит (на поврежденном эндокарде при очередном рецидиве болезни возникают новые тромботические наложения – «бородавки»). В исходе эндокардита развиваются склероз и гиалиноз эндо- карда, что приводит к его утолщению и деформации створок клапана, т.е. развитию порока сердца. Миокардит – воспаление миокарда, постоянно наблюдающееся при рев- матизме. Выделяют три его формы: 1) узелковый продуктивный (гранулематозный), характеризуется образо- ванием гранулем в соединительной ткани различных отделов сердца, карди- омиоциты находятся в состоянии белковой или жировой дистрофии. Закан- чивается узелковый миокардит диффузным мелкоочаговым кардиосклерозом; 2) диффузный межуточный экссудативный характеризуется диффузной инфильтрацией стромы лимфоцитами, гистиоцитами, нейтрофилами, сосу- ды полнокровные, выражен отёк стромы. Миокард теряет тонус, становится дряблым, что клинически проявляется тяжелой сердечно‐сосудистой недо- статочностью; 3) очаговый межуточный экссудативный имеет те же морфологические проявления, что и диффузный, только процесс носит очаговый характер. Ревматический перикардит имеет характер серозно‐фибринозного или фибринозного и нередко заканчивается образованием спаек. Возможна об- литерация полости сердечной сорочки и обызвествление образующейся в ней соединительной ткани (панцирное сердце). Нодозная (узловая) форма характеризуется возникновением плотных, безболезненных ревматических узелков диаметром от 1–2 мм до 1 см в коже, околосуставных тканях, в области больших апоневрозов. Наблюдается преимущественно у детей. К осложнениям ревматизма относятся: пороки сердца, бородавчатый эн- докардит может стать источником тромбоэмболий сосудов большого круга кровообращения с развитием инфарктов в различных органах, очаги размяг- чения ткани головного мозга, гангрена конечностей, пневмонии и др.
128. Ревматический эндокардит: определение, виды, патологическая анатомия, исходы, осложнения, причины смерти больных.
ндокардит - воспаление эндокарда - одно из ярких проявлений ревматизма. По локализации различают
эндокардит клапанный, хордальный ипристеночный. Наиболее выраженные изменения развиваются в створках митрального или аортального клапанов. Изолированное поражение клапанов правого сердца наблюдается очень редко и при наличии эндокардита клапанов левого сердца.
При ревматическом эндокардите отмечаются дистрофические и некробиотические изменения эндотелия, мукоидное, фибриноидное набухание и некроз соединительной основы эндокарда, клеточная пролиферация (гранулематоз) в толще эндокарда и тромбообразование на его поверхности. Сочетание этих процессов может быть различным, что позволяет выделить несколько видов эндокардита. Выделяют 4 вида ревматического клапанного эндокардита 1) диффузный, или вальвулит; 2) острый бородавчатый; 3) фибропластический; 4) возвратнобородавчатый.
Диффузный эндокардит, или вальвулит (по В.Т. Талалаеву), характеризуется диффузным поражением створок клапанов, но без изменений эндотелия и тромботических наложений. Острый бородавчатый эндокардитсопровождается повреждением эндотелия и образованием по замыкающему краю створок (в местах повреждения эндотелия) тромботических наложений в виде бородавок. Фибропластический эндокардит развивается как следствие двух предыдущих форм эндокардита при особой склонности процесса к фиброзу и рубцеванию. Возвратно-бородавчатый эндокардит характеризуется повторной дезорганизацией соединительной ткани клапанов, изменением их эндотелия и тромботическими наложениями на фоне склероза и утолщения створок клапанов. В исходе эндокардита развиваются склероз и гиалиноз эндокарда, что приводит к его утолщению и деформации створок клапана, т.е. к развитию порока сердца.
Исходы эндокардита:
1)выздоровление
2)формирование порока сердца
3) летальный исход в раннем периоде болезни (от осложнений).
4)летальные эмболии
Отдаленные исходы:
1) смерть от прогрессировали недостаточности кровообращения
2)формирование хронического нефрита и смерть от ПН.
Осложнения:тромбонмболический синдром с инфарктами селезенки, почек, головного мозга, нижних конечностей.
Причины смерти-
1) прогрессирующая сердечная недостаточность
2) тромбоэмболии
3)полированная недостаточность
4)почечная недостаточность
129. Изменения в сердце, большом и малом кругах кровообращения при митральных пороках.
Пороки сердца (vicia cordis) - стойкие отклонения в строении сердца, нарушающие его функцию.
Механизм формирования приобретенного порока сердца тесно связан с эволюцией эндокардита,завершающейся организацией тромботических масс, рубцеванием, петрификацией и деформацией клапанов и фиброзных колец. Прогрессированию склеротических изменений способствуют возникающие при формировании порока нарушения гемодинамики.
Патологическая анатомия. Склеротическая деформация клапанного аппарата приводит к недостаточности клапанов, которые не в состоянии плотно смыкаться в период их закрытия, или сужению (стенозу) предсердно-желудочковых отверстий или устий магистральных сосудов. При комбинации недостаточности клапанов и стеноза отверстия говорят о комбинированном пороке сердца. Возможно поражение клапана(изолированный порок) или клапанов сердца (сочетанный порок).
Наиболее часто развивается порок митрального клапана, или митральный порок, возникающий обычно при ревматизме и очень редко при атеросклерозе. Различают недостаточность митрального клапана, стеноз левого предсердно-желудочкового (митрального) отверстия и их комбинацию (митральную болезнь). Чистые формы недостаточности встречаются редко, чистые формы стеноза - несколько чаще. В большинстве случаев отмечается их комбинация с преобладанием той или иной разновидности порока, которая в конечном итоге завершается стенозом отверстия. Прогрессирование склероза, а следовательно, и порока обусловлено чаще всего повторными атаками ревматизма (эндокардита), а также гиперпластическими изменениями клапана, возникающими в связи с непрерывной травматизацией измененного клапана током крови. В результате этого в створках митрального клапана появляются сосуды, затем соединительная ткань створок уплотняется, они превращаются в рубцовые, иногда обызвествленные, сросшиеся образования. Отмечаются склероз и петрификация фиброзного кольца. Хорды также склерозируются, становятся толстыми и укороченными. При преобладании недостаточности митрального клапана вследствие обратного тока крови (регургитация) при диастоле левое сердце переполняется кровью, развивается компенсаторная гепертрофия стенки левого желудочка.
Сужение отверстия митрального клапана чаще развивается на уровне фиброзного кольца, и отверстие имеет вид узкой щели, напоминающей пуговичную петлю, реже отверстие клапана имеет вид «рыбьей пасти» (рис. 140). Сужение митрального отверстия может достигать такой степени, что оно едва пропускает браншу пинцета. При преобладании стеноза возникает затруднение тока крови в малом круге кровообращения, левое предсердие расширяется, стенка его утолщается, эндокард склерозируется, становится белесоватым. В результате гипертонии в малом круге стенки правого желудочка подвергаются резкой гипертрофии (утолщаются до 1-2 см), полость желудочка расширяется.
130. Изменения при аортальных пороках( в сердце, мкк и бяк).
Райана объясняет все своими словами, потому что не нашла норм инфы.
1)Стеноз устья аорты.
-СУА препятствует току крови из ЛЖ в БКК. Снижается МОК И УОК.
-Включаются компенсаторные механизмы, такие как удлинение систолы левого желудочка ( когда кровь в течение бОльшего времени переходит в аорту) и в левом желудочке увеличивается давление. Эти механизмы приводят к гипертрофии левого желудочка, и так как он самый мощный. сочный, восточные долгое время декомпенсации не наблюдается.
-Спустя длительное время все таки наступает декомпенсация и тогда левый желудочек дилятируется (расширяется), диастолическое давление в его полости увеличивается. Далее давление повышается в ретроградном направлении-сначала в предсердиях, потомм в легочных венах. Возникает легочная гипертензия, правый желудочек гипертрофируется умеренно.
-далее правожелудочковая недостаточность .
2) Недостаточность аортального клапана
-При этом пороке кровь обратно отекает из аорты в ЛЖ в диастолу. Это называется регургитация. Левый желудочек расширяется.
-ЛЖ усиленно работает, поэтому гипертрофируется. Это компенсаторные механизмы.
-Кровь течет обратно, значит давление в ЛЖ возрастает.
-Левое предсердие функционирует нормально, пока основную работу выполняет ЛЖ. Однако далее при развитии декомпенсации в нем повышается давление. Возникает дилатация левого желудочка и возникает относительная недостаточность митрального клапана, значит это приведет к гипертрофии и дилятации левого предсердия.
-Ретроградно повышается давление в легочной артерии, правый желудочек тоже гипертрофируется. Развивается застой в МКК. За ним следует застой в системе БКК.
131. Врожденные пороки сердца-принципы, классификации. Гемодинамические изменения в органах кровообращения при наличии дефектов межпредсердной и межжелудочковой перегородок, незаращении артериального протока.
Врожденным пороком развития называют стойкое морфологическое изменение органа, части тела или всего организма, выходящее за пределы вариаций нормального строения определенного биологического вида, возникащее внутриутробно в результате нарушений морфогенеза
1)Дефект межпредсердной перегородки в виде изолированного порока встречается редко. Он возникает либо при нарушениях развития первичной предсердной перегородки на 5-й неделе эмбриогенеза, либо позднее, при формировании вторичной перегородки и овального отверстия. Дефект первичной перегородки имеет вид отверстия, расположенного непосредственно над клапанами желудочков; при дефекте вторичной перегородкиимеется широко открытое овальное отверстие, лишенное заслонки. В том и в другом случае ток крови происходит слева направо, гипоксии и цианоза не бывает (белый тип порока). Переполнение кровью правой половины сердца сопровождается гипертрофией правого желудочка и расширением ствола и ветвей легочной артерии. Полное отсутствие межжелудочковой или межпредсердной перегородок приводит к развитию трехкамерного сердца - тяжелого порока, при котором, однако, в период компенсации не наблюдается полного смешения артериальной и венозной крови, так как основной ток той или другой крови сохраняет свое направление и поэтому степень гипоксии нарастает по мере прогрессирования декомпенсации.
Гемодинамика: Cмысл порока заключается в сбросе артериальной крови из большого круга кровообращения (левого предсердия) в малый круг кровообращения (правое предсердие), что приводит к перегрузке малого круга кровообращения избыточным объемом крови с поражением, в первую очередь, легких. Крайней формой поражения является формирование легочной гипертензии (высокого давления в сосудах легких). Легочная гипертензия при дефекте межпредсердной перегородки носит злокачественный характер, приводя к тяжелой сердечной недостаточности и гибели пациента
2)Дефект межжелудочковой перегородкивстречается часто, возникновение его зависит от отставания в росте одной из структур, формирующих перегородку, вследствие чего между желудочками развивается ненормальное сообщение. Чаще наблюдается дефект в верхней соединительнотканной (мембранозной) части перегородки (рис. 295). Кровоток через дефект осуществляется слева направо, поэтому цианоза и гипоксии не наблюдается (белый тип порока). Степень дефекта может варьировать, вплоть до полного отсутствия перегородки. При значительном дефекте развивается гипертрофия правого желудочка сердца, при незначительном - существенных изменений гемодинамики не происходит.
Гемодинамика: Внутрисердечные гемодинамические нарушения при ДМЖП начинают формироваться спустя некоторое время после рождения, как правило, на 3—5 сутки жизни. В раннем неонатальном периоде шум в сердце может отсутствовать вследствие одинакового давления в правом и левом желудочках из-за так называемой неонатальной лёгочной гипертензии. Постепенное падение давления в системе легочной артерии и в правом желудочке создаёт разность (градиент) давлений между желудочками, вследствие чего появляется сброс крови слева направо (из области высокого давления в область низкого давления). [7] [8] Дополнительный объём крови, поступающий в правый желудочек и лёгочную артерию, приводит к переполнению сосудов малого круга кровообращения, где развивается лёгочная гипертензия.
2) Незаращение артериального (боталлова) протока можно считать пороком при наличии его с одновременным расширением у детей старше 3 мес жизни. Ток крови осуществляется при этом слева направо (белый тип порока). Изолированный порок хорошо поддается хирургической коррекции.
Гемодинамическая сущность порока состоит в постоянном сбросе артериальной крови в малый круг кровообращения, вследствие чего происходит перемешивание артериальной и венозной крови в легких и развивается гиперволемия малого круга, которая сопровождается необратимыми морфологическими изменениями в сосудах легких и последующим развитием легочной гипертензии. При этом левый желудочек вынужден работать интенсивнее для поддержания устойчивой гемодинамики, что приводит к гипертрофии левых отделов. Прогрессирующее повышение сопротивления сосудов малого круга вызывает перегрузку правого желудочка сердца, обусловливая его гипертрофию и последующую дистрофию миокарда. Степень нарушения кровообращения зависит от диаметра протока и объема сбрасываемой через него крови.
132. Миокардиты: определение, классификация, этиология, патогенез, патологическая анатомия, осложнения, исходы.
Миокардит - воспаление миокарда, т.е. мышцы сердца. Возникает обычно вторично при вирусных (полиомиелит, корь, мононуклеоз, острые вирусные респираторные инфекции), риккетсиозных (сыпной тиф), бактериальных (дифтерия, скарлатина, туберкулез, сифилис, сепсис) и протозойных (трипаносомоз) инфекционных и инфекционно-аллергических (ревматизм) заболеваниях (вторичный миокардит). Как самостоятельное заболевание представлен идиопатическим миокардитом.
Идиопатический миокардит (миокардит Абрамова-Фидлера, идиопатический злокачественный, инфекционно-аллергический миокардит) характеризуется избирательным воспалительным процессом в миокарде(изолированный миокардит) и тяжелым прогрессирующим течением с частым летальным исходом(злокачественный миокардит). Течение болезни острое или хроническое рецидивирующее.
Этиология и патогенез. В настоящее время признана аллергическая природа идиопатического миокардита, обоснованная А.И. Абрикосовым и Я.Л. Рапопортом. Заболевание рассматривается как крайний вариант неспецифического инфекционно- аллергического миокардита, хотя некоторые авторы отождествляют его с застойной (конгестивной) кардиомиопатией (см. Кардиомиопатии). В пользу инфекционно- аллергического
генеза миокардита свидетельствует частое его развитие после вирусной или бактериальной инфекции, введения сывороток и вакцин, неупорядоченного приема лекарств. Прогрессирование болезни связано, вероятно, с аутоиммунизацией.
Патологическая анатомия. Типичным для идиопатического миокардита является распространенное поражение миокарда всех отделов сердца. Оно увеличено в размерах, дряблое, полости растянуты, как правило, с тромботическими наложениями; мышца на разрезе пестрая, клапаны интактны. Выделяют 4 морфологических (гистологических) типа идиопатического миокардита (Рапопорт Я.Л., 1951): дистрофический (деструктивный); воспалительно-инфильтративный; смешанный; сосудистый.
Дистрофический (деструктивный) тип характеризуется преобладанием гидропической дистрофии и лизисом кардиомиоцитов, причем реактивные изменения отсутствуют (ареактивный миолиз). В участках гибели мышечных клеток происходит лишь коллапс ретикулярной стромы.
Воспалительно-инфильтративный тип представлен серозным отеком и инфильтрацией стромы миокарда разнообразными клетками - нейтрофилами, лимфоцитами, макрофагами, плазматическими клетками. Среди них находят также многоядерные гигантские клетки. Дистрофические изменения кардиомиоцитов выражены умеренно.
Смешанный тип отражает сочетание деструктивных и воспалительноинфильтративных изменений.
Сосудистый тип характеризуется преобладанием поражения сосудов - васкулитами; кроме того, находят дистрофические и воспалительноинфильтративные изменения миокарда.
В исходе изменений, типичных для каждого морфологического типа идиопатического миокардита, развиваетсяочаговый или (и) диффузный кардиосклероз, нередко в сочетании с гипертрофией миокарда.
Пестрота морфологических изменений миокарда (миолиз, межуточное воспаление, склероз, гипертрофия) определяет полиморфизм клинических проявлений идиопатического миокардита, его клинические варианты (аритмичный, псевдокоронарный, инфарктоподобный и др.).
Изменения других органов (помимо сердца) и тканей связаны с сердечной недостаточностью и тромботическими наложениями на париетальном эндокарде. Они проявляются застойным полнокровием и дистрофическими изменениями паренхиматозных элементов, тромбоэмболией сосудов, инфарктами и кровоизлияниями в легких, головном мозге, почках, кишечнике, селезенке и т.д.
Осложнения. Наиболее часто встречаются и являются грозными тромбоэмболические осложнения, которые могут быть первыми проявлениями миокардита.
Смерть наступает от сердечной недостаточности или тромбоэмболических осложнений.
133. Кардиомиопатии: определение, причины, классификация, патологическая анатомия, осложнения, исходы.
Кардиомиопатии
Кардиомиопатии (от греч. kardia - сердце, myos - мышца, pathos - болезнь) - группа заболеваний, характеризующихся первичными дис-
трофическими изменениями миокарда. Эта группа включает различные заболевания некоронарного(некоронарогенные кардиомиопатии) и неревматического (неревматогенные кардиомиопатии)происхождения, разные по этиологии и патогенезу, но сходные клинически. Основное клиническое проявление кардиомиопатии - недостаточность сократительной функции миокарда в связи с его дистрофией.
Классификация. Кардиомиопатии делят на первичные (идиопатические) и вторичные.
Среди первичных (идиопатических) кардиомиопатий различают: 1) гипертрофическую (констриктивную); 2) дилатационную (конгестивную); 3) рестриктивную (эндомиокардиальный фиброз). Вторичные кардиомиопатиивстречаются при: 1) интоксикациях (алкоголь, этиленгликоль, соли тяжелых металлов, уремия и др.); 2) инфекциях (вирусные инфекции, тифы, трипаносомоз - болезнь Шагаса, трихинеллез и др.); 3) болезнях обмена наследственного (тезаурисмозы - кардиопатический амилоидоз, гликогеноз) и приобретенного (подагра, тиреотоксикоз, гиперпаратиреоз, первичный амилоидоз, авитаминоз, нарушения электролитно-стероидного обмена) характера; 4) болезнях органов пищеварения (синдром нарушенного всасывания, панкреатит, цирроз печени и др.).
Первичные (идиопатические) кардиомиопатии
1. Гипертрофическая (констриктивная) кардиомиопатия имеет наследственный характер. Средиморфогенетических гипотез обсуждаются следующие: 1) повышенная сократимость, возможно обусловленная увеличением чувствительности к катехоламинам, приводит к повреждению кардиомиоцитов, фиброзу и гипертрофии сократительного миокарда; 2) повышенная сократимость миокарда в эмбриональном периоде (пренатальная фаза) ведет к развитию гиперплазии кардиомиоцитов в определенных отделах миокарда, преимущественно в межжелудочковой перегородке. Гиперплазия кардиомиоцитов сменяется в постнатальной фазе прогрессирующей гипертрофией миокарда; 3) первичная патология коллагена с нарушением фиброзного скелета миокарда ведет к дезорганизации миофибрилл.
Гипертрофическая кардиомиопатия может проявляться в виде двух форм: диффузной (идиопатическая гипертрофия миокарда) или локальной (идиопатический гипертрофический субаортальный стеноз). При первой форме отмечается диффузное утолщение миокарда левого желудочка и межжелудочковой перегородки, правые отделы сердца гипертрофируются редко, размер полостей сердца нормальный или уменьшенный. При микроскопическом исследовании находят хаотичное расположение кардиомиоцитов,
383
особенно в межжелудочковой перегородке. При второй, локальной, форме гипертрофия миокарда охватывает в основном верхние отделы левого желудочка, что ведет к субаортальному сужению (субаортальный мышечный стеноз). При диффузной и локальной формах клапанный аппарат сердца и венечные артерии интактны.
2. Дилатационную (конгестивную) кардиомиопатию связывают с вирусным миокардитом (особенно вирусом Коксаки). Высказываются предположения о значении в развитии этого вида кардиомиопатии сочетанного действия вируса и алкоголя.
Для дилатационной кардиомиопатии характерно резкое расширение полостей сердца, мышца которого может быть в той или иной степени гипертрофирована. Сердце приобретает шаровидную форму, масса его увеличивается, особенно за счет левого желудочка. Миокард дряблый, тусклый, пронизан белесоватыми прослойками, характерно чередование гипертрофированных и атрофичных кардиомиоцитов. Клапанный аппарат и венечные артерии сердца не изменены. В полостях сердца нередко возникают тромбы.
3. Рестриктивную кардиомиопатию некоторые авторы рассматривают как исход париетального эндокардита Леффлера (см.), хотя это мнение не имеет достаточных оснований. При этом виде первичной кардиомиопатии находят диффузный или очаговый фиброз эндокарда левого, реже правого желудочка; иногда в процесс вовлекается задняя створка митрального клапана. Часто встречаются пристеночные тромбы с последующей их организацией. Утолщение эндокарда, иногда резко выраженное (до 3-5 см), ведет к уменьшению (облитерации) полости желудочка.
Вторичные кардиомиопатии
Морфологические проявления вторичных кардиомиопатии достаточно полиморфны в связи с разнообразием вызывающих их причин. Но в основе вторичных кардиомиопатии независимо от этиологических факторов лежит дистрофия кардиомиоцитов. Алкогольная кардиомиопатия имеет наибольшее значение среди вторичных кардиомиопатии.
Патогенез алкогольной кардиомиопатии связан в первую очередь с биологическими свойствами этанола - его прямым токсическим действием на кардиомиоциты, а также влиянием метаболита этанола - ацетальдегида. Безусловно значение также сосудистых нарушений и связанной с ними гипоксии, повреждающего действия на миокард катехоламинов.
Морфологические изменения сердца сводятся к умеренной гипертрофии миокарда, расширению полостей сердца с пристеночными тромбами. Миокард дряблый, глинистого вида, иногда с небольшими рубчиками. Коронарные артерии интактны, возможны липидные пятна и полоски в интиме, выраженные атеросклеротические изменения отсутствуют. При микроскопическом исследовании отмечается сочетание дистрофии (гидропической и жировой), атрофии и гипертрофии кардиомиоцитов, встречаются очажки лизиса кардиомиоцитов и склероза. Поврежденные участки миокарда чередуются с неизмененными.
384
При электронномикроскопическом исследовании биоптатов сердца находят кистозное расширение саркоплазматической сети и Т-системы кардиомиоцитов, что считается характерным для алкогольной кардиомиопатии.
Осложнения алкогольной кардиомиопатии - внезапная смерть (фибрилляция желудочков) или хроническая сердечная недостаточность, тромбоэмболический синдром.
Осложнения кардиомиопатии выражаются обычно хронической сердечно-сосудистой недостаточностью или тромбоэмболическим синдромом в связи с наличием тромбов в полостях сердца.
134. Системные васкулиты: определение, этиология, классификация, патологическая анатомия, примеры заболеваний.
Васкулиты - заболевания, характеризующиеся воспалением и нередко присоединяющимся некрозом сосудистой стенки. Они могут иметь местньпй или системный характер. Местные васкулиты обычно развиваются в очагах воспаления вследствие перехода процесса на сосудистую стенку с окружающих тканей (например, гнойно-некротический васкулит при флегмоне). Для системных васкулитов, которые могут быть основой самостоятельных болезней (первичные васкулиты) или проявлением какого-либо другого заболевания (вторичные васкулиты), характерно распространенное поражение сосудов.
В зависимости от типа воспалительной реакции, преобладания альтеративно- экссудативных или продуктивных изменений васкулиты делят на некротические (деструктивные), деструктивно-продуктивные, продуктивные, выделяя среди них отдельно гранулематозные. Руководствуясь глубиной поражения сосудистой стенки, т.е. вовлечением в воспалительный процесс внутренней, средней или наружной ее оболочки, различают эндоваскулит, мезоваскулит и периваскулит, а при сочетанном поражении оболочек -эндомезоваскулит и панваскулит. Подавляющее большинство системных васкулитов характеризуется поражением всех оболочек сосудистой стенки с исходом в склероз и кальциноз, что ведет в одних случаях к резкому стенозу просвета, вплоть до облитерации его, в других - к развитию аневризмы.
Топография и распространенность изменений в сосудистой системе при системных васкулитах самые разнообразные - в процесс могут вовлекаться сосуды всех калибров и типов: аорта (аортит), артерии(артериит), артериолы (артериолит), капилляры (капиллярит), ве ны (флебит), лимфатические сосуды(лимфангит). Однако при разных видах васкулитов поражаются преимущественно сосуды определенного калибра: аорта и ее крупные ветви, крупные, средние и мелкие артерии (эластически-
мышечного и мышечного типа), мелкие артерии и сосуды микроциркуляторного русла, вены.
Изменения в органах и тканях в связи с развитием васкулита носят вторичный характер и представлены инфарктами, постинфарктным крупноочаговым и ишемическим мелкоочаговым склерозом, атрофией паренхиматозных элементов, гангреной, кровоизлияниями. Помимо местных, могут наблюдаться общие изменения, связанные с васкулитом питающего тот или иной орган сосуда. Так, при вовлечении в процесс почечных артерий развивается ренальная гипертензия, сосудов легких - гипертония малого круга и симптом легочно-сердечной недостаточности, сосудов кожи - геморрагический диатез.
Этиология и патогенез. Этиология подавляющего большинства первичных системных васкулитов неизвестна. Патогенез системных васкулитов (как первичных, так и вторичных) связан с иммунными реакциями гиперчувствительности, возникающими на различные антигены. В зависимости от преобладания того или иного механизма гиперчувствительности системные васкулиты делят на три группы: 1) васкулиты гиперчувствительности немедленного типа; 2) васкулиты гиперчувствительности замедленного типа; 3) васкулиты гиперчувствительности смешанного типа. При ведущей роли гиперчувствительности немедленного типа (иммунокомплексное повреждение сосудистой стенки) преобладают альтеративные (фибриноидные изменения, вплоть до некроза) и экссудативные (инфильтрация стенки полиморфно-ядерными лейкоцитами, макрофагами) процессы, развиваются деструктивные (некротические) васкулиты, чаще некротические артерииты (узелковый периартериит, синдром Вегенера, аллергический гранулематоз, васкулиты при ревматических заболеваниях, «ангииты повышенной гиперчувствительности»). При преобладании гиперчувствительности замедленного типа основное значение приобретают клеточные реакции в виде лимфогистиоцитарных инфильтратов и образование гранулем. Возникают продуктивные васкулиты, в том числе гранулематозные артерииты (болезнь Такасу, болезнь Хортона). Васкулиты, обусловленные гиперчувствительностью немедленного типа и характеризующиеся деструктивным характером изменений, обычно протекают остро, а васкулиты, обусловленные гиперчувствительностью замедленного и смешанного типа, имеющие характер продуктивных, гранулематозных, - подостро и хронически.
Классификация системных васкулитов учитывает следующие критерии (Серов В.В., Коган А.Е., 1982): этиологию, патогенез, нозологическую принадлежность, преимущественный характер и распространенность воспалительной реакции, морфологический тип пораженных сосудов, преимущественную локализацию, обусловливающую заинтересованность определенных органов (органная патология), клиническую картину заболевания. При этом следует придерживаться нозологического принципа, на основании которого васкулиты разделены на первичные и вторичные.
Классификация системных васкулитов (по Серову В.В. и Коган Е.А., 1982) А. Первичные васкулиты.
I. С преимущественным поражением аорты и ее крупных ветвей и гигантоклеточной гранулематозной реакцией: неспецифический аортоартериит (болезнь Такаясу), височный артериит (болезнь Хортона).
II. С преимущественным поражением артерий среднего и мелкого калибра и деструктивно- продуктивной реакцией: 1) узелковый периартериит; 2) аллергический гранулематоз; 3) системный некротизирующий васкулит; 4) гранулематоз Вегенера; 5) лимфатический синдром с поражением кожи и слизистых оболочек.
III. С преимущественным поражением артерий мелкого калибра, сосудов микроциркуляторного русла и вен: облитерирующий тромбангит (болезнь Бюргера).
IV. С поражением артерий различных калибров - смешанная (неклассифицируемая) форма.
Б. Вторичные васкулиты.
V. При инфекционных заболеваниях: 1) сифилитические; 2) туберкулезные; 3) риккетсиозные, в том числе сыпнотифозные; 4) септические; 5) прочие.
VI. При системных заболеваниях соединительной ткани: 1) ревматические; 2) ревматоидные; 3) волчаночные.
VII. Васкулиты «гиперчувствительности» при: 1) сывороточной болезни; 2) пурпуре Шенлейна- Геноха; 3) эссенциальной смешанной криоглобулинемии; 4) злокачественных новообразованиях.
Среди первичных системных васкулитов наибольшее значение имеют неспецифический аортоартериит, узелковый периартериит, гранулематоз Вегенера и облитерирующий тромбангит. Вторичные системные васкулиты описаны в главах, посвященных инфекционным и ревматическим заболеваниям.
135. Атеросклероз: определение, этиология, патогенез. Макро- и микроскопические изменения артерий, осложнения, исходы, клиническое значение.
Атеросклероз (от греч. athere - кашица и sklerosis - уплотнение) - хроническое заболевание, возникающее в результате нарушения жирового и белкового обмена, характеризующееся поражением артерий эластического и мышечно- эластического типа в виде очагового отложения в интиме липидов и белков и реактивного разрастания соединительной ткани.
В развитии атеросклероза наибольшее значение имеют следующие фак- торы: 1) обменные; 2) гормональные; 3) гемодинамические; 4) нервные; 5) со- судистые; 6) наследственные и этнические.
Патогенез атеросклероза учитывает все факторы, способствующие его развитию, но при этом прежде всего те, которые ведут к атерогенной липопротеидемии и повышению проницаемости мембран стенки артерий. С ними связано в дальнейшем повреждение эндотелия артерий, накопление плазменных модифицированных липопротеидов (ЛПОНП, ЛПНП) в интиме, нерегулируемый захват атерогенных липопротеидов клетками интимы, пролиферация в ней гладкомышечных клеток и макрофагов с последующей трансформацией в так называемые пенистые клетки, которые причастны к развитию всех атеросклеротических изменений.
Патологическая анатомия и морфогенез. Сущность процесса хорошо отражает термин: в интиме артерий появляются кашицеобразный жиробелковый детрит (athere) и очаговое разрастание соединительной ткани (sclerosis), что приводит к формированию атеросклеротической бляшки, суживающей просвет сосуда. Обычно поражаются, как уже упоминалось, артерии эластического и мышечно-эластического типа, т.е. артерии крупного и среднего калибра; значительно реже в процесс вовлекаются мелкие артерии мышечного типа.
Атеросклеротический процесс проходит определенные стадии (фазы), которые имеют макроскопическую и микроскопическую характеристику (морфогенез атеросклероза).
При макроскопическом исследовании различают следующие виды атеросклеротических изменений, отражающие динамику процесса (рис. 142, 143, см. на цв. вкл.): 1) жировые пятна или полоски; 2) фиброзные бляшки; 3) осложненные поражения, представленные фиброзными бляшками с изъязвлением, кровоизлияниями и наложениями тромботических масс; 4) кальциноз, или атерокальциноз.
Жировые пятна или полоски - это участки желтого или желто-серого цвета (пятна), которые иногда сливаются и образуют полоски, но не возвышаются над поверхностью интимы. Они содержат липиды, выявляемые
при тотальной окраске сосуда красителями на жиры, например Суданом. Раньше всего жировые пятна и полоски появляются в аорте на задней стенке и у места отхождения ее ветвей, позже - в крупных артериях.
У 50% детей в возрасте моложе 1 года можно обнаружить в аорте липидные пятна. В юношеском возрасте липидоз усиливается, жировые пятна появляются не только в аорте, но и в венечных артериях сердца. С возрастом изменения, характерные для физиологического раннего липидоза, в подавляющем большинстве случаев исчезают и не являются источником развития дальнейших атеросклеротических изменений.
Фиброзные бляшки - плотные, овальные или круглые, белые или беложелтые образования, содержащие липиды и возвышающиеся над поверхностью интимы. Часто они сливаются между собой, придают внутренней поверхности сосуда бугристый вид и резко суживают его просвет (стенозирующий атеросклероз). Наиболее часто фиброзные бляшки наблюдаются в брюшной аорте, в отходящих от аорты ветвях, в артериях сердца, мозга, почек, нижних конечностей, сонных артериях и др. Чаще поражаются те участки сосудов, которые испытывают гемодинамическое (механическое) воздействие (в областях ветвления и изгибов артерий, на стороне их стенки, которая имеет жесткую подстилку).
Осложненные поражения возникают в тех случаях, когда в толще бляшки преобладает распад жиробелковых комплексов и образуется детрит, напоминающий содержимое ретенционной кисты сальной железы, т.е.атеромы. Поэтому такие изменения называют атероматозными. Прогрессирование атероматозных изменений ведет к деструкции покрышки бляшки, ее изъязвлению (атероматозная
язва), кровоизлияниям в толщу бляшки (интрамуральная гематома) и образованию тромботических наложений на месте изъязвления бляшки. С осложненными поражениями связаны: острая закупорка артерии тромбом и развитие инфаркта, эмболия как тромботическими, так и атероматозными массами, образование аневризмы сосуда в месте его изъязвления, а также артериальное кровотечение при разъедании стенки сосуда атероматозной язвой.
Кальциноз, или атерокальциноз, - завершающая фаза атеросклероза, которая характеризуется отложением в фиброзные бляшки солей кальция, т.е. их обызвествлением. Бляшки приобретают каменистую плотность(петрификация бляшек), стенка сосуда в месте петрификации резко деформируется.
Различные виды атеросклеротических изменений нередко сочетаются: в одном и том же сосуде, например в аорте, можно видеть одновременно жировые пятна и полосы, фиброзные бляшки, атероматозные язвы с тромбами и участки атерокальциноза (см. рис. 142, 143), что свидетельствует о волнообразности течения атеросклероза.
Микроскопическое исследование позволяет уточнить и дополнить характер и последовательность развития изменений, свойственных атеросклерозу. На основании его результатов выделены следующие стадии морфогенеза атеросклероза (рис. 144): 1) долипидная; 2) липоидоз; 3) липосклероз; 4) атероматоз; 5) изъязвление; 6) атерокальциноз.
Долипидная стадияхарактеризуется изменениями, отражающими общие нарушения метаболизма при
атеросклерозе (гиперхолестеринемия, гиперлипопротеидемия, накопление грубодисперсных белков и мукоидных веществ в плазме крови, повышение активности гиалуронидазы и т.д.) и «травму» интимы продуктами нарушенного метаболизма. К этим изменениям относятся: 1) повышение проницаемости эндотелия и мембран интимы, что ведет к накоплению во внутренней оболочке белков плазмы, фибриногена (фибрина) и образованию плоских пристеночных тромбов; 2) накопление кислых гликозаминогликанов в интиме, с чем связано появление мукоидного отека внутренней оболочки, а поэтому благоприятных условий для фиксации в ней липопротеидов очень низкой и низкой плотности, холестерина, белков (рис. 145); 3) деструкция эндотелия, базальных мембран интимы, эластических и коллагеновых волокон, способствующая еще большему повышению проницаемости интимы для продуктов нарушенного обмена и пролиферации гладкомышечных клеток.
Продолжительность долипидной стадии определяется возможностью липолитических и протеолитических (фибринолитических) ферментов интимы «очищать» ее от «засорения» продуктами нарушенного метаболизма. Как правило, активность этих ферментов интимы в долипидной стадии повышена, истощение их знаменует начало стадии липоидоза.
В стадии липоидоза отмечается очаговая инфильтрация интимы, особенно поверхностных ее отделов, липидами (холестерином), липопротеидами, белками (рис. 146), что ведет к образованию жировых пятен иполос. Липиды диффузно пропитывают интиму и накапливаются в гладкомышечных клетках и макрофагах, которые получили название пенистых, или ксантомных, клеток (от греч.xanthos - желтый). В эндотелии также появляются липидные включения, что свидетельствует об инфильтрации интимы липидами плазмы крови. Отчетливо выражены набухание и деструкция эластических мембран.
Липосклероз характеризуется разрастанием молодых соединительнотканных элементов интимы в участках отложения и распада липидов и белков, разрушением эластических и аргирофильных мембран. Очаговое разрастание в интиме молодой соединительной ткани и ее последующее созревание ведут к формированиюфиброзной бляшки (рис. 147), в которой появляются тонкостенные сосуды, связанные с vasa vasorum.Существует точка зрения, что формирование фиброзной бляшки связано с пролиферацией гладкомышечных клеток, возникающей в ответ на повреждение эндотелия и эластических волокон артерий.
При атероматозе липидные массы, составляющие центральную часть бляшки, а также прилежащие коллагеновые и эластические волокна распадаются (рис. 148). При этом образуется мелкозернистая аморфная масса, в которой обнаруживаются кристаллы холестерина и жирных кислот, обрывки эластических и коллагеновых волокон, капельки нейтральных жиров (атероматозный детрит). В краях у основания бляшки появляются много новообразованных сосудов, врастающих из vasa vasorum, а также ксантомные клетки, лим-
фоциты, плазматические клетки. Атероматозные массы отграничены от просвета сосуда слоем зрелой, иногда гиалинизированной, соединительной ткани (покрышка бляшки). В связи с тем что атероматозному распаду подвергаются гладкие мышечные волокна средней оболочки, бляшка «погружается» довольно глубоко, достигая в некоторых случаях адвентиции. Атероматоз - начало осложненных поражений. При прогрессировании атероматоза в связи с разрушением новообразованных сосудов происходит кровоизлияние в толщу бляшки (интрамуральная гематома), покрышка бляшки разрывается. Наступает стадия изъязвления,характеризующаяся образованием атероматозной язвы. Края ее подрытые, неровные, дно образовано мышечным, а иногда наружным, слоем стенки сосуда. Дефект интимы очень часто покрывается тромботическими наложениями, причем тромб может быть не только пристеночным, но и обтурирующим.
Атерокальциноз - завершающая стадия морфогенеза атеросклероза, хотя отложение извести начинается уже в стадии атероматоза и даже липосклероза. Известь откладывается в атероматозные массы, в фиброзную ткань, в межуточное вещество между эластическими волокнами. При значительных отложениях извести в покрышке бляшки образуются плотные и ломкие пластинки. Обызвествлению бляшек способствует эластолиз. В связи с деструкцией эластических мембран происходит накопление аспарагиновой и глутаминовой кислот. Ионы кальция связываются со свободными карбоксильными группами этих кислот и осаждаются в виде фосфата кальция.
Морфогенез атеросклероза в значительной мере определяет выделение клинических периодов и стадий болезни.
Морфологическое обоснование получило и волнообразное течение атеросклероза, складывающееся из чередований фаз прогрессирования (активная фаза), стабилизации (неактивная фаза) и регрессирования.Прогрессирование атеросклероза характеризуется морфологией волны липоидоза, которая наслаивается на старые изменения (липосклероз, атероматоз, атерокальциноз) и ведет к развитию осложненных поражений (атероматоз, кровоизлияние в толще бляшки, тромбоз). Следствием раз-
вивающейся острой ишемии органов и тканей становятся инфаркт, гангрена, кровоизлияния. Прирегрессировании атеросклероза происходят макрофагальная резорбция и вымывание липидов из бляшек, разрастание соединительной ткани увеличивается. Хроническая ишемия органов и тканей усиливается, что ведет к дистрофии и атрофии паренхиматозных элементов, нарастанию склероза интерстиция.
Осложнения атеросклероза очень разнообразны и опасны. Наиболее частые: ишемическая болезнь сердца; инфаркт миокарда (в 95% случаев возникает на фоне стенозирующего атеросклероза коронарных артерий); транзиторно-ишемическая атака; острое нарушение мозгового кровообращения (инфаркт мозга, геморрагический инсульт); вторичная мезентериальная недостаточность и мезентериальный тромбоз; аневризма аорты; гангрена кишки или конечности, возникающая в результате острой непроходимости артериального сосуда, как следствие стенозирующего атеросклероза; хроническая почечная недостаточность.
Может произойти один из 5 исходов:
• Образовавшийся тромб может организоваться и встроиться в бляшку, что приводит к изменению структуры и быстрому ее росту.
• Тромб может быстро закрыть просвет сосуда, что приводит к острому ишемическому событию.
• Развитие тромботической эмболии.
• Заполнение бляшки кровью, увеличение ее в размере с быстрой окклюзией артерии.
• Развитие эмболии содержимым бляшки (отличным от тромботических масс), приводящей к окклюзии более дистальных сосудов.
136. Атеросклероз: определение понятия.
Атеросклероз – хроническое волнообразно текущее прогрессирующее за- болевание преимущественно лиц пожилого возраста, возникающее в резуль- тате нарушения жиро‐белкового обмена, характеризующееся деструктивно‐ пролиферативными и склеротическими изменениями стенок крупных арте- рий с формированием на их внутренней поверхности атеросклеротических бляшек, обусловливающих нарушение гемодинамики в органах.
Атеросклероз характеризуется образованием неоднородных бляшек (атером) в интиме средних и крупных артерий; бляшки содержат липиды, воспалительные клетки, гладкомышечные клетки и соединительную ткань. Факторы риска включают дислипидемию, сахарный диабет, курение, семейную предрасположенность, сидячий образ жизни, ожирение и АГ. Симптомы появляются с увеличением размеров или при разрыве бляшки, когда уменьшается или прекращается кровоток; картина заболевания зависит от пораженной артерии.
137. Атеросклероз: определение, строение стабильной и нестабильной атеросклеротических бляшек. Осложнения и причины смерти больных.
Атеросклероз – хроническое заболевание артерий эластического и мышечно-эластического типа, обусловленное нарушением жиро-белкового обмена и характеризующееся отложением белков и липидов в интиме сосудов, реактивным разрастанием соединительной ткани, последующим склерозом и кальцинозом, формированием бляшек со стенотическим поражением сосудов, приводящим к органным или общим расстройствам кровообращения.
Осложнения:
Ишемические:
Острая ишемия-тромбоз,ТЭ,кровоизлияние в бляшку, эмболия фрагментами бляшки
Хроническая прогрессирующая ишемия-если бляшка стабильна и медленно растет
Деструктивные
Образование аневризмы
Расслаивание стенки сосуда излевшейся кровью
Сдавление бляшкой окр.тканей/органов
Причины смерти:
При атеросклерозе смерть наступает в результате ишемической болезни сердца, ишемического инфаркта головного мозга, гангрены кишечника или нижних конечностей, разрыва аневризмы аорты
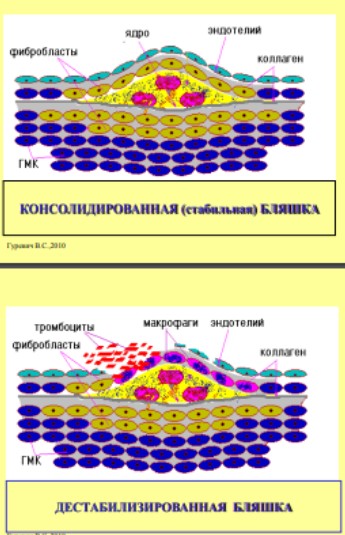
СТАБИЛЬНАЯ И НЕСТАБИЛЬНАЯ
Нестабильная бляшка — это образование на основе жира (большая часть). Такие наросты характеризуются рыхлой структурой, за счет чего повышается вероятность их разрыва. В результате такого процесса формируется тромб, который перекрывает кровоток. Это смертельно опасно.

Строение атеросклеротической бляшки стабильного типа будет немного отличаться составом. Большая часть такого нароста состоит из коллагеновых волокон, что делает его более эластичным. Вероятность разрыва в этом случае будет значительно ниже. Главное отличие стабильных бляшек — постоянство и медленное развитие. Из минусов — за счет кальцинирования наросты стабильны, что с одной стороны очень хорошо, но с другой стороны, такие бляшки не рассасываются.
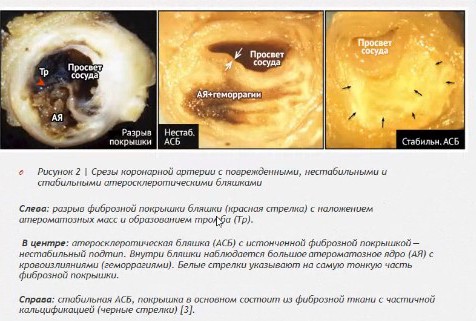
138. Клинико-анатомические формы атеросклероза и связанные с ними осложнения.
Клинико-морфологические формы:
1. Атеросклероз аорты – осложняется истончением стенки аорты, ее расширением (аневризмой), разрывом аневризмы; возможен пристеночный тромбоз.
(Проявления АА)Характеризуется обычно атероматозом, изъязвлениями, атерокальцинозом.
В связи с этим атеросклероз аорты часто осложняется тромбозом, тромбоэмболией и эмболией атероматозными массами с развитием инфарктов (например, почек) и гангрены (например, кишечника, нижней конечности).
Нередко на почве атеросклероза развивается аневризма аорты ,, т.е. выбухание стенки в месте ее поражения, чаще изъязвления. Аневризма может иметь различную форму, в связи с чем различают цилиндрическую, мешковидную, грыжевидную аневризмы. Стенку аневризмы в одних случаях образует аорта (истинная аневризма), в других - прилегающие к ней ткани и гематома (ложная аневризма). Если кровь отслаивает среднюю оболочку аорты от интимы или от адвентиция, что ведет к образованию покрытого эндотелием канала, то говорят о расслаивающей аневризме. Образование аневризмы чревато ее разрывом и кровотечением. Длительно существующая аневризма аорты приводит к атрофии окружающих тканей (например, грудины, тел позвонков).
2. Атеросклероз венечных артерий (коронарных) – группа ишемических болезней сердца (ИБС).
3. Атеросклероз сосудов головного мозга – цереброваскулярные болезни (ЦВБ).
Длительная ишемия головного мозга на почве стенозирующего атеросклероза мозговых артерий приводит к дистрофии и атрофии коры мозга, развитию атеросклеротического слабоумия.
4. Атеросклероз почечных артерий – осложнения при этом связаны с острыми и хроническими нарушениями кровообращения (острые – инфаркт почек, хронические – атрофия, склероз).
сужение просвета бляшкой обычно наблюдается у места ответвления основного ствола или деления его на ветви первого и второго порядка. Чаще процесс односторонний, реже - двусторонний. В почках развиваются либо клиновидные участки атрофии паренхимы с коллапсом стромы и замещением этих участков соединительной тканью, либо инфаркты с последующей организацией их и формированием втянутых рубцов. Возникает крупнобугристая атеросклеротическая сморщенная почка (атеросклеротический нефросклероз), функция которой страдает мало, так как большая часть паренхимы остается сохранной. В результате ишемии почечной ткани при стенозирующем атеросклерозе почечных артерий в ряде случаев развивается симптоматическая (почечная) гипертония.
5. Атеросклероз артерий кишечника – острые нарушения кровообращения – гангрена, хронические – ишемический колит.
6. Атеросклероз сосудов нижних конечностей – острое – гангрена, хронические – атрофия, «перемежающаяся хромота» .
чаще поражаются бедренные артерии. Процесс длительное время протекает бессимптомно благодаря развитию коллатералей. Однако при нарастающей недостаточности коллатералей развиваются атрофические изменения мышц, похолодание конечности, появляются характерные боли при ходьбе - перемежающаяся хромота. Если атеросклероз осложняется тромбозом, развивается гангрена конечности - атеросклеротическая гангрена.
139. Симптоматические артериальные гипертензии: причины, механизмы развития, осложнения, причины смерти больных.
Симптоматические гипертонии – артериальная гипертензия, развившаяся на фоне какого-либо . заболевания
Основные причины:
1. Заболевания почек и мочевыводящих путей (почечная, или нефрогенная, гипертония): гломерулонефриты, пиелонефрит, гидронефроз, нефросклероз, диабетическая и печеночная нефропатии, амилоидоз почек, врожденные аномалии, поликистоз почек, опухоли.
2. Эндокринной заболевания: первичный и вторичный гиперальдостеронизм, болезнь и синдром Иценко-Кушинга, диффузный тиреотоксический зоб, опухоли надпочечников (феохромоцитома).
3. Поражения центральной нервной системы, в том числе сопровождающиеся повышением внутричерепного давления: абсцесс, кровоизлияние, опухоли и травмы мозга; поражения гипоталамуса и ствола мозга.
4. Сосудистые заболевания: атеросклероз дуги и коарктация аорты на разных уровнях, сужение крупных артерий (подключичной, сонной), системный васкулит, сужение устьев и аномалии почечных артерий (реноваскулярная гипертония). Увеличение ОЦК ятрогенного характера.
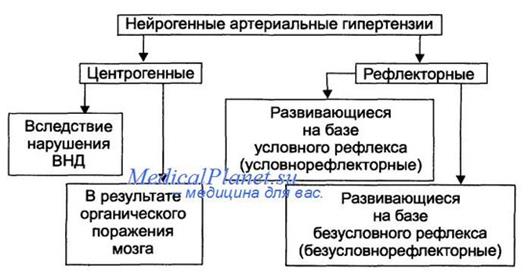
В развитии гипертонической болезни имеют значение следующие факторы:
1) нервный фактор объясняет развитие артериальной гипертензии истощением центров сосудистой регуляции с вовлечением в процесс рефлекторных и гуморальных факторов. При психоэмоциональном перенапряжении, хронических стрессах в коре головного мозга возникают очаги возбуждения, распространяющиеся на подкорковые узлы и сосудодвигательный центр. Происходит нарушение нервной регуляции периферического кровообращения, развиваются ангиоспазмы, повышается кровяное давление.
2) рефлекторный: определенное значение в механизме развития гипертонической болезни имеют выключение депрессорных влияний каротидного синуса, дуги аорты и активация симпатической нервной системы.
3) гормональный: в возникновении стойкой артериальной гипертензии играют роль усиление прессорных влияний гипофизарно-диэнцефальной области, избыточное выделение катехоламинов, и активация ренин-ангиотензиновой системы.
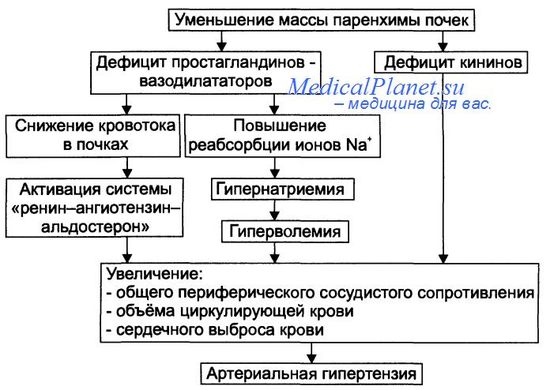
4) почечный: почки обладают тремя основными системами, принимающими участие в регуляции артериального давления, дисбаланс которых создает предпосылки для развития артериальной гипертензии:
а) ренин-ангиотензиновая система. Посредством выработки ренина образуется ангиотензин II, который увеличивает периферическое сопротивление и объем циркулирующей крови, вызывая вазоконстрикцию путем воздействия на гладкомышечную оболочку сосудов либо путем стимуляции секреции альдостерона, повышающего реабсорбцию натрия и воды в канальцах;
б) гомеостаз натрия. С уменьшением объема циркулирующей крови снижается скорость клубочковой фильтрации, повышается реабсорбция натрия с одной стороны. С другой – натрийуретический пептид, вырабатываемый мышечной тканью предсердий в ответ на их расширение, тормозит реабсорбцию натрия и способствует вазодилатации;
в) почечные вазодепрессорные субстанции. Почки вырабатывают простагландины, мочевую калликреин-кининовую систему, фактор, активирующий тромбоциты, окись азота, «уравновешивающие» вазопрессорный эффект ангиотензина.
5) наследственный: предполагают генетически детерминированные генетические нарушения в почках, затрагивающие реабсорбцию натрия, или в гладкой мускулатуре сосудов, регулирующие транспорт натрия и кальция.

Осложнения :
- гипертрофия левого желудочка сердца
- ИБС
- гипертонические кризы с транзиторной ишемией различной локализации
- ишемические инсульты (инфаркты мозга)
- геморрагические инсульты
- протеинурия в результате повреждения сосудов клубочков
- почечная недостаточность
- ретинопатия
- аневризмы аорты, ее разрывы
- облитерирующий эндартериит
- экстракраниальные стенозы сонных артерий
Мозговые инсульты - частая причина смерти больных атеросклерозом и гипертонической болезнью.
140. Изменения в головном мозге при артериальной гипертензии и связанные с этим осложнения.
Цереброваскулярные заболевания характеризуются острыми нарушениями мозгового кровообращения, фоном для развития которых являются атеросклероз и гипертоническая болезнь. По своему существу - это церебральные проявления атеросклероза и гипертонической болезни, реже - симптоматических гипертензий.
Классификация:
1.Транзиторная ишемия
2.Инсульт-остарое локальное расстройство мозгвоого кровообращения, сопровождающееся повреждением вещества мозга и нарушениями его функций
Геморрагический инсульт(гематома, геморрагическое пропитывание)
Ишемический инсульт(ишемический, геморрагический,смешанный инфаркт)
Транзиторная ишемия представлена сосудистыми расстройствами (спазм артериол, плазматическое пропитывание ихстенок, периваскулярный отек и единичные мелкие геморрагии) и очаговыми изменениями мозговой ткани (отек, дистрофические изменения групп клеток). Эти изменения обратимы; на месте бывших мелких геморрагий могут определяться периваскулярные отложения гемосидерина.
При образовании гематомы мозга, которая встречается в 85% при геморрагическом инсульте, находят выраженную альтерацию стенок артериол и мелких артерий с образованием микроаневризм и разрывом их стенок. В месте кровоизлияния ткань мозга разрушается, образуется полость, заполненная свертками крови и размягченной тканью мозга (красное размягчение мозга). Кровоизлияние локализуется чаще всего в подкорковых узлах головного мозга (зрительный бугор, внутренняя капсула) и мозжечке. Размеры его бывают разными: иногда оно охватывает всю массу подкорковых узлов, кровь прорывается в боковые, III и IV желудочки мозга, просачивается в область его основания (рис. 164). Инсульты с прорывом в желудочки мозга всегда заканчиваются смертью. Если больной переживает инсульт, то по периферии кровоизлияния в ткани мозга появляется много сидерофагов, зернистых шаров, клеток глии и свертки крови рассасываются. На месте гематомы образуется киста с ржавыми стенками и буроватым содержимым
При геморрагическом пропитывании вещества мозга как разновидности геморрагического инсульта обнаруживают мелкие сливающиеся очаги кровоизлияний. Среди пропитанного кровью мозгового вещества определяются нервные клетки с некробиотическими изменениями. Кровоизлияния типа геморрагического пропитывания встречаются обычно в зрительных буграх и мосту мозга (варолиев мост) и, как правило, не возникают в коре мозга и мозжечке.
Ишемический инфаркт мозга, образующийся при тромбозе атеросклеротически измененных прецеребральных или церебральных артерий, имеет разнообразную локализацию. Это - самое частое (75% случаев) проявление ишемического инсульта. Выглядит ишемический инфаркт как очаг серого размягчения мозга. При микроскопическом исследовании среды некротических масс можно обнаружить погибшие нейроны.
Геморрагический инфаркт мозга внешне напоминает очаг геморрагического пропитывания, но механизм его развития другой: первично развивается ишемия мозговой ткани, вторично - кровоизлияния в ишемизированную ткань. Чаще геморрагический инфаркт встречается в коре мозга, реже - в подкорковых узлах.
При смешанном инфаркте, который всегда возникает в сером веществе мозга, можно найти участки как ишемического, так и геморрагического инфаркта. На месте инфарктов мозга, как и гематомы, образуются кисты, причем стенка кисты на месте геморрагического инфаркта содержит скопление гемосидерина («ржавая киста»).
Осложнения инсультов (кровоизлияний и инфарктов мозга), как и их последствий (кисты мозга), - паралич. Мозговые инсульты - частая причина смерти больных атеросклерозом и гипертонической болезнью.

141. Гипертоническая болезнь: этиология, патогенез, патологическая анатомия, причины смерти.
Гипертоническая болезнь (ГБ) - это хроническое заболевание, основным клиническим признаком которого является длительное и стойкое повышение артериального давления систолического выше 140 мм.рт.ст. и диастолического выше 90 мм.рт.ст.

Также алкоголь, курение, ожирение, избыточное потребление соли
Патогенез. В механизме развития гипертонической болезни участвует ряд факторов:
1) нервный;
2) рефлекторные;
3) гормональные;
4) почечный;
5) наследственные.

Считают, что психоэмоциональное перенапряжение (нервный фактор) ведет к истощению центров сосудистой регуляции с вовлечением в патогенетический механизм рефлекторных и гуморальных факторов. Среди рефлекторных факторов следует учитывать возможное выключение депрессорных влияний каротидного синуса и дуги аорты, а также активацию симпатической нервной системы.
Среди гормональных факторов имеют значение усиление прессорных влияний гипофизарнодиэнцефальной области (гиперплазия клеток задней и передней долей гипофиза), избыточное выделение катехоламинов (гиперплазия мозгового вещества надпочечников) и активация ренин-гипертензивной системы в результате нарастающей ишемии почек (гиперплазия и гипергранулярность клеток юкстагломерулярного аппарата, атрофия интерстициальных клеток мозгового вещества почек).
Почечному фактору в патогенезе гипертонической болезни придается исключительное значение, так как экскреция почками натрия и воды,секреция ими ренина, кининов и простагландинов - один из основных механизмов регуляции артериального давления.
В системе кровообращения почка выполняет роль своеобразного регулятора, определяющего величину систолического артериального давления и обеспечивающего по механизму обратной связи его долгосрочную стабилизацию на определенном уровне (баростатная функция почки). Обратную связь в этой системе осуществляют нервные и эндокринные механизмы регуляции артериального давления: автономная нервная система с баро- и хеморецепторами и центрами сосудистой регуляции в стволе головного мозга, ренин- ангиотензиновая система, нейроэндокринная система (вазопрессин, окситоцин), кортикостероиды, натрий-уретический гормон и предсердный натрийуретический фактор. В связи с этим обязательным условием развития хронической артериальной гипертензий становится смещение кривой зависимости выделительной функции почки от величины систолического артериального давления в сторону более высоких ее значений. Этот феномен получил название «переключения почки» (Гайтон А., 1980), которое сопровождается сокращением приносящих артериол, торможением работы противоточно- множительной системы почек, усилением реабсорбции воды в дистальных канальцах.
Наследственный фактор- экскреторные и инкреторные функции почек, регулирующие уровень артериального давления, могут быть детерминированы генетически

Причины смерти при гипертонической болезни:
1. Кровоизлияние в мозг (геморрагический инсульт) развивается на фоне изменений в стенке артериол (спазм, плазматическое пропитывание, разрывы эластических мембран и формированием микроаневризм с последующим их разрывом).
2. Хроническая сердечная недостаточность с застоем в МКК и БКК.
3. Острый инфаркт миокарда из-за дефицита кислорода при гипертрофии миокарда.
4. Хроническая почечная недостаточность (уремия).
142. Клинико-морфологические формы гипертонической болезни, патологическая анатомия, причины смерти. Связан с 143
Сердечная форма гипертонической болезни, как и сердечная форма атеросклероза, составляет сущность ишемической болезни сердца (см. Ишемическая болезнь сердца).
Мозговая форма гипертонической болезни в настоящее время стала основой цереброваскулярных заболеваний (см. Цереброваскулярные заболевания).
Почечная форма гипертонической болезни характеризуется как острыми, так и хроническими изменениями:
А) К острым изменениям относятся инфаркты почек и артериолонекроз почек. Инфаркты почек появляются при тромбоэмболии или тромбозе артерий. Иногда они бывают субтотальными или тотальными. Артериолонекроз почек - морфологическое выражение злокачественной гипертонии. Помимо артериол, фибриноидному некрозу подвергаются капиллярные петли клубочков, в строме возникают отек и геморрагии, в эпителии канальцев - белковая дистрофия. В ответ на некроз в артериолах, клубочках и строме развиваются клеточная реакция и склероз (злокачественный нефросклероз Фара). Почки выглядят несколько уменьшенными в размерах, пестрыми, поверхность их мелкогранулярная.
Исход: Артериолонекроз приводит к острой почечной недостаточности и заканчивается обычно летально при отсутствии возможности проведения гемодиализа.
Б) Изменения почек при хроническом доброкачественном течении гипертонической болезни связаны с гиалинозом артериол, артериолосклерозом. Гиалиноз артериол сопровождается коллапсом капиллярных петель и склерозом клубочков - гломерулосклерозом. В результате недостаточного кровоснабжения и гипоксии канальцевая часть большинства нефронов атрофируется и замещается соединительной тканью, которая разрастается также вокруг погибших клубочков. На поверхности почек появляются множественные мелкие очаги западения. Нефроны, соответствующие относительно сохранным клубочкам, гипертрофируются (регенерационная гипертрофия почек) и выступают над почечной поверхностью в виде серо-красных гранул. Почки выглядят маленькими, плотными, поверхность их мелкогранулярная, паренхима атрофична, особенно истончено корковое вещество. Такие почки, являющиеся исходом их склероза на почве гиалиноза артериол (артериолосклеротический нефросклероз), называют первично-сморщенными . Клиническое выражение артериолосклеротического нефросклероза -хроническая почечная недостаточность, завершающаяся азотемической уремией.
Изменения глаз при гипертонической болезни вторичные, связанные с характерными изменениями сосудов. Они представлены отеком соска зрительного нерва, кровоизлияниями, отслойкой сетчатки, белковым выпотом и отложением в ней белковых масс, некрозом сетчатки и тяжелыми дистрофическими изменениями нервных клеток ганглиозного слоя.
Изменения эндокринных желез: в надпочечниках происходит гиперплазия мозгового и коркового слоев с образованием в последнем регенераторных аденом. В дальнейшем эти изменения сменяются атрофическими. В передней доле гипофиза отмечается гиперплазия базофильных клеток, как и клеток задней доли, выделяющих вазопрессорные вещества. В других органах нередко возникают изменения, служащие проявлением гипертонических кризов или следствием хронической гипоксии.
Причины смерти при гипертонической болезни:
1. Кровоизлияние в мозг (геморрагический инсульт) развивается на фоне изменений в стенке артериол (спазм, плазматическое пропитывание, разрывы эластических мембран и формированием микроаневризм с последующим их разрывом).
2. Хроническая сердечная недостаточность с застоем в МКК и БКК.
3. Острый инфаркт миокарда из-за дефицита кислорода при гипертрофии миокарда.
4. Хроническая почечная недостаточность (уремия).
143. Патологическая анатомия доброкачественной гипертонической болезни, причины смерти.

Доброкачественная гипертензия 3 стадии:
1) доклиническую;
2) распространенных изменений артерий;
3) изменений органов в связи с изменением артерий и нарушением внутриорганного кровообращения.
Однако следует учитывать, что в любой стадии доброкачественной гипертензии может возникнуть гипертонический криз с характерными для него морфологическими проявлениями.
1.О доклинической стадии гипертонической болезни говорят в тех случаях, когда появляются эпизоды временного повышения артериального давления (транзиторная гипертензия).
В этой стадии находят гипертрофию мышечного слоя и эластическихструктур артериол и мелких артерий, морфологические признаки спазма артериол или более глубокие их изменения в случаях гипертонического криза. Отмечается умеренная компенсаторная гипертрофия левого желудочка сердца.
2.Стадия распространенных изменений артерий характеризует период стойкого повышения артериального давления. В артериолах, артериях эластического, мышечно-эластического и мышечного типов, а также в сердце возникают характерные изменения.
1)Плазматическое пропитывание-под действием повышенного АД происходит пропитывание компонентами плазмы крови интимы и медии стенок артериол
2)гиалиноз-белки плазмы остаются и превращаются в гиалин, который в дальнейшем замещается фиброзной тканью---(3)
3)склероз
Плазматическое пропитывание артериол и мелких артерий развивается в связи с гипоксическим повреждением эндотелия, его мембраны, мышечных клеток и волокнистых структур стенки, к которому ведет спазм сосуда. Элементы деструкции стенки, как и пропитывающие ее белки и липиды, резорбируются с помощью, макрофагов, однако эта резорбция, как правило, неполная.
Затем белковые массы уплотняются и превращаются в гиалиноподобные, просвет сосуда резко сужается, стенка теряет свои основные функциональные свойства, а именно способность отвечать изменением просвета на те или иные физиологические импульсы. Развивается гиалиноз артериол (артериолосклероз). Наиболее часто гиалинозу подвергаются артериолы и мелкие артерии почек, сетчатки глаза, головного мозга
Изменения артерий эластического, мышечно-эластического и мышечного типов представлены эластофиброзом и атеросклерозом. Эластофиброз характеризуется гиперплазией и расщеплением внутренней эластической мембраны, развивающимися компенсаторно в ответ на стойкое повышение артериального давления, и разрастанием между расщепившимися мембранами соединительной ткани, т.е. склерозом.
При стойкой и длительной артериальной гипертонии развивается выраженный атеросклероз, который отличается некоторым своеобразием: атеросклеротические изменения имеют более распространенный характер, «спускаясь» в артерии мышечного типа, чего не наблюдается при отсутствии гипертонии; при гипертонии фиброзные бляшки располагаются циркулярно, а не сегментарно, что ведет к более резкому сужению просвета сосуда.
Эластофиброз и стенозирующий атеросклероз резко выражены в артериях сердца, мозга, почек, поджелудочной железы, в сонных и позвоночныхартериях.
В этой стадии гипертрофия миокарда нарастает, масса сердца может достигать 900-1000г («бычье сердце»), толщина левого желудочка 2-3см..
В условиях кислородного голодания и усиливающихся нарушений трофики миокарда вследствие патологии интрамуральной нервной системы сердца развивается диффузный мелкоочаговый кардиосклероз (гипертонический кардиосклероз).
3.(КЛИНИКО-МОРФОЛОГИЧЕСКИЕ ФОРМЫ ТУТ ПРИВЕСТИ ) Вторичные изменения органов в связи с изменением артерий и нарушением внутриорганного кровообращения. Характеризуется вторичными изменениями внутренних органов в связи с изменениями артерий и нарушением внутриорганного кровообращения. Вторичные изменения в органах могут развиваться медленно на почве артериолосклероза и атеросклероза с окклюзией сосудов, что ведет к атрофии паренхимы и склерозу органов.
ПОЧКИ
В почках в следствие склеротических изменений артерий и артериол развивается артериолосклеротический нефросклероз – первично сморщенная почка. Макроскопически: почки уменьшены в размерах, плотные, капсула снимается с трудом, поверхность почек зернистая с участками западений. На разрезе заметно истончение слоя почечной ткани, особенно коры, рисунок стерт.
Микроскопически: в запавших участках находят разрастания соединительной ткани, среди которой встречаются группы склерозированных (гиалинизированных) клубочков, канальцев мало, эпителий их низкий, атрофичный. В мелких артериях картина эластофиброза, в артериолах гиалиноз
. В сетчатке глаза обнаруживаются очаги уплотнившегося белкового выпота, мелкие кровоизлияния, частичное отслоение сетчатки, в таких 15 местах отмечается гибель палочек и колбочек нейроэпителиального слоя. В сосудистой оболочки глаза наблюдаются проявления плазморрагии и последующего гиалиноза.
ГОЛОВНОЙ МОЗГ
В головном мозге - диапедезные кровоизлияния, иногда обширные гематомы, возникающие вследствие разрыва сосуда.
Микроскопически: гиалинизированные артериолы, периваскулярные скопления эритроцитов, отек сохранной ткани мозга


Возможна смерть в результате выраженных атеросклеротических изменений
144. Патологическая анатомия злокачественной гипертонической болезни, причины смерти.
От доброкачественной формы отличается более высокими показателями АД – 220/140 мм. рт. ст., причем рост АД быстро прогрессирует. Характерно течение болезни по типу повторяющихся гипертонических кризов. Патогенез связан с повышением в крови концентрации сосудосуживающих веществ из-за увеличения выработки ренина и стимуляцией ренин-ангиотензин-альдостероновой системы (РААС), водноэлектролитными нарушениями, проявляющимися гипонатриемией гиповолемией и нередко гипокалиемией.
При злокачественной гипертензии доминируют проявления гипертонического криза, т. е. резкого повышения артериального давления в связи со спазмом артериол.
Морфологические проявления гипертонического криза достаточно характерны и представлены гофрированностью и деструкцией базальной мембраны эндотелия и своеобразным расположением его в виде частокола, что является выражением спазма артериолы (см. рис. 1), плазматическим пропитыванием или фибриноидным некрозом ее стенки (см. рис. 2) и присоединяющимся тромбозом. В связи с этим развиваются инфаркты, кровоизлияния.
Чаще поражаются капилляры почечных клубочков, что сопровождается быстро прогрессирующей ХПН и уремией. Длительность заболевания в большинстве не превышает 6-9 месяцев.


При злокачественном течении гипертонической болезни в связи с часто повторяющимися кризами фибриноидный некроз и тромбоз артериол различных органов приводит к множественным инфарктам и кровоизлияниям
В почках развивается злокачественный нефросклероз (Фара), который проявляется некрозом и лейкоцитарной инфильтрацией почечных клубочков
Отмечается отек стромы и множественные кровоизлияния (клинически проявляющиеся гематурией), придающие почкам пестрый вид (некротизирующий гломерулонефрит). В исходе формируется грубая склеротическая деформация почечной ткани (нефросклероз )
В глазах - двусторонний отек зрительного нерва с плазменным выпотом и кровоизлияниями в сетчатку
В головном мозге может возникать гипертензивная энцефалопатия, проявляющаяся потерей сознания вследствие отека и множественных мелких кровоизлияний (за счет фибриноидного некроза артериол) головного мозга
Причина смерти: При злокачественном варианте течения - хроническая и острая почечная недостаточность
145. Ишемическая болезнь сердца (ИБС): определение, причины, формы. Факторы риска, патогенез. Роль нестабильной атеросклеротической бляшки в морфогенезе ИБС.
Ишемическая болезнь сердца - группа заболеваний, обусловленных абсолютной или относительной недостаточностью коронарного кровообращения.
факторы риска 1-го порядка, при сочетании которых вероятность заболевания достигает 60%.
гиперлипидемия, (имеет значение не только для развития коронарного атеросклероза - морфологической основы болезни, но и для образования тромбов, так как тромбозу венечныхартерий, как правило, предшествует волна липидоза, связанная с атеросклеротическим кризом. Понятным становится значение при ишемической болезни сердца сахарного диабета, сопровождающегося гиперлипидемией).
артериальная гипертензия (в генезе инфаркта миокарда играет важную и неоднозначную роль. Она утяжеляет течение атеросклероза, в том числе и венечных артерий сердца, ведет к функциональному отягощению миокарда, способствует развитию плазморрагических, геморрагических и тромбоэмболических изменений).
Курение(предпосылки вазомоторного характера, способствующие развитию ишемии миокарда и ее последствий)
гиподинамия (предпосылки обменного характера, способствующие развитию ишемии миокарда и ее последствий)
Мужской пол
К факторам риска 2-го порядка относят :
пожилой возраст,
тучность,
стрессы,
нарушение обмена веществ типа сахарного диабета, подагры,
дефицит магния, селена, цинка,
Гиперкальциемия
Среди непосредственных причин развития ИБС :
длительный спазм,
тромбоз и тромбоэмболию венечных артерий сердца
функциональное перенапряжение миокарда в условиях атеросклеротической окклюзии этих артерий.
Патогенез . Развитие различных видов острой ИБС связано с внезапным нарушением коронарного кровообращения, приводящим к ишемическим повреждениям миокарда. Степень повреждений зависит от длительности ишемии и , в ряде случаев, от реперфузии миокарда после восстановления кровообращения по стенозированным коронарным артериям
Внезапная коронарная смерть- длительность ишемии до 1 ч, возникают выраженные ишемические повреждения миокрада, приводящие к его электрической нестабильности
Стенокардия- ишемия 3-25 мин
Стенокардия Принцметаля(покоя)-15-30 мин
Острый инфаркт миокарда- ишемия 18-24 ч

Формы ИБС:
Стенокардия (стабильная, нестабильная,Принцметала)
Стабильная-В основе заболевания лежит стенозирующий атеросклероз венечной артерии, приводящий к длительной ишемии. Сердечная мышца становится чувствительной к любой функциональной нагрузке
Нестабильная форма проявляется частыми нарастающими приступами (при физической нагрузке и в состоянии покоя) большой продолжительности. В основе лежит разрушение атеросклеротической бляшки с пристеночным тромбозом венечных артерий, возможны ангиоспазм, эмболия.
Деструктивные изменения фиброзной бляшки могут быть вызваны спазмом венечной артерии, разрушающим бляшку, продолжительной тахикардией, гиперхолестеринемией и кровоизлиянием в бляшку
Стенокардия покоя (стенокардия Принцметала)- Характерен спазм венечных артерий сердца (даже без наличия атеросклеротических бляшек), приводящий к трансмуральной ишемии миокарда
Внезапная коронарная смерть (острая коронарная недостаточность)- смерть, наступившая в первые 6 ч после возникновения острой ишемии миокарда в результате фибрилляции желудочков. Обязательным условием является отсутствие каких-либо других болезней, вызывающих быструю смерть. В основе лежит длительный спазм атеросклеротически стенозированных венечных артерий сердца или их тромбоз.
Острый инфаркт миокарда
При стенокардии морфологически отмечаются отек миокарда, дистрофия кардиомиоцитов с уменьшением содержания гликогена в цитоплазме. Эти изменения обратимы, часто повторяющиеся приступы приводят к развитию диффузного мелкоочагового кардиосклероза
146. Инфаркт миокарда: определение, причины, классификация, патогенез. стадии развития и исход.
Инфаркт миокарда - сосудистый коагуляционный некроз сердечной мышцы.
По размерам:
Мелкоочаговый
Крупноочаговый
обширный
По локализации выделяют:
инфаркт передней, задней и боковой стенок левого желудочка,
межжелудочковой перегородки,
верхушки сердца
обширный инфаркт
По отношению к слою сердечной мышцы различают
трансмуральный, -все слои
субэндокардиальный, -субэндокардиальный слой
интрамуральный –средний слой миокарда
субэпикардиальный инфаркт миокарда-под эпикардом
По времени возникновения можно говорить о:
1) первичном (остром) инфаркте миокарда, протекающем в течение 4 нед (28 дней) до формирования рубца
2) повторном, развивающемся через 4 нед. после острого (когда на месте первичного инфаркта возникает постинфарктный кардиосклероз)
3) рецидивирующем, наблюдающемся на протяжении 4 нед. первичного или повторного инфаркта
Стадии:
Доклиническая - +набухание митохондрий, уменьшение числа гранул гликогена, разрыв сарколеммы, отек, мелкие кровоизлияния и выход в миокард отдельных нейтрофилов. В зоне ишемии исчезают: гликоген, дыхательные ферменты
Некротическая- При микроскопическом исследовании сердечной мышцы выделяют три зоны : 1) некротическую, 2) демаркационную и 3) сохранного миокарда
Зона некроза представлена: кардиомиоциты с явлениями кариолизиса, плазмолизиса и плазморексиса, окружены демаркационным воспалением, большое количеств гиперемированных сосудов, множество полиморфноядерных нейтрофилов (лейкоцитарный вал)
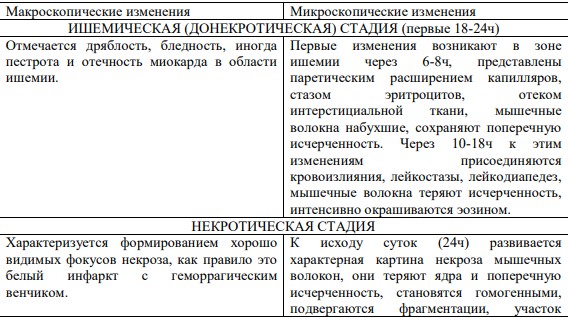

Исходы острого инфаркта миокарда:
1.Благоприятный-
организация
Петрификация
Инкапсуляция
2.Неблагоприятные –гнойное расплавление
3. Смерть от ранних осложнений ИМ.
4. Крупноочаговый постинфарктный кардиосклероз, часто с формированием и прогрессированием синдрома хронической сердечной недостаточности
147. Осложнения инфаркта миокарда: ранние и поздние, патологическая анатомия, причины смерти больных.
Осложнения инфаркта миокарда:
Осложнения раннего периода:
1. Кардиогенный шок (от секунд до первых часов от начала приступа ишемии) – связан с резким нарушением сократительной функции сердечной мышцы, падением сердечного выброса и снижением АД.
2. Острая левожелудочковая недостаточность (от нескольких минут до суток от начала приступа ишемии) - резкое снижение сердечного выброса с формированием острого полнокровия в малом круге кровообращения (отек легких)
3. Нарушения ритма (аритмия) – связаны с вымыванием из очага некроза т.н. аритмогенных субстанций, способных вызывать электрическую нестабильность в неповрежденном миокарде из-за перераспределения ионов Са вне- и внутри клетки. Развиваются при перфузии (восстановлении кровотока) в зоне некроза.
4. Формирование острой аневризмы миокарда (3-10 сутки).
5. Разрыв миокарда (в период 3-10 суток) с тампонадой полости перикарда на фоне острой аневризмы или без нее.
6. Тромбоз коронарных артерий (в течение нескольких суток 48-72ч) продолжает расширяться зона некроза миокарда в области первоначального инфаркта.
7. Отрыв некротизированной сосочковой мышцы (3-5 сутки) возникает при обширных инфарктах с вовлечением в зону некроза папиллярных мышц.
8. Внутрижелудочковый тромбоз, тромбоэмболия (3-10 сутки), источником эмболии служат свежие тромботические массы, образующиеся на эндокарде в области инфаркта или в полости аневризмы.
Осложнения позднего периода:
1. Образование хронической аневризмы (2-4 недели) – формируется по мере организации острой аневризмы.
2. Хроническая сердечная недостаточность - развивается по мере организации обширных инфарктов и после их рубцевания, сопровождается развитием застойного полнокровия в малом (МКК) и большом (ББК) кругах кровообращения
Причинами смерти служат:
острая сердечно-сосудистая недостаточность, кардиогенный шок, фибрилляция желудочков, асистолия
В результате размягчения сердечной мышцы в области трансмурального инфаркта (миомаляция) возможно развитие острой аневризмы сердца с последующим разрывом. В этом случае смерть наступает от тампонады полости перикарда
148. Хроническая ишемическая болезнь сердца (ХИБС): определение, причины, формы. Патологическая анатомия ХИБС, осложнения, исходы, клиническое значение. Хроническая ишемическая болезнь сердца – дисфункция сердца, возникающая вследствие уменьшения снабжения миокарда артериальной кровью Причины: гиперлипидемия, артериальная гипертензия, ожирение, малоподвижный образ жизни, курение, нарушение толерантности к углеводам (СД), мочекислый диатез, генетическая предрасположенность, мужской пол, стресс Формы: -хроническая аневризма сердца -ишемическая кардиомиопатия (дистрофия миокарда) -стенокардии (напряжения, Принцметалла, впервые позникшая) -атеросклеротический кардиосклероз (диффузный мелкоочаговый) (ДАКС) -постинфарктный кардиосклероз крупно и мелкоочаговый (ПИКС) Пат.анатомия: Под ишемической кардиомиопатией подразумевается не отдельная форма ХИБС, а финальные стадии ДАКС или ПИКС, характеризующиеся резким расширением полостей сердца и значительным увеличением его размеров, схожими по своим характеристикам с идиопатической КМП. Диффузный атеросклеротический кардиосклероз (ДАКС) Морфогенез изменений в миокарде связан со стенотическими поражениями венечных артерий, которые сопровождаются ишемией, дистрофическими изменениями, и гибелью отдельных мышечных клеток или небольших групп и замещением их соединительной тканью. С течением времени процесс прогрессирует и приводит к уменьшению функциональной (сократительной) способности миокарда. На начальных этапах заболевания процесс может компенсироваться гипертрофией неповрежденных кардиоцитов, что обеспечивает достаточную насосную функцию. По мере прогрессирования заболевания происходит истощение этого механизма. Развивается дилатация полостей, возникают и прогрессируют признаки сердечной недостаточности, связанные с нарушением кровообращения, которые сопровождаются развитием бурой индурации легких, застойным полнокровие печени, селезенки, почек. Появляются периферические и полостные отеки. Формируется гидроторакс, асцит, в финале развивается анасарка. Осложнения: -хроническая сердечная недостаточность -нарушения ритма сердца, чаще всего мерцательная аритмия -тромбоэмболии артерий головного мозга, почек, кишечника -разрыв хронической аневризмы, гемоперикард и тампонада Исходы: -развитие сердечно-сосудистой недостаточности -повторные инфаркты миокарда -смерть Клиническое значение: Хроническая ИБС может иметь сравнительно доброкачественное течение на протяжении многих лет. Выделяют стабильную симптомную или бессимптомную фазы, которые могут прерваться развитием ОКС. Постепенное прогрессирование атеросклероза коронарных артерий и сердечной недостаточности приводят к снижению функциональной активности больных, а у некоторых — к острым осложнениям (нестабильная стенокардия, ИМ), которые бывают фатальными (внезапная сердечная смерть).
149. Цереброваскулярные заболевания: определение, этиология, виды, морфологическая характеристика. Изменения в головном мозге при гипертонии и связанные с этим осложнения. Цереброваскулярные заболевания – острые нарушения мозгового кровообращения, фоном для развития которых являются атеросклероз и гипертоническая болезнь
Этиология: спазм, тромбоз, тромбоэмболия церебральных и прецеребральных артерий, психоэмоциональное перенапряжение Виды: -транзиторная ишемия головного мозга -инсульт (геморрагический, ишемический) Морфологическая характеристика: Морфология транзиторной ишемии головного мозга представлена сосудистыми расстройствами (спазм артериол, плазматическое пропитывание их стенок, периваскулярный отек и единичные мелкие геморрагии) и очаговыми изменениями мозговой ткани (отек, дистрофические изменения групп клеток). Эти изменения обратимы; на месте бывших мелких геморрагий могут определяться периваскулярные отложения гемосидерина. При образовании гематомы мозга, которая встречается в 85% при геморрагическом инсульте, находят выраженную альтерацию стенок артериол и мелких артерий с образованием микроаневризм и разрывом их стенок. В месте кровоизлияния ткань мозга разрушается, образуется полость, заполненная свертками крови и размягченной тканью мозга (красное размягчение мозга). Кровоизлияние локализуется чаще всего в подкорковых узлах головного мозга (зрительный бугор, внутренняя капсула) и мозжечке. Размеры его бывают разными: иногда оно охватывает всю массу подкорковых узлов, кровь прорывается в боковые, III и IV желудочки мозга, просачивается в область его основания (рис. 164). Инсульты с прорывом в желудочки мозга всегда заканчиваются смертью. Если больной переживает инсульт, то по периферии кровоизлияния в ткани мозга появляется много сидерофагов, зернистых шаров, клеток глии и свертки крови рассасываются. На месте гематомы образуется киста с ржавыми стенками и буроватым содержимым. У больных, длительно страдавших мозговой формой гипертонической болезни и умерших от инсульта, наряду со свежими кровоизлияниями нередко находят кисты как следствие бывших ранее геморрагии. При геморрагическом пропитывании вещества мозга как разновидности геморрагического инсульта обнаруживают мелкие сливающиеся очаги кровоизлияний. Среди пропитанного кровью мозгового вещества определяются нервные клетки с некробиотическими изменениями. Кровоизлияния типа геморрагического пропитывания встречаются обычно в зрительных буграх и мосту мозга (варолиев мост) и, как правило, не возникают в коре мозга и мозжечке. Ишемический инфаркт мозга, образующийся при тромбозе атеросклеротически измененных прецеребральных или церебральных артерий, имеет разнообразную локализацию. Это - самое частое (75% случаев) проявление ишемического инсульта. Выглядит ишемический инфаркт как очаг серого размягчения мозга. При микроскопическом исследовании среды некротических масс можно обнаружить погибшие нейроны. Теморрагический инфаркт мозга внешне напоминает очаг геморрагического пропитывания, но механизм его развития другой: первично развивается ишемия мозговой ткани, вторично - кровоизлияния в ишемизированную ткань. Чаще геморрагический инфаркт встречается в коре мозга, реже - в подкорковых узлах. При смешанном инфаркте, который всегда возникает в сером веществе мозга, можно найти участки как ишемического, так и геморрагического инфаркта. На месте инфарктов мозга, как и гематомы, образуются кисты, причем стенка кисты на месте геморрагического инфаркта содержит скопление гемосидерина («ржавая киста»). Осложнения инсультов (кровоизлияний и инфарктов мозга), как и их последствий (кисты мозга), - параличи. Мозговые инсульты - частая причина смерти больных атеросклерозом и гипертонической болезнью. Изменения в головном мозге при гипертонии и связанные с этим осложнения: -отек мозга с вклинением миндалин мозжечка в большое затылочное отверстие со сдавлением жизненно важных центров продолговатого мозга -прорыв крови в систему желудочков – гемоцефалия (тампонада желудочков мозга) -пневмонии -ТЭЛА -пролежни - сепсис
150. Кровоизлияние в головной мозг: классификация, причины, патологическая анатомия, осложнения, исходы, клиническое значение. Кровоизлияния в головной мозг Классификация: 1) по локализации -эпидуральные -субдуральные -субарахноидальные -белое вещество разных долей полушария мозга -подкорковые ядра -желудочки мозга (первичные и вторичные) -ствол 2) по внешнему виду и размерам -петехии -гематомы -геморрагическая инфильтрация 3) по этиологии 4) по механизму поражения сосудов Причины: атеросклероз, ГБ, васкулиты, гемофилия, СД, аневризмы сосудов головного мозга, травмы головного мозга, злокачественные опухоли Пат.анатомия: артериальная гипертензия => изменение стенок сосудов => фибриноидная дегенерация и гиалиноз артерий мозга => формирование аневризмы => разрыв сосуда => мозговое кровотечение При образовании гематомы мозга находят выраженную альтерацию стенок артериол и мелких артерий с образованием микроаневризм и разрывом их стенок. В месте кровоизлияния ткань мозга разрушается, образуется полость, заполненная свертками крови и размягченной тканью мозга. По периферии кровоизлияния в ткани мозга появляется много сидерофагов, зернистых шаров, клеток глии и свертки крови рассасываются. На месте гематомы образуется киста с ржавыми стенками и буроватым содержимым. Осложнения: -коматозное состояние -параличи Исходы: -пневмония -пролежни -летальный исход Клиническое значение: -Быстрое развитие неврологических синдромов, вызванных поражением головного мозга -Нарушение сознания (сознание может сохраняться при небольших кровоизлияниях) -Менингеальные симптомы и головная боль (они могут отсутствовать при небольших кровоизлияниях)
151. Ишемический инфаркт головного мозга: причины, патологическая анатомия, осложнения, исходы, клиническое значение. Ишемический инфаркт ГМ Причины: тромбоз атеросклеротических артерий Пат.анатомия: Выглядит ишемический инфаркт как очаг серого размягчения мозга. При микроскопическом исследовании среды некротических масс можно обнаружить погибшие нейроны. Осложнения: Осложнения инсульта могут включать в себя нарушения сна, спутанность сознания, депрессию, недержание, ателектазы, пневмонию и нарушение глотания, которое может привести к аспирации, дегидратацию или недостаточность питания. Исходы: Исходы инсульта Каждый 8-й инсульт заканчивается смертью. Ишемический инсульт случается при сдавливании или закупоривании мозговых артерий. Он встречается более чем в 80% случаев. В большинстве случаев инсульт приводит к инвалидности и лишь 10-13% пациентов возвращается к прежней жизни. Клиническое значение:
152. Пневмококковая пневмония: патологическая анатомия, осложнения и патоморфоз. Пневмококковая пневмония – форма пневмококковой инфекции, протекающая в виде очаговой бронхопневмонии или крупозной плевропневмонии. Пат.анататомия: 4 стадии: -прилива, -красного опеченения, -серого опеченения, -разрешения. Все стадии занимают 9-11 дней.
Стадия прилива продолжается сутки и характеризуется резкой гиперемией и микробным отеком пораженной доли; в отечной жидкости находят большое число возбудителей. Отмечается повышение проницаемости капилляров, начало диапедеза эритроцитов в просвет альвеол. Легкое несколько уплотнено, резко полнокровно.
Стадия красного опеченения возникает на 2-й день болезни. На фоне полнокровия и микробного отека усиливается диапедез эритроцитов, которые накапливаются в просвете альвеол. К ним примешиваются нейтрофилы, между клетками выпадают нити фибрина. В экссудате альвеол обнаруживается большое число пневмококков, отмечается фагоцитоз их нейтрофилами. Лимфатические сосуды, расположенные в межуточной ткани легкого, расширены, переполнены лимфой. Ткань легкого становится темно-красной, приобретает плотность печени (красное опеченение легкого). Регионарные в отношении пораженной доли легкого лимфатические узлы увеличены, полнокровны.
Стадия серого опеченения возникает на 4-6-й день болезни. В просвете альвеол накапливаются фибрин и нейтрофилы, которые вместе с макрофагами фагоцитируют распадающиеся пневмококки. Можно видеть, как нити фибрина через межальвеолярные поры проникают из одной альвеолы в другую. Число эритроцитов, подвергающихся гемолизу, уменьшается, снижается и интенсивность гиперемии. Происходит фибринолитическое воздействие нейтрофилов на выпавший фибрин, которое, начавшись в стадии серого опеченения, в дальнейшем усиливается (рис. 183). Доля легкого в стадии серого опеченения увеличена, плотная, тяжелая, на плевре значительные фибринозные наложения (плевропневмония). На разрезе легкое серой окраски (см. рис. 183), с зернистой поверхности стекает мутная жидкость. Лимфатические узлы корня легкого увеличены, бело-розовые; при гистологическом их исследовании находят картину острого воспаления.
Стадия разрешения наступает на 9- 11-й день болезни. Фибринозньгй экссудат под влиянием протеолитических ферментов нейтрофилов и макрофагов подвергается расплавлению и рассасыванию. Происходит очищение легкого от фибрина и пневмококков: экссудат элиминируется по лимфатическим дренажам легкого и с мокротой. Фибринозные наложения на плевре рассасываются. Стадия разрешения растягивается иногда на несколько дней после клинически безлихорадочного течения болезни.
Классическая схема течения крупозной пневмонии иногда нарушается (Цинзерлинг В.Д., 1939; Лешке, 1931) - серое опеченение предшествует красному. В некоторых случаях очаг пневмонии занимает центральную часть доли легкого (центральная пневмония), кроме того, он может появляться то в одной, то в другой доле(мигрирующая пневмония). Осложнения: Легочные осложнения развиваются в связи с нарушением фибринолитической функции нейтрофилов. При недостаточности этой функции массы фибрина в альвеолах подвергаются организации, т.е. прорастают грануляционной тканью, которая, созревая, превращается в зрелую волокнистую соединительную ткань. Этот процесс организации называется карнификацией (от лат. сагпо - мясо). Легкое превращается в безвоздушную плотную мясистую ткань. При чрезмерной активности нейтрофилов возможно развитие абсцесса и гангрены легкого. Присоединение гноя к фибринозному плевриту ведет к эмпиеме плевры.
Внелегочные осложнения наблюдаются при генерализации инфекции. При лимфогенной генерализации возникают гнойные медиастинит и перикардит, при гематогенной - перитонит, метастатические гнойникив головном мозге, гнойный менингит, острый язвенный или полипозноязвенный эндокардит, чаще правого сердца, гнойный артрит Патоморфоз: дистрофические изменения паренхиматозных органов, их полнокровие, гиперплазия селезенки и костного мозга, полнокровие и отек головного мозга. В шейных симпатических ганглиях наблюдаются резкая гиперемия, лейкоцитарная инфильтрация вокруг сосудов и дистрофические изменения ганглиозных клеток
153. Бронхопневмонии: этиология, патологоанатомическая характеристика пневмококковой, стафилококковой, стрептококковой, грибковой, вирусной пневмоний. Особенности пневмоний у детей. Бронхопневмония Этиология: Обычно возбудителем очаговых пневмоний являются низковирулентные микроорганизмы, особенно у лиц с иммунодефицитами, которые у здоровых людей не приводят к развитию аналогичного заболевания. Обычно это стафилококки, стрептококки, Haemophilus influ en zae, кишечная палочка и грибы. У больных часто развивается септицемия и токсинемия, что проявляется лихорадкой и нарушением сознания. Пневмония развивается также при воздействии химических и физических факторов, что позволяет выделять уремическую, липидную, пылевую, радиационную пневмонии. Пат.анат.хар-ка пневмоний: Стафилококковая пневмония При микроскопическом исследовании в острой стадии болезни в бронхах и респираторных отделах легких обнаруживаются скопления стафилококков в серозном или серозно-геморрагическом экссудате, и которому примешиваются вначале единичные, а затем все возрастающие в числе лейкоциты. В дальнейшем очаги воспаления приобретают типичную зональность. В центральных участках содержится много стафилококков. В области их скоплений наблюдаются явления некроза, которому подвергаются лишь отдельные клетки экссудата. В других случаях некротические изменения выражены значительно сильнее, они захватывают не только клетки, но и межальвеолярные перегородки и стенки бронхов. В окружности участка некроза образуется разной ширины вал из зернистых лейкоцитов. В самых периферических участках пневмонического очага нередко располагаются альвеолы, выполненные преимущественно фибринозным и серозным экссудатом.
Стрептококковая
пневмония.
При
микроскопическом исследовании в легочной
ткани определяются очаги некроза. На
ранних стадиях легочная ткань в этих
местах еще сохраняет свою структуру,
хотя ядра клеток уже отсутствуют; позже
она оказывается разрушенной. По периферии
такие очаговые некрозы окружены зонами
легочной ткани, содержащей фибринозный
выпот и далее от центра серозный экссудат.
Однако временно на границе некроза
образуется вал, состоящий вначале из
отдельных лейкоцитов, а затем из
значительного их количества.
Обычно
соответственно очагу некротизируется
и плевра, что приводит к быстро
развивающемуся сначала серозному, а
затем серозно-гнойному плевриту и
пиопневмотораксу.
В плевре и в
прослойках соединительной ткани легкого
развивается лимфангит, распространяющийся
от очага по направлению к корню, что
сопровождается поражением регионарных
лимфоузлов. На ранних стадиях болезни
в них наблюдаются токсические и
гиперпластические, а позже - некротические
и гнойные изменения. Может возникнуть
также флегмона средостения. Процесс
захватывает вены, в которых наблюдается
септический тромбофлебит.


Особенности пневмоний у детей: Пневмония имеет некоторые особенности в разные возрастные периоды. У новорожденных при пневмонии на поверхности альвеол нередко образуются так называемые гиалиновые мембраны, состоящие из уплотненного фибрина. У ослабленных детей до 1-2 лет очаги воспаления локализуются преимущественно в задних, прилежащих к позвоночнику и не полностью расправленных после рождения отделах легких (II, VI и Х сегменты). Такая пневмония называется паравертебральной. Благодаря хорошей сократительной способности легких и дренажной функции бронхов, богатству легких лимфатическими сосудами очаги пневмонии у детей сравнительно легко рассасываются.
154.
Хронические обструктивные болезни
легких: терминология, этиология,
патогенез, клинико-морфологическая
характеристика, осложнения, причины
смерти.
ХОБЛ
– заболевание, характеризующееся
частично необратимым ограничением
воздушного потока. Ограничение воздушного
потока имеет прогрессирующий характер
и вызвано аномальной воспалительной
реакцией легочной ткани на раздражение
различными патогенными частицами и
газами.
Этиология:
курение,
профессиональные вредности, дым сжигания
БАВ, мужчины, возраст старше 40 лет,
хронический бронхит
Патогенез:
 Клинико-морфологическая
хар-ка:
У
пациентов со среднетяжелым и тяжелым
течением заболевания выделяют две
клинические формы:
-
эмфизематозная (панацинарная эмфизема,
"розовые пыхтелки");
-
бронхитическая (центроацинарная
эмфизема, "синие отёчники").
Жалобы (их
выраженность зависит от стадии и фазы
заболевания):
1. Кашель является
самым ранним симптомом и проявляется
обычно в возрасте 40-50 лет. В холодные
сезоны у таких больных отмечаются
эпизоды респираторной инфекции, которые
сначала не связываются пациентом и
врачом в одно заболевание. Кашель
может быть ежедневным или носит характер
перемежающегося; более часто наблюдается
днем.
В беседе с пациентом необходимо
установить частоту возникновения кашля
и его интенсивность.
2. Мокрота,
как правило, выделяется в небольшом
количестве утром (редко > 50 мл/сутки),
имеет слизистый характер. Увеличение
количества мокроты и ее гнойный характер
являются признаками обострения
заболевания. При появлении крови в
мокроте следует заподозрить иную причину
кашля (рак легких, туберкулез, бронхоэктазы).
У больного ХОБЛ прожилки крови в мокроте
могут появляться как результат упорного
надсадного кашля.
В беседе с пациентом
необходимо выяснить характер мокроты
и ее количество.
3. Одышка
является основным признаком ХОБЛ и для
большинства больных служит поводом для
обращения к врачу. Зачастую диагноз
ХОБЛ устанавливают именно на этой
стадии заболевания.
По мере
прогрессирования заболевания одышка
может варьировать в широких пределах:
от ощущения нехватки воздуха при
привычных физических нагрузках до
тяжелой дыхательной недостаточности. Одышка
при физической нагрузке появляется
в среднем на 10 лет позже кашля (крайне
редко заболевание дебютирует одышкой).
Выраженность одышки возрастает по мере
снижения легочной функции.
При
ХОБЛ характерными чертами одышки
являются:
- прогрессирование
(постоянное нарастание);
- постоянство
(каждый день);
- усиление при физической
нагрузке;
- усиление при респираторных
инфекциях.
Пациенты описывают одышку
как "нарастание усилий при дыхании",
"тяжесть", "воздушное голодание",
"затрудненное дыхание".
В беседе
с пациентом необходимо оценить
выраженность одышки и ее связь с
физической нагрузкой. Существует
несколько специальных шкал для
оценки одышки и других симптомов
ХОБЛ - BORG, mMRC Dyspnea Scale, CAT.
Клинико-морфологическая
хар-ка:
У
пациентов со среднетяжелым и тяжелым
течением заболевания выделяют две
клинические формы:
-
эмфизематозная (панацинарная эмфизема,
"розовые пыхтелки");
-
бронхитическая (центроацинарная
эмфизема, "синие отёчники").
Жалобы (их
выраженность зависит от стадии и фазы
заболевания):
1. Кашель является
самым ранним симптомом и проявляется
обычно в возрасте 40-50 лет. В холодные
сезоны у таких больных отмечаются
эпизоды респираторной инфекции, которые
сначала не связываются пациентом и
врачом в одно заболевание. Кашель
может быть ежедневным или носит характер
перемежающегося; более часто наблюдается
днем.
В беседе с пациентом необходимо
установить частоту возникновения кашля
и его интенсивность.
2. Мокрота,
как правило, выделяется в небольшом
количестве утром (редко > 50 мл/сутки),
имеет слизистый характер. Увеличение
количества мокроты и ее гнойный характер
являются признаками обострения
заболевания. При появлении крови в
мокроте следует заподозрить иную причину
кашля (рак легких, туберкулез, бронхоэктазы).
У больного ХОБЛ прожилки крови в мокроте
могут появляться как результат упорного
надсадного кашля.
В беседе с пациентом
необходимо выяснить характер мокроты
и ее количество.
3. Одышка
является основным признаком ХОБЛ и для
большинства больных служит поводом для
обращения к врачу. Зачастую диагноз
ХОБЛ устанавливают именно на этой
стадии заболевания.
По мере
прогрессирования заболевания одышка
может варьировать в широких пределах:
от ощущения нехватки воздуха при
привычных физических нагрузках до
тяжелой дыхательной недостаточности. Одышка
при физической нагрузке появляется
в среднем на 10 лет позже кашля (крайне
редко заболевание дебютирует одышкой).
Выраженность одышки возрастает по мере
снижения легочной функции.
При
ХОБЛ характерными чертами одышки
являются:
- прогрессирование
(постоянное нарастание);
- постоянство
(каждый день);
- усиление при физической
нагрузке;
- усиление при респираторных
инфекциях.
Пациенты описывают одышку
как "нарастание усилий при дыхании",
"тяжесть", "воздушное голодание",
"затрудненное дыхание".
В беседе
с пациентом необходимо оценить
выраженность одышки и ее связь с
физической нагрузкой. Существует
несколько специальных шкал для
оценки одышки и других симптомов
ХОБЛ - BORG, mMRC Dyspnea Scale, CAT.
Наряду с основными жалобами, больных могут беспокоить следующие внелегочные проявления ХОБЛ:
- утренняя головная боль; - сонливость днем и бессонница ночью (следствие гипоксии и гиперкапнии); - снижение веса и потеря массы тела.
Осложнения: -дыхательная недостаточность -гипертония МКК -гипертрофия правого желудочка сердца -легочное сердце -хроническая правожелудочковая недостаточность сердца -пневмония Причины смерти: сопутствующие забоелвания, возраст, пол
155.
Бронхоэктатическая болезнь: определение,
классификация, патогенез, морфогенез,
патологическая анатомия, осложнения,
клиническое значение.
Бронхоэктатическая
болезнь
–
хроническое прогрессирующее заболевание
дыхательных путей, характеризующееся
стойкой патологической дилатацией
(расширением) одного или нескольких
бронхов с нарушением их дренажной
функции, обусловленной деструкцией
(разрушением) эластического и мышечного
слоев бронхиальной стенки.
Классификация:
1)
врожденные бронхоэктазы – нарушение
развития бронхолегочной системы во
внутриутробном периоде
2) приобретенные
бронхоэктазы – развиваются после
различных бронхо-легочных заболеваний
3)
по харакретру расширения бронхов
(цилиндрические, мешотчатые, ветеренообразные
и смешанные)
4) по распространенности
процесса ()одно- и двусторонние, с
указанием точной локализации по
сегментам
5) по киническому течению
(бронхитическая ст, ст.выраженных
клинических проявлений и
ст.осложнений)
Патогенез:
 Морфогенез:
Наиболее
часто бронхэктазы развиваются в нижних
долях. В бронхоэктазах накапливается
бронхиальный секрет, что создает условия
для развития микроорганизмов. У таких
больных основными симптомами являются
постоянный кашель и отхождение мокроты
с неприятным запахом, иногда с прожилками
крови. Инфекционный процесс из бронхов
может распространяться локально или
системно.
Пат.анатомия:
В
легких определяются расширения бронхов
или бронхиол, наблюдается их воспалительная
инфильтрация, особенно полиморноядерными
лейкоцитами. Воспаление и фиброз
распространяются на близлежащую легочную
ткань. Бронхоэктазы могут быть
цилиндрическими, мешотчатыми или
веретенообразными; их форма не имеет
какого – либо прогностического или
этиологического значения. Они появляются
в очаге неразрешившейся пневмонии, в
участках ателектаза (активного спадения
респираторного отдела легких вследствие
обтурации или компрессии бронхов) и
коллапса (спадение респираторных
структур легкого вследствие механического
его сдавления со стороны плевральной
полости). Внутрибронхиальное давление,
повышающееся во время кашлевых толчков,
воздействуя на измененную при хроническом
воспалении бронхиальную стенку, ведет
к ее выяпячиванию в сторону наименьшего
сопротивления, просвет бронха расширяется.
Расширенные на почве воспаления бронхиолы
обозначают как бронхиолоэктазы. Они
бывают обычно множественными, поверхность
разреза легкого при этом имеет
мелкоячеистый вид, такое легкое называют
сотовым, так как оно напоминает пчелиные
соты. Полость бронхоэктаза выстлана
призматическим эпителием, но нередко
многослойным плоским, возникшим в
результате метаплазии. В стенке
бронхоэктаза наблюдается хроническое
воспаление, эластические и мышечные
волокна на значительном протяжении
разрушены и замещены соединительной
тканью. В полости бронхоэктаза имеется
гнойное содержимое. Прилежащая к
бронхоэктазам легочная ткань резко
изменяется, в ней возникают фокусы
воспаления (абсцессы, участки организации
экссудата), поля фиброза. Возникает
обструктивная эмфизема, которая ведет
к гипертензии в малом круге кровообращения
и гипертрофии правого желудочка сердца
(легочное сердце). В связи с этим у больных
появляется гипоксия с последующим
нарушением трофики тканей. Очень
характерно утолщение тканей ногтевых
фаланг пальцев рук и ног: пальцы
приобретают вид барабанных палочек.
Весь комплекс легочных и внелегочных
изменений при наличии бронхоэктазов
называют бронхоэктатической
болезнью.
Осложнения:
-скопление
мокроты и гноя в бронхоэктазах
-склероз
легочной ткани
-нарушение кровообращения
МКК
-гипертрофия правого
желудочка
-легочно-сердечная
недосттаочность
Морфогенез:
Наиболее
часто бронхэктазы развиваются в нижних
долях. В бронхоэктазах накапливается
бронхиальный секрет, что создает условия
для развития микроорганизмов. У таких
больных основными симптомами являются
постоянный кашель и отхождение мокроты
с неприятным запахом, иногда с прожилками
крови. Инфекционный процесс из бронхов
может распространяться локально или
системно.
Пат.анатомия:
В
легких определяются расширения бронхов
или бронхиол, наблюдается их воспалительная
инфильтрация, особенно полиморноядерными
лейкоцитами. Воспаление и фиброз
распространяются на близлежащую легочную
ткань. Бронхоэктазы могут быть
цилиндрическими, мешотчатыми или
веретенообразными; их форма не имеет
какого – либо прогностического или
этиологического значения. Они появляются
в очаге неразрешившейся пневмонии, в
участках ателектаза (активного спадения
респираторного отдела легких вследствие
обтурации или компрессии бронхов) и
коллапса (спадение респираторных
структур легкого вследствие механического
его сдавления со стороны плевральной
полости). Внутрибронхиальное давление,
повышающееся во время кашлевых толчков,
воздействуя на измененную при хроническом
воспалении бронхиальную стенку, ведет
к ее выяпячиванию в сторону наименьшего
сопротивления, просвет бронха расширяется.
Расширенные на почве воспаления бронхиолы
обозначают как бронхиолоэктазы. Они
бывают обычно множественными, поверхность
разреза легкого при этом имеет
мелкоячеистый вид, такое легкое называют
сотовым, так как оно напоминает пчелиные
соты. Полость бронхоэктаза выстлана
призматическим эпителием, но нередко
многослойным плоским, возникшим в
результате метаплазии. В стенке
бронхоэктаза наблюдается хроническое
воспаление, эластические и мышечные
волокна на значительном протяжении
разрушены и замещены соединительной
тканью. В полости бронхоэктаза имеется
гнойное содержимое. Прилежащая к
бронхоэктазам легочная ткань резко
изменяется, в ней возникают фокусы
воспаления (абсцессы, участки организации
экссудата), поля фиброза. Возникает
обструктивная эмфизема, которая ведет
к гипертензии в малом круге кровообращения
и гипертрофии правого желудочка сердца
(легочное сердце). В связи с этим у больных
появляется гипоксия с последующим
нарушением трофики тканей. Очень
характерно утолщение тканей ногтевых
фаланг пальцев рук и ног: пальцы
приобретают вид барабанных палочек.
Весь комплекс легочных и внелегочных
изменений при наличии бронхоэктазов
называют бронхоэктатической
болезнью.
Осложнения:
-скопление
мокроты и гноя в бронхоэктазах
-склероз
легочной ткани
-нарушение кровообращения
МКК
-гипертрофия правого
желудочка
-легочно-сердечная
недосттаочность
