
3 курс / Общая хирургия и оперативная хирургия / Весенний семестр / Лекция 2. ГНОЙНЫЕ ЗАБОЛЕВАНИЯ СЕРОЗНЫХ ПОЛОСТЕЙ. СЕПСИС
.pdf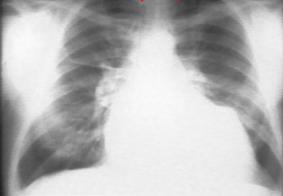
1.Серозный перикардит 2.Гемморагический перикардит 3.Слипчивый перикардит 4.Гнойный перикардит
5.Фибринозный перикардит («панцирное сердце»).
В процессе развития хронического перикардита экссудат частично всасывается, а образовавшийся фибрин замещается грануляционной тканью, которая постепенно превращается в соединительную, а затем в рубцовую. Позднее рубцовая ткань гиалинизируется сморщивается и в ней часто откладывается известь. В этом случае говорят о панцирном сердце. Рубцовые изменения в сердечной сорочке наиболее выражены на участке, покрывающем правое предсердие и правый желудочек. Менее плотным остаётся перикард в области левого желудочка сердца.
Клиника. Жалобы больных с перикардитом связана с воспалительным процессом и явлениями нарастающей его тампонады, т.е. развития сердечной недостаточности. Наиболее частыми из них являются: одышка, сердцебиение, общая слабость, увеличение объёма живота, отёки нижних конечностей, иногда боли в правом подреберье, связанные с увеличением печени. Одышка определяется в первую очередь низким сердечным выбросом, а также изменениями миокарда. Она наблюдается в основном при физической нагрузке и очень редко встречается в покое. Следует отметить, что одышка при сдавливающем перикардите всегда менее выражена, чем у больных с приобретёнными пороками сердца.
Клиническая картина перикардита становится более ясной при скоплении жидкости в сердечной сорочке. Больные жалуются на лёгкую боль в области сердца и сердцебиение. При скоплении более значительного количества жидкости боль становится более мучительной, отдающей нередко в левую руку, у больных появляется ощущения сдавления в груди и чувство страха, как при стенокардии. При скоплении большого количества жидкости наблюдаются одышка, цианоз, набухание шейных вен вследствие сдавления сердца и лёгких. Больные вынуждены принимать положение сидя.
При рентгенологическом исследовании органов грудной клетки в двух проекциях определяется трапециевидная (шарообразная) тень сердца без свойственных ему дуг по контурам.
Рис.6. Рентгенологическим признаком накопления экссудата в сердечной сорочке является не столько увеличение размеров, сколько изменение силуэта сердечной тени
Лечение выпотного перикардита комплексное. В первую оно должно быть направлено на устранение первичного заболевания. При значительном скоплении экссудата в полости сердечной сорочки показана пункция, а иногда и дренирование

перикарда. Пункция перикарда выполняется в сидячем положении больного под местной анестезией. Толстой иглой прокалывают кожу в точке между основанием мечевидного отростка и местом прикрепления VII рёберного хряща слева. Затем производят прокол перикарда и иглу проводят по задней поверхности грудины на 1,5-2 см и пунктируют содержимое полости перикарда. Если эвакуируемое содержимое имеет гнойный характер густой консистенции, то целесообразно произвести вскрытие сердечной сорочки, промыть полость раствором фибринолизина и антибиотиков и поставить дренаж типа Бюлау.
После пункции или операции проводят антибактериальную, дезинтоксикационную, кардиотропную терапию.
«Сепсис - это болезнь, при которой смерть запланирована» В.Вазен
СЕПСИС
Сепсис – общее инфекционное заболевание, характеризующееся ацикличностью течения, полиэтиологичностью при изменённой реактивности организма, когда местный инфекционно-воспалительный очаг служит источником повторной гематогенной генерализации возбудителя.
Большинство хирургов считают, что сепсис — это генерализованная форма неспецифического инфекционного заболевания вызванного постоянным или периодическим проникновением в кровеносное русло микроорганизмов и их токсинов в условиях своеобразной реактивности организма. Для возникновения хирургического сепсиса обязательным является первичный очаг инфекции.
По классификации Санкт-Петербурского института скорой помощи Ю.Ю.Джанелидзе, сепсис – это неспецифическое инфекционное заболевание, характеризующееся синдромом системной воспалительной реакцией (ССВР), возникающей в условиях постоянного или периодического поступления из очага инфекции в циркулирующую кровь микроорганизмов и их токсинов и приводящих к развитию инфекционной полиорганной недостаточности (ПОН) вследствие неспособности иммунных сил организма к локализации инфекции.
Согласно одному из основоположников учения о сепсисе И.В.Давыдовскому, основной критерий сепсиса – это независимость общих проявлений от местного очага инфекции. Так, если после санации источника очага инфекции общие проявления идут на спад и ликвидируются – это гнойно-резорбтивная лихорадка. Если же общие явления не купируются, а наоборот нарастают, - это и есть настоящий сепсис.
Рис.1. Аристотель
Термин «сепсис» ввел Аристотель (рис.1). Он определял сепсис как отравление организма продуктами гниения собственной ткани

Древние хирурги не могли понять суть патологического процесса. Они связывали его развитие с изменениями состава или нарушением соотношения “четырёх жидкостей” (кровь, слизь, желчь жёлтая, желчь чёрная).
Гиппократ также связывал развитие сепсиса с недостатком, изобилием или диспропорцией этих элементов. Он один из первых в книге о “пышащей лихорадке” и ряде других сочинений описывает клиническую симптоматику сепсиса и дифференцирует его от бешенства и летаргии.
Амбруаз Паре, Парацельс и другие хирурги в XVI-XVIII веках начали связывать «гнилокровие» с интоксикацией организма какими-то химическими веществами. Огромный вклад в развитие учения о сепсисе внёс Н. И. Пирогов. Ещё до наступления эры асептики он выдвинул идею, что в развитии сепсиса существенную роль играют активные факторы, проникновение которых в организм вызывает септицемию. Н. И. Пирогов выделял две основные формы сепсиса: пиемия и септикемия (ихоремия, токсикемия)
Рис.2. Роберт Кох (R. Koch) Рис.3. И.В.Давыдовский
По микробиологической теории Роберта Коха (рис.2) сепсис — гнилокровие, представляется как процесс развития, размножения микроорганизмов в крови. Последующие исследования показали, что наблюдаемая при сепсисе бактериемия — процесс вторичный, обусловлен выходом микроорганизмов в кровь из первичных очагов, локализованных в тканях и органах.
По Н. Schottmuller, сепсис представляет собой особый местный воспалительный процесс. Эту теорию поддерживал Р. Вирхов. Однако последующие исследования такую специфичность местного воспалительного процесса не подтвердили.
И.В. Давыдовский (рис.3) представлял сепсис как особую реакцию организма на инфекцию, на воспаление. В этом отношении существенная роль отводилась сенсибилизации организма, аллергии. Эта теория является по существу основной, общепризнанной, и предлагаемые в последние годы новые теории не только не отвергают, но и подтверждают и дополняют эту теорию на современном уровне знаний.
По Royx, бактериальные токсины могут быть аллергенами, а сепсис представляет собой аллергическую реакцию организма, в которой роль аллергенов играют бактериальные токсины — аллергическая теория сепсиса (Абрикосов А.И., 1942; Чистович Н.Я., 1961).
Существует и цитокиновая теория. W. Ertel отводит ведущую роль в развитии сепсиса выбросу цитокинов и секреции интерлейкинов (IL-1, IL-6, IL-8), имеющих основное значение в развитии общего ответа организма на воспаление. Это является пусковым моментом в развитии сепсиса, а падение секреции IL-2 приводит к снижению уровня Т- и В-лимфоцитов, уменьшению синтеза иммуноглобулинов. Изменения в иммунной системе служат одной из основных причин развития сепсиса.
Аллергическую и цитокиновую теории нельзя рассматривать как самостоятельные, они по существу дополняют и развивают теорию И.В. Давыдовского, раскрывают суть реакции организма на инфекцию, воспаление.
Основные теории сепсиса.
1.Токсическая теория (В. С. Савельев с соавт., 1976). Основная роль в патогенезе отводится не микробному фактору, а воздействию экзо- и эндотоксинов.
2.Аллергическая теория (I.C.Royx,1983).
Патогенетические сдвиги в организме обусловлены реакцией аллергического типа на бактериальные токсины.
3.Бактериологическая теория (Давыдовский И.В., 1928). Все изменения наступающие в организме, являются результатом развития гнойного очага. Они происходят вследствие роста, размножения и попадания микробов в кровяное русло.
4.Нейротрофическая теория (Сперанский Г.Н., 1937. и др.) Основывается на
работах |
И.П.Павлова, показавших главенствующее значение ЦНС в |
развитии |
патологии вообще. Согласно данной теории основная роль в |
развитии сепсиса отводится состоянию ЦНС и периферической нервной системы, которые определяют тканевые реакции пораженного участка
5.Цитокиновая теория (W. Ertel, 1991).В настоящее время занимает доминирующее положение. Согласно данной теории эндотоксины вызывают поступление в кровь большого количества цитокинов. Они являются веществами, регулирующими иммунитет. В результате увеличения в крови цитокинов поражается эндотелий и развивается синдром системной воспалительной реакции и иммунодепрессия
Как отмечают эксперты, в 1991 г (systemic inflammatory response syndrome — SIRS). При этом его диагностировали при наличии 2 из нижеперечисленных критериев:
•температура тела >38 или <36° C;
•частота сердечных сокращений >90 уд./мин;
•частота дыхательных движений >20/мин или PaCO2 <32 мм рт. ст.;
•количество лейкоцитов >12 тыс./мм3 или <4 тыс. мм3, или >10% незрелых форм.
В 1991 году на Согласительной Конференции Американского общества торакальных врачей и общества медицины экстренных состояний (реаниматологов) в Чикаго была принята классификация сепсиса, основанная на работах R.Bone. На этой Конференции по сепсису были утверждены чёткие его критерии, а также ранжирование тяжести течение сепсиса, разработаны первые рекомендации по определению сепсиса,
вкоторых отображается взгляд на патологию как результат системного воспалительного ответа организма на инфекцию
Согласной этой классификации выделены следующие состояния, связанные с сепсисом. От термина септицемия рекомендовано отказаться.
1.Бактериемия – наличие жизнеспособных бактерий в крови. Выявляется бактериемия не всегда (20-30%) и поэтому не является обязательным критерием сепсиса.
2.Синдром системного воспалительного ответа (ССВО) - Systemic In-flammatory Response Syndrome (SIRS) - неспецифическая генерализованная реакция организма в ответ на тяжелую травму, инфекционный процесс или другие стресс-реакции.
Диагноз ССВО устанавливается при наличии двух и более следующих клинических симптомов:
• температура тела > 38°С или < 36°С;
• частота сердечных сокращений > 90 в минуту;

•частота дыхания > 20 в минуту или рС02 < 32 мм рт. ст. (для больных на аппарате искусственной вентиляции легких (ИВЛ);
•количество лейкоцитов периферической крови > 12 х 109/л или < 4 х 109/л (или не менее 10 % незрелых клеток).
Выделяют три стадии ССВО (SIRS):
Стадия 1. Локальная продукция воспалительных медиаторов в ответ на травму или инфекцию. Воспалительные медиаторы участвуют в процессах заживления ран и клеточной защите от патогенных факторов.
Стадия 2. Выброс малого (необходимого и строго дозированного) коли-чества воспалительных медиаторов в системный кровоток. Последние активизируют клеточные популяции и способствуют развитию острофазовой реакции, которая контролируется противовоспалительными медиаторами и их эндогенными антагонистами. За счёт баланса между основными цитокинами, антагонистами медиаторных рецепторов и антителами создаются условия для заживления ран, уничтожения патогенных микроорганизмов и поддержания гомеостаза.
Стадия 3. Генерализация воспалительной реакции. Происходит в тех случаях, когда регулирующие системы не способны поддерживать гомеостаз. Начинают доминировать деструктивные эффекты медиаторов. При этом нарушается проницаемость и функция эндотелия капилляров, формируются отдаленные очаги системного воспаления, развивается моно- и полиорганная недостаточность.
Сепсис - состояние, при котором наблюдается не менее двух признаков ССВО при наличии инфекционного очага (выявляемого клинически или подтвержденного бактериологически, но не обязательно с наличием бактериемии).
Тяжелый сепсис - сепсис в сочетании с проявлениями ПОН, перфузионными нарушениями (ацидоз, лактатемия, нарушение сознания) и артериальной гипотензией, корригирующихся с помощью средств и методов интенсивной терапии.
Септический, или инфекционно-токсический, шок - тяжелый сепсис при наличии синдрома гипоциркуляции, гипоперфузии и падении систолического артериального давления ниже 90 мм рт. ст. (или на 40 мм рт. ст. ниже обычного), несмотря на проводимую интенсивную инфузионную инотропную и вазопрессорную поддержку.
Синдром полиорганной недостаточности (дисфункции) (ПОН) -
симптомокомплекс острых нарушений функций органов и систем, при котором организм не способен самостоятельно стабилизировать возникшие в них изменения.
СПОН ставится при наличии одной или нескольких форм недостаточности внутренних органов и систем. Например, дыхательной недостаточности, сердечнососудистой, почечной недостаточности и др.
Вразвитии полиорганной недостаточности выделяют три основные фазы: индукционную (её результатом является синтез ряда гуморальных факто-ров, запускающих реакции ССВО); каскадную (сопровождается активацией опосредованных каскадов воспа-лительных медиаторов и реакций);
вторичной аутоагрессии (характеризуется выраженной ПОН и стабиль-ным гиперметаболизмом, при которых организм теряет Способность к самостоятельной регуляции гомеостаза.
На съезде экспертов Европейского сообщества интенсивной медицины (European Society of Intensive Care Medicine) и Сообщества реанимационной медицины (Society of Critical Care Medicine) было принято решение пересмотреть понятие сепсиса.
С этой целью в 2014 г. собрана специальная комиссия из 19 ведущих специалистов в области реанимацинной медицины, инфекционных заболеваний, хирургии
ипульмонологии. В период 2014-2015 гг. проведено обсуждение старых дефиниций
ипредложены новые. В результате этой работы в 2016 году был принят III Международный консенсус в отношении определения сепсиса и септического шока
(Sepsis-3). По результатам анализа сделано заключение, что сепсис следует
рассматривать не только как прогрессирующее системное воспаление, а в силу многогранности ответа как жизнеугрожаемое нарушение регуляции реакции макроорганизма (дисрегуляцию) на инфекцию с остро возникшей органной дисфункцией, отражающей повреждение собственных тканей. В качестве инструмента для постановки диагноза следует использовать шкалу SOFA.
Оценка по шкале SOFA степени полиорганной недостаточности при септическом синдроме
Оценка органной недостаточности SOFA (Sepsis-related Organ Failure) является балльной шкалой для оценки полиорганной недостаточности у больных с септическим синдромом, находящихся на интенсивной терапии. Эта шкала была создана для быстрого расчета и описания ряда осложнений у больных в критическом состоянии. Шкала больше предназначена для быстрого подсчета баллов и описания ряда осложнений, чем для прогноза исхода заболевания. Она была разработана Рабочей Группой по проблемам сепсиса Европейского Общества Медицины Критических Состояний.
Эксперты Сепсис-3 предложили следующие определения:
•сепсис - угрожающая жизни органная дисфункция, причиной которой является дисрегуляторный ответ организма на инфекцию;
•органную дисфункцию следует рассматривать как острые изменения в общем
количестве баллов по шкале Sepsis-related Organ Failure Assessment (SOFA) на ≥2 пункта как следствие инфекции. При этом, если исходное количество баллов по шкале неизвестно, его следует принимать как «0» для оценки настоящего состояния. Баллы по SOFA ≥2 пунктов отображают вероятность летального исхода на уровне 10% в общебольничной популяции, что подчеркивает всю тяжесть состояния;
•простыми словами, сепсис является угрожающим жизни состоянием, которое
возникает, когда ответ организма на инфекцию повреждает собственные ткани
и органы;
•пациентов с инфекцией, которые имеют высокий риск смерти или длительного
нахождения в отделении интенсивной терапии, можно идентифицировать при помощи индекса quick SOFA (qSOFA). Он учитывает парциальное давление кислорода, долю вдыхаемого O2, число тромбоцитов, баллы по шкале комы Глазго, уровень билирубина, степень гипотензии и уровень креатинина;
•септический шок следует рассматривать как разновидность сепсиса, при котором наблюдаемые циркуляторные, клеточные и метаболические изменения достаточно выражены для существенного повышения риска смерти;
•наличие септического шока у пациента можно констатировать, если он соответствует критериям сепсиса и у больного выявлена персистирующая
артериальная гипотензия, требующая применения вазопрессоров для поддержания среднего артериального давления ≥65 мм рт. ст., в сочетании с уровнем лактата >2 ммоль/л, несмотря на адекватную инфузионную терапию. При наличии этих критериев вероятность внутрибольничной смерти превышает 40%.
КЛАССИФИКАЦИЯ
I.По характеру первичного очага («входных ворот») инфекции:
-раневой сепсис (первичный очаг - ранения или операционная рана; разновидность этой формы заболевания - послеоперационный сепсис);
-послеродовой сепсис (гнойно-воспалительные осложнения в послеродовом периоде);
-ожоговый сепсис (поверхность после термических ожогов);
- сепсис при заболеваниях внутренних органов (холангиты, эндокардиты, перикардиты, колиты и др.).
II. По клиническому течению:
-молниеносный сепсис (чрезвычайно бурное начало и быстрое развитие (в течение 1-2 сут.); как правило, сопровождается септическим шоком; наблюдается у 2-3
%больных при летальности до 80 %;
-острый сепсис (продолжительность — 5-10 сут. без ремиссий; наблюдается у 40
%больных);
-подострый сепсис (менее выраженные клинические симптомы; продолжительность заболевания — от 2 до 10-12 недель; наблюдается у 50-60 % больных);
-хронический, или рецидивирующий, сепсис (выраженные клинические симптомы; наличие периодов ремиссий и обострения; продолжительность - более 3 мес., нередко - в течение нескольких лет).
III. По наличию или отсутствию первичного очага:
-первичный, или криптогенный, сепсис (первичный очаг отсутствует); возможность существования данной формы сепсиса достаточно спорна;
-вторичный сепсис (при наличии первичного гнойно-септического очага или «входных ворот»).
IV. По виду и характеру возбудителя:
-сепсис, вызванный аэробной микрофлорой: а) грамположительный (стафилококковый, стрептококковый и т.д.; чаще дает метастатические гнойные очаги); б) грамотрицательный (колибациллярный, псевдомонадный, про-тейный и т.д.;
характеризуется выраженной картиной интоксикации, нередко септическим шоком); -сепсис, вызванный анаэробными возбудителями клостридиальный,
неклостридиальный);
-смешанный (аэробно-анаэробный сепсис);
-сепсис, вызванный отдельными видами грибков (кандидозный, аспергиллезный);
-сепсис, вызванный нозокомиальной инфекцией.
VI. По характеру генерализации инфекции:
-септицемия (сепсис без метастазов);
-септикопиемия (сепсис с метастазами гнойной инфекции).
VII. С учётом фаз развития сепсиса:
-фаза напряжения;
-фаза катаболических расстройств: а) стадию формирования ПОН; б) стадию исхода.
Фаза напряжения представляет собой первичную реакцию макроорганизма на
микробную агрессию в условиях несостоятельности механизмов антиинфекционной защиты. Клинически характеризуется преобладанием гемодинамических расстройств и симптомов эндогенной интоксикации. Сопровождается также ухудшением функционирования детоксикационных систем и изменением показателей периферической крови.
Фаза катаболических расстройств характеризуется прогрессирующей дисфункцией основных систем гомеостаза (сердечно-сосудистой, дыхательной, почечно-печёночной и др.), повышением катаболизма белков, углеводов и жиров; декомпенсацией водно-электролитного и кислотно-щелочного состояния. При проведении патогенетически направленного лечения и благоприятном течении заболевания ПОН и тяжелые метаболические нарушения регрессируют. Болезнь переходит в анаболическую форму, наступает выздоровление с восстановлением утраченных функций и структурных компонентов организма. Это один из вариантов исхода сепсиса. Ряд авторов трактуют этот период болезни как анаболическую фазу сепсиса. В случае прогрессирования катаболических расстройств и ПОН заболевание может приобрести неуправляемый характер. Ведущими проявлениями в таком случае
становятся тяжёлая (декомпенсированная) ПОН, глубокие метаболические сдвиги и тяжелые нарушения со стороны иммунной системы (иммунопаралич). При таком варианте исход, как правило, неблагоприятный.
Отличительной особенностью хирургического сепсиса является наличие в организме больных первичного или вторичного гнойно-септического очага. Чаще всего он может быть устранен только путем хирургического вмешательства. К этой группе относится сепсис, являющийся следствием, как хирургических заболеваний, так и осложнений послеоперационного периода. Одной из причин возникновения хирургического сепсиса является длительное существование обширных гнойнонекротических очагов при недостаточно радикальной их санации.
IX. Осложнения:
-инфекционно-токсический шок,
-кровотечение,
-тромбоэмболия легочной артерии и сосудов головного мозга,
-истощение.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ СЕПСИСА
Начальный этап развития сепсиса связан с проникновением микробов и их токсинов (так называемых «микробных модулинов») из первичного гнойного очага в кровеносное русло или лимфатические пути.
Роль первичного септического очага в этиопатогенезе сепсиса
Квозникновению первичного септического очага чаще всего приводят:
▪гнойные заболевания кожи и подкожной клетчатки (абсцессы, флегмоны, фурункулы, карбункулы и др.), ожоги, обморожения, раны (в том числе и операционные), острые (реже хронические) гнойно-воспалительные про-цессы различных органов и тканей (остеомиелит, распространенный гнойный перитонит, абсцессы брюшной полости и внутренних органов, гнойный отит, тонзиллит, сальпингоофорит и др.);
▪ различного рода процедуры при проведении лечебно-диагностических вмешательств и операций (введение катетеров в венозное или артериальное русло, длительная катетеризация мочевого пузыря, продленная ИВЛ, пункция и дренирование плевральной и брюшной полостей, различные вмешательства на сердце, в том числе и диагностические, и др.).
Бактериемия, обусловленная поступлением инфекции из первичных септических очагов, выявляется у 30-35 % больных. При этом в 1/3 наблюдений она не имеет ярких клинических проявлений. Это обусловлено влиянием ряда факторов на иммунологическую (антиинфекционную) защиту организма.
Факторы, способствующие генерализации гнойного процесса
Кфакторам, способствующим генерализации гнойного процесса, относятся:
•массивность инфектанта, его видовая специфичность, биологические особенности бактериальных модулинов;
•размеры и характер первичного септического очага;
•повторная сенсибилизация организма;
•генетически обусловленная индивидуальная резистентность тканей к окружающей микрофлоре.
Устойчивость организма больного к инфекции зависит от анатомических и структурных особенностей его тканей и органов, их биологических и химических свойств, кровоснабжения, лимфооттока, возможности к репарации. Следует отметить, что правило «чем лучше кровоснабжение тканей — тем надежнее их барьерная функция и антиинфекционная защита» имеет исключения. Так, ряд тканевых структур (хрящ, роговица и др.), обладающих диффузионным типом питания, в то же время характеризуются высокой устойчивостью к инфекционному фактору. Источником эндогенного инфицирования и интоксикации при сепсисе может стать пищеварительный тракт больного. Происходит это, когда стенка кишки становится
проницаемой для микрофлоры, содержащейся в ее просвете. Микроорганизмы и их токсины в условиях нарушенного внутрикишечного биоценоза могут поступать в системный кровоток через лимфатическую или портальную систему. При этом они инициируют процессы патологической активации медиаторных воспалительных систем, усугубляют эндотоксикоз и способствуют развитию ПОН. Описанный процесс называется кишечной бактериальной транслокацией и является одним из ведущих факторов бактериемии при сепсисе. Кишечной бактериальной транслокации способствуют нарушения системной гемодинамики, замедление пассажа содержимого по кишечнику, эндотоксемия, снижение общей иммунореактивности, белковое голодание, изменение микрофлоры кишечника в результате лечения антибиотиками, гипоксия, стресс и др.
Патогенность бактериальных модулинов зависит от совокупности факторов вирулентности микробной клетки, к которым относятся:
•адгезины — бактериальные белки, ответственные за взаимодействие с клетками хозяина (преимущественно эпителиальными);
•агрессины — бактериальные молекулы, обладающие повреждающим действием на клетки-мишени;
•инвазины — бактериальные белки, позволяющие бактериям проникать внутрь клетки;
•импедины — бактериальные компоненты, ингибирующие действие защитных сил макроорганизма;
•модулины — бактериальные молекулы, индуцирующие синтез цитокинов.
Бактериальные модулины, воздействуя на моноциты, фибробласты, лимфоциты и эпителиальные клетки, индуцируют в них синтез цитокинов, которые влияют на эти клетки ауто-, пара- и эндокринным путями – хемотаксис, метаболическая активность, пролиферация, дифференцировка и запуск клеточного апоптоза.
Механизмы действия на организм человека грамположительных и грамотрицательных микроорганизмов имеют определенные особенности.
Грамположительные бактерии благодаря слабым электростатическим (Ван-дер-вальсовым) силам связываются с белками макроорганизма (фибронектином, фибриногеном, коллагеном и др.). Это способствует выработке бактериями внеклеточного гликокаликса, защищающего их от действия антибиотиков, а также специфических, биологически активных веществ - факторов агрессии. Белки макроорганизма связываются с микробами и взаимодействуют с соответствующими рецепторами на поверхности нейтрофилов, способствуя их активации.
До 25-30 % грамположительной микрофлоры, инициирующей развитие сепсиса, составляют стафилококки (St. albus, St. aureus и др.). Патогенные свойства последних обусловлены выработкой специфических ферментов (коагулазы, гиалорунидазы, фибринолизина) и токсинов (лейкотоксина, энтеротоксина, дермонекротоксина и др.). В какой-то степени именно в силу этого стафилококковый сепсис в 95 % случаев сопровождается появлением метастатических гнойных очагов.
Реже возбудителями сепсиса являются стрептококки (Str. pyogenes, Str. haemoliticus и др.). Их патогенные свойства связаны с набором повреждающих факторов (стрептолизина, гемолизина, фибринолизина, некротоксина, лейкоцидина). Стрептококковый сепсис отличается более редким развитием септико-пиемических очагов при общей тяжести клинического течения.
Грамотрицательные бактерии после взаимодействия входящего в их состав липополисахарида (он образует макромолекулярный комплекс эндотоксина) с протеинами макроорганизма образуют липид-А-связанные комплексы. Последние представляют собой ключевые медиаторы поведения лейкоцитов и являются индукторами активации макрофагов. Эндотоксины грамотрицательных микроорганизмов увеличивают секрецию интерлейкинов (ИЛ) - 1, 6, 10, фактора некроза опухолей-α (ФНО-α), способствуют высвобождению нейтрофилов из костного мозга. Кроме того, важно отметить способность эндотоксина к агломерации или

опсонизации клеток организма (в первую очередь эндотелиальных макрофагов и нейтрофилов), приводящей к гемокоагуляции, некрозу эндотелия и развитию ПОН.
В последнее время среди этиологических факторов хирургического сепсиса существенно выросло значение грамотрицательной микрофлоры (рис.4). Особое место в ней занимает синегнойная палочка (Pseudomonas aeruginosa), которая чаще всего встречается на ожоговых ранах, в перитонеальном экссудате, и при возникновении госпитальной инфекции. Патогенность синегнойной палочки обусловлена, прежде всего, её способностью вырабатывать эндотоксин, обладающий и протеолитическими свойствами. Хирургический сепсис, вызванный данным возбудителем, обычно протекает по типу молниеносного, нередко - с явлениями септического шока.
Среди грамотрицательной микрофлоры в развитии сепсиса важную роль играет кишечная палочка (Е. coli). Последняя является представителем семейства энтеробактерий (Enterobacterium), относится к условно-патогенным микроорганизмам. Однако, при попадании в инфицированные ткани она является источником гнойносептического процесса. Классическим примером служит участие кишечной палочки в развитии перитонита и абдоминального сепсиса. Патогенные формы Е. coli выделяют как экзо-, так и эндотоксин.
Грамотрицательная микрофлора
Эндотоксин (липополисахарид)
Липид А |
Ядерный |
0-специфический |
|
антиген |
антиген |
Полисахаридсвязывющий белок в организме больного
Клетки-мишени (моноциты/макрофаги, лимфоциты Фибробласты, эндотелиоциты сосудов)
Хемотакс |
Метаболическ |
Проли- |
Клеточн |
Диффе- |
ис |
ая |
ферац |
ый |
ренциров |
|
активность |
ия |
апоптоз |
ка |
Рис.4. Роль граммотрицательной микрофлоры в патогенезе хирургического сепсиса
Среди анаэробных возбудителей сепсиса чаще всего выявляются представители неклостридиальной анаэробной инфекции (бактероиды, фузобактерии, пептококки, пептострептококки, эубактерии, фузобактерии, вейлонеллы и др.). Сепсис, вызываемый ими, протекает тяжело, зачастую со скудной клинической симптоматикой и требует наиболее интенсивных методов лечения.
Одним из представителей неклостридиальной анаэробной микрофлоры является семейство бактероидов (Bacteroides). Как правило, они продуцируют многочисленные протеолитические ферменты, в том числе гепариназу. Этот фермент способствует образованию микротромбов и клеточных агрегатов в системе микроциркуляторного русла, существенно ухудшая тканевой кровоток, стимулирует процессы диссеминированного внутрисосудистого свертывания крови, может вести к разнообразным эмболическим осложнениям. Отмечен синергизм действия бактероидов
