
- •1. Пептиды. Определение. Классификация. Кислотно-основные свойства пептидов.
- •2. Химические свойства пептидов.
- •3. Биологически активные пептиды.
- •4.Белки. Определение. Классификация.
- •5. Функции белков.
- •6. Особенности структурных организации белков.
- •7. Третичная структура белка: химические связи, структура, пример белка.
- •8. Четвертичная структура белка: химические связи, строение, пример белка
- •4. Липопротеины: укажите простетическую группу, приведите примеры.
- •9. Вторичная структура белка: химические связи, строение.
- •10. Нуклеопротеины: укажите простетическую группу, приведите примеры.
1. Пептиды. Определение. Классификация. Кислотно-основные свойства пептидов.
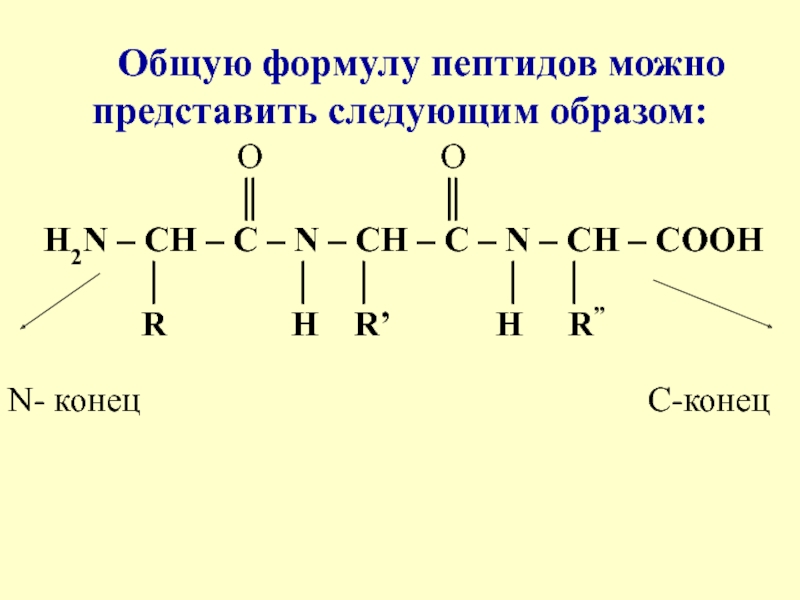
Пептиды-это соединения, построенные и содержащие в своем составе до 100 аминокислотных остатков.( семейство веществ, молекулы которых построены из двух и более остатков аминокислот, соединённых в цепь пептидными (амидными) связями —C(O)NH—)
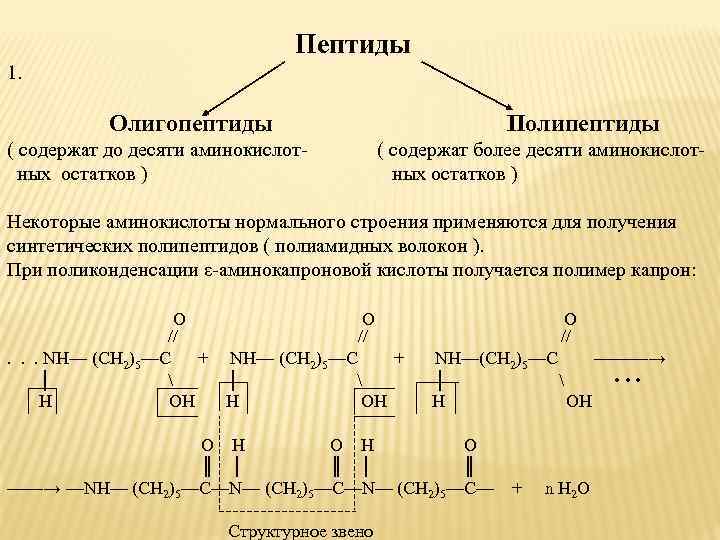
Классификация: 1.Олигопептиды (низкомолекулярные) содержат в цепи не более 10 аминокислотных остатков; 2.Полипептиды(высокомолекулярные) содержат в цепи от10-100 аминокислотных остатков.



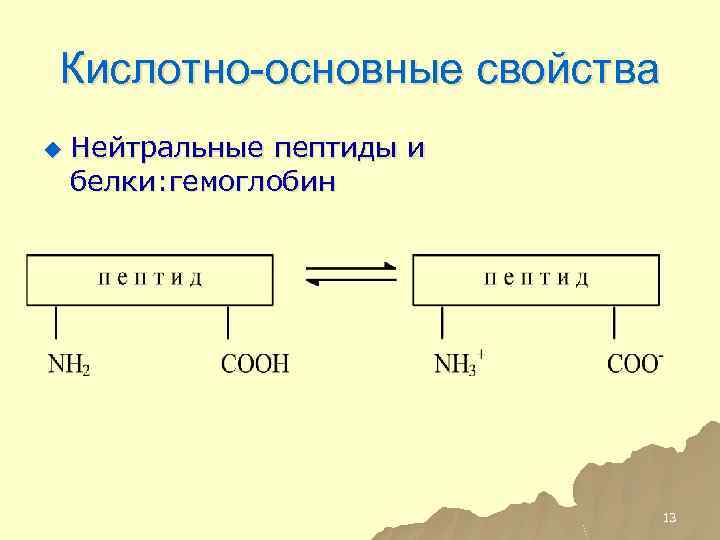
Кислотно-основные свойства пептидов
Пептиды могут быть нейтральными, кислыми и основными.
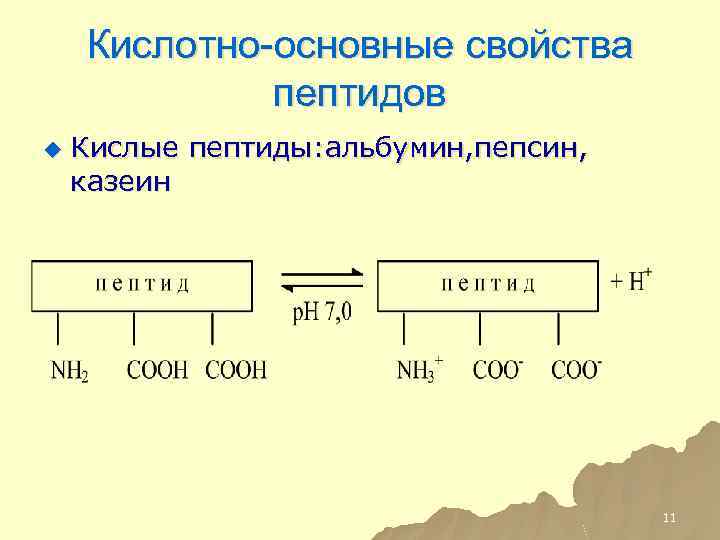
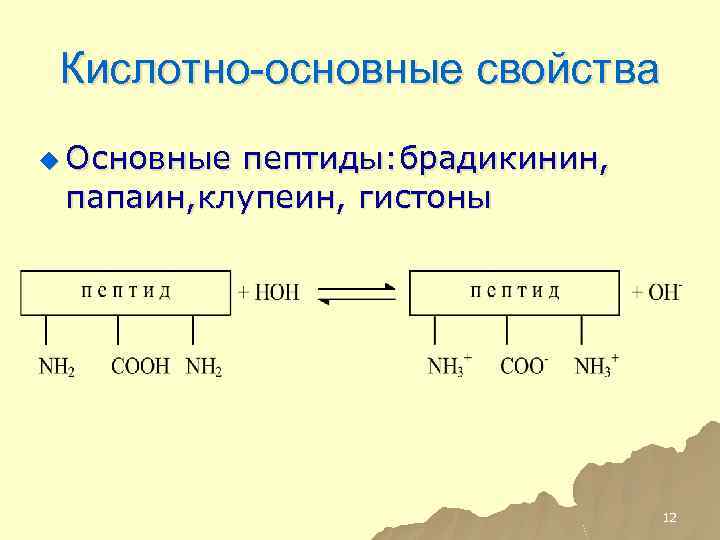
Им соответствуют определѐнные ИЭТ (Изоэлектрические точки), т.е. те значения рН при которых они находятся в ИЭС.
Это определяется:
1.Аминокислотным составом
2.Соотношением (R-) радикальных аминокислотных остатков
Растворы пептидов и белков в ИЭТ наименее устойчивы т.к. имеют определенные факторы устойчивости
1.Лишены заряда
2.Не имеют электрофоретической подвижности
2. Химические свойства пептидов.
Определяются наличием в структуре, альфа и R-функциональных групп аминокислотных остатков.
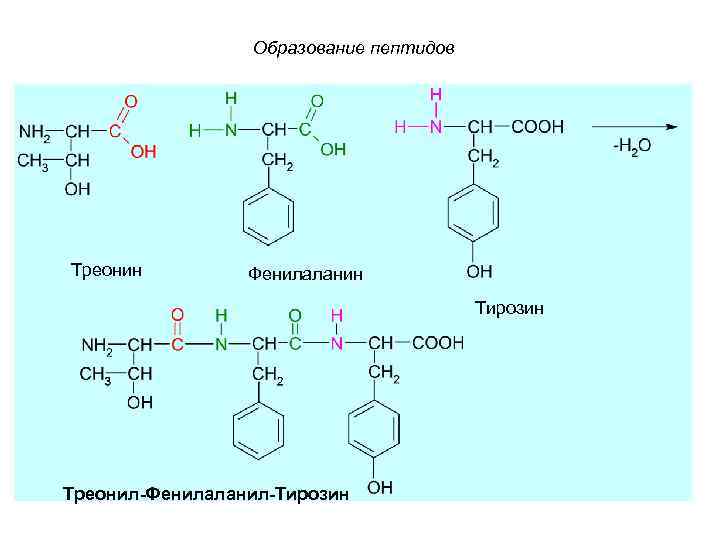
Пептидную молекулу формально можно представить, как продукт поликонденсации альфа а.к протекающей с образованием пептидной(амидной) связи между а.к.
Конституция пептидной цепи одинакова для всех пептидов. Цепь имеет неразветвленное строение и состоит из чередующихся амидных и метиновых групп.

Один конец цепи, на которым находится, а.к со свободной NH2-группой, называется N-концом другой на котором находится, а.к, имеющая свободную-СООН группу называют С-концом
Пептиды и белковые цепи принято записывать, начиная с N-конца.
Пептидные связи способны гидролизироваться как в кислой, так и в щелочной среде.
Пептиды гидролизируются с образованием более коротких цепей (частичный гидролиз), либо смеси aльфа-а.к при полном гидролизе
В живых системах процесс гидролиза катализируется ферментамипептидазами.
Ферменты избирательно расщепляют пептидные связи.
Например: E-трипсин гидролизирует только те пептидные связи, в которых принимают участие –СООН-группа лизина и аргенина,а хемотрипсин –связи с участием –СООН-ароматических а.к(фен,три,тир).
В клеточной среде существуют много свободных пептидов, обладающих высокой биологической активностью




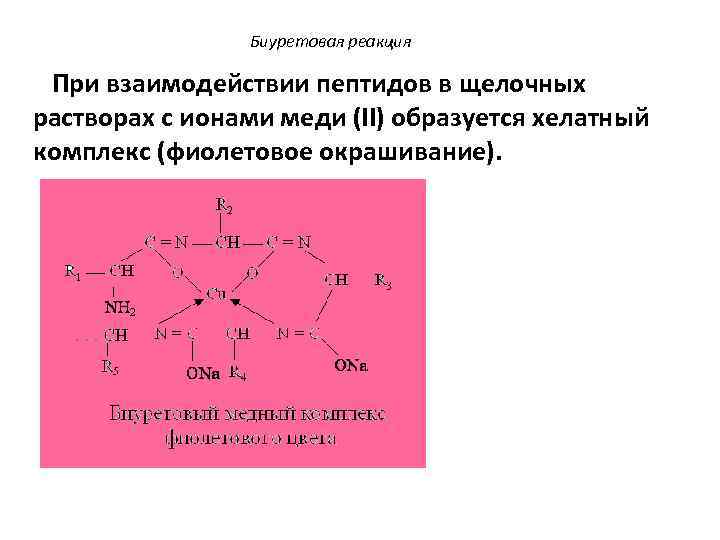
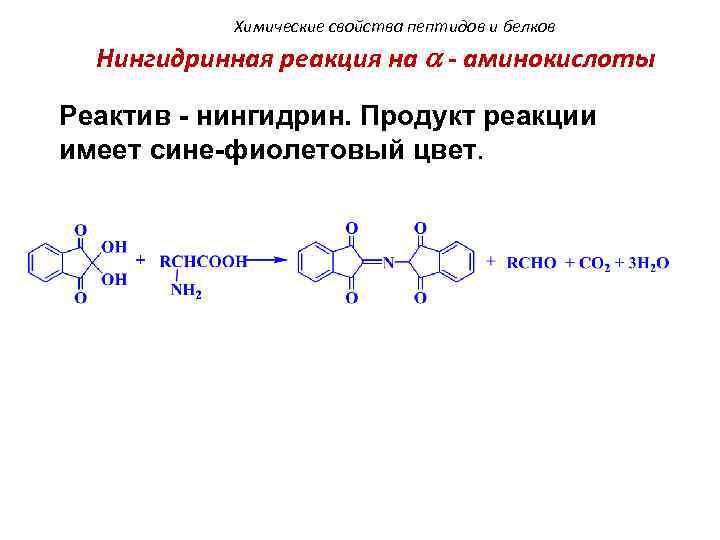


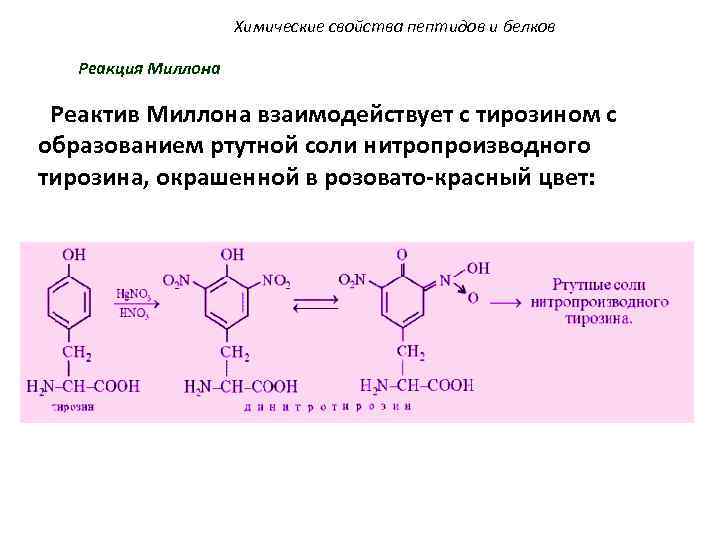



3. Биологически активные пептиды.
Их можно разделить на несколько групп:
1.Пептиды-гормоны
Они вырабатываются эндокринными железами и с током крови переносятся в ткани и органы.в которых регулируют специфические функции.
Например: гормоны поджелудочной железы.
Инсулин (51 а.к.)-вырабатывается В-клетками поджелудочной железы, понижает уровень глюкозы в крови.
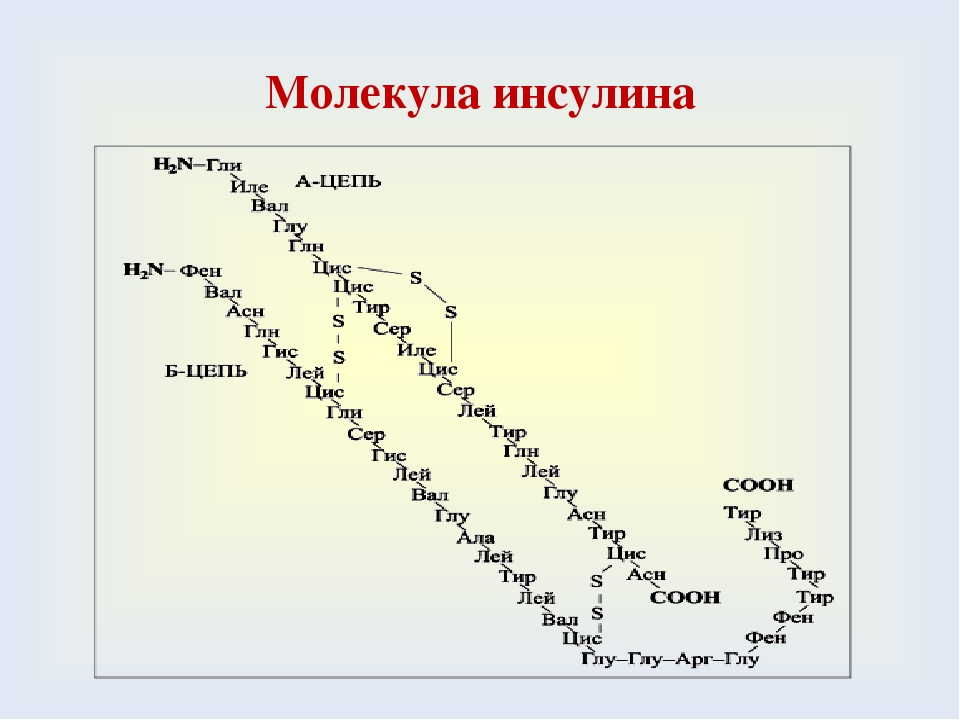
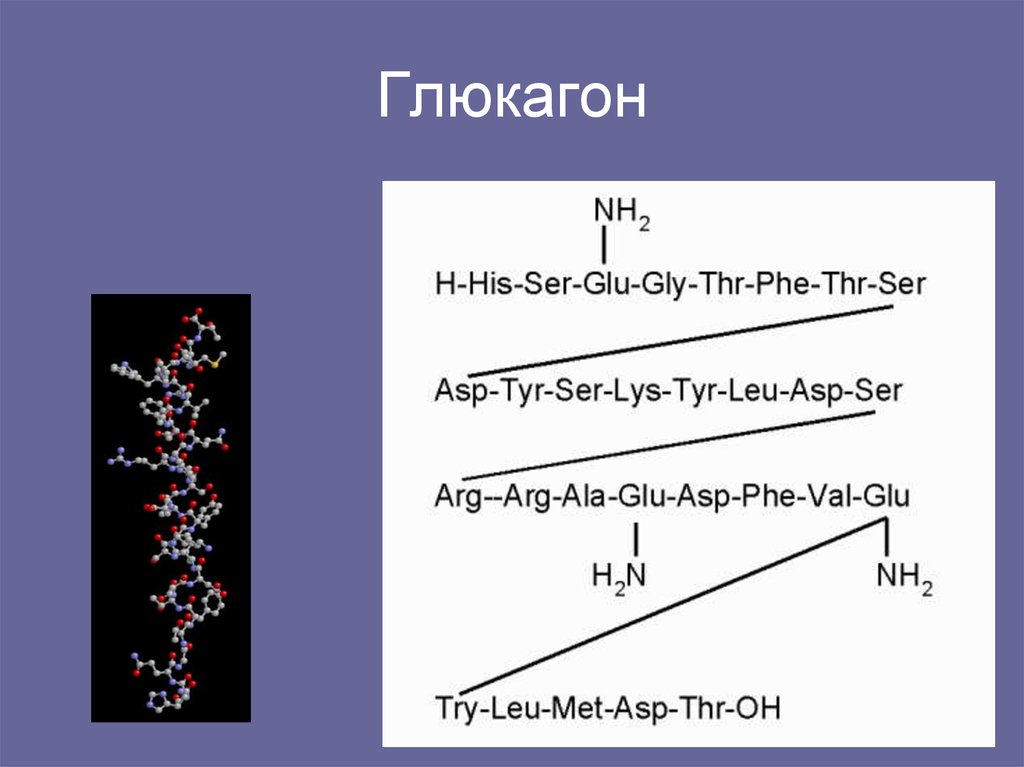
Глюкагон (29 а.к)-вырабатывается альфа-клетками поджелудочной железы, повышает уровень глюкозы в крови.
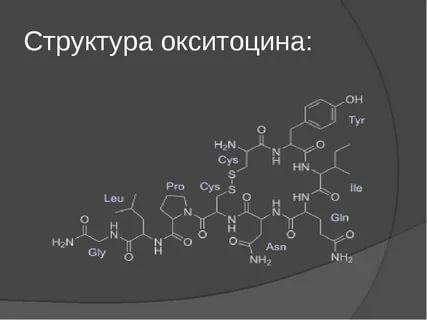
Гормоны гипоталамуса, которые концентрируются в задней доле гипофиза:
Окситоцин-стимулирует сокращение гладкой мускулатуры.
Вазопрессин (антидиуретический гормон)-задерживает воду в организме.

2.Пептиды, принимающие участие в пищеварении.
Гастрин(17 а.к)-синтезируется в желудке, стимулирует синтез соляной кислоты.

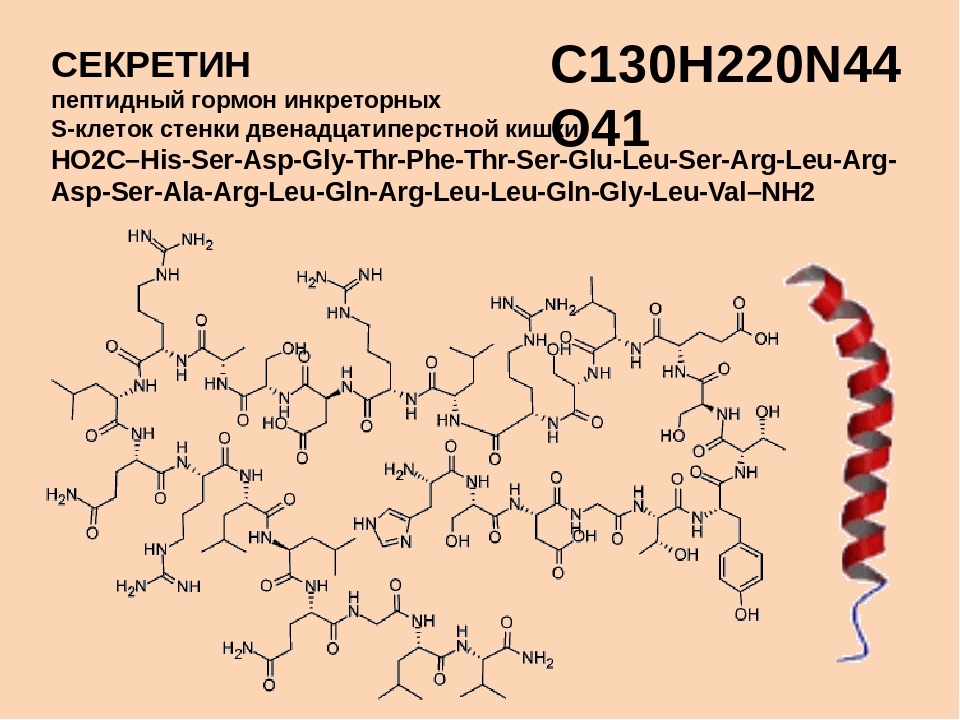
Секретин (27 а.к)-синтезируется в слизистой 12перстной кишки, стимулирует секрецию панкреатического сока.
3.Группа вазоактивных пептидов, влияющих на тонус сосудов.
Ангиотензин II (98 а.к)-оказывает сосудосуживающее действие
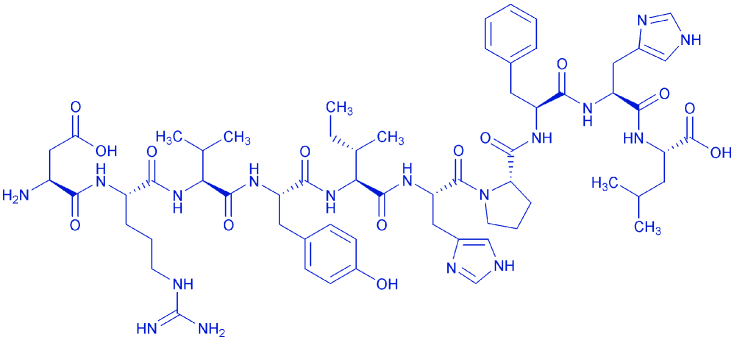
Брадикинин (9 а.к)-мощное сосудорасширяющее средство, повышает проницаемость капилляров, вызывает боль при воспалении.
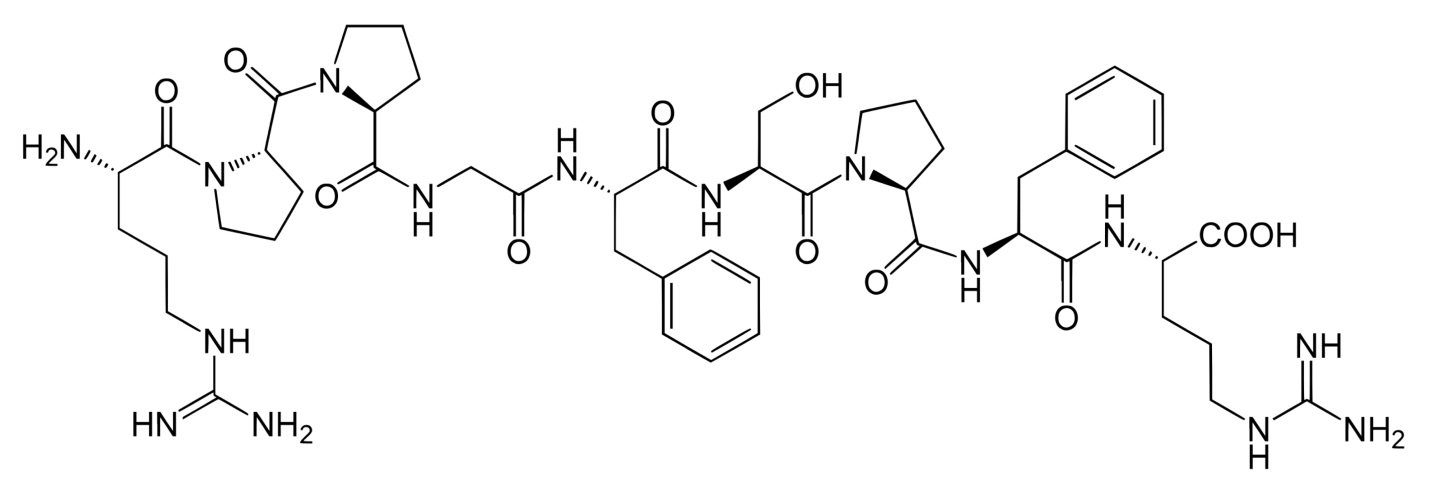
Атриопептиды(от 23 до 90 а.к остатков)-вырабатываются в предсердии,оказывают сосудорасширяющее действие .
4.Нейропептиды-синтезируются нервной тканью. К ним относят:
Энкефалины(5 а.к пентапептиды)-вызывают в клетках нервной ткани аналгезию, то есть ослабление болевых ощущений, проявляют наркотическое действие.
Эндорфины (32 а.к)-вызывают обезболивание, влияют на поведение (питание, эмоции, обучение) регулируют температуру тела и кровяное давление.
5.К пептидам относятся многие антибиотики.
Например:
Гликопептиды: Ванкомицин, Тейкопланин -препараты выбора для лечения стафилококковой инфекции.
6.Отдельно выбирают глутатион (3 АК - трипептид)
Глу-цис-гли
Наличие в его составе SH –групп-цис определяет его защитные свойства для поддержания целостности клеток(например эритроцитов)
Биологическая активность и специфичность действия пептидов полностью определяется последовательностью аминокислотных остатков.
