
271
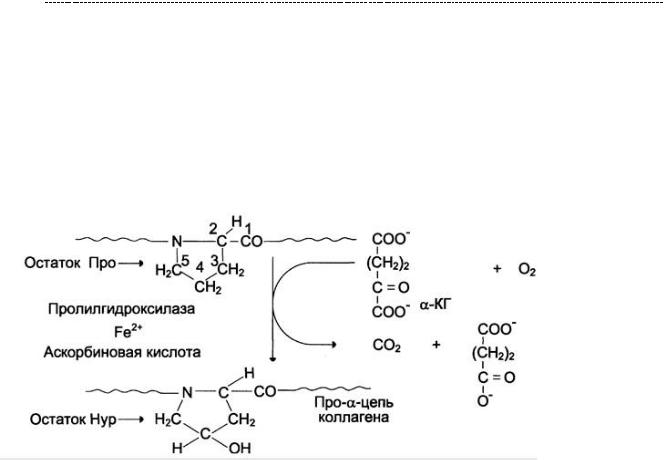
16.2.2. Синдром Элерса – Данлоса.
Пациентам с синдромом Элерса – Данлоса (СЭД) всегда рады в одном месте: в
цирке. Эти ребята могут гнуть свои суставы как хотят. Согнуть колено голенью вперёд до прямого угла или разогнуть большой палец, чтобы он доставал до предплечья? Ерунда. Правда и платят за такую «суперспособность» эти ребята тоже достаточно дорого, я бы сказал, переплачивают.
Структурные дефекты коллагена в связках, суставах, коже делают суставы гипермобильными, а кожу – чрезмерно эластичной. И всё бы ничего, только повреждаются такие суставы очень часто. Переломы костей, вывихи тут является обычным делом. А малейшие повреждения кожи чреваты обширностью и длительностью заживления.
Особенность данного синдрома заключается и в его гетерогенности. В случае СЭД может нарушаться синтез I, III или V типов коллагена. В некоторых случаях имеется дефект лизиноксидазы – того самого фермента, что обеспечивает гидроксилированиелизинаиформированиеводородныхсвязейвколлагане. Вещё более редких случаях – это дефект N – пептидазы проколлагена, при котором тоже ничего хорошего. Любопытно, что даже среди заболевших, пациенты являются
( https://medicalplanet.su/Patfiz/patogenez_sindroma_elersa-danlo.html )
272
по - своему уникальными: выделяют аж 6 типов СЭД, который характеризуется своими клиническими особенностями. Общим является только одно: дефект синтеза коллагена.
16.2.3. Цынга. Авитаминоз С.
Предлагаю тебе ещё раз вспомнить некоторые этапы синтеза коллагена.
Аскорбиновая кислота, она же витамин С, наряду с ионами железа, является важным кофактором гидроксилирования аминокислоты пролил, значение этого прцоесса для прочности коллагена я разжёвывал уже раза два точно, третий не буду.
Логично предположить, что в условиях отсутствия витамина С коллаген не будет таким прочным, а ткани, содержащие любые виды коллагена, тем более.
Будут ли твои кости в такихусловияхломаться чаще, чем улюбителей спортивных мини – велосипедов или мотоциклов? Думаю, нет. Но то, что зубов будет меньше,
чемхотелосьбы,этода,таккаквусловияхнарушениягидроксилированияпролина в коллагене, будет ослабевать дентин, его будет меньше, и зубы не будут также прочно держаться в своей лунке. Бонусом к такому подарку судьбы будет и повышенная ломкость капилляров, т.к. коллаген– он и в микрососудистом русле коллаген. Справедливости ради стоит сказать, что даже в нашей высокоразвитой стране цынга является достаточно редким явлением. Всё же её достаточно во многих продуктах, похожих на овощи и фрукты, распространение коих повсеместное.
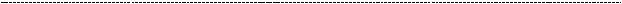
273
16.2.4. Синдром Альпорта.
В гломелурярной мембране почек, а также в хрусталике глаза нашёл свою нишу коллаген IV типа. Там он обеспечивает нормальную архитектонику ткани, в
клубочках не пропускает того, чего не следует. Но проблемы в нашей жизни случаются с каждым. Существуют счастливчики, унаследовавшие от матери Х – хромосому с дефектным COL4A5 – геном, который неправильно кодирует а5 –
цепь коллагена. Коварство данного заболевания в том, что манифестировать оно может когда угодно. А манифестирует оно гематурией (просачиванием эритроцитовизкровивпросветканальца вмочу).Самопосебеявлениенеявляется прям жизнеугрожающим, но постепенно грубые нарушения в структуре гломерулярной мембраны почек, наряду с гематурией, приводят к развитию хронического гломерулонефрита (фокально – сегментарный или же иной вариант)
снеизбежнымразвитиемхроническойпочечнойнедостаточности,чтосамопосебе одно из самых неприятных явлений в этой жизни. В ряде случаев, при синдроме Альпорта поражение почек сочетается спатологией хрусталика и сенсоневральной глухотой. по - видимому, в результате отложения дефектного коллагена в соответствующих структурах. (хотя в отношении глухоты врать не буду – точные механизмы для меня не понятны).
Любая гематурия без очевидных причин является поводом подозревать возможность наличия синдрома Альпорта у жертвы твоего медицинского курирования. Особенно если есть отягощённый семейный анамнез, т.е. ранняя хроническая почечная недостаточность в семье. Иногда наблюдается протеинурия, что вполне закономерно в условиях нарушения пространственной организации гломерулярной мембраны. И особенно должно настораживать наличие нарушений со стороны органов зрения и слуха. Возможно ли манифестация этих нарушений раньше гематурии? Теоретически, в этой жизни возможно всё. Можно ли вылечить человека с этим синдромом раз и навсегда?
Только если пересадкой почки, но проблем с глазом и слухом это не решит.
274
16.3. Фибриллинопатии. Синдром Марфана.
Ранее мы обсуждали важную роль фибриллина в формировании эластических волокон соединительной ткани. Так вот, мутация в гене фибриллина (чаще всего
FBN 1) приводит к развитию синдрома Марфана, синдрому с достаточно характерным фенотипом и законмерными патологическими нарушениями. Чтобы понять особенность данного синдрома, стоит вспомнить, где же эластические волокна приобретают наиболее важное значение.
Несмотря на их повсеместное распространение, наиболее выраженно их содержание в проксимальных отделах аорты, в связках и цилиарном теле хрусталика глаза, в лёгких, в меньшей степени – створки клапанов и хорды.
В аорте они необходимы для сглаживания давления, возрастающего при сердечном выбросе. Давление, создаваемое левым желудочком (у обычных людей
120 мм рт. ст), могло бы быстро привести к уничтожению аорты, если бы кинетическая энергия сердечного выброса не превращалась в потенциальную энергию за счёт мгновенного расстягивания эластических волокон аорты. Эта же потенциальная энергия передаётся дальше, на дальнейшие участки сосудистой стенки, что лежит в основе формирования пульсовой волны. Со створками клапанов и хордами история такова, что при повышении давления в желудочках велик риск регургитации (т.е. заброса крови из желудочков в предсердия, что не является нормальным). Этому препятствует эластическая тяга хорд, которые переброшены от сосочковых мышц миокарда до створок клапанов и препятсвующие этой самой регургитации, они как бы тянут створки обратно в желудочек, не давая им отклоняться в полость предсердий.
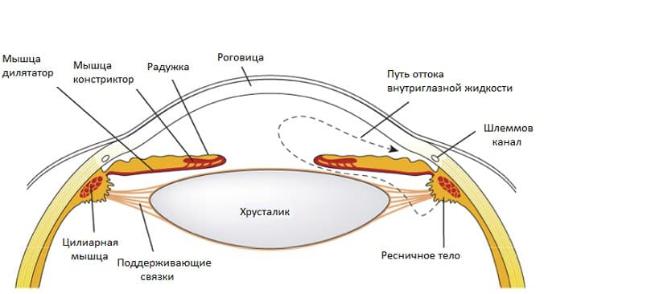
В отношении цилиарного тела и связок, здесь нужно углубляться в биомеханику зрения.
275
Посредством изменения натяжения поддерживающих связок хрусталика,
изменяется преломление хрусталика, что позволяет глазу адаптироваться к восприятию предметов, располагающихся от глаза на разных расстояниях, т.е.
прцоесс аккомодации. Это позволяет только различать предметы на разных расстояниях, а понимать, что они располагаются на разных расстояниях, можно только при условии целостности зрительной коры головного мозга.
Эластические волокна лёгких и их роль обсуждается в главе 14, где я рассказывал о дефекте а1 – антитрипсина.
Таких счастливчиков, которые приобрели путём аутосомно – доминантного насильственного наследования синдром Марфана, приблизительно один на пять тысяч человек, что можно назвать достаточно частым явлением. Вероятность встречи с таким пациентом выше, чем твои шансы поступить в бюджетную ординатуру.
Фенотип, как я уже сказал, у таких людей уникален и характеризуется как костными, так и внекостными проявлениями. Но если внекостные проявления, о
которых мы скажем далее, можно объяснить снижением качества и количества эластических волокон, то вот костные изменения этим не объясняются. Но есть нюанс, о котором я не сказал тебе ранее.
Фибриллин очень непростой белок, и помимо участия в формировании эластических волокон и клеточной адгезии, он способен к секвестрации очень важного цитокина – трансформирующего фактора роста – В (TGF – B). Данный
276
цитокин усиливает продукцию межклеточного матрикса, но это далеко не всегда приводит к правильному её формированию. Секвестрация TGF - B цитокина фибриллином обеспечивает своего рода регуляцию содержания этого цитокина в тканях. Говоря проще, фибриллин препятствует чрезмерному воздействию TGF – B на фибробласты, обеспечивая более дозированное и равномерное действие данного белка, т..е контролируя его биодоступность.
(Для тех, кто вообще в танке. Представь ситуацию: мать (в роли фибриллина)
принесла тебе кучу конфет (TGF – B), но заявила, что ты (юный фибробласт)
можешь брать по одной конфетке в день, ибо у тебя диабет (компенсированный).
Но случается непоправимое, и у твоей мамы появляется личная жизнь и она больше не следит за твоей диетой. И ты съедаешь за раз месячный запас этих конфет. И тебе конец. С фибриллином и TGF – B в тканях ситуация примерно такая же). Эту способность свзяывают с наличием доменом в фибриллине,
которым он может связывать TGF – B, но точные биохимические нюансы мне не известны. Тем не менее, гипотеза избыточной активации TGF – B – сигнального вполне объясняет наблюдаемые при синдроме Марфана изменения костной ткани,
т.е. избыточное и неадекватное образование соединительной ткани. Имеются данные успешного предотвращения изменений в аорте и хрусталике посредством введения антител к TGF – B.
Клинические проявления. Внешне такие люди характеризуются высоким ростом, длинных конечностей, длинные пальцы, узнать их чрезвычайно легко.
Поскольку этический комитет заброкует эту книгу, если я выложу фотографии пациентов с данным синдромом, просто вбей в гугле и ты больше никогда их не пропустишь.
При данном синдроме также имеется гипермобильность суставов, так как связки не имеют должной эластичности и не возвращают сустав в исходное физиологическое положение, если ты решишь поиграться с суставом. К другим костным деформациям также отностися долихоцефалия (длинная голова) с
выпуклостями и деформациями, а тажке деформация позвоночника (кифоз,
сколиоз).
277
Но это всё лишь внешние проявления, и сами по себе они не несут непосредственной угрозы (с этим можно жить), хотя и снижают качество жизни.
Более серьёзными являются внекостные проявления. В первую очередь,
дислокация хрусталика, его смещение кнаружи и кверху, что обусловлено слабостью связочного аппарата цилиарной мышцы. Хрусталик болтается как не знаю (знаю) что, и никакую аккомодацию не обеспечивает (как и адекватное зрение). Но даже это не является ведущей причиной проблем у таких пациентов.
Наиболее серьёзные изменения в аорте. Отсутствие достаточного эластического каркаса, нарядус чрезмерной активацией сигнального пути TGF– Bв толще аорты приводит к тому, что вместо медии аорты, полной эластических сосудов, готовой к любому сердечному выбросу, как Хабиб перед ирландцем, при синдроме Марфана вместо мидии формируется фиброзная ткань, не способная оказывать сопротивление высокому давлению крови. В результате формируется растяжение фиброзного каркаса проксимальной аорты и тяжёлая аортальная недостаточность
– клапанный порок, при котором часть крови, выброшенная в аорту, вовзращается в левый желудочек, ибо аортальный клапан не способен её удержать. Последствия для гемодинамики чрезвычайные, так как об адекватном снабжении органов и тканей можно говорить лишь условно (ну, это при декомпенсации, естественно).
Другой проблемой становится пролапс атриовентрикулярных клапанов, чаще всего митрального. Его опасность – риск перейти в недостаточность соответствующего клапана, что чревато уже описанной нами регургитации крови в предсердия. Это ведёт за собой целый ворох кардиологических проблем и приближает пациента к койке ближайшего морга. Но и на сердце проблемы не кончаются.
Своими глазами, работая на отделении торакальной хирургии, видел пациента с рецидивирующим спонтанным пневмотораксом. Ему было лет 19, но эпизодов спонтанного пневмоторакса в его жизни было достаточно. Его внешность была очень похожа на ту, что описывали в книгах: высокий, худощавый, с длинными пальцами и кифотически – изменённой грудной клеткой. Бросалась в глаза и некоторая инфантильность, хотя вполне вероятно, что это отпечаток частых
278
госпитализаций и длительной болезни. Взглянув в его карту, я подтвердил свои догадки: в сопутсвтующих забоелваниях был указан синдром Марфана. У молодых людей с данным синдромом пневмоторакс случается чаще, чем хотелось бы.
Несмотря на описанные мною ужасы, стоит сказать, что такое наблюдается не всгеда. Считается, что синдром Марфана гетерогенен как в отношении характера мутаций, так и клинического фенотипа. Дело в том, что ген фибриллина FBN 1
достаточно велик и допускает наличие различных вариантов аллелей, которые и обусловливают различную пенетрантность данного состояния. И что интересно:
изменения скелета не коррелируют с изменениями внутренних органов. Поэтому стоит быть чрезвычайно внимательным при обнаружении изменений в аорте или клапанах на ЭХО – КГ, дислокации хрусталика или рецидивирующего пневмотораксаумолодыхпациентов,возможнозаэтимкроетсясиндромМарфана.
Иногда единственным проявлением синдрома Марфана в течение жизни может служить пролапс митрального клапана, хотя не каждый пролапс ассоциирован с синдромом Марфана. И пусть тебя не смущает, что далеко не всегда в жизни всё так, как описываются в книжках или на фотографиях в интернете.
16.4. Белки клеточной адгезии и их значение при патологии
16.4.1. Фибронектин как индикатор эндотелиальной дисфункции
Наследственной патологии, которая была бы вызвана дефектом синтеза или структуры фибронектина, на сегодняшний день не описано. Полагаю, дети с таким дефектом были бы нежизнеспособными, если вспомнить, что фибронектин обеспечивает миграцию клеток в эмбриогенезе – важного элемента развития зародыша.
Однако, про фибронектин всплывает иная информация, которая потенциально может стать важным элементом лабороторной диагностики множества патологических состояний, сопровождающихся эндотелиальной дисфункцией.
279
Фибронектин в организме существует в двух фракциях: в тканевой (где он выполняет свои функции в виде межклеточной адгезии и пр., это так называемый клеточный фибронектин) и в плазменной. Источником плазменного фибронектина
98 % является печень. И лишь 1 – 2 % плазменного пула фибронектина являются ткани. Повышение уровня плазменного фибронектина может свидетельствовать о развитии патологических процессов. Но каких? И в чём биохимическое обоснование такого феномена?
Вопрос корреляции уровня плазменного фибронектина и развития тех или иных патологических состояний интересовал и интересует многих исследователей. Ими получены данные, что рост плазменного фибронектина характерен для сахарного диабета, сопровождающегося характерной для него микроангиопатией. (глава 7).
Не менее характерно это и для прогрессирюующего атеросклероза артерий. Эти состояния объединяет наличие при них эндотелиальной дисфункции, и
фибронектин плазмы в данном случае является отражением процессов,
происходящих в стенке сосудов: разрастание компонентов межуточного вещества и соединительной ткани в целом.
Эндотелий не является обычным инертным пластом, выстилающим сосуды изнутри. Эндотелиальные клетки являются чрезвычайно активными элементами поддержания реологии крови, баланса в системе гемостаза, тонуса сосудов.
Эндотелиальная дисфункция заключается в невозможности адекватно обеспечивать регуляцию вышеуказанных физиологических параметров и выражается в неспособности эндотелия поддерживать равновесие между образованием вазодилатирующих, атромбогенных, антипролиферативных факторов, с одной стороны, и вазоконстриктивных, протромботических и пролиферативных веществ, которые синтезирует эндотелий, — с другой, т.е.
сдвиг происходит во вторую сторону, что и порождает целый ворох проблем.
Дисфункция эндотелия может быть самостоятельной причиной нарушения кровообращения в органе, поскольку нередко провоцирует ангиоспазм или тромбоз сосудов.
280
Исходя из этого, другой группой исследователей была обнаружена корреляция риска тромботическихявлений, в частности, атеротромбоза, с повышением уровня плазменного фибронектина. В данном случае, такое повышение может быть отражением усиления мембранной активации тромбоцитов при повреждении эндотелия. Насколько сам фибронектин имеет патогенное значение в реализации тромбозов, пока не совсем ясно, но продукты его деградации – фрагменты фибронектина – являются протромботическим фактором.
Фибронектин, под действием матриксных металлопротеиназ 2 и 9 распадаются до фрагментов, которые, в силу своего связывания с фибрином, становятся дополнительным компонентом в стимуляции активности тромбоцитов, что может привести к внутрисосудистому тромбообразованию. Исходя из этого, нормальный уровень фибронектина в условиях тромбообразования может сбивать с толку в виду повышенной деградации и диктует необходимость дополнительной оценки содержания фрагментов фибронектина в крови.
Таким образом, фибронектин может иметь определённое диагностическое значение в лабораторном элементе диагностики патологических состояний,
сопровождающих эндотелиальной дисфункцией: атеросклероза, артериальной гипертензии, варикозного поражения вен, хронической сердечной недостаточности, сахарного диабета с микроангиопатией, хронической обструктивной болезни лёгких (хотя у меня пока сомнения на этот счёт),
хроническая болезнь почек и пр. Насколько это способно изменить алгоритмы введения таких пациентов? Кардинально нет, но в качестве дополнения и для мониторинга выраженности патологического состояния, почему бы и нет.
При написании данного параграфа были использованы статьи, которые указаны в библиографическом списке под номерами 2527.
