

Задача 4.
Используя рисунок 2.10, определите, в каком участке биомембраны (А – Г) будет осуществляться максимальный транспорт липидорастворимых молекул.
Задача 5.
Пять ЛС имеют различные коэффициенты распределения масло/вода (К). У какого из этих веществ скорость пассивной диффузии через билипидную биологическую мембрану будет максимальной, если они имеют следующие значения К: первое вещество – 0,05, второе – 0,3, третье – 0,7, четвертое – 1,5, пятое – 2,0?
Задача 6.
Вычислите долю ЛС, которая будет находиться в крови в неионизированной форме? Препарат является слабой кислотой с рКа=7,4.
Задача 7.
Какая часть ЛС, являющегося слабым основанием с рКа=8,4, будет находиться в крови в неионизированной форме? Ответ выразите в процентах.
Задача 8.
Какая часть ЛС Х (слабая кислота с рКа 2,5) всосется из двенадцатиперстной кишки (pH = 4,5), если предположить, что в нее попадет вся доза, принятая внутрь? Ответ выразите в процентах.
Задача 9.
Определите в процентах часть ЛС, которая всосется из двенадцатиперстной кишки (рН содержимого равно 7,0) в кровь (рН плазмы составляет 7,4), если это вещество является слабым основанием с рКа=4,0.
Задача 10.
Какая часть ЛС, являющегося слабым основанием с рКа=8,4, всосется из двенадцатиперстной кишки в кровь, если рН ее содержимого и плазмы крови одинаков и имеет значение 7,4?
Задача 11.
Определите часть ЛС, являющегося слабым основанием с рКа=8,4, которая не всосется из желудка в кровь (рН=7,4) при приеме его после еды, если рН желудочного содержимого имеет значение 1,4.
Задача 12.
41
Определите кажущийся (мнимый) объем распределения ЛС, концентрация которого в плазме в зависимости от времени изображена на рисунке 2.11. ЛС было введено внутривенно в дозе
0,5 г.
Задача 13.
Определите биодоступность ЛС, принятого в дозе 1,0, если известно, что он распределяется по всей водной фазе организма. а концентрация его в плазме крови равна 0,012 г/л.
Рис. 2.11. Кривая концентрации ЛС в крови в зависимости от времени
Задача 14.
Какова биодоступность ЛС, принятого в дозе 0,5, если известно, что концентрация его в плазме крови составляет 0,0001 г/мл? Препарат распределяется только в плазме крови и не депонируется.
Задача 15.
Во время клинических исследований четыре лекарственные формы одного и того же ЛС назначались внутрь здоровым добровольцам. Были построены кривые «концентрация – время» для всех 4-х лекарственных форм, которые приведены на рисунке. 2.12. Что определяет самые высокие параметры биодоступности лекарственной формы А?
1. Высокая абсорбция из кишечника. 2. Низкий уровень пресистемной биотрансформации.
3. Самый низкий печеночный клиренс 4. Самый высокий почечный клиренс. 5. Наибольший объем распределения
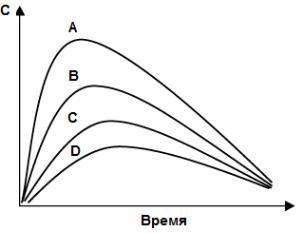
Рис. 2.12. Кривые зависимости «концентрация – плазма» для ЛФ A, B, C, D
Задача 16.
Какова величина объема плазмы крови (в литрах) у человека массой тела
100 кг?
Задача 17.
Каков объем распределения ЛС, если оно не выходит из кровеносного русла, не связывается с белками плазмы крови и не депонируется?
Задача 18.
Вычислите объем распределения сердечного гликозида дигоксина, если известно, что после его внутривенного введения в дозе 0,2 мг концентрация свободной фракции в плазме крови будет равна 0,0004 мг/л.
Задача 19.
В каком из отсеков водной фазы организма взрослого человека (плазма крови, интерстициальная жидкость, экстрацеллюлярная вода, цитоплазматическая жидкость, вся водная фаза организма) распределяется ЛС, если известно, что после внутривенного введения его в дозе 1,0 концентрация его в плазме крови составляет 58 мг/л?
Задача 20.
Вычислите величину объема распределения тиопентала, если известно, что он распределяется равномерно по всей водной фазе организма и депонируется в жировой ткани. Коэффициент распределения масло/вода его равен 10, а Vd жировой ткани = 14,5 л.
Задача 21.
Вычислите процент экскреции слабой кислоты фенобарбитала, имеющей рКа=7,4, если рН мочи составляет 5,4.
42
ГЛАВА 3.
РЕЖИМ ДОЗИРОВАНИЯ ЛС. ЭФФЕКТЫ ПОВТОРНЫХ ВВЕДЕНИЙ. ЛЕКАРСТВЕННЫЕ ВЗАИМОДЕЙСТВИЯ. БЕЗОПАСНОСТЬ ПРИМЕНЕНИЯ ЛС. ВЛИЯНИЕ РАЗЛИЧНЫХ ФАКТОРОВ НА ФАРМАКОКИНЕТИКУ
ИФАРМАКОДИНАМИКУ ЛС.
3.1.Режим дозирования и дозы
Режим дозирования – количество вводимого ЛС (доза) и частота его назначения.
Выделяют следующие виды доз:
•разовая – количество ЛС на один прием;
•суточная – количество ЛС, назначаемое на сутки в один или несколько приемов;
•курсовая – общее количество ЛС на курс лечения;
•терапевтическая – доза, в которой ЛС используют с лечебными или профилактическими целями (пороговые, или минимальные действующие, средние терапевтические и высшие терапевтические дозы);
•нагрузочная – количество ЛС, которое необходимо для заполнения объема распределения в терапевтической концентрации;
•поддерживающая – вводимое в течение длительного времени количество ЛС с целью поддержания терапевтической концентрации в плазме крови, компенсирующее его потери за интервал времени между введениями;
•токсическая – количество вводимого ЛС, при котором оно начинает оказывать выраженное токсическое действие;
•смертельная – доза ЛС, вызывающая смерть организма.
От частоты введения ЛС зависит интервал между его введениями (междозовый интервал), обозначаемый « ». Например, если ЛС назначено 3 раза в сутки, то = 8 часов.
Режим дозирования обеспечивает поддержание постоянной действующей концентрации в крови при различных путях введения и влияет на приверженность пациента к лечению. Он зависит от фармакокинетики и широты терапевтического действия ЛС, а также состояния пациента.
Вне зависимости от того какой подход для введения ЛС выбран (постоянный внутривенный, прерывистый – энтеральный или парентеральный) целью режима дозирования является достижение
стационарной (равновесной) концентрации (steady-state concentration, Css). При создании Css
развивается полный клинический эффект ЛС. Стационарная концентрация устанавливается, когда
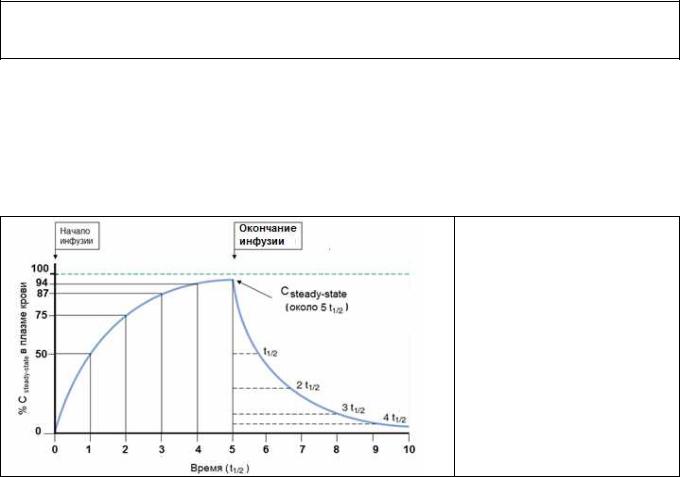
скорость выведения ЛС равна скорости его введения, а содержание в плазме и тканях остается относительно постоянным. Время достижения Css зависит только от периода полувыведения ЛС и достигается через 4–5 периодов полувыведения, не зависит от дозы и частоты введения (при условии, что элиминация ЛС подчинена кинетике первого порядка).
Рис. 3.1.
Период полувыведения и Css при постоянной инфузии
50% |
= |
___ t1/2 |
~ 90% |
= |
___ t1/2 |
~ 95% |
= |
___ t1/2 |
100% > ___ t1/2
43

Если состояние пациента (приступ бронхиальной астмы, острая сердечная недостаточность, гипертонический криз) требует быстрого достижения терапевтической концентрации используют
нагрузочную (ударную) дозу (НД, Loading dose) с последующим введением поддерживающей (ПД,
Maintenance dose), смысл которой в компенсации удаленного за интервал времени между введениями количества ЛС.
НД = Сss ∙Vd, где F
НД – нагрузочная доза, Css – стационарная концентрация, Vd – кажущийся объем распределения, F – биодоступность.
ПД = Сss ∙Cl ∙τ , где F
ПД – поддерживающая доза, Css – стационарная концентрация, –междозовый интервал, F – биодоступность.
При выраженных заболеваниях почек или печени, поддерживающая доза ЛС снижается с учетом уменьшения его клиренса.
Нагрузочная доза обычно не изменяется, так как время, необходимое для создания Css зависит в первую очередь от t1/2, а не от дозы и частоты введения!
3.2. Эффекты повторных введений ЛС
Действие большинства ЛС при повторных введениях практически не изменяется. Однако некоторые ЛС (особенно применяемые в течение длительного времени) могут вызывать развитие толерантности, лекарственной зависимости, кумуляции, гиперчувствительности.
Толерантность (от лат. tolerantia – терпение)
– ослабление эффекта при повторном введении ЛС в той же дозе. Обычно речь идет о постоянном приеме ЛС в течение нескольких дней или недель.
Развитие этого феномена характерно, в частности, для нитратов, бензодиазепинов, опиоидов, барбитуратов, фенитоина. При увеличении дозы ЛС толерантность обычно преодолевается.
В случае, когда речь идет о толерантности к опиоидным анальгетикам часто используют синонимичный термин – привыкание. Скорость развития толерантности может быть неодинакова к различным терапевтическим эффектам, которые вызывают ЛС. Так, например, привыкание, быстро возникает к эйфории, вызываемой опиоидами, но длительно не развивается к миозу и запору, которые также связаны с их применением. Нередко толерантность бывает перекрестной: прием одного ЛС повышает толерантность к приему других ЛС (как правило из той же группы).
Полное отсутствие терапевтического эффекта при применении ЛС называется термином «резистентность» и обычно используется, когда речь идет о противоопухолевых и антибактериальных ЛС.
Если при повторном применении ЛС толерантность развивается быстро (минуты или часы)
говорят о тахифилаксии.
Механизмы развития толерантности:
•снижение чувствительности рецепторов (десенситизация);
•уменьшение плотности рецепторов (down-регуляция);
•истощение запасов медиатора;
•повышенная метаболическая деградация ЛС;
•физиологическая адаптация (стимуляция неАПФ-пути образования ангиотензина II при лечении артериальной гипертензии ингибиторами ангиотензинпревращающего фермента).
44

Лекарственная зависимость
Развивается при применении психоактивных ЛС (опиоиды, этиловый спирт, бензодиазепины, галлюциногены, эфирные растворители и т.п.), вызывая адаптацию нейронов головного мозга к их воздействиям и способность функционировать только в их присутствии.
Различают психическую и физическую зависимости. В случае психической зависимости у
человека имеется непреодолимое желание вновь испытать эффект, вызываемый веществом. Физическая зависимость рассматривается в контексте абстинентного синдрома (лат. abstinentia воздержание) – комплекса психопатологических, неврологических и соматических расстройств по типу синдрома отдачи (нарушения функций противоположны тем, которые вызывает ЛС).
Лекарственная зависимость часто сочетается с толерантностью.
Кумуляция (от лат. cumulatio – увеличение, скопление)
– накопление в организме ЛС или вызываемых им эффектов.
Материальная кумуляция характерна для липофильных, хорошо проникающих в ткани и обладающих низким печеночным и/или почечным клиренсом и длительным периодом полувыведения ЛС (барбитураты, сердечные гликозиды). Может наблюдаться при патологии основных органов элиминации (печени и/или почек), превышении доз ЛС при повторных приемах.
Функциональную кумуляцию объясняют наложением эффекта от повторной дозы на еще не закончившийся эффект от предыдущей, а не накоплением ЛС (хронический алкоголизм при злоупотреблении этиловым спиртом).
Отрицательное значение кумуляции заключается в опасности интоксикации ЛС. С целью минимизации риска ее развития кумулирующие ЛС принимают в поддерживающих дозах с учетом квоты (коэффициента) элиминации (часть дозы в процентах, элиминируемая за сутки).
Гиперчувствительность
Реакции гиперчувствительности являются иммунологически опосредованными и возникают после предварительной сенсибилизации (латентный период после первой экспозиции составляет 1– 2 недели), чаще у пациентов с атопическими заболеваниями в анамнезе (поллиноз, бронхиальная астма, экзема), не связаны с дозой и могут оказаться смертельными. ЛС или его метаболит действуют как антигены или чаще гаптены – неполные антигены (ЛС будучи небольшими молекулами становятся антигенами только после связывания с эндогенными белками), которые индуцируют продукцию антител. ЛС, имеющие схожую химическую природу, могут обладать перекрестной чувствительностью. Одно и тоже ЛС может вызывать различные типы аллергических реакций у разных пациентов.
Табл. 3.1. Реакции гиперчувствительности, вызываемые ЛС
Тип реакции |
Механизм развития |
ЛС |
|
|
и клинические проявления |
I тип (реагиновый) |
Фиксация антител (IgE) на тучных клетках |
Пенициллин |
|
при первичном контакте с ЛС. |
Йодсодержащий контраст |
|
При повторном введении взаимодействие |
|
|
ЛС с IgE на тучных клетках → |
Анафилаксия |
|
дегрануляция |
Крапивница |
|
высвобождение гистамина и других БАВ |
Ангионевротический отек |
II тип (цитотоксический) |
Взаимодействие IgG, IgM и комплемента c |
Метилдофа → |
|
клеточными элементами крови. Лизис |
гемолитическая анемия, |
|
эритроцитов, гибель лейкоцитов и |
клозапин → агранулоцитоз, |
|
тромбоцитов. |
хинидин → тромбоцитопения |
III тип (иммунокомплексный) |
Образование и циркуляция иммунных |
Хинидин, метотрексат |
|
комплексов (антиген – антитело), |
|
|
повреждение эндотелия и базальной |
Лихорадка, васкулит, артрит, |
|
мембраны сосудов. |
кожная сыпь |
IV тип |
Обусловлены клеточными иммунными |
Ампициллин |
(гиперчувствительность |
реакциями, развиваются не ранее чем |
|
замедленного типа ) |
через 12 ч после повторного введения |
Контактный дерматит |
|
антигена. |
|
|
45 |
|
|
Сенсибилизированные Т-лимфоциты и |
Иногда эпидермальный |
|
макрофаги выделяют цитокины. |
некролиз (смертность 35%) |
3.3. Лекарственные взаимодействия
Имеется множество клинических ситуаций, когда пациенту необходимо одновременное назначение сразу нескольких ЛС. В этом случае следует стараться избегать полипрагмазии (poly – много и греч. pragma – предмет, вещь) – одновременного (часто неоправданного) назначения множества ЛС, без учета их взаимодействий. Альтернативой ей должна стать рациональная комбинированная терапия с максимальным учетом возможных взаимодействий ЛС, которая преследует следующие основные цели:
•повышение эффективности лечения;
•уменьшение токсичности ЛС за счет уменьшения доз комбинируемых ЛС;
•предупреждение и коррекция побочных эффектов ЛС.
Под взаимодействием ЛС понимают явление, при котором применение двух и более ЛС вызывает эффект, отличный от эффекта каждого ЛС в отдельности.
Выделяют три вида взаимодействия ЛС:
•фармацевтическое;
•фармакокинетическое;
•фармакодинамическое.
Фармацевтическое взаимодействие (фармацевтическая несовместимость)
Результат физико-химических реакций ЛС до их поступления в организм. Данный вид взаимодействия чаще всего происходит при смешивании ЛС в инфузионных растворах.
Фармакокинетическое взаимодействие
Происходит на этапах:
а) всасывания
•физико-химическое взаимодействие, приводящее к связыванию препарата, его инактивации и утрате растворимости (одновременное использование ЛС с адсорбентом; тетрациклина с ионами 2-х и 3-х валентных металлов – кальция, магния, алюминия, железа);
•изменение величины рН в желудке и степени ионизации слабых кислот (одновременное использование ЛС с антацидом, ингибитором протонной помпы);
•влияние на моторику ЖКТ (стимуляция/торможение);
•изменение всасывания при парентеральном введении (адреналин вызывая сужение сосудов,
уменьшает абсорбцию местных анестетиков).
б) распределения
• взаимодействие в процессе связывания с белками плазмы и тканей.
в) биотрансформации
Выделяют индукторы и ингибиторы ферментов системы цитохрома Р450. Типичными индукторами, ускоряющими биотрансформацию ряда ЛС, являются барбитураты, фенитоин, карбамазепин, рифампицин, а ингибиторами, замедляющими биотрансформацию ЛС, – эритромицин, итраконазол, амиодарон.
г) выведения (экскреции)
•увеличение почечного кровотока и обусловленного им фильтрационного давления – ускорение выведения ЛС (сердечные гликозиды, теофиллин);
•влияние на процессы гломерулярной фильтрации;
•влияние на процессы канальцевой секреции;
•влияние на процессы канальцевой реабсорбции.
46
Фармакодинамическое взаимодействие
Результат прямого или косвенного взаимодействия ЛС на уровне рецепторов, клеток, органов или физиологических систем: конкуренция за связывание с рецептором, изменение кинетики связывания на уровне рецептора, взаимодействие на уровне медиаторов, изменение чувствительности рецепторов, химическое и физико-химическое взаимодействие.
Виды фармакодинамического взаимодействия
Синергизм (греч. syn – вместе, erg – работа) – усиление действия одного ЛС другим.
Виды синергизма:
а) суммация, или аддиция (лат. addition – добавление)
При взаимодействии двух ЛС А и Б их общий эффект будет равен простому сложению эффектов: Эффект АБ = Эффект А + Эффект Б.
Характерна для ЛС одной фармакологической группы, влияющих на одни и те же мишени (рецепторы, ферменты и др.).
б) потенцирование Одно ЛС значительно усиливает фармакологический эффект другого. При потенцировании
общий эффект комбинации двух ЛС превышает сумму их эффектов.
Антагонизм (греч. anti – против, agon – борьба) – ослабление фармакологического эффекта одного ЛС другим.
Виды антагонизма:
а) Функциональный
•Прямой антагонизм (может быть конкурентным и неконкурентным – см. главу I) – действие на одни и те же рецепторы (адреномиметики и адреноблокаторы);
•Косвенный антагонизм (физиологический) – действие на разные типы рецепторов (эффекты 1,2-адреноблокаторов и М-холиноблокаторов на тонус бронхов).
б) Физический
Уменьшение абсорбции и резорбтивного действия (при одновременном приеме с ЛС адсорбентом, ЛС изменяющим pH биологических сред).
в) Химический
Химическая реакция между ЛС с образованием неактивных продуктов. Антагонисты с таким механизмом получили название антидотов. Например, протамин является химическим антагонистом гепарина, т.к. его катионные группы связываются с анионными центрами этого ЛС.
3.4. Факторы, влияющие на фармакокинетику и фармакодинамику ЛС
3.4.1. Химическая структура, стереоизомерия и физико-химические свойства ЛС. Лекарственные формы с заданной фармакокинетикой
Близкие по химической структуре ЛС вызывают, как правило, схожие фармакологические эффекты. Это обусловлено не только их химической структурой, но и пространственным расположением атомов – стереоизомерией, которая обеспечивает комплементарное взаимодействие с рецептором.
47
Физико-химические свойства ЛС (липо-, гидрофильность, способность к ионизации) определяют выраженность их абсорбции, распределения, способы и пути элиминации.
Лекарственные формы (ЛФ) с заданной фармакокинетикой
Наряду с традиционными ЛФ существуют формы с модифицируемым высвобождением (МВ), применение которых изменяет время возникновения и продолжительность фармакологического эффекта. Это связано с их возможностью влиять на скорость развития Cmax ЛС в плазме крови и поддержание его терапевтической концентрации в течение заданного временного периода.
ЛФ с улучшенной растворимостью и всасыванием, повышающие биодоступность ЛС обеспечивают быстрое начало его действия (ЛФ «рапид»). Их применяют, как правило, эпизодически, например для устранения острого болевого синдрома.
Для обеспечения постоянного уровня терапевтической концентрации в плазме крови используются ЛФ с замедленным (или контролируемым) высвобождением, которое происходит, как правило, в течение 12–24 часов. Процесс высвобождения из них ЛС характеризуется предсказуемостью и точностью по скорости, продолжительности и месту высвобождения, что позволяет прогнозировать развитие терапевтического эффекта. К таким ЛФ относятся гастроинтестинальные терапевтические системы (ГИТС) и другие системы, обеспечивающие кинетику «нулевого» порядка (обозначают как ZOK – zero-order kinetics, XL – extra long, CR – controlled release). Это уменьшает возможность развития токсических эффектов ЛС, поскольку обеспечивается отсутствие концентрационных пиков в плазме. Применение таких ЛФ, как правило, повышает комплаентность (приверженность пациента к лечению), поэтому они широко используются в терапии хронических заболеваний (артериальная гипертензия, сердечная недостаточность, хронический болевой синдром, заместительная гормонотерапия и др.).
Таблетированные ЛФ МВ нельзя делить, измельчать, разжевывать, т.к. в этом случае нарушается «программа» высвобождения из них ЛС. Кроме того, при развитии побочных эффектов их продолжительность может оказаться клинически значимой.
Вслучае, если ЛС оказывает негативное действие на слизистую желудка или разрушается под действием желудочного сока, их покрывают специальными кишечнорастворимыми (энтеросолюбильными) оболочками.
3.4.2Возраст
Вразличных возрастных группах фармакокинетика и фармакодинамика ЛС неодинаковы.
Пациенты детского возраста
Основные различия в фармакокинетике и фармакодинамике ЛС в детской и взрослой популяциях наблюдаются у недоношенных детей, в период новорожденности (0–12 месяцев) и детей до 5 лет.
При применении ЛС у детей могут наблюдаться парадоксальные эффекты (стимулирующее действие дифенгидрамина, бензодиазепинов, контроль гиперактивности амфетаминами), механизмы развития которых до сих пор неизвестны.
Данные об изменениях фармакокинетики у детей представлены в табл. 3.2.
Пациенты пожилого и старческого возрастов
Характер влияния ЛС на организм в пожилом и старческом возрасте имеет существенные особенности, при этом они лучше изучены в отношении фармакокинетических, чем фармакодинамических процессов.
Возрастные изменения фармакодинамики обусловлены тем, что при ухудшении условий доставки ЛС к тканям число специфических рецепторов уменьшается, однако их чувствительность к лекарственным воздействиям увеличивается и извращается. Этим объясняется разнонаправленный и трудно прогнозируемый характер ответа старческого организма на ЛС. Возникновению извращенных реакций на препараты способствуют также сниженная физическая активность, меньшее потребление пищи и воды, склонность к запорам, витаминная недостаточность, ухудшение кровоснабжения тканей и др.
Данные об изменениях фармакокинетики у пожилых пациентов представлены в табл. 3.3.
48

Табл. 3.2. Влияние детского возраста на фармакокинетику ЛС
Фармакокинетический |
Возрастные физиологические |
Клиническое значение |
|
|
процесс |
изменения |
|
Абсорбция |
|
|
|
При приеме внутрь |
В период до 2-х лет: |
скорость абсорбции |
|
|
|
желудочный pH |
время начала действия |
|
|
опорожнение желудка |
|
При местном (накожном) |
роговой слой кожи проницаемость |
риск передозировки ЛС |
|
применении |
кожи |
|
|
Распределение |
|
|
|
• |
водный и жировой |
общая вода организма |
Vd водорастворимых ЛС |
|
компартменты |
|
(аминогликозиды) |
|
организма |
масса жировой ткани |
Vd липидорастворимых ЛС |
|
|
|
(бензодиазепины) |
|
|
|
|
• |
связь с белками |
альбумин |
свободная фракция ЛС |
|
|
кислый 1-гликопротеин |
(сульфаниламиды) |
|
|
|
|
• |
ГЭБ |
проницаемость у новорожденных и |
риск побочных действий ЛС со |
|
|
детей раннего возраста |
стороны ЦНС |
|
|
|
|
Биотрансформация |
синтез ферментов печени |
пресистемная элиминация |
|
|
|
(«незрелость» ферментативных систем) в |
t1/2 риск токсических эффектов |
|
|
первые 4 недели после рождения и у |
(хлорамфеникол → «серый» коллапс |
|
|
недоношенных детей |
новорожденных) |
|
|
Масса печени на 50% больше, чем у |
печеночный клиренс |
|
|
взрослых по отношению к массе тела |
|
Экскреция (почечная) |
у новорожденных: |
|
|
|
|
скорость клубочковой фильтрации |
почечный клиренс |
|
|
(СКФ) |
|
|
|
активная секреция |
|
|
|
реабсорбция |
|
|
|
почечный кровоток |
|
|
|
В течение первых 4-х недель СКФ |
постепенное приближение значений |
|
|
повышается |
СКФ к таковой у взрослых |
|
|
|
|
Табл. 3.3. Влияние пожилого возраста на фармакокинетику ЛС
Фармакокинетический |
|
Возрастные физиологические |
Клиническое значение |
процесс |
|
изменения |
|
Абсорбция |
секреция HCl желудочный pH |
скорость растворения ЛС |
|
|
кровообращение ЖКТ |
скорость абсорбции ЛС |
|
|
синтез панкреатических ферментов |
время начала действия |
|
|
моторика ЖКТ |
|
|
Распределение |
|
|
|
водный и жировой |
общая вода организма |
Vd водорастворимых ЛС |
|
компартменты организма |
( масса мышечной ткани) |
(аминогликозиды, строфантин) |
|
|
жировой ткани |
Vd липидорастворимых ЛС |
|
|
|
|
(бензодиазепины, лидокаин, |
|
|
|
трициклические антидепрессанты) |
связь с белками |
альбумин |
свободная фракция слабых кислот |
|
|
|
|
(варфарин, диазепам) |
|
кислый 1-гликопротеин |
свободная фракция слабых |
|
|
|
|
оснований (пропранолол, лидокаин) |
Биотрансформация |
синтез ферментов печени |
биотрансформация ЛС |
|
|
|
печеночный кровоток |
печеночный клиренс |
|
|
масса печеночной ткани |
(значение возрастает при тяжелых |
|
ацетилирование |
заболеваниях печени) |
|
|
глюкуронирование |
|
|
Экскреция (почечная) |
СКФ, |
почечный клиренс t1/2 ЛС |
|
|
почечный кровоток |
|
|
49
|
активная секреция |
(аминогликозиды, дигоксин, соли лития, |
|
|
дабигатран) |
3.4.3 Заболевания и патологические состояния
Заболевания и патологические состояния могут оказывать клинически значимое влияние на выраженность фармакологических эффектов многих лекарств, изменяя их фармакокинетику и/или фармакодинамику.
Желудочно-кишечные заболевания, замедляющие опорожнение желудка, снижают эффективность принятых внутрь анальгетиков для купирования болевого приступа, поскольку создание Cmax в этой ситуации отсрочено.
При сердечной недостаточности уменьшается абсорбция ряда препаратов (например, фуросемида), что обусловлено отеком слизистой ЖКТ и снижением органного кровотока. Объем распределения (Vd), например хинидина и лидокаина, у пациентов с ХСН также заметно уменьшен из-за пониженной тканевой перфузии, что может привести к повышению их концентрации в плазме и развитию побочных эффектов. Уменьшение сердечного выброса вызывает задержку элиминации ЛС, поскольку печеночный и почечный кровоток снижены. В связи с этим замедляется выведение таких препаратов как лидокаин и теофиллин, аминогликозидные антибиотики и дигоксин, что может привести к развитию судорог, нарушению сердечного ритма, почечной недостаточности, проявлениям интоксикации сердечными гликозидами.
Почечная недостаточность сопровождается снижением экскреции водорастворимых ЛС. В связи с этим необходимо иметь представление о выраженности поражения почек, особенно если ЛС более чем на 50% выводится с мочой. С этой целью рассчитывают или определяют клиренс креатинина, отражающий скорость клубочковой фильтрации (СКФ), а затем, согласно полученным данным, корригируют режим дозирования. Для этого используют формулу Кокрофта – Голта:
для мужчин:
Clcr= (140 - возраст) х вес / 72 х Cr;
для женщин:
Clcr= (140 - возраст) х вес) / (72 х Cr) х 0,85, где
Clcr – клиренс креатинина, мл/мин; вес – масса тела, кг; Cr – концентрация креатинина в плазме, мг/дл.
В последнее время для оценки СКФ рекомендуется более точные формулы MDRD (Modification of Diet in Renal Disease Study) или CKD-EPI (Chronic Kidney Desease Epidemiology Collaboration),
Расчет по ним, как и по формуле Кокрофта – Голта, удобно производить с помощью калькуляторных приложений к мобильным устройствам.
Заболевания печени, приводящие к выраженному уменьшению белкового синтеза, снижают абсорбцию (из-за отека слизистой) и пресистемную элиминацию ЛС, увеличивая при этом биодоступность таких препаратов как пропранолол, морфин, верапамил и циклоспорин. В случае развития гипоальбуминемии Vd целого ряда ЛС увеличивается. Процессы биотрансформации нарушаются только при очень тяжелой печеночной недостаточности. Пониженный кровоток в печени (обусловленный как поражением самого органа, так и снижением сердечного выброса), предрасполагает к развитию гипоксии (особенно при имеющемся поражении легких) и увеличивает риск развития лактацидоза при применении метформина.
Сепсис характеризуется массивным высвобождением цитокинов, протеаз и активных форм кислорода, вызывающих повреждение клеток, полиорганную и эндотелиальную дисфункцию. Развивающаяся в этих условиях вазодилатация сопровождается синдромом «капиллярной утечки», когда альбумины и жидкость из сосудистого русла перемещаются в интерстиций, увеличивая тем самым объем распределения водорастворимых ЛС (например, бета-лактамных антибиотиков) и концентрацию свободной фракции слабых кислот. Наряду с этим резко снижаются возможности основных элиминирующих органов (почек и печени), что требует коррекции доз ЛС.
Нарушение функций щитовидной железы вызывает изменение восприимчивости организма к ЛС. Так при гипотиреозе увеличивается чувствительность к дигоксину и опиоидам, а при
50
