
презы Зорникова / 18. Вакцины и антительные препараты
.pdfмРНК вакцины
•Состав: мРНК поверхностного белка SARS-CoV- 2, упакованная в липосомы
•В данные момент только вакцины против COVID-19 одобрены к применению у людей
•BNT162b2 (Pfizer, US)
•mRNA-1273 (Moderna, US)
•Механизм действия: липосомы доставляют мРНК поверхностного белка SARS-CoV-2 в клетки → клетки несколько суток транслируют данный ген → образовавшийся поверхностный белок стимулирует выработку специфических антител

Механизм действия мРНК вакцин
https://doi.org/10.1038/s41541-020-0159-8
Пентаксим: пример комбинированной вакцины
•Назначение: профилактика дифтерии, столбняка, коклюша, полиомиелита, гемофильной B инфекции
•Адъювант: гидроксид алюминия
•Активные компоненты:
–Анатоксин дифтерийный
–Анатоксин столбнячный
–Анатоксин коклюшный
–Гемагглютинин филаментозный
–Вирус полиомиелита 1 типа инактивированный
–Вирус полиомиелита 2 типа инактивированный
–Вирус полиомиелита 3 типа инактивированный
–Полисахарид Haemophilus influenzae тип b (полирибозилрибитол фосфат), конъюгированный со столбнячным анатоксином
Порядок разработки и испытания вакцин

Требования к разрабатываемой вакцине
https://www.roitt.com/I_EM1202/index.html
Основные пути разработки вакцин
•Аттенуированные вакцины – полностью эмпирический подход (метод проб и ошибок)*
–Пассажи через разных хозяев
–Пассажи через разные питательные среды (для бактерий)
–Пассажи через различные культуры клеток (для вирусов)
•Инактивированные вакцины – отчасти эмпирический подход
–Инактивация разными концентрациями определенных веществ (например, формальдегидом)
•Субъединичные вакцины
–Культивирование микробов с последующей очисткой целевых белков/полисахаридов (с дальнейшей обработкой формальдегидом в случае анатоксинов)
–Внедрение гена целевого белка в микроба-продуцента (E. coli или S. cerevisae)
•Рекомбинантные аденовирусные вакцины*
•мРНК вакцины
–Синтез целевой мРНК с последующей упаковкой в липосомы
*Смотри следующие два слайда
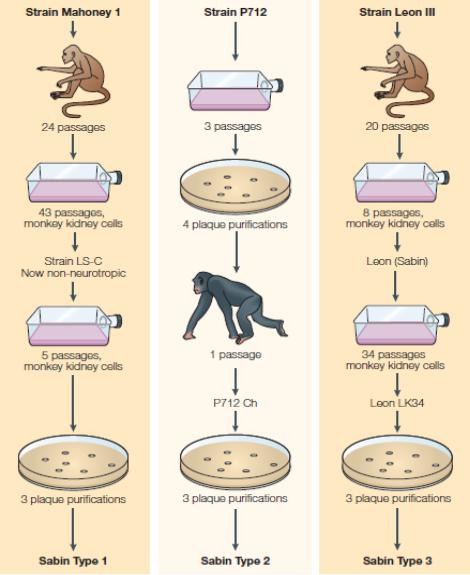
Пример: получение аттенуированных полиовирусных вакцинных штаммов Сэбина
https://doi.org/10.1038/nrmicro906

Создание рекомбинантных аденовирусов,
используемых как векторы для доставки целевых генов в клетки человека
• Отсутствие функционального E1 белка не позволяет рекомбинантным аденовирусам реплицироваться in vivo
• Рекомбинантный аденовирус является вектором для доставки целевых генов в клетки человека
• После инфицирования клетки рекомбинантный аденовирус не реплицируется; целевая ДНК транскрибируется в мРНК, которая затем транслируется в белок
https://doi.org/10.1038/mtm.2016.30
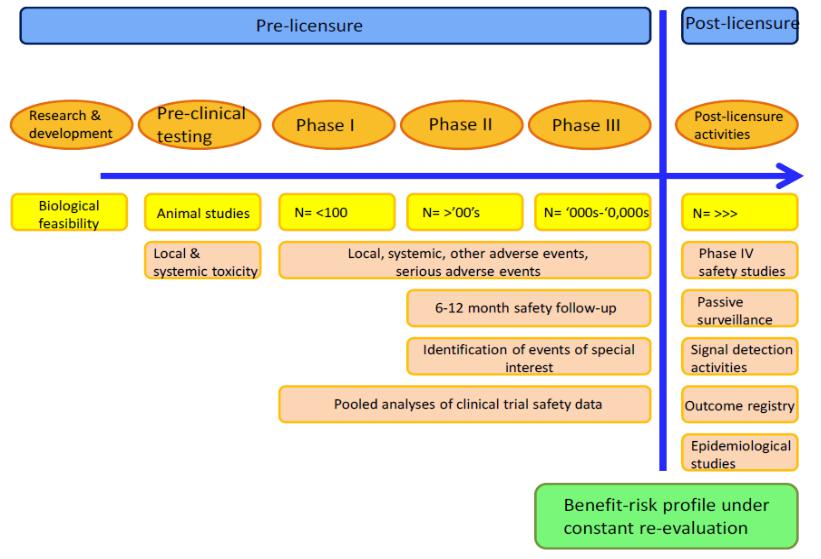
Алгоритм испытания новых вакцин (общая продолжительность для большинства
вакцин – порядка 5-10 лет)
https://doi.org/10.3390/vaccines3020320

Пример: расчет эффективности Спутника V (3 фаза клинических испытаний препарата)
https://doi.org/10.1016/S0140-6736(21)00234-8
