
БИОХИМИЯ СОЕДИНИТЕЛЬНОЙ И КОСТНОЙ ТКАНИ
.pdf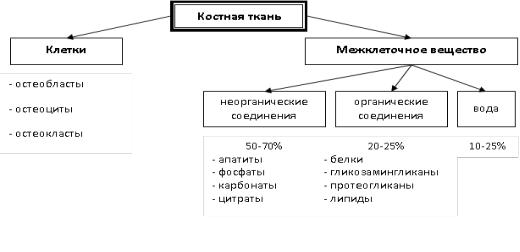
пищеварительная – зубы участвуют в процессе измельчения пищи и формирования пищевого комка.
зубы часть речевого аппарата.
Костная ткань имеет строение, которое не встречается в других видах соедини-
тельной ткани. В ней преобладает межклеточное вещество, содержащее большое количество минеральных компонентов, главным образом - солей кальция.
Структурная организация костной ткани
Особенности костной ткани.
1)высокая минерализация (или кальцификацияя) межклеточного матрикса;
2)сочетание высокой прочности на разрыв с лёгким весом.
Клетки костной ткани и их функции
Клетки |
|
Функции |
|
|
|
Остеобласты- клетки, формирующие |
1. |
Синтез органического матрикса |
костную ткань, клетки анаболизма, |
|
костной ткани: |
т.к. синтезируют в 100 раз больше |
|
коллагеновых белков (коллаген I |
своей массы |
|
типа), неколлагеновых белков |
|
|
(остеонектин, остеокальцин и др.) |
|
|
гликозамингликанов и белковых |
|
|
компонентов протеогликанов. |
|
2. |
Синтез и секреция ферментов и |
|
|
|

|
|
биологически активных веществ |
|
3. |
Участие в минерализации |
|
|
костной ткани |
|
4. |
Активация остеокластов |
|
|
|
Остеоциты – |
Обмен воды, белков и ионов в |
|
высокодифференцированные |
костной ткани. |
|
клетки костной ткани (взрелом |
|
|
скелете – 90% остеоциты) Процессы |
|
|
катаболизма и анаболизма в |
|
|
остеоците уравновешены |
|
|
|
|
|
Остеокласты – клетки катаболизма |
клетки, осуществляющие резорбцию |
|
(слабо развит ЭР, но много лизосом) |
костной ткани |
|
|
|
|
Характеристика минеральных компонентов
В организме взрослого человека содержится более 1 кг кальция, который почти целиком находится в костях и зубах, образуя вместе с фосфатом нерастворимый гидроксиапатит.
В поверхностных слоях кости содержится небольшое количество аморфного Са3(РО4)2, который придает гибкость костной ткани и является лабильным резервом кальция и фосфатов в организме. С возрастом его содержание уменьшается.потому что кальций связывается с гидроксилапатитом.
Основной кристалл костной ткани - гидроксиапатит Са10(РО4)6(ОН)2. -(75%), 25% - другие апатиты (хлорапатиты, фторапатиты, карбонатапатиты и др.)
Апатиты – образуют прочную ионную решетку гексагональной формы, в которой ионы расположены согласно размеру и заряду. Фосфат-анион имеет наибольший размер, а вокруг фосфатов и между ними располагаются Са2+, ОН-, F- и др. Гидроксильные группы расположены вдоль гексагональной оси,
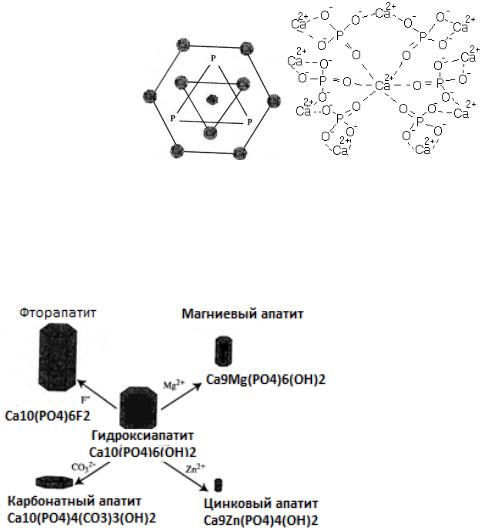
а фосфатные группы распределяются как равнобедренные треугольники вокруг гексагональной оси. Между кристаллами находятся микропространства, заполненные водой (свободная вода), снаружи каждый апатит покрыт гидратной оболочкой (связанная вода).
Рис.24. Гексогональная форма кристалла гидроксиапатит
В «идеальном» апатите соотношение Са/Р = 1, 67. Это отношение может колебаться от 1,33 до 2, что связано со способностью апатита замещать ионы в ионной решетке. Обмен ионов кристаллов апатита на ионы, находящиеся в растворе, называется изоморфное замещение.
Возможность замены определяется сходством размера и заряда ионов. Кроме изоморфного замещения, состав кристалла апатита можно изменить путем заполнения другими ионами вакантных мест в кристаллической решетке апатита.
Рис.25. Типы гидроксиавпатитов
Этапы проникновения различных элементов в кристаллы ГА
▪проникновение элементов в воду гидратной оболочки кристалла (длится несколько минут);
▪обмен между ионами гидратной оболочки и поверхностью кристалла
(длится несколько часов); ▪ проникновение ионов в кристалл (длится месяцами и годами).
Наиболее часто имеют место следующие варианты обмена:
Са2+ замещается катионами Sr2+, Ba2+, Mo2+, Mg2+, Pb2+ Катионы Са2+ поверхностного слоя кристаллов, могут на короткое время замещаться катионами K+, Na+.
PO43- обменивается с HPO42-, CO32-
OHзамещается анионами галогенов Cl-, F-, I-, Br-.
В результате замены изменяются свойства апатита. Например, замена Са2+ на H+ снижаетпрочность кристалла (т.к. размер Н+ < Са2+, то протоны внедряются в кристалл, в результате чего кристалл апатита разрушается). В кислой среде разрушение происходит наиболее интенсивно.
Замена ОНна F увеличивает прочность кристалла апатитов. В водной среде реакция взаимодействия фтора с фосфатами кальция зависит от концентрации фтора. Если она не более 500мг/л, то образуются кристаллы фторапатита Са10(РО4)6F2. Оптимальная концентрация F в воде 1 мг%, при увеличении содержания образуется нерастворимый флюорит кальцияСа10(РО4)6(ОН)2 + 20F→ 10CaF2 + 6PO43- + 2HO-и кристаллы не образуются. В связи с этим, в щелочной среде развивается флюороз.
При замещении Са2+ на Sr, Са10(РО4)6(ОН)2 + Sr2+ →
Са9Sr2+(РО4)6(ОН)2 + Ca2+
особенно наSr90, который является β- излучателем, развивается стронциевый рахит, для которого характерны хрупкость и ломкость костей и зубов, переломы, деформации скелета.
Органический матрикс кости.
Органические вещества костного матрикса представлены белками, липидами и небольшим количеством протеогликанов.
|
|
|
Белки |
|
|
|
|
|
межклеточного матрикса |
||||
|
|
|
|
|
|
|
95% |
|
|
|
|
5% |
|
коллагеновые белки |
|
|
|
неколлагеновые белки |
||
|
|
|
|
|
||
|
|
|
- остеонектин |
|||
90% |
5% |
|
- остеокальцин |
|||
|
- остеопонтин |
|||||
коллаген I типа |
другие типы |
|||||
- костные сиалопротеины |
||||||
|
коллагена |
|
||||
|
|
- кислый костный гликопротеин |
||||
|
(V, XII) |
|
||||
|
|
- фибронектин |
||||
|
|
|
||||
|
|
|
- тромбоспондин |
|||
|
|
|
- |
Gla-протеин |
||
Особенности белков всех минерализованных тканей:
наличие остатков фосфосерина, глутамата, ϒ-карбоксиглутаминовой кислоты и аспартата, которые способны связывать Са2+ и таким образом участвовать в образовании кристаллов апатитов;
наличие последовательности аминокислотных остатков арг-глу-асп (R-G-D) в первичной структуре белков, что обеспечивает их связывание с клетками и с белками, формирующими межклеточный матрикс.
Часть белков встречается в межклеточном матриксе всех
минерализованных тканей. Это белки адгезии, кальций-связывающие белки, протеолитические ферменты, факторы роста. Другие белки присущи только данной ткани и связаны с определенными процессами, характерными для этого типа ткани.
Приблизительно 95% органического матрикса костной ткани приходится на коллаген, т.е. коллаген - основной белок костной ткани. Вместе с минеральными компонентами коллаген является главным фактором, определяющим механические свойства кости. Коллагеновые фибриллы костного матрикса образованы коллагеном I типа. Известно, что данный тип коллагена входит также в состав сухожилий и кожи, однако коллаген костной ткани обладает некоторыми особенностями.
Особенности костного коллагена
содержит больше оксипролина, чем в коллагене сухожилий и кожи;
характерно большое содержание свободных ε-амино-групп лизиновых и оксилизиновых остатков;
повышенное по сравнению с коллагеном других тканей содержание фосфосерина.
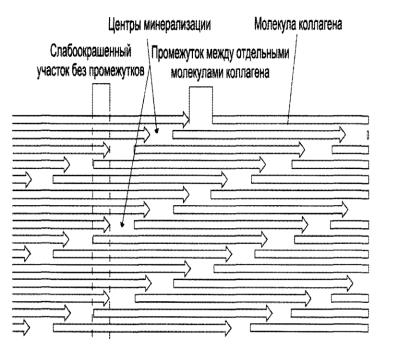
Молекулы коллагена не связаны между собой «конец в конец», а смещены на ¼
длины молекулы. Промежутки между молекулами тропоколлагена в костной ткани вы-полняют роль центров минераплизации, где начинается отложение фосфата кальция сначала в аморфном виде с последующим образованием гидроксиапатита.
Роль неколлагеновых белков костной ткани
1)Связывают Са2+, входящий в состав гидроксиапатитаи участвуют в росте кристаллов гидроксиапатитов костной ткани;
2)Являются матрицей вминерализации костной ткани;
3)Связываются с коллагеном, с поверхностями клеток и другими белками костной ткани.
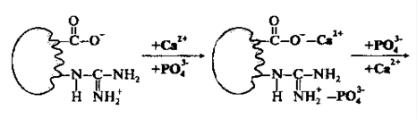
Рис.26. Участие остеонектина в минерализации
Ферменты костной ткани.
1 группа – ферменты общие для любого типа ткани, участвуют в производстве энергии, синтезе АТФ, поставляют субстраты для обмена веществ.
2 группа – тканеспецифичные ферменты соединительной ткани:
•пролил- и лизилгидроксилазы участвуют в гидроксилировании пролина и лизина,
•лизилоксидаза окисляет лизин, поэтому коллагеновые волокна связаны поперечными связям;
•гликозидазы участвуют в прикреплении углеводов к коллагену;
•специфические пептидазы;
•УДФ-трансферазы участвуют в обновлении костного матрикса;
•коллагеназа, гиалуронидаза и сульфатаза.
3 группа – тканеспецифичные ферменты костной ткани:
•щелочная фосфатаза (в остеобластах, рН 9,0) переносит фосфор от органических эфиров на коллагеновую матрицу – главный фермент минерализации;
•кислая фосфатаза (в остеокластах рН 4,5) отщепляет фосфор от органической матрицы, отвечает за резорбцию,
•пирофосфатаза гидролизует пирофосфат до фосфатов (рН 7,0), пирофосфат – ингибитор минерализации в матриксе митохондрий,
•костная АТФ-аза активна в деминерализованных клетках при перестройке костной ткани.
Протеогликаны межклеточного матрикса костной ткани
- высокомолекулярные соединения, состоящие из белка (5-10%) и гликозамингликанов (90-95%), составляют 10% межклеточного матрикса. Гликозамингликаны – линейные гетерополисахариды:
1.Хондроитин-сульфаты
2.Кератансульфат
3.Дерматансульфат
4.Гиалуроновая кислота
Минерализация костной ткани и твердых тканей зуба Минерализация - отложение неорганических веществ в ранее
образованный органический коллагеновый матрикс кости. При этом минеральные кристаллы включаются внутрь коллагеновых фибрилл и скрепляются с ними с помощью протеогликанов.
Роль матрицы выполняют коллаген, протеогликаны, гликозаминогликаны, Са-связывающие белки: фопротеины и белки, содержащие γ-карбоксиглутаминовую кислоту (γ-КГК), для синтеза которой нужен витамин К.
Особенностью процесса минерализации является пересыщение среды ионами кальция и фосфора.
В целом минерализация кости характеризуется взаимодействием трех факторов:
1)местное повышение концентрации ионов фосфата;
2)адсорбция ионов Са2+
3)сдвиг рН.
Образование кости или ее воссоздание в процессе перестройки костной ткани начинается секрецией остеобластами молекул коллагена и
межклеточного основного вещества костной ткани (главным образом протеогликанов). Мономеры коллагена быстро полимеризуются, образуя коллагеновые волокна.
|
В результате |
образуется |
|||
|
остеоид - подобие кости. |
||||
|
Через несколько дней после |
||||
|
образования |
остеоида, |
на |
||
|
поверхностях |
коллагеновых |
|||
|
волокон |
|
|
начинают |
|
|
осаждаться |
соли кальция. |
|||
|
Осаждение |
прежде |
всего |
||
|
происходит |
в |
промежутках |
||
|
вдоль каждого коллагенового |
||||
|
волокна, образуя мельчайшие |
||||
|
очаги |
|
кристаллизации, |
||
|
которые в течение дней и |
||||
|
недель |
быстро |
множатся и |
||
Рис.27. Ступенчатое расположение молекул коллагена в |
растут, |
превращаясь в конце |
|||
коллагеновой фибрилле и образование центров минерализации
.
Важную роль в минерализации играют:
концов в кристаллы гидроксиапатита
Остеобласты – регулируют транспорт ионов кальция и фосфата через свои мембраны.
Тропоколлаген – обеспечивает промежутки между молекулами, создавая центры минерализации.
Остеонектин – гликофосфопротеин, способный связывать Са2+ и РО43-.
Остеопонтин гликофосфопротеин, содержащий N- и О-связанные олигосахариды; участвует в адгезии клеток
Остеокальцин - белок, синтезируемый остеобластами и содержащий 3 остатка γ-рбоксиглутаминовой кислоты. Связывается с гидроксиапатитом;
локализуется во внеклеточном матриксе костной ткани
Костный сиалопротеин-адгезивный гликопротеин, содержащий до 50% углеводов
5.Щелочная фосфатаза – высвобождает неорганический фосфат из органических фосфорсодержащих соединений.
Этапы минерализации костной ткани |
|
||
Выделяют 2 этапа осаждения фосфата кальция: |
|
|
|
1-й этап: нуклеация — образование плотного осадка (ядра). |
|
||
|
Начало |
|
минерализации |
|
характеризуется |
усиленным |
|
|
поглощением |
|
остеобластами |
|
молекул |
О2, |
активацией |
|
окислительно-восстановительных |
||
|
процессов, |
|
окислительного |
|
фосфорилирования и накаплением |
||
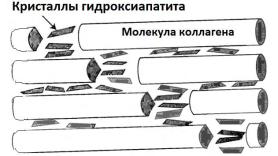
Рис. 28. Отложение кристаллов |
АТФ. |
|
|
гидроксиапатитов между молекулами коллагена |
|
|
|
Остеобласты начинают синтезировать костный коллаген, который связывает кальций и фосфор. Увеличивается проницаемость мембран митохондрий и ЭР и освобождение кальция. Из лизосом освобождаются гидролазы (гиалуронидаза и протеиназа). На клеточной мембране остеобласта образуются везикулы, которые содержат много Са, Р, щелочной
фосфатазы, ФЛ (ионы кальция в мембранных везикулах связаны в основном
сотрицательно заряженным фосфатидилсерином).
Вмежклеточном матриксе мембранные везикулы разрушаются с освобождением ионов Са2+, пирофосфата, органических соединений,
связанных с остатками фосфорной кислоты. Щелочная фосфатаза отщепляет фосфат от органических соединений. Ионы Са2+соединяются с фосфором, что приводит к образованию аморфного фосфата кальция. Одновременно происходит разрушение протеогликанов, связанных с коллагеном I типа. Освобождающиеся фрагменты протеоглиепнов, заряженные отрицательно, начинают в свою очередь связывать ионы кальция. Часть ионов Са2+ и РО43- связываются с коллагеновыми и неколлагеновыми белками, формирующими
матрицу., что сопровождается образованием ядер кристаллизации. Неколлагеновые белки переносят Са2+ на –NH2 группы лизина, аргинина, на – ОН группы сер, тре, на –СООН группы глу и асп. Из белков костной ткани наиболее активно связывают ионы Са2+ и РО43- остеонектин и GIa-протеины.
В результате ионы кальция и фосфора, которые были связаны с белково-
углеводным |
комплексом, переходят в |
растворимое |
состояние |
и |
формируют кристаллы гидроксилапатита. |
|
|
|
|
2-й |
этап: эпитаксия – самоорганизованный, |
саморегулируемый |
||
процесс роста кристалла апатита на первичных ядрах кристаллизации в зоне минерализации. По мере роста кристаллы гидроксилапатита вытесняют протеогликаны и даже воду до такой степени, что плотная ткань становится практически обезвоженной.
Вэтих условиях коллаген составляет примерно 20% от массы и 40% от объема костной ткани, остальное приходится на долю минеральных компонентов.
Ингибитор процесса минерализации - неорганический пирофосфат.
Его накопление в кости может препятствовать росту кристаллов. Чтобы этого не происходило, в остеобластах есть пирофосфатаза, которая расщепляет пирофосфат на два фосфатных остатка.
Вкостной ткани много цитрата (1 % от общего содержания) – растворимая, транспортная форма кальция в костной ткани.На поверхности кристаллов может накапливаться много натрия в форме цитрата натрия. Кость выполняет функции лабильного (изменчивого) депо натрия, который выделяется из кости при ацидозе и, наоборот, при избытке поступления натрия с пищей, чтобы предотвратить алкалоз - натрий депонируется в кости.
Ремодулирование костной ткани

Большая часть кальция в костях постоянно обновляется. Ежедневно
кости скелета теряют и вновь восстанавливают примерно 700–800 мг кальция.
Известно, что каждые 30 лет костная ткань изменяется почти полностью. В норме кость «растет» до 20-летнего возраста, достигая пика костной массы. В этот период прирост костной массы составляет до 8% в год. Далее до 30-35-летнего возраста идет период более или менее устойчивого состояния.
Затем начинается естественное постепенное снижение костной массы, составляющее обычно не более 0,3-0,5% в год. После наступления менопаузы у женщин отмечается максимальная скорость потери костной ткани, которая достигает 2-5% в год и продолжается в таком темпе до 60-70 лет. В итоге женщины теряют от 30 до 50% костной ткани. У мужчин эти потери обычно составляют 15-30%.В зрелом организме процессы минерализации и резорбция кости находятся в состоянии динамического равновесия.
Ремоделирование — это сопряженные во времени процессы локальной резорбции и формирования кости в небольших блоках. Известно, что костная ткань служит основным депо кальция в организме и активно участвует в кальциевом обмене. Высвобождение кальция достигается путем разрушения (резорбция) костной ткани, а его связывание – путем образования костной ткани. С этим связан процесс постоянной перестройки костной ткани, продолжающийся в течение всей жизни организма.
Процесс ремоделирования костной ткани происходит в несколько фаз [активации, резорбции, реверсии, формирования (остеогенеза)], в каждую из которых ведущую роль выполняют те или иные клетки.
Остеокласты и остеобласты вовлечены в процесс ремоделирования кости, остеоциты и покровные клетки участвуют в обменных процессах, обеспечивая питание кости и сохранение кальциевого гомеостаза.
