
Обмен кетоновых тел. Кетонемия, кетонурия, причины их развития
.pdf
Обмен кетоновых тел. Кетонемия, кетонурия, причины их развития.
1.Синтез кетоновых тел, регуляция.
2.Использования кетоновых тел как источника энергии различными тканями.
3.Схема обмена кетоновых тел. Кетоацидоз.
Обмен кетоновых тел
Кетоновые тела (историческое название) являются важными метаболитами во многих периферических тканях, в частности в сердечных и скелетных мышцах.
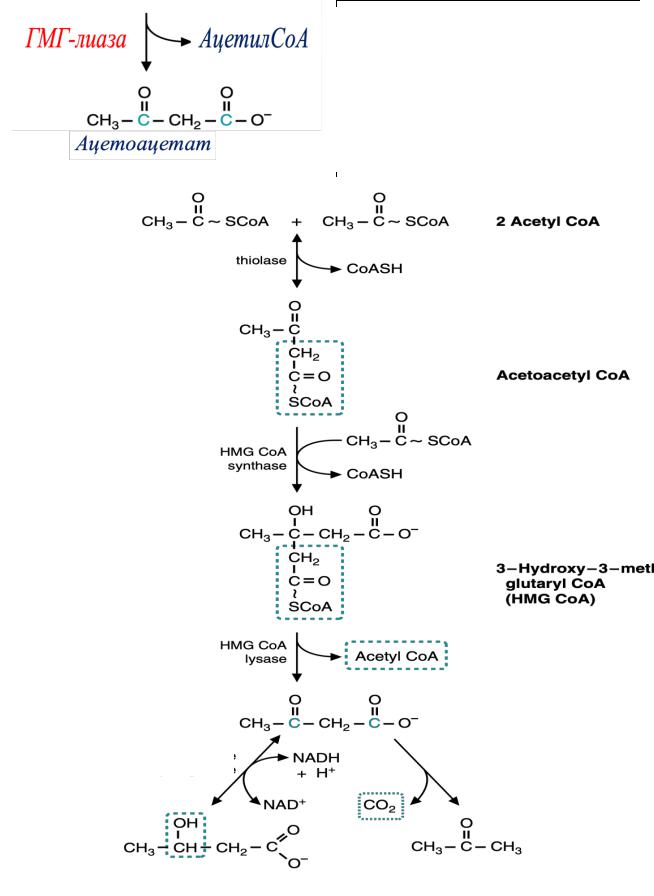
Синтез кетоновых тел протекает в несколько стадий:
2 |
Фермент |
тиолаза |
катализи-рует |
|
конденсацию |
2 молекул АсСоА в |
|||
|
||||
|
ацетоацетилСоА. |
|
||
ГМГ-КоА-синтаза присоединяет еще
один ацетильный остаток к молекуле ацето-ацетил-КоА и образуется 3-
гидрокси-3-метилглутарил КоА (ГМГ КоА)
ГМГ-КоА-лиаза (есть только в митохондриальном матриксе) отрезает ацетильный остаток, включенный в молекулу ГМГ-КоА в 1-й реакции и образуется ацетоацетат, а ацетилКоА вновь используется в синтезе.
Мозг при нормальных условиях в качестве источника нергии использует только глюкозу (жирные кислоты не проходят через гемато нцефалический барьер), однако в период голодания водорастворимые кетоновые тела становятся его главным источником
нергии.
У здоровых нормально питающихся людей кетоновые тела синтезируются только в
митохондриях гепатоцитов в незначительном количестве из АсКоА, который может либо поступить в ЦТК, либо превратиться в кетоновые тела: ацетон, ацетоацетат, β-
гидроксибутират.
В клетках печени, при активном β-окислении, создаётся высокая концентрация НАДН, по тому большая часть ацетоацетата превращается в β-гидроксибутират. Эта реакция легко обратима и относительные количества образующихся ацетоацетата и β-
гидроксибутирата зависят от соотношения НАДН/ НАД+ в матриксе митохондрий.
При высокой концентрации ацетоацетата часть его неферментативно декарбоксилируется с образованием ацетона, который полностью удаляется из организма с потом, мочой и выдыхаемым воздухом:
|
-гидроксибутиратДГ |
Ацетоацетат |
|
β |
Самопроизвольно |
||
|
β-гидроксибутират |
Ацетон |
Регуляторный фермент синтеза кетоновых тел – гидроксиметилглу-тарил-КоА
синтаза (ГМГ-КоА синтаза). Это индуцируемый фермент, синтез которого
увеличивается при повышении концентрации жирных кислот в крови. Это происходит при увеличении мобилизации жиров из жировой ткани под действием глюкагона,
адреналина, секреция которых усиливается |
при голодании или физической нагрузке. |
Синтез ГМГ-КоА-синтазы репрессируется |
при высоких концентрациях в клетке НS- |
КоА. |
|
Окисление кетоновых тел
Молекулы β-гидроксибутирата и ацетоацетата из печени с током крови транспортируются в другие органы и ткани, где являются топливными молекулами. β-
гидроксибутират вновь окисляется до ацетоацетата (рис. 2-9).
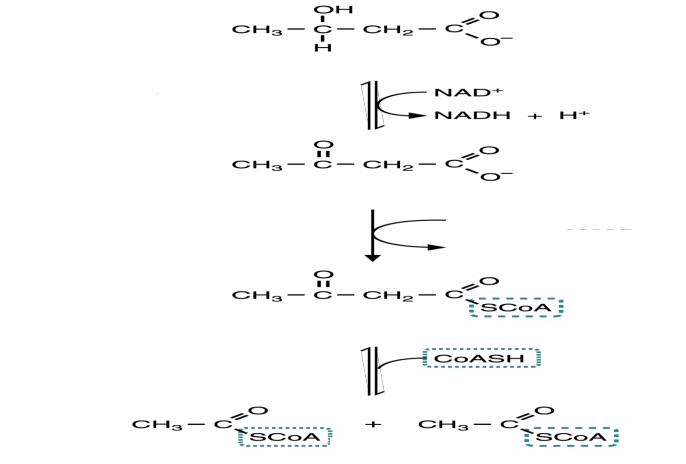
Метаболизм ацетоацетата начинается с превращения его в активную молекулу, в
основном, за счет переноса -S-КоА от молекулы сукцинил-КоА при участии фермента
сукцинил-КоА-ацетоацетат-трансферазы (β-кетоацил-СоАтрансфераза), который
отсутствует в печени, по тому кетоновые тела печенью не используются). Сукцинил-
СоА, используемый в качестве донора кофермента А, удаляется из цикла Кребса.
бразовавшийся ацетоацетил-СоА под действием тиолазы и участии НSСоА расцепляется на 2 молекулы ацетил-КоА, которые затем включаются в цикл Кребса:
β-гидроксибутират
β-гидроксибутиратДГ
Ацетоацетат |
|
|
СукцинилСоА: |
СукцинилКоА |
|
ацетоацетатСоА |
Сукцинат |
|
трансфераза |
||
|
АцетоацетилСоА
Тиолаза
АцетилСоА
Рис.2-9. Метаболизм кетоновых тел во внепеченочных тканях
Энергетический ффект полного окисления каждой молекулы
ацетоацетата равен 23 АТФ (12 АТФ образуется при окислении каждой молекулы АсСоА, -1АТФ – на активацию)
β-гидроксибутирата - 26 моль АТФ (за счет окисления НАДН+Н+)
бразование и кспорт кетоновых тел печенью способствует непрерывному окислению жирных кислот, поскольку высвобождается кофермент А (накопление ацетил-
СоА замедляет β-окисление из-за нехватки свободного кофермента).
Регуляция синтеза кетоновых тел осуществляется гормонами и зависит от
поступления ВЖК в печень.
Активация синтеза кетоновых тел.
У лиц, получающих сбалансированную пищу, главным «топливом» для мозга является глюкоза. В противоположность тому, сердечная и скелетная мышцы, корковый слой почек предпочтительно используют в качестве «топлива» ацетоацетат, а не глюкозу.
При голодании и диабете, мозг начинает активно использовать ацетоацетат. Установлено,
что в условиях длительного голодания 75 % потребности мозга в «топливе» удовлетворяется за счет ацетоацетата.
Синтез кетоновых тел активируется при физиологических состояниях:
–голодании,
–длительной физической нагрузке,
–сахарном диабете,
-употреблении жирной пищи,
-алкогольном отравлении.
Синтез кетоновых тел активируется при: повышении концентрации Ас-КоА и увеличении активности ГМГ синтазы.
АсКоА накапливается, когда его образование превышает потребление.
Повышение образования АсКоА при голодании, усиленных физических нагрузках,
инсулинзависимом сахарном диабете объясняется тем, что в крови увеличивается уровень гормонов: адреналина и глюкагона и снижается уровень инсулина. Активируются:
-липолиз и повышается концентрация ВЖК (адреналин и глюкагон – активаторы ТАГ-
липазы),
-β-окисление (ВЖК – активаторы карнитин-ацилтрансферзы I), снижается уровень НSСоА (используется в данном процессе).
Снижается потребление АсКоА за счет замедления скорости процессов:
-ЦТК: из-за снижения концентрации оксалоацетата, который расходуется на глюконеогенез и повышения уровня NADH и FADH2, (ускорено β-окисление) -
ингибиторов регуляторных ферментов ЦТК.
-биосинтеза ВЖК: адреналин, глюкагон, ВЖК – ингибируют малонилкарбоксилазу.
Индуцируется синтез ГМГ-синтазы, поскольку повышается уровень ВЖК
(индукторы) и снижается концентрация НSCoA (репрессор).
Эти процессы приводят к активации синтеза кетоновых тел и глюконеогененза в период голодания, физической нагрузки и нелеченном сахарном диабете.
ри бо ато ирами иете, особенно у детей, жирные кислоты не успевают
включиться в состав триацилглицеролов и липопротеиновых частиц и частично переходят
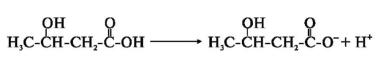
в митохондрии, что увеличивает синтез кетоновых тел.
ри алко ольном отравлении субстратом для синтеза кетонов является ацетил-
СоА, синтезируемый при обезвреживании танала.
Кетонемия, кетонурия, причины их возникновения.
В норме содержание кетоновых тел в крови очень невелико (в норме 1-3 мг/дл или до до 0,2 ммоль/л), однако при длительном голодании и нелеченном сахарном диабете оно может быть высоким. Концентрация кетоновых тел повышается после ночного голодания до 1–2 мг/дл, после недельного голодания она составляет 20–30 мг/дл , а при тяжелых формах сахарного диабета может достигать 300–400 мг/дл.
Ацетоацетат и β-гидроксибутират являются кислотами, которые в крови диссоциируют:
Небольшое повышение концентрации Н+ в крови не влияет на рН, так как функционирующие буферные системы, связывая свободные протоны, препятствуют отклонению его от нормы. Накопление протонов в крови нарушает связывание кислорода гемоглобином, влияет на ионизацию функциональных групп белков, нарушая их конформацию и функцию. Увеличение кислотности обусловлено высокой скоростью синтеза в печени и поступления в кровь ацетоацетата, β-гидроксибутирата и в норме низкой потребностью тканей в использовании тих молекул.
днако когда концентрация Н+ превышает емкость буферных систем, рН крови снижается (ацидоз).
Ацидоз, вызванный повышением уровня кетоновых тел, носит название кетоза или
кетоаци оза. Увеличение концентрации кетоновых тел в крови называют кетонемией,
выделение кетоновых тел с мочой - кетонурией.
При кетозе (состояние организма, когда в качестве основного источника нергии начинает использоваться нергия кетоновых тел) ацетоацетат не успевает весь метаболизироваться и в крови больного находится повышенная концентрация ацетона,
что придаёт специфический запах дыханию и может быть одним из симптомов, например,
сахарного диабета. бразование и выведение ацетона из организма при высокой
концентрации ацетоацетата способствует снижению ацидоза.
Кетоацидоз наблюдается у больных, страдающих тяжелой формой сахарного диабета и не получающих инсулина. рН снижается до 6,8 при норме 7,4, такой сдвиг кислотно-основного равновесия может угрожать жизни больного.
У детей до 7 лет под влиянием различных стимулов (краткое голодание, инфекции,
моциональное возбуждение) ускоряется синтез кетоновых тел и может легко возникать кетоацидоз, сопровождающийся неукротимой рвотой («ацетонемическая рвота»).
Причиной тому служит неустойчивость углеводного обмена и малые запасы гликогена у детей, что усиливает липолиз в адипоцитах, накопление жирных кислот в крови и,
следовательно, кетогенез в печени.
