
Методичка по биохимии. 1 курс - 2 модуль
.pdfТема: «Распад глюкозы по пути гликолиза»
Цель занятия: систематизировать современные сведения о
промежуточном обмене глюкозы для понимания особенностей метаболизма
глюкозы в различных органах и тканях в норме и патологии.
План:
1.Гликолиз: основные этапы, последовательность реакций,
ферменты, значение.
2.Аэробное окисление глюкозы: этапы, энергетический эффект.
3.Пути использования пирувата: анаэробный гликолиз,
энергетический эффект и биологическая роль.
4.Обмен лактата в печени и мышцах. Цикл Кори.
5. Челночные механизмы переноса НАДН из цитозоля в
митохондрии (малатаспартатная и α-глицерофосфатная челночная системы).
6.Образование АТФ при аэробном и анаэробном гликолизе.
1. Гликолиз - специфический путь катаболизма глюкозы, в
результате которого происходит расщепление глюкозы с образованием двух молекул пирувата (аэробный гликолиз) или двух молекул лактата
(анаэробный гликолиз). При наличии кислорода пировиноградная кислота превращается в ацетил-S-КоА и далее сгорает в реакциях тканевого дыхания
до СО2 и Н2О.
2. Аэробный распад глюкозы можно выразить суммарным
уравнением:
С6Н12О6 + 6 О2 → 6 СО2 + 6Н2О + 2820 кДж/моль.
Этот процесс включает несколько стадий:
•Аэробный гликолиз - процесс окисления глюкозы с образованием двух молекул пирувата;
•Общий путь катаболизма, включающий превращение пирувата в ацетил-КоА и его дальнейшее окисление в цитратном цикле;
•ЦПЭ, сопряжённая с реакциями дегидрирования, происходящими в процессе распада глюкозы.
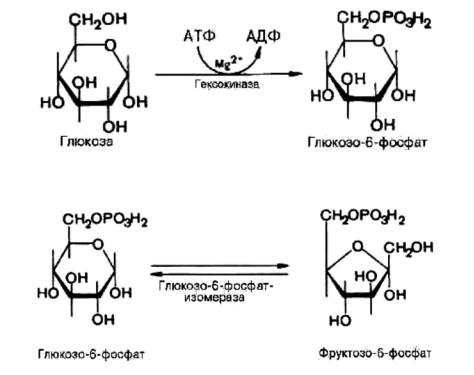
2.1 Этапы аэробного гликолиза
В аэробном гликолизе можно выделить 2 этапа:
1.Подготовительный этап, в ходе которого глюкоза фосфорилируется
ирасщепляется на две молекулы фосфотриоз. Эти реакци протекают с использованием 2 молекул АТФ.
2.Этап, сопряжённый с синтезом АТФ. В результате этой серии реакций фосфотриозы превращаются в пируват. Энергия, высвобождающаяся на этом этапе, используется для синтеза АТФ.
Большинство реакций гликолиза обратимы, за исключением трех (1,3 и
10-й реакции). Гликолиз функционирует во всех живых клетках. Все ферменты локализованы в цитозоле.
1-я реакция: фосфорилирования глюкозы (активация глюкозы), т.е.
перенос остатка ортофосфата на глюкозу за счет ATP.
2-я реакция – изомеризации
3-я реакция – фосфорилирования фруктозо-6-фосфата
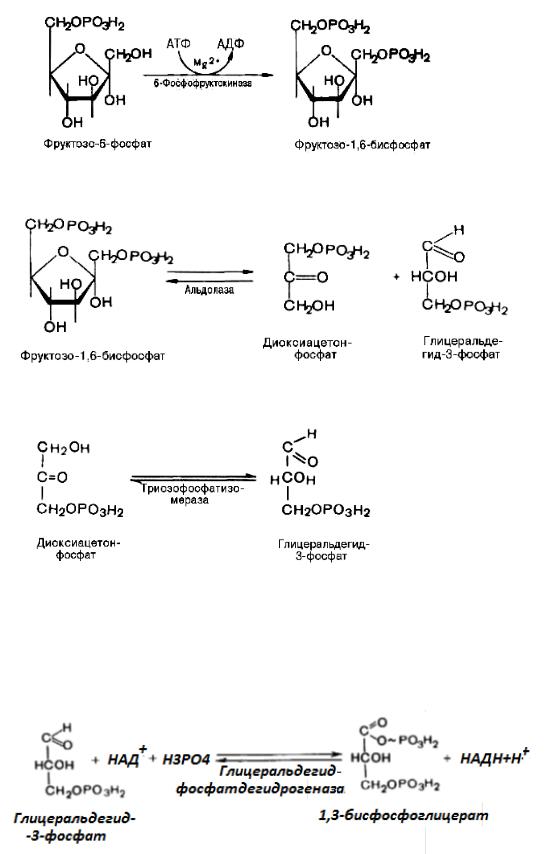
4-я реакция – альдольного расщепления
5-я реакция - изомеризации триозофосфатов
Образованием глицеральдегид-3-фосфата завершается первая стадия гликолиза
6-я реакция - реакция окисления (дегидрирования). Образовавшийся
1,3-бисфосфоглицерат представляет собой высокоэнергетическое соединение.
7-я реакция – субстратного фосфорилирования. Происходит передача богатого энергией фосфатного остатка на ADP с образованием ATP и 3-
фосфоглицериновой кислоты (3-фосфоглицерат).
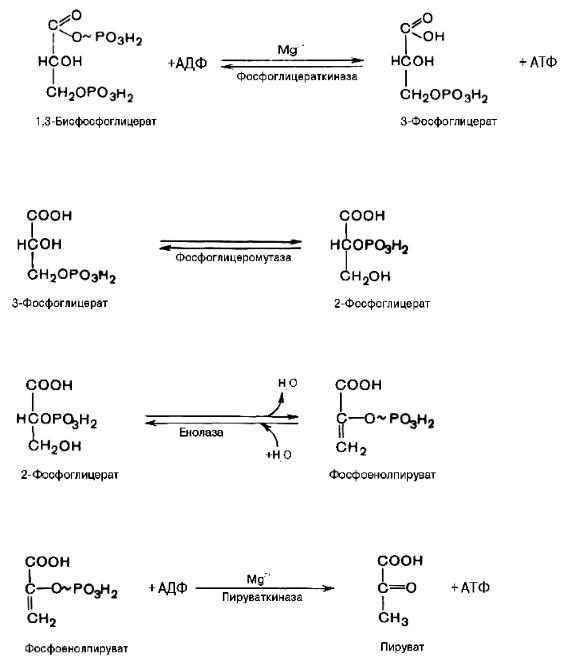
8-я реакция – изомеризации
9-я реакция - дегидратации
10-я реакция – субстратного фосфорилирования.
2.2 Значение аэробного окисления глюкозы
•генерация АТФ для большинства клеток организма, особенно для клеток головного мозга;
•поставляет строительные блоки для реакций синтеза других веществ:
- диоксиацетонфосфат является субстратом для синтеза
триацилглицеридов;
Физиологическая роль гликолиза в печени и жировой ткани
несколько иная, чем в других тканях. В печени и жировой ткани гликолиз в период пищеварения функционирует в основном как источник субстратов для синтеза жиров (ДАФ – для образования α-глицерофосфата).
-ПВК – используется для синтеза незаменимых аминокислот;
-1,3-дифосфоглицерат в эритроцитах результате изомеризации превращается в 2,3-дифосфоглицерат, который служит
аллостерическим регулятором сродства гемоглобина к кислороду.
3 Анаэробный гликолиз
Анаэробным гликолизом называют процесс расщепления глюкозы с образованием в качестве конечного продукта лактата.
Анаэробный гликолиз: позволяет синтезировать АТФ при недостатке кислорода в тканях, особенно:
•в мышцах в первые минуты мышечного сокращения;в
эритроцитах, не имеющих митохондрии;
•в клетках злокачественных опухолей.
Для большинства тканей – это аварийный путь, т.к. обеспечивает энергией в условиях гипоксии, при тяжелом физическом труде, болезнях
органов дыхания и сердечно-сосудистой системы.
При анаэробном гликолизе в цитозоле протекают все 10 реакций,
идентичных аэробному гликолизу.
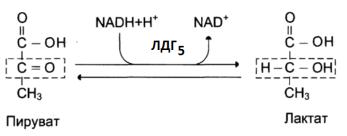
В результате 11-ой реакции происходит восстановление ПВК и образуется
молочная кислота.
Рис.1 Восстановление ПВК в лактат
Реакция протекает при участии фермента лактатдегидрогеназы 5 и
кофермента НАДН, образовавшегося в шестой реакции.

Рис.2 Общая схема аэробного и анаэробного гликолиза
4 Обмен лактата в печени и мышцах. Цикл Кори.
Лактат не является конечным продуктом метаболизма, полностью удаляемым из организма. Однако, сама мышечная клетка ни при работе, ни во время отдыха не способна превратить лактат в пируват из-за низкого сродства изофермента ЛДГ-5 к лактату.
Поэтому во время и после нагрузки (при восстановлении) лактат удаляется из скелетных мышц. Это происходит довольно быстро, всего через
0,5-1,5 часа в мышце лактата уже нет, и только малая часть молочной кислоты выводится с мочой. Большая часть лактата захватывается гепатоцитами и в условиях тяжелой физической нагрузки миокардом. В печени и миокарде отношение НАДН/НАД+ ниже, чем в сокращающейся мышце, поэтому активны ЛДГ1 и ЛДГ2, обладающие большим сродством к лактату, чем ЛДГ5.
В этих органах лактатдегидрогеназная реакция протекает в обратном направлении, т.е. в сторону образования пирувата из лактата. Образовавшийся пируват в миокарде преимущественно вступает в общий путь катаболизма,
окисляясь до конечных продуктов, и получения энергии для деятельности сердечной мышцы.
.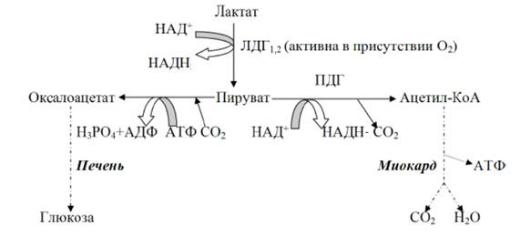
Рис.3 Метаболизм лактата в присутствии кислорода
Энергия окисления ПВК в печени может использоваться для синтеза АТФ, необходимого в реакциях глюконеогенеза. Глюкоза, образованная в печени из лактата, возвращается обратно в мышцы, восстанавливая во время отдыха запасы гликогена (цикл Кори), или в другие ткани.
Цикл Кори выполняет 2 важнейшие функции:
1 - обеспечивает утилизацию лактата;
2 - предотвращает накопление лактата и, как следствие этого, опасное снижение рН (лактоацидоз).

Рис.4 Цикл Кори
Концентрация лактата в крови зависит от интенсивности и длительности работы. В условиях покоя концентрация лактата равна
1 ммоль/л, при тяжелой работе она может превышать 15 ммоль/л, что приводит к понижению рН крови - лактоацидозу. Уровень лактата в крови зависит от интенсивности его использования в двух процессах:
1)окисления до СО2 и Н2О;
2)в качестве субстрата для синтеза глюкозы
Лактоацидоз может возникать при ряде патологических состояний,
когда нарушается снабжение тканей кислородом. В этих случаях (инфаркт миокарда, легочная эмболия, кровотечение и др.) энергетические потребности клеток удовлетворяются на счет анаэробного гликолиза, что приводит к повышению уровня лактата и падению рН ниже оптимального уровня,
необходимого для активной работы ферментных систем. Результатом этого могут быть резкие нарушения в клеточном метаболизме.
5. Челночные механизмы переноса водорода от НАДН+Н+ из
цитозоля в митохондрии.
Молекулы НАДН+Н+, образованные в шестой реакции гликолиза, в
зависимости от наличия кислорода могут:
•либо остаться в цитозоле и вступить в лактатдегидрогеназную реакцию (анаэробные условия),
• либо проникнуть в митохондрию и окислиться в дыхательной цепи (аэробные условия).
Так как сама молекула НАДН+Н+ через митохондриальную мембрану не проходит, то существуют системы, принимающие этот водород в цитоплазме и отдающие его в матриксе митохондрий. Они называются
челночные системы.
Определены две основные челночные системы – глицеролфосфатная
и малат-аспартатная, которые отличаются друг от друга акцепторами водорода для ЦПЭ и, следовательно, количеством синтезированного АТФ. В
глицерофосфатной системе водород передается на FAD-зависимую дегидрогеназу, поэтому Р/О = 1,5. Вторая система энергетически более эффективна, так как водород поступает в ЦПЭ через митохондриальный
NAD+ и отношение Р/О составляет 2,5.
Глицеролфосфатный челночный механизм
Глицеролфосфатная челночная система работает в клетках белых мышц и гепатоцитов.
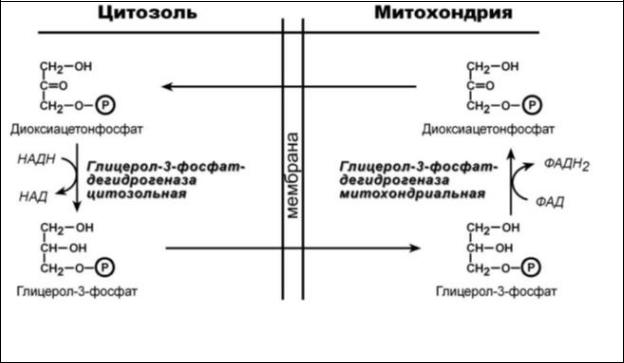
Рис.5 Схема работы глицерофосфатного челночного механизма
Ключевыми ферментами глицеролфосфатного челнока являются изоферменты глицерол-3-фосфатдегидрогеназы – цитоплазматический и
митохондриальный. Они отличаются своими коферментами: у
цитоплазматической формы – НАД, у митохондриальной – ФАД.
В цитозоле метаболиты гликолиза – диоксиацетонфосфат и НАДН образуют глицерол-3-фосфат, поступающий в матрикс митохондрий. Там он окисляется с образованием ФАДН2. Далее ФАДН2 направляется в дыхательную цепь и используется для получения энергии.
Работа глицеролфосфатного челночного механизма актуальна при необходимости получить энергию из глюкозы при работе клетки.
Однако, если в клетке имеется избыток энергии (состояние покоя, после еды), то глицерол-3 фосфат будет использоваться в цитозоле для синтеза жиров.
Малат-аспартатный челночный механизм.
Малат-аспартатный челночный механизм является более универсальным и распространен практически во всех тканях.
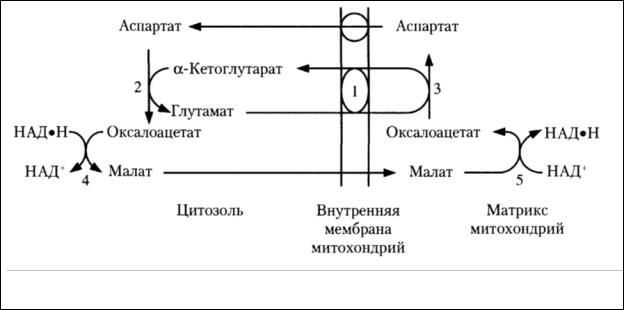
Рис.6 Схема работы малат-аспартатного челночного механизма
Ключевыми ферментами этого челнока являются изоферменты малатдегидрогеназы цитоплазматический и митохондриальный. Постоянно идущие в цитоплазме реакции трансаминирования аспартата поставляют оксалоацетат, который под действием цитозольного пула малатдегидрогеназы и "гликолитического" НАДН восстанавливается до яблочной кислоты.
Последняя антипортом с α-кетоглутаратом проникает в митохондрии и,
