
книги / 860
.pdfФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
СИБИРСКИЙ ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ
М. В. Вульф Р. А. Цыкин
ЗЕМЛЕВЕДЕНИЕ
Утверждено редакционно-издательским советом университета в качестве учебного пособия
Красноярск ИПК СФУ
2009
1
УДК 549.1 + 552.3/5 + 543.3 + 551.5 ББК 26.3:26.2
В88
Рецензенты: О. Ю. Перфилова, кандидат геолого-минералоги- ческих наук, доцент каф. ГМиМР СФУ; Т. А. Ананьева, кандидат геолого-минералогических наук, доцент декан географического факультета КГПУ
Вульф, М. В.
В88 Землеведение : лаб. практикум / М. В. Вульф, Р. А. Цыкин. – Красноярск : ИПК СФУ, 2009. – 84 с.
Впрактикуме приведены краткие сведения о минералах земной коры
идана характеристика изучаемых минералов. Изложены минимально необходимые сведения о горных породах с характеристикой магматических, метаморфических и осадочных пород. Одна лабораторная работа посвящена химическому составу природных вод и одна – составу и экологическим характеристикам атмосферного воздуха.
Для студентов специальности 080100 «Экономика и управление на предприятии».
УДК 549.1 + 552.3/5 + 543.3 + 551.5 ББК 26.3:26.2
© Сибирский федеральный университет, 2009
2
ВВЕДЕНИЕ
Всоответствии с Государственным образовательным стандартом специальности лабораторный практикум знакомит студентов с основами минералогии и петрографии горных пород. Кроме того, студенты получают знания о химическом составе природных вод и способе формирования названия воды, а также о составе и экологической оценке атмосферного воздуха. Будущих специалистов в сфере экономики и управления на предприятиях горной отрасли практикум знакомит с геологическими процессами, протекающими в недрах Земли и на её поверхности, дает им представление о минералах, горных породах и рудах.
Учебной программой курса «Землеведение» предусмотрено 17 ч лабораторных занятий, из них 8 ч приходится на изучение раздела «Минералогия», 6 ч – на изучение горных пород в разделе «Петрография», 2 ч – на ознакомление с разделом «Гидрогеология» и 1 ч – «Климатология и метеорология».
Вглаве «Минералогия» дано понятие о минералах, их морфологии, физических свойствах и классификации. В табличном виде приведены основные свойства минералов, которые студенты учатся различать
спомощью лабораторного практикума и учебной коллекции. Перечень изучаемых минералов по классам включает в себя класс самородных элементов (золото, медь, графит, алмаз, сера), класс сульфидов (пирит, халькопирит, пирротин, пентландит, галенит, сфалерит, киноварь, молибденит), оксидов (кварц, корунд, магнетит, хромит, пиролюзит) и гидрооксидов (боксит), галоидов (флюорит, галит), а также карбонатов (кальцит, магнезит, сидерит, малахит), сульфатов (гипс, барит), фосфатов (апатит) и самый многочисленный класс силикатов, который делится на подклассы: островные (оливин, гранаты), кольцевые (берилл, турмалин), цепочечные (пироксены), ленточные (амфиболы); слоистые (тальк, слюды, хлориты, каолинит) и каркасные (калиевые полевые шпаты, плагиоклазы, нефелин).
Глава «Петрография» знакомит студентов с горными породами. Классификация приведена в соответствии с Петрографическом кодексом 2008 г., выделено 6 типов горных пород: магматический, осадочный, метаморфический, метасоматический, мигматитовый и импактный. В лабораторном практикуме приведены базовые сведения для приобретения
3
навыков описания и распознавания горных пород по их структурнотекстурным особенностям и минеральному составу.
Тип магматических пород рассматривается по трем классам: плутонические, вулканические и гипабиссальные породы. Отряды выделены по содержанию кремнезема: ультраосновные, основные, средние и кислые, подотряды – по щелочности: щелочные, умеренно щелочные, нормальной щелочности и низкощелочные. Далее в классификации выделяют семейства (базальты, андезибазальты, андезиты) и виды пород. На изучение студентам вынесены следующие виды пород: перидотит, пикрит, габбро, базальт, диорит, андезит, сиенит, трахит, гранит, риолит и уритит.
Осадочный тип горных пород подразделяется на классы терригенных (конгломераты, брекчии, песчаники), хемогенных (известняки, кремни, яшмы, соли) глинистых, хемогенно-биогенных (ракушечники, диатомиты) и вулканогенно-обломочных пород (вулканический песок, пепел, бомбы).
Метаморфический тип пород рассмотрен по трем классам: контактовый, региональный и дислокационный. Примеры пород для изучения: кристаллические сланцы, гнейсы, кварциты, мраморы, роговики, катаклазиты.
Тип метасоматических пород представлен скарнами, грейзенами, серпентинитами. Тип мигматиты рассматривается с позиции ультраметаморфизма на примере расслоенных и частично расплавленных пород. Импактный тип пород дан как продукты ударного метаморфизма – брекчии, тагамиты, зювиты.
Вглаве «Гидрогеология» рассматривается химический состав подземных вод, формы выражения, определение основных показателей. Приведены примеры решения задач по нормированию качества водных объектов для питьевого и промышленного водоснабжения.
Глава «Климатология и метеорология» знакомит студентов с решением типовой задачи по нормированию качества атмосферного воздуха.
Врезультате выполнения всех предусмотренных учебной программой курса практических занятий студенты получают необходимый минимум знаний, умений и навыков по дисциплине «Землеведение».
4
1. МИНЕРАЛОГИЯ
Минералогия – это наука о природных химических соединениях (минералах), их составе, свойствах, особенностях и закономерностях физического строения (структуры), а также об условиях образования и изменения в природе.
1.1.Понятие о минерале, кристалле
икристаллическом строении
Минерал (франц. mineral, от позднелат. minera – руда) – природное тело, приблизительно однородное по химическому составу и физическим свойствам, образовавшееся в результате физико-химических процессов, происходивших на поверхности или в недрах Земли (и других космических тел), главным образом как составная часть горных пород, руд, метеоритов. Минералы состоят из химических элементов, находящихся в твердом фазовом состоянии вещества, исключение составляет жидкая самородная ртуть. Они относительно однородны по составу и в большинстве случаев (98 %) имеют кристаллическое строение (исключение – аморфные вещества).
Минералы с кристаллическим строением способны самоограняться, т.е. минерал в процессе роста обретает форму в виде кристалла, например, кубические кристаллы каменной соли, снежинки кристаллов льда, октаэдрические кристаллы алмазов и т.д., по форме проявления минералы весьма разнообразны. Форма кристалла зависит от химического состава, вида химических связей и типа пространственной кристаллической решетки. В малом количестве встречаются в природе минералы без кристаллической решетки, их строение аморфно. Они состоят из субмикроскопических частиц продуктов распада или очень тонкого дробления кристаллических минералов, заключенных в воде или водном растворе (гидрогели), например, опал – гель кремнезёма и т.п.
Минералы могут состоять из одного химического элемента (золото, медь, сера), но чаще – из нескольких, например, минерал кварц состоит из двух химических элементов: кремния и кислорода, полевой шпат – из кремния, кислорода, калия и натрия, объединенных между собой химическими связями. Кроме того, в химической формуле анионный комплекс (–) выделяют от катионного (+) квадратными скобка-
5
ми: Na[AlSi3O8]. Тип химической связи во многом определяет свойства минералов. Рассмотрим виды химических связей.
Металлическая связь образуется при взаимодействии катионов металлов и свободных блуждающих электронов, за счет которых минералы обладают высокой тепло- и электропроводностью, для нее характерна высокая отражательная способность.
Ионная связь существует за счет электростатического взаимодействия между катионами и анионами. Минералы с ионной связью имеют низкую электропроводность (диэлектрики), часть из них растворима в воде, например, соль – галит.
Ковалентная связь – это связь между атомами, которые соединяются за счет спаривания электронов с противоположными спинами, образуются минералы с повышенными плотностью (алмаз) и температурой плавления, полупроводники (синтетические кристаллы кремния, германия).
Связь Ван-дер-ваальса соединяет между собой молекулы вещества за счет относительно слабых дипольных моментов. Так образуются минералы с низкими твердостью и температурой плавления, огнеупоры (слюда, глина).
Водородная связь формируется между атомами водорода одной молекулы с атомами кислорода, фтора, хлора соседних молекул.
Вминералах может быть один вид химической связи или комбинация двух или трех видов. Например, в графите атомы углерода ковалентно связаны в двумерные слои, которые в свою очередь соединяются между собой вандерваальсовыми связями, так как последние слабы и легко разрываются, графит мягок и легко расщепляется на чешуйки, параллельные слоям атомов углерода. Среди минералов часто встречается ионно-ковалентный тип связи.
Минералы, как правило, имеют форму кристаллических многогранников. В кристаллах атомы и ионы располагаются в постоянных точках – узлах кристаллической решётки, её параметры строго индивидуальны для каждого минерала.
Вкристаллической решетке частицы расположены строго закономерно. Атомы, ионы или молекулы представляют собой узлы, которые объединяются в ряды (одномерное пространство) с расстоянием между узлами а (рис. 1). Совокупность двух рядов с параметрами a и b формирует двухмерное пространство в виде плоских сеток. Система трех рядов, не лежащих в одной плоскости, формирует трехмерное пространство кристаллической решетки, которое состоит из множества элементарных ячеек со сторонами а, b и c.
6
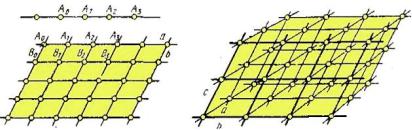
Элементарная ячейка – это самая маленькая часть кристалла, которая многократно повторяется в трехмерном пространстве. Грани кристаллов соответствуют плоской сетке, ребра – рядам, вершины – узлам кристаллической решетки. Грани пересекаются по ребрам, а ребра соединяются в вершинах, образуя объемные кристаллы. Характерными признаками кристаллов являются симметричность, способность самоограняться, минимум внутренней энергии, статичность, однородность и анизотропия свойств.
а
б в
Рис. 1. Элементы кристаллической решетки: а – ряды; б – плоские сетки; в – элементарные ячейки
Анизотропия проявляется в том, что свойства тела одинаковы по параллельным направлениям и неодинаковы по непараллельным направлениям.
Однородность – свойство физического тела быть одинаковым во всем объеме. Статичность определяется взаимодействием сил притяжения и отталкивания, которые удерживают всю кристаллическую структуру в равновесии, а центры материальных частиц (условно шары), колеблются (вибрируют) возле так называемых узлов кристаллической решетки.
Минимальная внутренняя энергия устанавливается в твердых телах и соответствует состоянию термодинамического равновесия. Кристаллическое состояние твердого тела более устойчиво, чем аморфное, так как требует меньших затрат внутренней энергии, именно поэтому аморфные вещества с течением времени обнаруживают тенденцию к кристаллизации.
Способность самоограняться – свойство кристаллов принимать многогранную форму при определенных условиях их роста.
Симметрия (соразмерность) – правильная повторяемость граней, ребер и вершин при повороте и отражении кристалла относительно
7
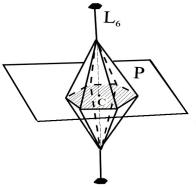
элементов симметрии. Основными элементами симметрии кристаллической решётки являются центры, оси и плоскости симметрии.
Ось симметрии (L) – это воображаемая прямая, при повороте кристалла вокруг оси грань кристалла совмещается сама с собой 2, 3, 4 или 6 раз, соответственно, различают оси симметрии 2-го, 3-го, 4-го и 6-го порядка.
Плоскость симметрии (Р) – это воображаемая плоскость, которая делит кристалл на две равные зеркальные части. Центр симметрии (С) – представляет собой точку, равноудалённую от противоположных граней, рёбер и вершин кристалла. Например, на рис. 2 в кристалле изображены: ось симметрии 6-го порядка (L6), при повороте вокруг которой кристалл совместится сам с собой 6 раз; плоскость симметрии (Р), которая делит кристалл на две зеркально равные части, и центр симметрии (С) в виде точки, равноудаленной от противолежащих граней, ребер и вершин. Полный набор элементов симметрии для этого кристалла состоит из одной оси 6-го порядка, шести осей 2-го порядка (три проходят через противоположные ребра и три – через вершины в горизонтальной плоскости рисунка), семи плоскостей (три вертикальных плоскости пройдут через противоположные ребра, три – через середины противоположных граней и одна горизонтальная плоскость) и центр. Кратко данный набор элементов симметрии записывают в виде формулы – L66L27PC.
Рис. 2. Элементысимметриивкристалле: ось, плоскость и центр
Все кристаллы, обладающие одинаковым набором элементов симметрии, относятся к одному виду (классу) симметрии. Всего Е.С. Федоровым выделено и описано 32 вида симметрии, которые отражают все возможные варианты размещения атомов и молекул в кристаллах [1]. Виды симметрии объединяют в 7 сингоний, а сингонии – в 3 категории (табл. 1).
8
Т а б л и ц а 1
Элементы симметрии в кристаллах
Сингонии |
Характерные при- |
Элементарная |
Примеры кри- |
Примеры |
||||
симметрии |
|
знаки |
|
ячейка |
сталлов |
минералов |
||
|
|
|
Низшая |
категория симметрии |
|
|
||
(кристаллы несимметричные или удлиненные в двух направлениях: |
|
|||||||
|
|
таблитчатые, чешуйчатые, листоватые) |
|
|
||||
Триклин- |
Рёбра |
кристаллов |
Косоугольный |
|
Плагиок- |
|||
ная |
пересекаются под |
параллелепипед |
|
лазы |
|
|||
|
косым углом, |
нет |
|
|
|
|
||
|
элементов |
сим- |
|
|
|
|
||
|
метрии |
|
|
|
|
|
|
|
Моно- |
Две неравные оси |
Параллелепи- |
|
Полевые |
||||
клинная |
перпендикуляр- |
пед с одним уг- |
|
шпаты, |
||||
|
ны, третья накло- |
лом между гра- |
|
слюды, |
||||
|
нена, |
кристаллы |
нями ≠ 90о |
|
амфиболы, |
|||
|
перекошены |
|
|
|
пироксены |
|||
Ромбиче- |
Три неравные оси |
Прямоуголь- |
Ромбиче- |
Оливин, |
||||
ская |
пересекаются под |
ный параллеле- |
ская призма, |
сера, барит, |
||||
|
прямыми углами |
пипед |
пирамида |
топаз |
|
|||
|
|
|
Средняя |
категория симметрии |
|
|
||
(кристаллы удлинены по оси симметрии 3-го, 4-го или 6-го порядка: |
|
|||||||
|
|
призматические, столбчатые, игольчатые) |
|
|
||||
Триго- |
Все оси равны, но |
Ромбоэдр |
Тригональ- |
Киноварь, |
||||
нальная |
углы между ними |
|
ные призмы, |
кварц, |
|
|||
|
не равны 90о |
|
|
пирамиды, |
кальцит, |
|||
|
|
|
|
|
|
дипирамиды |
турмалин |
|
Тетра- |
Ребра |
по |
двум |
Тетрагональная |
Тетрагональ- |
Рутил, |
|
|
гональ- |
осям |
равны, |
все |
призма |
ные призмы, |
циркон, |
||
ная |
углы |
между |
гра- |
|
пирамиды, |
касситерит |
||
|
нями прямые |
|
|
дипирамиды |
|
|
||
Гексаго- |
Три равные оси в |
Шестигранная |
Гексагональ- |
Молибде- |
||||
нальная |
одной |
плоскости |
призма |
ные призмы, |
нит, графит, |
|||
|
пересекаются под |
|
пирамиды, |
апатит, |
бе- |
|||
|
углом 120о |
|
|
|
дипирамиды |
рилл, |
нефе- |
|
|
|
|
|
|
|
|
лин |
|
|
|
|
Высшая |
категория симметрии |
|
|
||
(кристаллы изометричны, одинаково развиты в трех направлениях: |
|
|||||||
|
|
|
кубические, октаэдрические) |
|
|
|||
Кубиче- |
Оси |
кристаллов |
Куб |
Куб, октаэдр, |
Галенит, |
|||
ская |
пересекаются под |
|
тетраэдр |
флюорит, |
||||
|
прямыми |
углами |
|
|
пирит, алмаз, |
|||
|
и равны |
между |
|
|
магнетит |
|||
|
собой |
|
|
|
|
|
|
|
9
Подсчитано, что около 38 % минералов кристаллизуется в триклинной и моноклинной сингониях, 23 % – в ромбической, 10 % – в тригональной, 7,5 % – в гексагональной, 9,5 % – в тетрагональной, 12 % – в кубической сингониях.
Симметрия внешней формы (огранки) кристалла определяется симметрией его атомного строения, которая обусловливает также и симметрию физических свойств кристалла.
1.2. Морфология минералов
Минералы различают по особенностям химического состава и кристаллического строения. Эти свойства определяют внешний вид (морфологию) минерала и его физические свойства (цвет, блеск, твёрдость, магнитность и т.п.).
Формы проявления минералов в природе очень разнообразны. Они могут быть представлены кристаллами, но чаще наблюдаются в виде срастаний кристаллических зерен определённой формы – минеральных агрегатов. Один и тот же минерал может образовать кристалл и кристаллические зернистые массы. Кристаллы вырастают при медленном остывании магмы на заключительных этапах её кристаллизации. Для роста кристалла необходимо свободное пространство (стенки трещин и пустот), иначе образуются срастания кристаллических зерен, и чем быстрее кристаллизуется расплав, тем мельче вырастут зёрна, при моментальном охлажденииформируютсяаморфныевулканическиестекла.
Минеральный агрегат, сложенный одним минералом, называют мономинеральным (рис. 3, 4), а из двух и более минералов – полимине-
ральным (рис. 5).
Минеральные агрегаты характеризуют по величине кристаллических зёрен: крупнозернистые сложены зёрнами крупнее 5 мм в попе-
речнике, среднезернистые – 2–5 мм, мелкозернистые – меньше 2 мм и
скрытокристаллические состоят из зерен, различимых только под микроскопом.
Кроме размера минерального агрегата при его диагностике важна форма кристаллов и зёрен, возможные варианты представлены на рис. 6.
Изометричные формы одинаково развиты в трех направлениях пространства. Примером изометричных кристаллов могут служить кубы пирита, октаэдры магнетита, ромбододекаэдры граната; примеры изометричных кристаллических зёрен характерны для оливина, галенита, сфалерита, флюорита и др.
10
