- •Эндометриоз
- •Оглавление
- •Список сокращений
- •Предисловие
- •Введение
- •Классификация эндометриоза
- •Этиология и патогенез
- •Клиническая картина
- •Эндометриоз тела матки (аденомиоз, внутренний эндометриоз)
- •Эндометриоз яичников
- •Ретроцервикальный эндометриоз (эндометриоз ректовагинальной перегородки)
- •Эндометриоз шейки матки и влагалища
- •Перитонеальный эндометриоз
- •Эндометриоз и бесплодие.
- •Эндометриоз и врт
- •Диагностика
- •7. Дифференциальная диагностика
- •8.Лечение
- •9. Направленная иммунотерапия в лечении эндометриоза.
- •9.1.Цитокинотерапия в комплексном лечении пациенток с бесплодием, ассоциированным с наружным генитальным эндометриозом.
- •9.2 Цитокинотерапия в дифференцированной терапии синдрома хронической тазовой боли у больных перитонеальным эндометриозом.
- •9.3 Цитокинотерапия в лечении аденомиоза.
- •10.Профилактика
- •11.Контрольные вопросы
- •12. Ситуационные задачи с решением:
- •13. Ситуационные задачи для самостоятельного решения.
- •14.Тестовый контроль
- •15.Эталоны ответов
- •16. Эталоны ответов к ситуационным задачам
- •17. Рекомендуемая литература
- •17.1 Основная
- •17.2 Дополнительная литература.
- •18. Литература, использованная авторами:
7. Дифференциальная диагностика
Дифференциальная диагностика эндометриоза проводится с рядом заболеваний.
Аденомиоз дифференцируют от ряда следующих заболеваний:
Миома матки;
Рак эндометрия .
Эндометриоз яичников дифференцируют от:
Опухолевидных образований воспалительного характера;
Доброкачественных и злокачественных опухолей;
Туберкулеза придатков матки.
Проводят дифдиагностику эндометриоза шейки матки от:
Истинная эктопия шейки матки;
Эндоцервицит;
Эритроплакии;
Рак шейки матки .
Ретроцервикальный эндометриоз отличают от:
Рака прямой кишки;
Рака влагалища;
Рака яичника III-IV степени.
8.Лечение
Тактика ведения пациенток зависит от таких факторов, как репродуктивные планы, возраст, клинические проявления и их тяжесть, стадия эндометриоза и особенности хирургического лечения, переносимость предыдущего лечения, риск побочных эффектов, состояние внутренних органов, свертывающей системы крови и центральной нервной системы, стоимость и предполагаемая длительность терапии. В каждом конкретном случае подход должен быть индивидуальным. Помимо хирургического предложено множество методов медикаментозного лечения, направленных на купирование симптомов заболевания, особенно болевого, и улучшение качества жизни пациенток. Существуют и проблемы терапии: недостаток доказательных данных по применению разных схем лечения и разрыв между руководствами и реальной практикой, например, широкое использование препаратов по незарегистрированным показаниям. Единственного подхода, который был бы идеальным для всех пациенток, не существует.
Сущность хирургического метода заключается в ликвидации очагов эндометриоза в пределах неизмененных тканей (визуально и пальпаторно). Выбор метода и объем хирургического вмешательства определяются индивидуально в соответствии с локализацией и распространенностью эндометриоидного процесса, вовлечением прямой кишки, мочевого пузыря, а также со стремлением сохранить или восстановить репродуктивную функцию.
Лапароскопическое лечение, несмотря на непрекращающиеся споры, считается "золотым стандартом", поскольку оно менее травматично, реже сопровождается образованием послеоперационных спаек, дает лучшие результаты в сравнении с другими методами терапии бесплодия. Эффективность хирургического лечения эндометриоза, несомненно зависит от радикальности операции. Однако расширение объема операции уменьшает шансы на сохранение специфических функций женского организма.
Отмеченное положение является причиной отсрочки операции, что приводит к прогрессированию заболевания, особенно у молодых пациенток, вовлечению в процесс смежных органов, появлению неврологических нарушений, и когда принимается решение об операции, то нередко объем ее становится таким, что речь может идти лишь об избавлении женщин от мучительных страданий и восстановлении работоспособности.
Более того хирургический и медикаментозные методы лечения не должны противопоставляться друг другу. При поражении смежных органов хирургическая бригада должна быть расширена и обязана включать профильных специалистов ( врач – уролог, врач – хирург и др.).
Рекомендована энуклеация стенки эндометриодной кисты после ее опорожнения, промывания полости для полного удаления патологического процесса, для верификации диагноза и уменьшения вероятности рецидива. Энуклеация капсулы позволяет сохранить овариальный резерв, что увеличивает шансы на наступление спонтанной беременности.
Оперативное лечение показано пациенткам с узловой формой эндометриоза при наличие аномальных маточных кровотечений.
К глубокому сожалению, частота наступления беременности у пациенток с аденомиозом 3-4-й стадии не превышает 10-15%, поскольку ни один метод лечения не позволяет создать благоприятные условия для имплантации эмбрионов. Единственным наиболее эффективным методом лечения остается тотальная гистерэктомия. При наличии бесплодия у пациенток с узловой формой аденомиоза, которые сопровождаются АМК, возможно выполнение реконструктивно-пластической операции с максимальным удалением пораженной ткани, для уменьшения маточных кровотечений и повышения возможности реализации репродуктивной функции.
Целью медикаментозного лечения в большинстве случаев – это облегчение тяжести симптомов, повышение качества жизни. Медикаментозное лечение эндометриоза включает эмпирическую медикаментозную терапию при наличии болей, характерных для эндометриоза, адъювантную терапию в послеоперационном периоде для профилактики рецидивов, лечение рецидивов для снижения риска повторных операций, терапию, направленную на восстановление фертильности. Из числа медикаментозных средств (гормональных препаратов) при лечении эндометоиза используется широкий спектр соединений - комбинированные эстроген-гестагенные препараты, прогестагены, антиэстрогены, антигестагены, антигонадотропины, аГнРГ (агонисты гонадотропинрилизинг гормонов). На сегодняшний день, из всего многообразия гормонмодулирущих препаратов практическую ценность сохраняют КОК, прогестагены, а-ГнРг. При проведении гормональной терапии следует учитывать, что эндометриоз представляет собой хроническое заболевание с рецидивирующим течением и признаками автономного роста имплантата. Ни один медикаментозный препарат не устраняет морфологический субстрат эндометриоза, оказывая только временное опосредованное влияние на его биологическую активность. В связи с этим современный подход к долгосрочному ведению пациенток с эндометриозом, включает не только медикаментозную терапию, но и хирургическое лечение, или сочетание этих методов.
В основе гормональной терапии лежит снижение уровня эстрогенов, что приводит к уменьшению размеров эндометриоидных образований и частоты рецидивов эндометриоза. В настоящее время для лечения пациенток наиболее часто используются комбинированные оральные контрацептивы (КОК). Несмотря на то что эти препараты не имеют аннотированного показаниям к терапии, препараты данной группы считаются терапией первой линии. Положительными моментами являются: низкая стоимость, возможность длительного и повторного использования, а также контрацептивный эффект, что немаловажно для молодых и сексуально активных женщин. КОК давно и прочно заняли определенную «нишу» в лечении эндометриоза, а именно – купирование дисменореи и прежде всего альгоменореи (эффективность – 60–95%). Для лечения теоретически используется любой монофазный КОК, но желательно, чтобы в нем доминировал прогестагенный компонент. Препаратами выбора являются КОК, содержащие в качестве гестагенного компонента диеногест (диеногеста – 2 мг, этинилэстрадиола – 0,03 мг). Способ применения обсуждается, но многие предпочитают назначать препарат в непрерывном режиме, что является более целесообразным, исходя из основных целей, которые стоят перед гинекологами при лечении эндометориоза (уменьшение выраженности болевого синдрома, ликвидация эндометриоидных гетеротопий и профилактика рецидивов), так как у многих женщин в течение 7-дневного перерыва начинается созревание фолликулов и возрастает уровень эстрогенов. Благодаря прогестагенам подавляется пролиферация эндометрия и часто возникает аменорея. Однако если в течение 3-х месяцев непрерывного приема КОК нет результата, целесообразно перейти на другую, более сильную гормональную терапию. Польза от перехода на другой КОК не доказана. Ранее было отмечено, что хотя КОК не эффективны для лечения рецидивов эндометриоза, они достаточно эффективны в качестве ингибирующей послеоперационной терапии для профилактики рецидивов.
Многие годы препаратами выбора для лечения и реабилитации пациенток с эндометриозом были агонисты гонадотропин – рилизинг – гормонов (аГРГ), обладающие антиэстрогенным, антигестагенным, антигонадотропным и антиандрогенным действием. Эффект опять же связан со способностью подавлять секрецию гонадотропинов, тем самым снижать концентрацию эстрогенов и повышать уровень андрогенов. Это приводит к атрофии нормального эндометрия и эндометриоидных очагов, в результате у женщин развивается аменорея. Высокая клиническая эффективность и удобство применения данных препаратов обусловили их преимущественное применение в последние десятилетия. Анализ данных литературы показывает, что благодаря применению агонистов ГнРГ повышается эффективность лечения больных эндометриозом, отмечается существенная положительная динамика в отношении болевого синдрома (включающего в себя дисменорею, диспареунию и собственно боли внизу живота, не связанные с менструацией или половой жизнью, а также болезненность при влагалищном исследовании) начиная со 2-го месяца лечения, а к концу курса лечения интенсивность болевого синдрома снижается в среднем в 4 раза. Однако высокая стоимость и наличие серьезных побочных эффектов аГРГ, связанных с индуцированным тяжелым эстрогендефицитным состоянием (головные боли, раздражительность, сухость кожных покровов, повышение АД, нарушение сна, повышенная потливость, приливы жара, снижение либидо, увеличение массы тела в среднем на 5%, снижение минеральной плотности костной ткани, снижение овариального резерва), обусловили необходимость использования возвратной терапии препаратами заместительной гормональной терапии в наиболее тяжелых случаях, а также предопределили поиск альтернативных препаратов с аналогичной эффективностью. В связи с чем выбор данной терапии на длительный срок является менее приемлем по сравнению с КОК и прогестагенами и поэтому относится к терапии второй линии.
К первой линии терапии эндометриоза и профилактики его рецидивов относят также прогестагены. Механизм действия прогестагенов при эндометриозе неоднозначен и остается предметом обсуждения. Данные препараты благоприятно воздействуют на важнейшие патогенетические звенья эндометриоза в независимости от этиологии. Препараты данной группы являются высокоэффективными в терапии, но их применений должно осуществляться в непрерывном режиме и в достаточно высоких дозах.
Одним из мощных прогестагенов для лечения эндометриоза, на данный момент является левоноргестел-выделяющая внутриматочная система. Данная форма прогестагена представляет широкую возможность с целью лечения, а также профилактикой терапии рецидива старых и появления новых очагов эндометриоза. Согласно последним международным рекомендациям данный препарат относят к терапии второй линии. Появление на нашем рынке перорального прогестагена- диеногеста в «чистом» виде в дозе 2 мг/сут (Визанна) значительно расширяет возможности долговременной медикаментозной терапии эндометриоза. Важно подчеркнуть, что в отличие от других прогестагенов для всех показаний (эндометриоз, контрацепция и заместительная гормональная терапия) применяется одинаковая доза этого прогестагена (2 мг/сут). Учитывая, что препарат диеногест (2 мг/сут) является новым, разрешенным для лечения эндометриоза и самым низкодозированным препаратом. Его отличает мощная прогестагенная активность, уступающая только несторону, а также выраженное антиэстрогенное воздействие на локальном уровне. ДНГ не имеет этинильного радикала и является метаболически нейтральным, что крайне важно для длительной терапии. Надежный антиовуляторный эффект за счет апоптоза гранулезных клеток доминантного фолликула сочетается со слабым центральным эффектом (ингибирование уровня ФСГ и ЛГ) и умеренным снижением уровня системного эстрадиола, что относится к особым преимуществам этого препарата. В многочисленных клинических исследованиях показано, что ДНГ в небольшой дозе (2 мг/сут) успешно купирует боль, связанную с эндометриозом, включая дисменорею, предменструальную боль, диспареунию и диффузную тазовую боль по сравнению с плацебо. По данным объективной оценки интенсивности боли ДНГ продемонстрировал сходную эффективность при прямом сравнении с различными формами аГнРГ. Доказано значимое снижение эндометриоидных очагов на тазовой брюшине по данным rAFS в ходе повторной лапароскопии после проведенного курса лечения ДНГ, в том числе в исследованиях продолжительностью до 52-75 недель. Диеногест также подходит для длительного применения благодаря своему благоприятному профилю безопасности и переносимости
В последние годы в гинекологической практике при лечении заболеваний, сопровождающихся дисфункциональными нарушениями иммунной системы, начали применять цитокиновую и антицитокиновую иммуномодулирующую терапию. Особый интерес представляет применение генно-инженерного (рекомбинантного) препарата интерлейкина-2 (рИЛ-2) - ронколейкина (ООО «БИОТЕХ», Санкт-Петербург), к действию которого восприимчивы различные клетки иммунной системы.
Рекомендовано использование НПВС у пациенток с эндометриозом для купирования болевого синдрома. Данного рода препараты могут быть назначены на короткий срок (до 3 мес.) при отсутствии противопоказаний самостоятельно или в сочетании с терапией первой линии.
Основной терапией ХТБ, ассоциированной с ПЭ, на современном этапе является хирургическая эксцизия и (или) деструкция эндометриоидных очагов, преимущественно лапароскопическим доступом, но по данным second-look лапароскопий через один год после произведенного оперативного лечения только в 25% случаев отмечается регрессия ПЭ, а в 33-42% - персистенция и в 29-45% прогрессирование перитонеального эндометриоза. Через 1-2 года после операции более чем в 20% отмечаются рецидивы ХТБ, количество которых в последующие годы прогрессивно увеличивается, нарастает интенсивность болевого синдрома, а также снижается его восприимчивость к лекарственному воздействию. Поэтому необходимость адъювантной и противорецидивной терапии у данного контингента больных не вызывает сомнений. Наряду с этим при ХТБ, в связи с высокой вероятностью наличия эндометриоза, возможна эмпирическая гормонотерапия (диеногест или диеногест-содержащие КОКи) без оперативного этапа лечения после исключения негинекологических причин боли и объемных образований в брюшной полости с оценкой эффективности лечения в течение трех месяцев. При рецидивах ХТБ повторные операции признаны нецелесообразными и основным методом остается медикаментозная, главным образом, гормонотерапия.
В настоящее время наиболее применяемыми препаратами для лечения ХТБ при ПЭ являются диеногест, диеногест-содержащие КОК и А-ГнРГ. В целом, эффективность диеногеста и диеногест-содержащих КОКов эквивалентна а-ГнРГ, но отсутствие эстрогендефицитных побочных эффектов, имеющихся у а-ГнРГ, обеспечивает возможность длительного применения диеногест-содержащих препаратов.Поэтому диеногест и диеногест-содержащие КОК одобрены как препараты первой линии терапии эндометриоза. КОК оправданы в качестве ингибирующей послеоперационной терапии с целью профилактики рецидивов, причем их эффективность возрастает в режиме непрерывного приема, но неэффективны для лечения рецидивов. А-ГнРГ рекомендуются пациенткам с рецидивами, тяжелыми инфильтративными формами ПЭ и при отсутствии эффекта от прогестинов и КОК. Однако, после отмены а-ГнРГ, как и других гормональных препаратов возникают рецидивы (через 5 лет у 53% больных, а при тяжелых формах - у 73%). Также для лечения болевых симптомов помимо гормонотерапии используют неспецифическую аналгетическую терапию, и при необходимости - коррекцию вегетативных и тревожно-депрессивных расстройств, но информации об их эффективности недостаточно и существуют ограничения в применении. Таким образом, до настоящего времени ни один из предложенных методов лечения не привел к полному регрессу ХТБ при ПЭ и не позволил избежать рецидивов.
Согласно современным подходам, лечение аденомиоза должно преследовать несколько целей: устранение или «облегчение» клинических симптомов заболевания и восстановление репродуктивной функции пациенток. С целью фармакотерапии аденомиоза рекомендованы препараты: прогестины, агонисты гонадотропин-рилизинг-гормона (аГнРГ), левоноргестрелвыделяющая внутриматочная система и нестероидные противовоспалительные средства (НПВС). Учитывая необходимость длительного лечения, при выборе препарата необходимо иметь в виду их эффективность, безопасность и переносимость. В настоящее время появились данные рандомизированного контролируемого исследования, свидетельствующие о лучшей эффективности прогестагенов с целью долгосрочной терапии эндометриоза. Патогенетическое воздействие диеногеста Диеногест относится к прогестагенам четвертого поколения, сочетает в себе свойства производных 19-нортестостерона и прогестерона и, таким образом, характеризуется хорошей переносимостью, отсутствием негативных метаболических эффектов, высокой биодоступностью при приеме внутрь, обладает антиандрогенным и антипролиферативным эффектом, умеренным ингибирующим действием на секрецию гонадотропинов. Воздействие диеногеста в первую очередь связано с индукцией состояния псевдодецидуализации с последующей блокадой пролиферации и атрофией очагов эндометриоза. Кроме того, диеногест воздействует на значительное количество звеньев патогенеза заболевания, а именно: ингибирует экспрессию ферментов ароматазы (фермента, благодаря которому в эндометриоидных очагах поддерживается локальная гиперэстрогения) и циклооксигеназы-2, снижает продукцию простагландинов, нарушает неоангиогенез и активирует апоптоз. Еще одним звеном патогенеза эндометриоза, на которое оказывает воздействие диеногест, является локальная резистентность к прогестерону в очаге, за счет которой также поддерживается гиперэстрогенный фон. Связан этот механизм с недостаточностью фермента 17-β-гидроксистероиддегидрогеназы, функция которого заключается в превращении наиболее активного эстрадиола в менее активный эстрон. В норме этот фермент активируется при взаимодействии прогестерона с прогестероновыми рецепторами типа B. Однако в эндометриоидных очагах экспрессия ПР-B снижена, что, в свою очередь, обусловлено локальным повышением экспрессии прогестероновых рецепторов типа А (ПР-А). Хотя в настоящее время функции изоформ фермента изучены недостаточно, известно, что ПР-А оказывает супрессивное воздействие. Зарубежные коллеги доказали способность диеногеста увеличивать экспрессию ПР-В в очагах эндометриоза, за счет чего также реализуется один из механизмов патогенетического воздействия на заболевание.
Также известно, что клетки эктопированных эндометриоидных очагов выделяют значительное количество цитокинов. Цитокины, в свою очередь, играют роль сигнальных молекул, которые способствуют пролиферации и дифференциации клеток в очаге эндометриоза. Кроме того, они сенситизируют периферические нервные окончания, что в том числе приводит к развитию и прогрессированию симптомов хронической тазовой боли у пациенток. Также в перитонеальной жидкости женщин с эндометриозом значительно повышено содержание фактора некроза опухоли-α (TNFα), который отражаетстепень прогрессирования заболевания и связанного с ним бесплодия, а также может способствовать злокачественной трансформации клеток в очаге. Исследованиями подтверждено снижение секреции интерлейкинов (IL) - IL-6, IL-8, а также TNFα на фоне лечения диеногестом, что отражается на его клинической эффективности. Дополнительным аспектом патогенетической терапии эндометриоза диеногестом является его участие в ингибировании внутриклеточного сигнального пути PI3K/AKT/ mTOR (отвечает за рост и пролиферацию клеток), индукции аутофагии (способ утилизации ненужных клеток или органелл) и, как следствие, активации апоптоза эндометриоидных клеток в эктопированном очаге.
Авторы недавно проведенного проспективного когортного рандомизированного исследования, включавшего 198 участниц с диагностированным эндометриозом, показали равную эффективность гозерелина и диеногеста в отношении снижения выраженности болевых симптомов (хроническая тазовая боль, дисменорея) и профилактики рецидива заболевания. Многие исследователи сделали вывод о предпочтительном назначении диеногеста с целью про-лонгированной терапии (более 6 месяцев), так как терапия агонистами ГнРГ сопряжена с гипоэстрогенными проявлениями, наиболее серьезным из которых является снижение показателя минеральной плотности костной ткани, и не может считаться оптимальной альтернативой с целью долгосрочного лечения аденомиоза. Кроме того, показано, что супрессивная гормональная терапия на протяжении 3-6 месяца перед протоколом ЭКО дает возможность повышения эффективности протокола. При этом частота клинической беременности у пациенток, применяющих диеногест, была достоверно выше аналогичного показателя у пациенток без гормонального лечения и была выше такового у женщин, пользующихся аГнРГ. Вероятно, эффект диеногеста обуславливается не только его влиянием на эктопическую ткань: препарат может оказываеть положительно евоздействие на эутопический эндометрий.
В частности, (А. Hayashi и соавт. 2012) было доказано, что его применение позволяет увеличить соотношение PR-B/PR-A и снизить соотношение ERβ/ERα, в результате чего снижается так называемая «прогестероновая резистентность» эндометрия, свойственная эндометриозу. Возможно, это способствует обеспечению оптимальных условий образования «окна имплантации». Также вполне вероятно, что благодаря более «мягкому» режиму угнетения образования эстрадиола яичниками при помощи диеногеста в сравнении с аГнРГ обеспечиваются оптимальные условия кровоснабжения матки перед планированием беременности.
Довольно большая частота рецидивов эндометриоза, незначительная частота восстановления фертильности и побочные эффекты гормонального лечения вынудили некоторых ученых выработать качественно новые методы противорецедивного лечения эндометриоза. Один из таких методов представлен селективной иммунотерапией. Предполагаемый механизм, которым объясняется имплантация и прогрессивная пролиферация эктопического эндометрия, представлен иммунной дисрегуляцией.
Благодаря расшифровке процессов клеточного и гуморального иммунитета удалось установить и привести характеристику большого числа цитокинов, которые, как оказалось, выступают в роли неотъемлемых модуляторов иммунного ответа.
Связываясь с особыми рецепторами на мембране клеток-мишеней, они воздействуют на процессы хемотаксиса, активации, дифференцировки и пролиферации клеток. Цитокины являются семейством пептидов, к которым примыкают ростовые факторы, факторы некроза опухолей трансформирующие факторы роста, колониестимулирующие факторы, интерфероны, интерлейкины. Продукцию цитокинов клетки осуществляют, только если в организме присутствует антиген. Благодаря этому развивается иммунная реакция, охраняющая постоянную внутреннюю среду организма от всего, что является генетически чужеродным. В связи с этим неудивительно, что применение цитокинов как иммунных средств открывает множество перспектив для клиницистов.
Целесообразное применение разных иммуномодуляторов с целью восстановить функцию иммунной системы - одна из основных задач нынешней медицины. Препарат деринат способствует активизации процессов клеточного и гуморального иммунитета. Иммуномодулирующий эффект обуславливает стимуляция В-лимфоцитов, активация Т-хелперов. Деринат способствует активации неспецифической резистентности организма, оптимизации воспалительных реакций, и иммунному ответу на комплекс бактериальных, вирусных и грибковых антигенов. Способствует стимулированию репаративных и регенераторных процессов, повышению усттойчивости организма к инфекциям, регуляции гемопоэза (нормализует число тромбоцитов, фагоцитов, гранулоцитов, лимфоцитов, лейкоцитов). Имея выраженную лимфотропность, Деринат способствует также стимулированию дренажно-детоксикационной функции лимфатической системы и значительному снижению чувствительности клеток к вредоносному воздействию химиотерапевтических средств и лучевой терапии. Препарат не обладает эмбриотоксическим, тератогенным и канцерогенным действиями, что дает нам возможность принимать в предгравидарной подготовке. После применения дерината отмечена нормализация числа CD4-лимфоцитов, активности каталазы, концентрации IgM, IL-1β, IL-16, IL-8, С3-, С4- и С5-компонeнтов системы комплемента, активности и интенсивности фагоцитоза неeйтрофилов, коррекция концентрации TNFα, IL-2, IL-18, INF-γ, G-CSF, продуктов ПОЛ, кислород зависимой активности нейтрофилов и активности СОД.
Резюмируя приведенные данные литературы, можно сделать заключение о том, что основным резервом, повышения эффективности ЭКО у пациенток с аденомиозом является улучшение имплантационного фактора эндометрия. В связи с этим предгравидарная подготовка больных аденомиозом, в том числе ранних степеней, требует поиска новых комплексных подходов, охватывающих многообразие факторов, способствующих развитию заболевания. Современные представления о характере иммунных нарушений при аденомиозе, предположительно диктуют необходимость введения в комплекс предгравидарной подготовки пациенток к циклу ЭКО адекватной, патогенетически обоснованной, в том числе и иммуномодулирующей терапии.
Тактика ведения пациенток зависит от таких факторов, как репродуктивные планы, возраст, клинические проявления и их тяжесть, стадия эндометриоза и особенности хирургического лечения, переносимость предыдущего лечения, риск побочных эффектов, состояние внутренних органов, свертывающей системы крови и центральной нервной системы, стоимость и предполагаемая длительность терапии. В каждом конкретном случае подход должен быть индивидуальным. Помимо хирургического предложено множество методов медикаментозного лечения, направленных на купирование симптомов заболевания, особенно болевого, и улучшение качества жизни пациенток. Существуют и проблемы терапии: недостаток доказательных данных по применению разных схем лечения и разрыв между руководствами и реальной практикой, например, широкое использование препаратов по незарегистрированным показаниям. Единственного подхода, который был бы идеальным для всех пациенток, не существует. Планирование терапии должно строиться в зависимости от потребностей и предпочтений пациентки. Можно сформулировать основные задачи дифференцированной терапии эндометриоза устранение жалоб, оптимизация соотношения профилей эффективности, безопасности и переносимости лечения, повышение приверженности лечению. Основные методы лечения эндометриоза: хирургический, медикаментозный, сочетанный. Несмотря на внедрение в практику в последние годы современных методов диагностики и лечения, эндометриоз продолжает оставаться причиной большого числа диагностических ошибок, что приводит к распространенному процессу с поражением смежных. Сущность хирургического метода заключается в ликвидации очагов эндометриоза в пределах неизмененных тканей (визуально и пальпаторно). Выбор метода и объем хирургического вмешательства определяются индивидуально в соответствии с локализацией и распространенностью эндометриоидного процесса, вовлечением прямой кишки, мочевого пузыря, а также со стремлением сохранить или восстановить репродуктивную функцию Берлев И. В. Опыт хирургического лечения сочетанных форм эндометриоидной болезни с использованием эндоскопических технологий. Лапароскопическое лечение, несмотря на непрекращающиеся споры, считается "золотым стандартом", поскольку оно менее травматично, реже сопровождается образованием послеоперационных спаек, дает лучшие результаты в сравнении с другими методами терапии бесплодия. Эффективность хирургического лечения эндометриоза, несомненно зависит от радикальности операции. Однако расширение объема операции уменьшает шансы на сохранение специфических функций женского организма. Отмеченное положение является причиной отсрочки операции, что приводит к прогрессированию заболевания, особенно у молодых пациенток, вовлечению в процесс смежных органов, появлению неврологических нарушений, и когда принимается решение об операции, то нередко объем ее становится таким, что речь может идти лишь об избавлении женщин от мучительных страданий и восстановлении работоспособности.
Эффективность противорецидивной терапии подтверждена всеми гинекологическими сообществами, занимающимися изучением эндометриоза. При проведении гормональной терапии следует учитывать, что эндометриоз представляет собой хроническое заболевание с рецидивирующим течением и признаками автономного роста имплантата. Ни один медикаментозный препарат не устраняет морфологический субстрат эндометриоза, оказывая только временное опосредованное влияние на его биологическую активность. В связи с этим современный подход к долгосрочному ведению пациенток с хронической тазовой болью, связанной с эндометриозом, включает не только медикаментозную терапию но и хирургическое лечение, или сочетание этих методов. В основе гормональной терапии лежит снижение уровня эстрогенов, что приводит к уменьшению размеров эндометриоидных образований и частоты рецидивов эндометриоза. В настоящее время для лечения пациенток страдающих СХТБ при эндометриозе наиболее часто используются комбинированные оральные контрацептивы (КОК). Согласно рекомендациям многих ведущих гинекологических обществ препараты данной группы считаются терапией первой линии в случае СХТБ, связанной с ПЭ. Положительными моментами являются: низкая стоимость, возможность длительного и повторного использования, а также контрацептивный эффект, что немаловажно для молодых и сексуально активных женщин. КОК давно и прочно заняли определенную «нишу» в лечении эндометриоза, а именно – купирование дисменореи и прежде всего альгоменореи (эффективность – 60–95%). Для лечения теоретически используется любой монофазный КОК, но желательно, чтобы в нем доминировал прогестагенный компонент. Препаратами выбора являются КОК, содержащие в качестве гестагенного компонента диеногест (диеногеста – 2 мг, этинилэстрадиола – 0,03 мг). Способ применения обсуждается, но многие предпочитают назначать препарат в непрерывном режиме, что является более целесообразным, исходя из основных целей, которые стоят перед гинекологами при лечении ПЭ (уменьшение выраженности болевого синдрома, ликвидация эндометриоидных гетеротопий и профилактика рецидивов), так как у многих женщин в течение 7-дневного перерыва начинается созревание фолликулов и возрастает уровень эстрогенов. По данным P. Vercellini и соавт., КОК после удаления эндометриоидных гетеротопий снижают риск рецидива или удлиняют продолжительность пострецидивного периода.Однако в последнее время появились данные о том, что КОК не купируют должным образом болевой симптом и диспареунию, а их назначение по поводу дисменореи коррелирует с хирургически подтвержденным эндометриозом в последующие годы, а в случае назначения этих препаратов по поводу тяжелой первичной дисменореи – с глубокими инвазивными формами эндометриоза. Хотя КОК используют для лечения эндометриоза в течение многих лет, только в нескольких рандомизированных контролируемых исследованиях (РКИ) проведено сравнение их эффективности с другими медикаментозными методами терапии или плацебо. Ранее было отмечено, что хотя КОК не эффективны для лечения рецидивов эндометриоза, они достаточно эффективны в качестве ингибирующей послеоперационной терапии для профилактики рецидивов, в том числе лечения СХТБ при ПЭ, что было продемонстрировано в систематическом обзоре.
Одним из мощных прогестагенов для лечения ПЭ, на данный момент является левоноргестел-выделяющая внутриматочная система. Данная форма прогестагена представляет широкую возможность с целью лечения СХТБ при ПЭ, а также профилактикой терапии рецидива старых и появления новых очагов эндометриоза. Согласно последним международным рекомендациям данный препарат относят к терапии второй линии. Появление на нашем рынке перорального прогестагена- диеногеста в «чистом» виде в дозе 2 мг/сут (Визанна) значительно расширяет возможности долговременной медикаментозной терапии эндометриоза. Важно подчеркнуть, что в отличие от других прогестагенов для всех показаний (эндометриоз, контрацепция и заместительная гормональная терапия) применяется одинаковая доза этого прогестагена (2 мг/сут). Учитывая, что препарат диеногест (2 мг/сут) является новым, разрешенным для лечения эндометриоза и самым низкодозированным препаратом. Его отличает мощная прогестагенная активность, уступающая только несторону, а также выраженное антиэстрогенное воздействие на локальном уровне. ДНГ не имеет этинильного радикала и является метаболически нейтральным, что крайне важно для длительной терапии. Надежный антиовуляторный эффект за счет апоптоза гранулезных клеток доминантного фолликула сочетается со слабым центральным эффектом (ингибирование уровня ФСГ и ЛГ) и умеренным снижением уровня системного эстрадиола, что относится к особым преимуществам этого препарата. В многочисленных клинических исследованиях показано, что ДНГ в небольшой дозе (2 мг/сут) успешно купирует боль, связанную с эндометриозом, включая дисменорею, предменструальную боль, диспареунию и диффузную тазовую боль по сравнению с плацебо. По данным объективной оценки интенсивности боли ДНГ продемонстрировал сходную эффективность при прямом сравнении с различными формами аГнРГ. Доказано значимое снижение эндометриоидных очагов на тазовой брюшине по данным rAFS в ходе повторной лапароскопии после проведенного курса лечения ДНГ, в том числе в исследованиях продолжительностью до 52-75 недель. Диеногест также подходит для длительного применения благодаря своему благоприятному профилю безопасности и переносимости.Исходя из множественных мировых исследований именно прием диеногеста в дозировке 2 мг. значительно снижает частоту рецидивов в послеоперационном периоде у больных СХБ при ПЭ, по сравнению с другими препаратами.
Относительно высокая частота рецидивов эндометриоза, низкая частота восстановления фертильности и достаточно тяжелые побочные эффекты гормональной терапии заставили ряд исследователей обратиться к разработке качественно новых методов противорецидивной терапии эндометриоза, одним из которых является селективная иммунотерапия.
Таким образом, тактика ведения пациенток зависит от таких факторов, как репродуктивные планы, возраст, клинические проявления и их тяжесть, стадия эндометриоза и особенности хирургического лечения, переносимость предыдущего лечения, риск побочных эффектов, состояние внутренних органов, свертывающей системы крови и центральной нервной системы, стоимость и предполагаемая длительность терапии. В каждом конкретном случае подход должен быть индивидуальным. Поэтому, помимо хирургического лечения, необходимо проведение медикаментозной терапии, которая в свою очередь будет направлена на купирование симптомов заболевания, особенно болевого, и улучшение качества жизни пациенток .Такие проблемы терапии, как недостаток доказательных данных по применению разных схем лечения и разрыв между руководствами и реальной практикой, делает данный вопрос актуальным. В терапии ПЭ должны выделяться основные задачи дифференцированного подхода, а именно устранение жалоб, оптимизация соотношения профилей эффективности, безопасности и переносимости лечения, повы шение приверженности лечению.
Единственного подхода, который был бы идеальным для всех пациенток, не существует. Планирование терапии должно строиться в зависимости от потребностей и предпочтений пациентки.
Традиционным методом лечения эндометриоидных кист яичников является хирургический с последующим консервативным этапом. Существуют различные методики хирургического лечения эндометриоидных кист яичников (дренирование с коагуляцией, цистэктомия, резекция яичников, пункционное склерозирование). Хотя мнение авторов об эффективности и безопасности различных методов оперативного лечения, в том числе с позиции сохранения овариального резерва, остается дискуссионным, предпочтение отдается цистэктомии, особенно у больных с нарушением репродуктивной функции.
В качестве послеоперационной закрепляющей терапии основная роль отводится гормональному лечению: аналогам люлиберина, синтетическим эстроген-гестагенным, гестагенным соединениям, прогестагенам; антипрогестинам. До последнего времени препаратами выбора являлись агонисты ГнРГ, отрицательной стороной которых являются значительные побочные эффекты.На сегодняшний день многочисленными клиническими исследованиями доказана эффективность прогестагена, структурно близкого 19-нортестостерону-диеногеста, терапевтическая ценность которого эквивалентна агонистам-ГнРГ (купирование болевого синдрома, уменьшение количества рецидивов и спаечного процесса, профилактика малигнизации). При этом отмечается отсутствие значимых гипоэстрогенных побочных эффектов, клинически значимых андрогенных эффектов и негативного влияния на уровень липидов, что определяет особую целесообразность длительного применения у пациенток репродуктивного возраста.
Вместе с тем, необходимо отметить, что с точки зрения сохранения овариального резерва проблема требует дальнейшей разработки. Исследованиями показано, что у больных с эндометриоидными кистами яичников, особенно в позднем репродуктивном возрасте, исходно отмечается снижение овариального резерва в связи с нарушением стероидогенеза, дистрофическими процессами в гранулезных и тека клетках фолликулов, изменением состава фолликулярной жидкости, повышенным апоптотическим индексом клеток гранулезы, дегенерацией ооцитов, под воздействием различных неблагоприятных факторов (активные фракции кислорода, оксид азота) на ооциты и фолликулярные клетки. Согласно современным представлениям, нормальное развитие и функционирование репродуктивной системы осуществляется при ее тесном взаимодействии с иммунной и эндокринной системами, в частности, действие гормонов на клеточном уровне реализуется через вовлечение множества пептидных ростовых факторов, среди которых особая роль отводится лимфогемопоэтическим цитокинам, продуцируемым иммунокомпетентными клетками. Присутствующие в тканях яичника клетки иммунной системы являются потенциальными модуляторами функций яичника, и они осуществляют свое регулирующее действие через продукцию цитокинов.
Согласно последним протоколам лечения эндометриоза, не требуется назначения специальных диет, приема пищевых добавок, витаминов и минеральных компонентов. Для уменьшения хронической тазовой боли можно пациенткам порекомендовать йогу, акупунктуру. При наличии у пациентки изменившегося психоэмоционального фона, сексуальных нарушений, возможно направлен ие женщины к смежным специалистам ( медицинскому психологу, врачу – сексопатологу).
Таким образом, тактика ведения пациенток зависит от таких факторов, как репродуктивные планы, возраст, клинические проявления и их тяжесть, стадия эндометриоза и особенности хирургического лечения, переносимость предыдущего лечения, риск побочных эффектов, состояние внутренних органов, свертывающей системы крови и центральной нервной системы, стоимость и предполагаемая длительность терапии. В каждом конкретном случае подход должен быть индивидуальным. Поэтому, помимо хирургического лечения, необходимо проведение медикаментозной терапии, которая в свою очередь будет направлена на купирование симптомов заболевания, особенно болевого, и улучшение качества жизни пациенток.
Единственного подхода, который был бы идеальным для всех пациенток, не существует. Планирование терапии должно строиться в зависимости от потребностей и предпочтений пациентки.
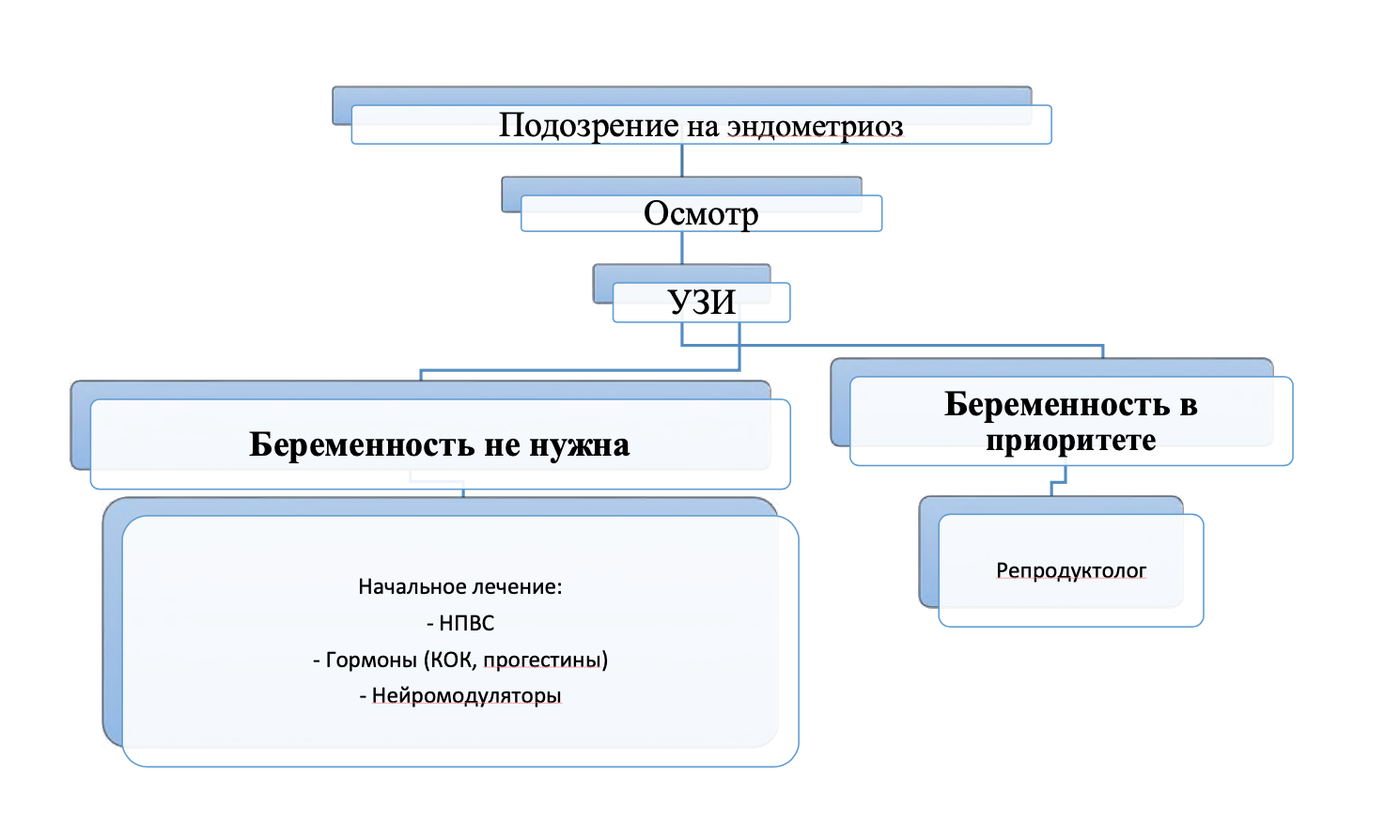
Алгоритм действий врача при подозрении на эндометриоз:
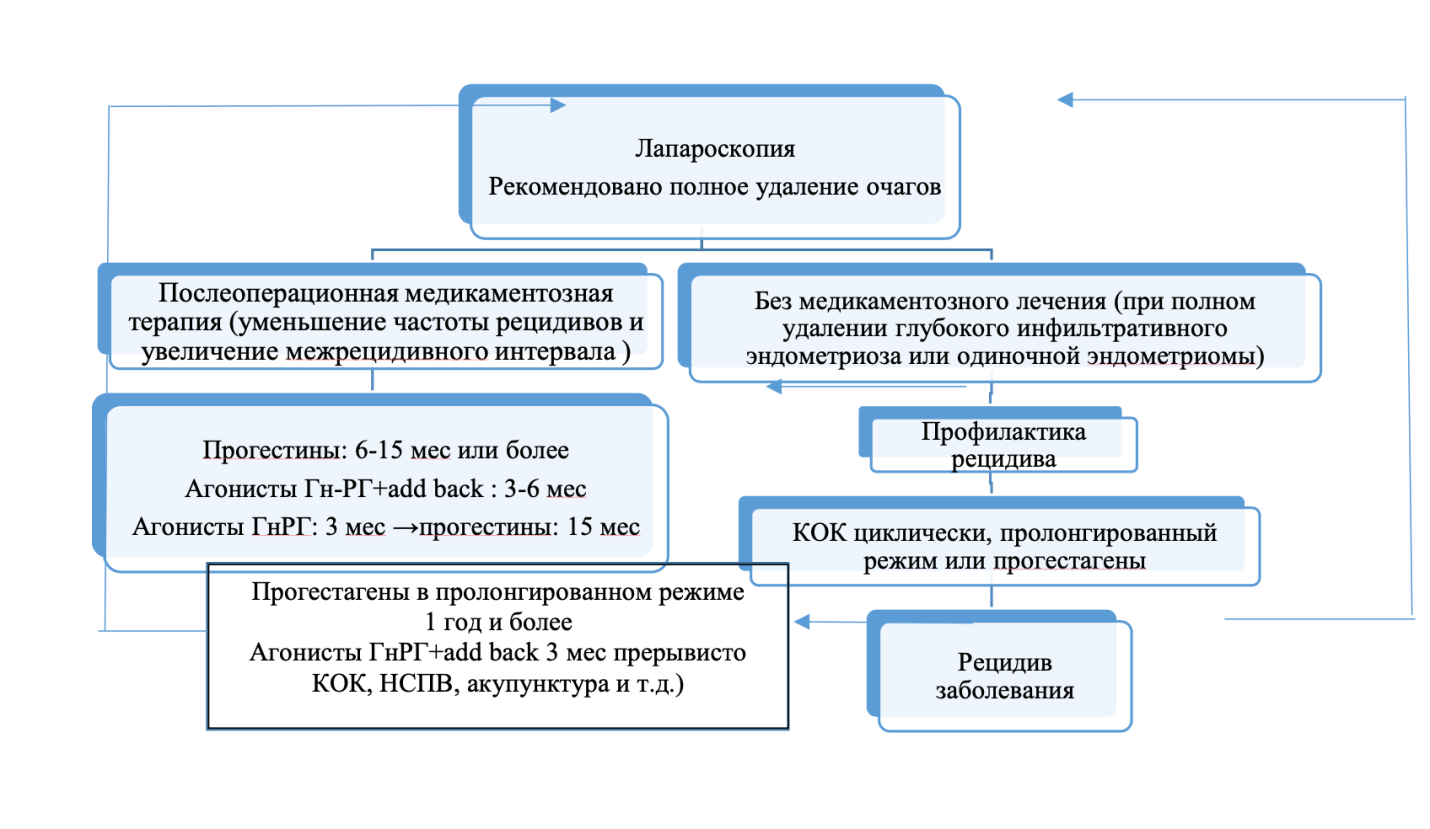
Тактика врача после оперативного лечения эндометриоза.