
- •БИЛЕТ 1
- •1) Стационарные, нестационарные и установившиеся состояния низкотемпературных систем. Открытые и закрытые системы.
- •2) Ожижение газов и газовых смесей. Минимальная работа ожижения в условиях p=const V=const. Сравнение Lmin для различных газов.
- •3) Применение дросселирования в низкотемпературных установках.
- •БИЛЕТ 2
- •2) Охлаждение газообразных веществ в условиях открытой и закрытой термодинамической системы. Минимальная работа, необходимая для охлаждения в условиях P=const и V=const.
- •3) Назначение теплообменных аппаратов. Простейший расчёт теплообменного аппарата.
- •БИЛЕТ 3
- •2) Откачка паров кипящей жидкости, основные отношения и способы реализации. Применение метода откачки, температруная стратификация при откачке.
- •3) Особенности ожижения неона,водорода и гелия.
- •БИЛЕТ 4
- •1) Методика применения принципа сохранения энергии для анализа и расчёта низкотемпературных машин, аппаратов и установок.
- •3) Изотермическое сжатие в компрессоре для различных газов. Соотношение между подведённой работой и отведённой теплотой.
- •БИЛЕТ 5
- •1) Примеры составления энергетического баланса для различных систем и элементов низкотемпературных установок
- •3) Особенности работы регенеративного теплообменного аппарата
- •БИЛЕТ 6
- •1) Второй и третий законы термодинамики. Теорема Нернста. Идеальная тепловая машина.
- •БИЛЕТ 7
- •1) Принцип возрастания энтропии как следствие 2 закона т-д
- •3) Особенности использования детандеров в низкотемпературных установок.
- •БИЛЕТ 8
- •3) Основные типы теплообменных аппаратов
- •БИЛЕТ 9 МЕНЯЙ К ЧЁРТОВОЙ МАТЕРИ БИЛЕТ!!!!
- •БИЛЕТ 10
- •2) Энтропийный баланс низкотемпературных систем. Следствие принципа аддитивности энтропии.
- •3) Изотермическое сжатие в компрессоре для различных газов. Соотношение между проведённой работой и отведённой теплотой.
- •БИЛЕТ 11
- •1) Компенсация возрастания энтропии. Теорема Гюи-Стодолы
- •2) Интегральный эффект дросселирования. Зависимость от температуры и давления
- •3) Способы вычисления приращения энтропии в результате недорекуперации двухпоточного теплоообменника
- •БИЛЕТ 12
- •2) Определение характеристик цикла простого дросселирования. Ожижительный режим.
- •3) Сравнение процессов выхлопа и изоэнтропного расширения
- •БИЛЕТ 13 МЕНЯЙ К ЧЁРТОВОЙ МАТЕРИ БИЛЕТ!!!!
- •БИЛЕТ 14
- •2) Расширение газа в вихревых трубах, особенности рабочего процесса. Оценка эффективности.
- •3) Дроссельные рефрижераторные циклы. Их основные характеристики.
- •БИЛЕТ 15
- •1) Разделение и очистка газов. Технологические процессы и очистки. Минимальная работа разделен газообр смесей
- •2) Дросселирование паров и жидкостей. Применение этих процессов в низотемпер циклах
- •3) Особенности применения детандеров в низкотемп установках
- •БИЛЕТ 16
- •2) Процессы сопровождающиеся понижением температуры в адиабатных условиях
- •3) Определение основных характеристик дроссельного цикла простого дросселирования для рефрижератного режима
- •БИЛЕТ 17
- •2) Типы низкотемпературных циклов.
- •3) Цикл парокомпрессионной холодильной машины и сравнение его с воздушным циклом простого дросселирования. Основные характеристики.
- •БИЛЕТ 18
- •1) Процессы размагничивания парамагнетиков
- •2) Понятие холодопроизводящего процесса в низкотемпературном цикле. Теорема о полной холодопроизводительности цикла.
- •3) Рефрижераторный цикл простого дросселирования с предварительным охлаждением. Схема, изображение на TS диаграмме. Последовательность расчета. Основные характеристики.
- •БИЛЕТ 19
- •1) Термодинамический анализ наиболее распространенных рабочих процессов, сопровождающихся понижением температуры
- •2) Основные холодопроизводящие процессы. Определение полезной и полной холодопроизводительности цикла
- •3) Термоэлектрические процессы
- •БИЛЕТ 20
- •1) Характеристики процессов дросселирования для чистых веществ и смесей
- •2) Понятие теоретического цикла и его сравнение с идеальным. Критерии оптимальности при термодинамическом анализе циклов.
- •3) Ожижительный цикл дросселирования с предварительным охлаждением. Схема, изображение на T-S диаграмме. Последовательность расчета. Основные характеристики
- •БИЛЕТ 21
- •1) Зависимость ah от давления и температуры.
- •2) Анализ процесса выхлопа – свободного выпуска газа из баллона постоянного объёма. Уравнение процесса выхлопа. Изменение температуры и энтальпии в процессе выхлопа. Способы реализации этого процесса.
- •3) Рефрижераторный цикл дросселирования с предварительным охлаждением. Схема, изображение на TS диаграмме. Последовательность расчёта. Основные характеристики.
- •БИЛЕТ 22
- •1) Полная и полезная холодопроизводительность. Виды потерь в низкотемпературных установках и их определение
- •2) Специфика организации низкотемпературных циклов с твердофазными рабочими телами
- •БИЛЕТ 23
- •1) Инверсия дроссель-эффекта. Кривые инверсии.
- •БИЛЕТ 24
- •1) Процесс Дросселирования. Способы реализации дросселирования.
- •2) Безмашинные способы понижения температуры.
- •3)Использование процесса выхлопа в криогенных установках. Машина Мак-Магона-Гиффорда
- •БИЛЕТ 25
- •1) Равновесное адиабатное расширение газа (s-const). Зависимость αs от давления и температуры.
- •2) Основные принципы построения низкотемпературной установки, использующей магнитокалорический эффект.
- •3) Идеальный и реальный циклы парокомпрессионной машины.
- •БИЛЕТ 26
- •2) Термоэлектрическое охлаждение.
- •3) Основные принципы построения низкотемпературных циклов.
- •БИЛЕТ 27
- •1) Изотермическое сжатие в компрессоре идеальных и реальных газов
- •2) Детандирование. Способы организации процессов детандирования. Оценка эффективности расширительных машин.
- •3) Особенности ожижения гелия
- •БИЛЕТ 28
- •2) Производство энтропии в двухпоточном противоточном теплообменнике.
- •3) Особенности ожижения и хранения жидкого водорода.
- •БИЛЕТ 29
- •1) Тепловой эффект дросселирования. Зависимость от температуры и давления.
- •2) Изотермическое сжатие в компрессоре реального газа. Соотношение между работой и теплотой.
- •3) Особенности ожижения неона.
- •БИЛЕТ 30
- •1) Интегральный эффект дросселирования. Зависимость от температуры. Сравнение с интегральным эффектом изоэнтропного расширения.
- •2) Закон сохранения энергии для закрытых систем.
- •3) Особенности процессов дросселирования газов, паров и жидкостей.
2)Производство энтропии в двухпоточном противоточном теплообменнике.
Обычно при расчёте производства энтропии в каком-либо элементе низкотемпературной системы выделяют отдельный необратимый процесс, в котором происходит необратимость и вычисляется производство энтропии, вследствие этой необратимости, считая все остальные процессы в данном элементе обратимыми, поэтому суммарное производство энтропии будет равно сумме всех
необратимых процессов в данном элементе:
∆′ = ∆′
=1
Пример определения энтропии в противоточном теплообменнике.
В данном случае существуют необратимые процессы, являющиеся источником производства энтропии:
11) Неидеальность теплообмена (недорекуперация на концах теплообменника)
12) Гидравлические потери из-за движения потока по каналу теплообменника
13) Теплоприток из окружающей среды 14) Тепловые потери из-за переноса теплоты с тёплого конца
теплообменника к холодному за счёт теплопроводности теплопередающей стенки
15) Неравновесность из-за утечек, перетечек потоков между собой (извне и внутри теплообменника за счёт неплотностей)
3) Особенности ожижения и хранения жидкого водорода.
Обычныйсобе ностиводороджиженприянормальных условиях имеет двемодификации: ортоводород и параводород. Эти двемодификации различаются направлением спина.
При нормальных условия доля ортоводорода 75%, параводорода– 25%, при понижениитемпературы до20Кдоля параводорода растёт до99,8 %.
Орто-пара конверсия.
Процессидётс выделениемтеплоты(706 кДж/кг при температуре менее70К),что больше теплоты испарения. Потерижидкого водорода: 18 %запервыесутки, 40% через100часов. Поэтому приожижении водорода в составожижителя входит орто-параконвертор на платиновых катализаторах, вкоторых теплотаорто-пара конверсии снимается теплотой испаренияжидкого водорода, охлаждающего конвертор.
Особенности хранения
Водород в жидком состоянии находится в узком интервале температур: от точки кипения 20К до точки замерзания 17К, когда он переходит в твёрдое состояние. Если температура поднимается выше точки кипения, водород мгновенно переходит из жидкого состояния в газообразное.
Чтобы не допустить местных перегревов, сосуды, которые заполняют жидким водородом, следует предварительно охладить до температуры, близкой к точке кипения водорода, только после этого можно заполнять их жидким водородом
К резервуарам для хранения жидкого водорода предъявляют ряд требований:
-конструкция резервуара должна обеспечивать прочность и надёжность в работе, длительную безопасную эксплуатацию;
-расход жидкого водорода на предварительное охлаждение хранилища перед его заполнением жидким водородом должен быть минимальным;
-резервуар для хранения должен быть снабжён средствами для быстрого заполнения жидким водородом и быстрой выдачи хранимого продукта.
В криогенных системах хранения жидкого водорода на 1 кг водорода приходится 6 – 8 кг массы криогенного сосуда, а по объёмным характеристикам криогенные сосуды соответствуют хранению газообразного водорода под давлением 40 МПа.
Жидкий водород в больших количествах хранят в специальных хранилищах объёмом до 5 тыс. м3.

БИЛЕТ 29
1) Тепловой эффект дросселирования. Зависимость от температуры и давления.
Тепловой эффект дросселирования.
Рисунок 84 Цикл простого дросселирования.
Рассмотрим процесс
T=const сжатия в компрессоре 1-2, последующим дросселированием 2- 1’,
сопровождающимся понижением температуры, и последующим подводом внешней теплоты qx. 1’-1. Для того, чтобы T понизилась, необходимо, чтобы энтальпия газа в конце процесса T=const сжатия была меньше чем вначале сжатия. Величина разности энтальпий в начале и конце сжатия называется тепловым эффектом дросселирования.В холодильной технике эта величина называется холодопроизводительностью компрессора.
Зависимость теплового эффекта дросселирования от p и T полностью тождественно зависимости интегрального эффекта дросселирования для тех же величин.
Рисунок 80. Зависимость интегрального дроссель эффекта от начального и конечного давления.

Рисунок 81. Зависимость интегрального дроссель эффекта от начального и конечного давления.
2) Изотермическое сжатие в компрессоре реального газа. Соотношение между работой и теплотой.
В механической системе, параметром, который наиболее часто используется для понижения температуры является давление.
Для его увеличения используется изотермическое сжатие в компрессоре.
|
Рисунок 35. Изотермическое сжатие в компрессоре. |
|
В результате изотермического сжатия получаем газ имеющий |
|
энтропию меньше чем в начальном состоянии, что позволяет при |
1 |
дальнейшем изоэнтропном расширении (в идеальном детандере) |
+ сж = 2 + сж |
|
|
получить понижение температуры. |
сж = сж − ( 1 − 2) |
|
0 |
= 1 = 2 => сж = 0( 1 − 2) |

Соотношение между теплотой и работой сжатия зависит от соотношений энтальпий в начале и в конце процесса изотермического сжатия.
Положение изоэнтальп на T-S диаграмме реального газа.
Рисунок 64. Изоэнтальпы азота в T-S координатах. Кривая инверсии проведена пунктиром.
Кривая инверсии делит газовую область на две части:
-выше линии инверсии изоэнтальпа имеет положительный угол наклона с осью энтропий
-ниже линии – отрицательный
-на самой линии угол равен нулю
В области малых давлений <0,1 атм газ ведёт себя как идеальный, и изоэнтальпа совпадает с изотермой.
Поэтому при рассмотрении изотермического сжатия газа в компрессоре и определении соотношения между L и Q необходимо учитывать, где относительно линии инверсии проходит процесс изотермического сжатия.
7) Сжатие ниже линии инверсии.
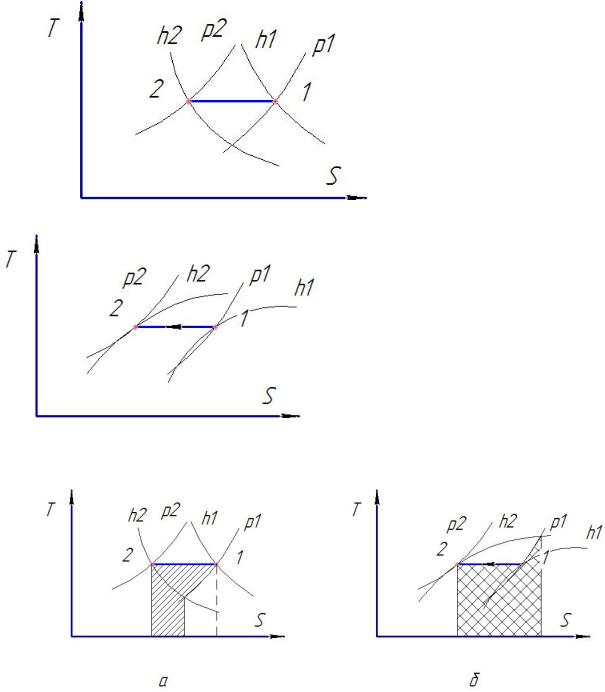
|
Рисунок 65. Сжатие ниже |
|||
|
кривой инверсии. |
− ( 1 |
||
|
h1>h2 сж = 0( 1 |
− 2) |
||
|
|
− 2) |
− 2) |
|
|
сж < сж = 0( 1 |
|
||
инверсии. |
8) Сжатие выше линии |
|||
|
|
|
|
|
Рисунок 66. Сжатие выше |
|
|||
кривой инверсии. |
− ( 1 |
− 2) |
||
h1<h2 |
сж = 0( 1 − 2) |
|||
|
сж > сж = 0( 1 |
− 2) |
|
|
Графическое отображение и сравнение работ при сжатии выше и ниже кривой инверсии.
Рисунок 67. Графическое отображение работ сжатия: а) ниже кривой инверсии; б) выше кривой= = инверсии− .
Рассмотрим случай когда сж сж 1 2 Это возможно в двух случаях:
7.Если газ – идеальный, и изоэнтальпы совпадают с изотермами.
8.Если сжатие началось под кривой инверсии, а закончилось выше кривой инверсии, попав на ту же изоэнтальпу.
