
диссертации / 20
.pdfКАГ 09.12.11.: правый тип ККО. Ствол ЛКА – неровность контуров.
ПМЖВ – диффузно изменена на всем протяжении. Стеноз в проксимальном сегменте около 70%. Стеноз в среднем сегменте 60-70 %. ОВ – диффузно изменена на всем протяжении. Стеноз в среднем сегменте около 75%. ПКА:
диффузно изменена на всем протяжении. Стеноз в проксимальном сегменте около 80%. Стенозы в дистальном сегменте около 75%. Стеноз ЗМЖВ 2
около 75%.
Проведена терапия: нитраты по требованию, ингибитор АПФ, β-
блокатор, антиагрегантная терапия, мочегонные, статины, антагонисты СА-
каналов. Консультирован кардиохирургом, профессором Н. Л. Баяндиным,
рекомендовано АКШ в плановом порядке, взят на учет. Выписан в удовлетворительном состоянии 16.12.2011 г. В последующем больной указывал на прогрессирование одышки, снижение толерантности к нагрузке,
учащение приступов стенокардии. В октябре 2012 г больной госпитализирован в 5 кардиохирургию ГКБ 15 для проведения МКШ ПМЖВ,
АКШ ЗМЖВ, ПКА. Послеоперационный период без осложнений. Выписан с улучшением.
Анализируя данный клинический пример, мы отметили определенные особенности ВСР, гемостаза, их связь и влияние на клиническое течение заболевания. Так, по показателям ВСР отмечается выраженное снижение парасимпатической регуляции: практически отсутствует удлинение meanNN
ночью (+60мс, ЦИ meanNN 0,90), снижение временных показателей SDNNi, RMSSD, pNN50% и в крайней степени выраженная редукция как LF, так и
HF с преобладанием центральных механизмов регуляции ритмом сердца
VLF. Конфигурация скаттерограммы - вытянутая. По показателю симпатовагального соотношения LF/HF отмечалась выраженная симпатикотония днем, и в большей степени ночью, таким образом ЦИ LF/HF
был 0,80, что подтверждает парадоксальную ночную активацию СНС.
Отмечены характерные нарушения и в системе гемостаза – активация
101
внешнего и внутреннего пути свертывания, проявившееся в укорочении ПТВ и АЧТВ ниже референсных значений, повышение уровня фибриногена. Вероятно все это отразилось на клиническом состоянии больного, неэффективности медикаментозной терапии, прогрессировании ХСН и стенокардии, что потребовало оперативного вмешательства.
Клинический пример №2
Пациентка У., 76 лет, поступила в кардиологическое отделение №20
ГКБ №15 10.01.12 г. с жалобами на одышку при ходьбе на 100 м, сухой кашель, отеки ног.
Из анамнеза известно, что с 1990 г. больная страдает артериальной гипертонией с максимальным повышением АД до 200/100 мм рт. ст. Приемлемое по самочувствию АД - 120/80 мм. рт. ст. 16.04. 2011 г. перенесла передний Q-ОИМ, осложненный кардиогенным шоком. В последующем беспокоила одышка при небольшой нагрузке, приступы стенокардии при умеренной нагрузке, пароксизмы фибриляции предсердий.
Принимает постоянную терапию: ингибитор АПФ, β-блокатор, антиагрегант, диуретик, сердечный гликозид. С конца декабря 2012 г отмечает ухудшение состояния – снизилась толерантность к нагрузке, усилилась одышка. Госпитализированна для подбора адекватной терапии. Перенесенные заболевания: язвенная болезнь 12-ти желудка, острое нарушение мозгового кровообращения (ОНМК) в 2006 г. В детстве - пневмония. Аллергоанамнез без особенностей. Профессиональный анамнез: пенсионерка, инвалид II
группы по ССЗ.
Объективно: состояние тяжелое. Сознание ясное. Положение на момент осмотра ортопноэ, ночью принимает возвышенное положение и просыпается в связи с одышкой. Нормостенического телосложения. ИМТ 25,0 кг/м2. Кожные покровы бледные, сухие, акроцианоз. Периферические лимфоузлы не увеличены. Умеренные отеки ног. Костно-мышечная система – без
102

видимых деформаций. Щитовидная железа не увеличена. ЧДД 22 в мин.
Перкуторно – легочный звук. Дыхание везикулярное, проводится во все отделы. Хрипы – влажные мелкопузырчатые в нижних отделах с 2 сторон.
Патологическая пульсация – нет. Границы относительной сердечной тупости расширены: левая + 1 см. от левой средне-ключичной линии в 5 м/р. АД –
130/80 мм рт. ст. Тоны сердца ритмичные, ослаблен I тон в V, IV точке аускультации, систолический шум на верхушке сердца. ЧСС 84 уд. в мин.
Живот мягкий, безболезненный. Печень + 3 см из под края реберной дуги.
Симптом поколачивания (-) с обеих сторон. Стул и диурез не нарушены.
Очаговой неврологической симптоматики нет.
Оценка по ШОКС – 8 баллов. Дистанция, пройденная в ТШХ – 225 м.
ЭКГ при поступлении: ритм синусовый, правильный с ЧСС 84 в мин.
Электрическая ось сердца отклонена влево. Рубцовые изменения передней стенки ЛЖ – патологический QS, -Т в V1-V3.
Диагноз клинический:
Основное заболевание: ИБС. Стенокардия напряжения 2 ФК.
Постинфарктный кардиосклероз. Атеросклероз коронарных артерий.
Гипертоническая болезнь 3 стадии, риск ССО – 4.
Осложнения основного заболевания: ХСН III ФК по NYHA.
Пароксизмальная форма фибриляции предсердий
Сопутствующие заболевания: Язвенная болезнь 12-ти перстной кишки,
ремиссия. ЦВБ. Хроническая ишемия головного мозга. ОНМК в 2006 г.
Данные обследования:
Общеклинический анализ крови: HCT 0,36 , PLT 228*10(9)/л, MPV 8,2
фл
Развернутая коагулограмма: фибриноген 1,36 г/л, АЧТВ 23,7 с, ПТИ
58,9%, ПТВ 15,2 с, спонтанная агрегация тромбоцитов – 1,32 ед.,
индуцированная 0,5 мкМоль АДФ агрегация тромбоцитов – 2,09 ед,
индуцированная 5,0 мкМоль АДФ агрегация тромбоцитов – 24%
103

ЭХО-КГ 13.01.12.: Увеличение левых полостей ЛП 4,52 см., ЛЖ - КДР
7,28 см, КСР 6,15 см, ПП 3,66 см, ПЖ 2,88 см, МЖП 0,76-0,5 см, ЗСЛЖ 0,96
см, митральная регургитация III ст., аортальная – 1 ст., трикуспидальная I-II
ст. ФВ 19%. ДДЛЖ II типа. Истончение миокарда передне-перегородочной области. Акинез до дискинеза передне-перегородочной области, верхушки,
боковой стенки ЛЖ. Аорта уплотнена, расширена в восходящем отделе до 4,3
см. Пристеночный тромб в области верхушки сердца Рентгенография легких от 10.01.2012 г – тень сердца расширена в
поперечнике за счет левых отделов. Признаки венозного застоя в легких Ультразвуковое исследование (УЗИ) брюшной полости от 13.01.2012 г –
застойное полнокровие печени, селезенки.
КАГ 27.01.12.: правый тип ККО. ПКА и ЛКА отходят одним стволом от правого коронарного синуса. ПНА – стенозы в проксимальной трети 90%,
средней трети – 55%. ОВ – стеноз в средней трети 85%, ПКА – стеноз в средней трети 30%. ФВ 19,4%.
Суточное ХМ ЭКГ 30.11.11.: за время мониторирования зарегистрирован синусовый ритм со ср. ЧСС 64 в мин. (53-76). Редкие изолированные НЖЭС – 56, изолированные мономорфные ЖЭС – 214. Пауз нет. Достоверной ишемической динамики нет. Данные ВСР указаны на рис. 2
104
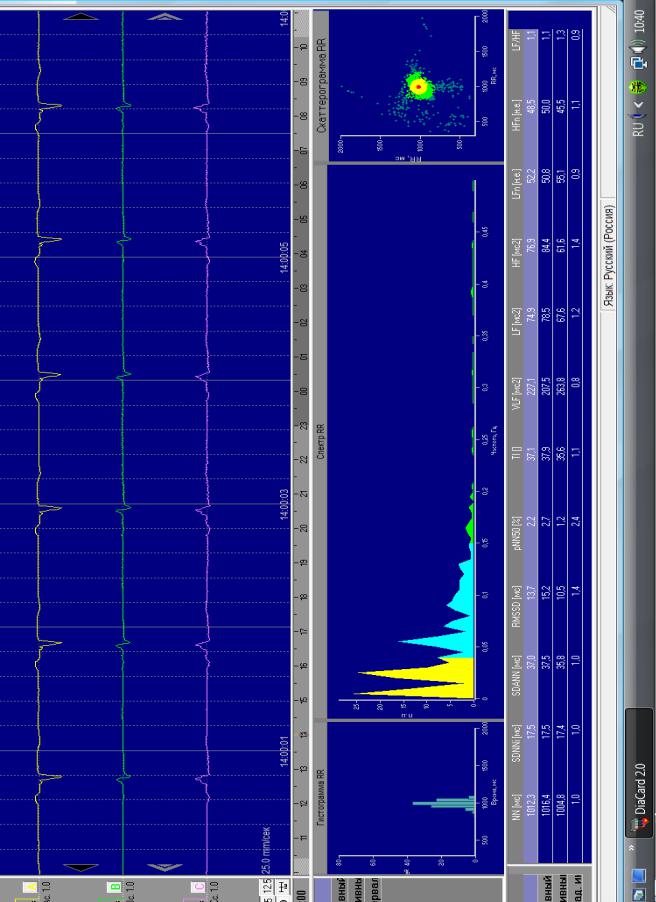
рис. 2 Показатели ВСР у больной У. из клинического примера №2
105
Проведена терапия: ингибитор АПФ, β-блокатор, антиагрегантная терапия, мочегонные, статин. Консультирована кардиохирургом,
профессором Н. Л. Баяндиным, рекомендовано АКШ в плановом порядке,
взята на учет. Выписана с улучшением 3.02.2012 г. После выписки через некоторое время больная вновь стала отмечать прогрессирование одышки,
снижение толерантности к нагрузке, госпитализировалась повторно в 8
кардиологическое отделение ГКБ 15, где проводилась консервативная терапия. От оперативного лечения больная отказалась. Выписалась с небольшим улучшением. 24.09.2012 дома произошла биологическая смерть,
на вскрытии диагноз, выставленный в ГКБ 15 подтвержден, причина смерти
–декомпенсация ХСН.
Вданном клиническом примере мы отметили в максимальной степени выраженное снижение всех показателей временного и спектрального анализа ВСР, точечная скаттерограмма и узкая гистограмма распределения RR-
интервалов подтверждали стабилизацию сердечного ритма, которая является неблагоприятным вариантом нарушения ВСР. Отмечалась псевдонормализация симпатовагального соотношения LF/HF, которая произошла в результате одинаковой редукции как LF, так и HF, однако сохранялась парадоксальная ночная активация СНС - ЦИ LF/HF 0,90. В
коагулограмме отмечается характерная для поздних стадий ИБС коагулопатия потребления – удлинение ПТВ и снижение ПТИ, фибриногена,
указывающее на повышенное потребление прокоагулянтов при ограниченном их синтезе измененной застойными явлениями ткани печени.
В то же время отмечалось характерное для больных с прогрессированием ИБС укорочение АЧТВ. Таким образом, у данной больной отмечались практически все признаки неблагоприятного прогноза заболевания, а
снижение относительного вклада СНС в ВСР сопровождалось снижением прокоагулянтного потенциала крови, реализуемого внешним путем свертывания (удлинение ПТВ, снижение ПТИ)
106
ГЛАВА 4. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
В последнее время имеется тенденция повышения интереса ко всем биоритмологическим процессам - не только к изменчивости ритма сердца,
артериального давления, но и флюктуации нейродинамических процессов,
суточному ритму гормонального фона и т.д. По мнению Баевского Р.М.,
«…изучение ВСР следует рассматривать как стимул к дальнейшему развитию исследований вариабельности физиологических, биохимических и других показателей с целью углубления представления о жизни как о движении материи во времени и пространстве» [3]. Целостная картина регуляции динамических процессов организма и особенности таковой при адаптации позволила бы приблизиться к пониманию общей патофизиологии.
ВСР как один из биоритмологических процессов на современном этапе вызывает несомненно большой интерес у кардиологов; огромное число исследований доказывает ценность данного метода для оценки тяжести заболевания, эффективности проводимого лечения и прогноза заболевания
[15,19,50,64,108]. Не остается сомнений в том, что снижение общей вариабельности ритма резко ухудшает прогноз у больных ИБС, в том числе за счет повышения у данной категории больных риска внезапной смерти
[Wolf MM, Varigos GA, Hunt D, 1978; Kleiger RE, Miller JP, Bigger JT et al. 1987; Bigger JT Jr, Fleiss JL, Steinman RC et al. 1992;]. По прогностической ценности у этой категории больных ВСР сравнима с оценкой фракции выброса левого желудочка, в то же время оставаясь независимым фактором прогноза. Изучены изменения в ВСР у больных артериальной гипертензией
[Guzzetti S, Dassi S, Pecis M et al., 1991], хронической сердечной недостаточностью [Kienzle MG, Ferguson DW, Birkett CL et al., 1992],
дилатационной кардиомиопатией [Binkley, 1991], у больных с нарушениями ритма [Huikuri, 1992; Vybrial, 1993], пролапсом митрального клапана
[Marangoni, 1993], перенесших трансплантацию сердца [Axelopoulos, 1988; Sands, 1989]. По ВСР можно судить о преобладании того или иного звена
107
ВНС, а соответственно и прогнозировать развитие нежелательных эффектов гиперактивации СНС либо ПСНС.
При ИБС одним из ведущих патогенетических звеньев является длительная патологическая активация СНС как компонента нейрогуморальной регуляции [21]. Науке известны не только висцеральные функции СНС, но и влияние этого звена ВНС на параметры гемостаза. Так или иначе затрагиваются все звенья свертывающей, противосвертывающей и фибринолитической системы крови [181,183,184,197]. Зарубежные авторы интересуются возможностью прогнозирования нарушений гемостаза с помощью ВСР, однако исследования пока не распространились на больных ХСН на фоне ИБС, либо рассматриваются изолированные показатели ВСР и гемостаза [102,142,143,170].
Целью нашего исследования было определить связь между ВСР и показателями гемостаза у больных ИБС, осложненной ХСН. Для достижения поставленной цели мы последовательно изучили особенности ВСР,
показателей гемостаза у данной категории больных, а затем рассмотрели их связь и влияние на клиническое течение заболевания.
В большинстве литературных источников указывается на снижение таких показателей ВСР как SDNN, SDNNi, HF, LF, VLF при ХСН на фоне ИБС. При этом авторы отмечают, что снижение HF происходит в большей степени, чем LF и VLF, что дает сохранение повышенного индекса симпатовагального баланса LF/HF. В нашем исследовании мы сравнивали больных ХСН, осложнившей течение ИБС, с больными АГ, не страдающими ИБС. В обеих группах отмечалась симпатотония по основным показателям спектрального анализа ВСР, более выраженная у больных контрольной группы, однако такая особенность отмечалась лишь за счет дневного показателя LF/HFд: в контрольной группе он был достоверно выше - 4,0±1,7
против 2,3±1,3 в основной группе, p<0,001, в то же время ночью этот показатель был недостоверно выше у больных основной группы 2,6±1,7
108
против 2,4±0,7, p>0,05. Наряду с симпатотонией, основная группа отличалась достоверным и значимым снижением активности парасимпатического звена ВНС, что можно проследить по таким показателям, как суточный SDNNi
(37,2±12,6 мс против 53,3±11,6 мс, p<0,01), дневной SDNNiд (35,1±11,9 мс против 50,8±12,1 мс, p<0,01), ночной SDNNiн (41,4±16,0 мс против 56,6±15,9
мс, p<0,01); суточный pNN50% (4,8±4,7 % против 8,3±5,8 %, p<0,05) и
ночной pNN50%н (6,5±7,5% против 12,4±8,5%, p<0,01).
Мы получили значимое и достоверное снижение волновой активности сердечного ритма практически по всем абсолютным показателям спектрального анализа. Суточные, дневные и ночные показатели VLF, LF, HF
были практически в 2 раза меньше у больных ИБС на фоне ХСН в сравнении с больными контрольной группы. Общая мощность спектра TP за сутки при этом составила 1936,6±1264,2 мс в основной группе против 3690±1994 мс в контрольной (p<0,01). Необходимо все же отметить, что несмотря на сохранение симпатикотонии у больных ХСН, осложнившей течение ИБС на фоне АГ, в сравнении с группой контроля, включившей больных с АГ без ИБС, маркеры парасимпатической активности за сутки были выше у основной группы за счет дневных показателей. Так, индекс симпатовагального баланса LF/HF был ниже у больных основной группы – в
среднем за сутки LF/HF составил 2,5±1,4 против 3,3±1,2 в контрольной группе (p<0,05), такая разница полностью была обусловлена более низким дневным показателем LF/HFд в основной группе 2,3±1,3 против 4,0±1,7 в
контрольной группе (p<0,01), в то время как ночью данные различия нивелировались. За сутки относительный вклад быстроволнового компонента
HFn составил 37,4±9,3 н.ед. в основной группе против 32,5±6,3 н.ед. в
контрольной группе (p<0,05), и эта закономерность была обусловлена изолированным повышением относительного вклада именно дневного HFnд
– 37,0±9,2 н.ед. против 28,5±6,4 н.ед. (p<0,01), в то время как ночной показатель HFnн был одинаков у обеих групп.
109
При анализе циркадных изменений выявлена интересная особенность – несмотря на то, что симпатотония отмечалась в обеих группах, в основной группе ночью не происходило адекватного прироста активности ПСНС, и
индекс LF/HF был выше, чем днем. Эту тенденцию наиболее отчетливо отражает ЦИ LF/HF, который в основной группе составил 1,0±0,5 , а в контрольной группе - 1,7±0,6, p<0,01. Учитывая литературные данные о том,
что наибольшее число сердечно-сосудистых катастроф происходит в ночные и раннее утренние часы, мы выдвинули предположение, что возможно такая особенность обусловлена нарушением циркадности симпатовагальных взаимодействий при ИБС.
Ранее опубликованные результаты других исследований говорят о снижении абсолютных спектральных компонентов с прогрессированием ХСН [15]. В нашем исследовании при анализе особенностей ВСР у больных с разным ФК ХСН, мы отметили недостоверную тенденцию уменьшения абсолютных спектральных показателей ВСР, причем показатели активности ПСНС были минимальны у больных ХСН ФК IV (212,2±161,3 мс), и у этих же больных показатели активации СНС имели разнонаправленные изменения за сутки – днем отмечалось их снижение (LFд минимально до 298,73±278,2
мс у больных ХСН ФК IV), а ночью – наоборот, повышение (LFн
максимально до 746,1±879,0 мс у больных ХСН ФК IV). Таким образом с увеличением ФК ХСН, нарушения циркадности вегетативной регуляции могут быть более выраженными.
Анализируя особенности клинического течения ИБС при наличии маркеров активации СНС, мы отметили, что повышение суточного LFn>60
н.ед. отмечалось достоверно чаще у больных, перенесших в анамнезе ОИМ - 78,0% (n=32) против 52,3% (n=11), p<0,01. Это согласуется с результатами других исследований, где симпатотония наблюдалась у больных, перенесших ОИМ [1]. Malliani A. отмечает, что это может быть вызвано усиленной афферентной импульсацией механически растяженных симпатических
110
