Справочники / Репетитор по химии - Белов Н.В
..pdf
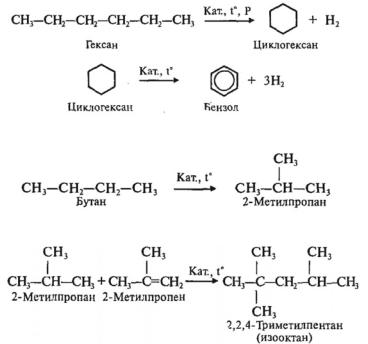
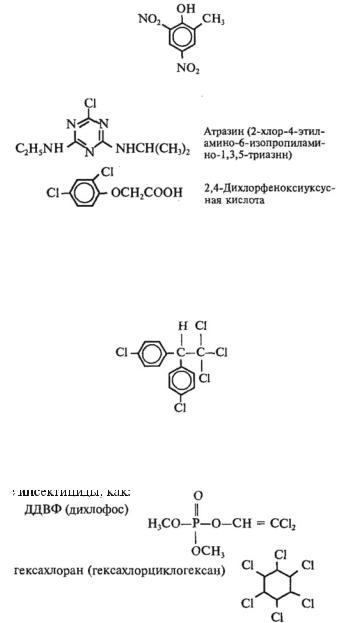
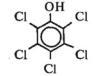
3. Фунгициды — вещества для борьбы с грибковыми болезнями растений. В качестве фунгицидов используют различные антибиотики, сульфаниламидные препараты. Одним из наиболее простых по химической структуре фунгицидов является пентахлорфенол:
Большинство пестицидов обладает отравляющими свойствами не только в отношении вредителей и возбудителей болезней. При неумелом обращении они могут вызвать отравление людей, домашних и диких животных или гибель культурных посевов и насаждений. Поэтому пользоваться пестицидами необходимо очень осторожно, строго соблюдая инструкции по их применению.
С целью минимизации вредного воздействия пестицидов на окружающую среду следует:
1.Применять вещества с более высокой биологической активностью и соответственно вносить их в меньшем количестве на единицу площади.
2.Применять вещества, которые не сохраняются в почве, а разлагаются на безвредные соединения.
3.Применять прогрессивные методы нанесения пестицидов на растения, включая электростатические методы, когда капли (туман) будут садиться только на растения, но не на почву.