
Підручники з Хімії / Хімія 9 клас / Ярошенко Хімія 9 клас. 2017
.pdf


§ 38. |
|
|
|
|
|
|
|
КРОХМАЛЬ І ЦЕЛЮЛОЗА — НАЙПО- |
|
|
|
|
|
||
|
Опанувавши матеріал |
|
|||||
ШИРЕНІШІ ПОЛІСАХАРИДИ У ПРИРОДІ. |
|
|
|||||
|
параграфа, ви зможете: |
|
|||||
Це природні полімери, склад яких передається |
|
|
|||||
розрізняти за складом крох- |
|
||||||
однаковою загальною формулою (С Н |
О ) . На |
|
|||||
6 10 |
5 n |
|
маль, сахарозу, глюкозу; |
|
|||
крохмаль багаті бульби картоплі, зерна злако- |
|
|
|||||
порівнювати крохмаль і це- |
|
||||||
вих рослин. Оболонки рослинних клітин утворе- |
|
||||||
ні із целюлози. Вона є своєрідним скелетом рос- |
|
люлозу; |
|
||||
характеризувати склад і фі- |
|
||||||
лин, надає їхнім тканинам механічну міцність. |
|
||||||
Тому целюлоза становить основу стовбурів дерев |
|
зичні властивості крохмалю |
|
||||
|
й целюлози; |
|
|||||
(50 % і більше), рослинних волокон. Понад 90 % |
|
|
|||||
складати молекулярні фор- |
|
||||||
вмісту коробочок рослини бавовнику припа- |
|
мули крохмалю й целюлози; |
|
||||
дає на целюлозу. Великим є вміст целюлози у |
визначати дослідним шля- |
|
|||||
стеблах конопель, тому наші предки здавна ви- |
|
хом крохмаль. |
|
||||
рощували коноплі, з яких за спеціальною тех- |
|
|
|
|
|
||
|
|
|
|
|
|||
нологією виготовляли пряжу, а вже з неї шили |
|
|
|
|
|
||
полотняний одяг, робили вітрила кораблів тощо. |
|
|
а |
||||
У ХІХ ст., невдовзі після завезення картоплі з |
|
||||||
|
|
|
|
||||
американського континенту до України, українці |
|
|
|
|
|||
навчилися виділяти з неї крохмаль і вживати його |
|
|
|
|
|||
в їжу у вигляді молочного чи фруктового киселю, |
|
|
|
|
|||
застосовувати для накрохмалювання тканин. Під- |
|
|
|
|
|||
крохмалена тканина не лише цупка, а й краще за- |
|
|
|
|
|||
хищена від глибокого проникнення в неї бруду, її |
|
б |
|||||
легше прати. |
|
|
|
||||
|
|
|
|
|
|
||
ВІДМІННОСТІ У ВЛАСТИВОСТЯХ КРОХМА- |
|
|
|
|
|||
ЛЮ ТА ЦЕЛЮЛОЗИ. Порівняння порошку крохма- |
|
|
|
|
|||
лю й вати, яка майже на 98 % складається із целю- |
|
|
|
|
|||
лози, переконливо доводить, що це різні речовини, |
|
|
|
|
|||
хоча вони мають однакову загальну формулу. Чим |
|
|
|
|
|||
зумовлена відмінність між крохмалем і целюлозою? |
|
|
|
|
|||
По-перше, ступенем полімеризації — у целюлози |
|
|
|
|
|||
він значно більший. Тому відносна молекулярна |
|
|
|||||
|
в |
|
|||||
маса целюлози теж більша. По-друге, просторовою |
|
|
|
|
|||
Мал. 49 |
|||||||
будовою структурної ланки. По-третє, будовою по- |
|||||||
лімерного ланцюга — у целюлози він лише лінійний |
Будова крохмалю |
||||||
(мал. 49, в), тоді як у крохмалю є дві форми ланцю- |
та целюлози: |
||||||
га — пряма (10–20 % макромолекул) (мал. 49, а) та |
а, б — схеми лінійної та роз- |
||||||
розгалужена (80–90 % макромолекул) (мал. 49, б). |
галуженої молекул крохмалю; |
||||||
|
|
|
|
||||
Розгалужена будова молекул крохмалю не дає
в — лінійні молекули
змоги виготовляти з нього нитки. Целюлоза підда-
целюлози
183





§ 39.
|
На початку теми ви довідалися про те, що |
|
Опанувавши матеріал |
||
до складу органічних речовин може входити і |
||
параграфа, ви зможете: |
||
Нітроген. Такими речовинами є білки та амі- |
||
розрізняти за складом білки; |
нокислоти. За цією ознакою вони належать до |
|
характеризувати склад і фі- |
нітрогеновмісних органічних сполук. |
|
зичні властивості білків; |
АМІНОЕТАНОВА КИСЛОТА ЯК ПРЕД- |
|
обґрунтовувати біологічну |
||
СТАВНИК АМІНОКИСЛОТ. З молекулярної |
||
роль амінокислот і білків; |
||
формули цієї речовини С2Н5О2N можна довіда- |
||
дізнатися про якісні реакції |
||
тися лише про її кількісний та якісний склад, |
||
на білки. |
||
зробити висновок про те, що це складна нітро- |
||
|
||
|
||
|
геновмісна органічна сполука. Напівструктурна |
та структурна формули дають змогу уявити порядок сполучення атомів у карбоновому ланцюгу і вказують на наявність двох груп атомів — карбоксильної — СООН та аміногрупи — NH2.
аміноетанова кислота
Аміноетанову кислоту можна розглядати як етанову, у карбон-карбо- новому ланцюзі якої один атом Гідрогену заміщений на аміногрупу. Вона є групою, яка присутня в молекулах представників деяких класів органічних сполук, у тому числі й амінокислот.
Аміноетанова кислота — перший і найпростіший представник амінокислот.
Уживій природі найбільше значення мають амінокислоти, у яких аміногрупа розміщена біля першого після карбоксильної групи атома
Карбону. Кислоти з таким розміщенням груп у молекулі дістали назву альфа-амінокислот (позначається -амінокислота). Вони беруть участь в утворенні білків.
Розглянемо структурну формулу амінокислоти, яку ще називають аланін.
Уїї молекулі аміногрупа також розташована біля першого після карбоксильної групи атома Карбону. Як вам відомо з біології, ця амінокислота входить до складу багатьох білків.
188


 Дослідним шляхом установіть, чи виявляє глюкоза спільну з гліцеролом хімічну властивість — взаємодію з купрум(ІІ) гідроксидом.
Дослідним шляхом установіть, чи виявляє глюкоза спільну з гліцеролом хімічну властивість — взаємодію з купрум(ІІ) гідроксидом. Обчисліть масову частку Карбону та відношення мас елементів у сахарозі.
Обчисліть масову частку Карбону та відношення мас елементів у сахарозі.
 Якісною реакцією на крохмаль є взаємодія з розчином йоду. Утворюється сполука, що має характерне синє забарвлення.
Якісною реакцією на крохмаль є взаємодія з розчином йоду. Утворюється сполука, що має характерне синє забарвлення. Дослідіть розчинність крохмалю у воді кімнатної температури. Крохмаль помістіть на дно хімічного стакана, вилийте в нього воду та перемішайте речовини скляною паличкою. Після перемішування залиште су-
Дослідіть розчинність крохмалю у воді кімнатної температури. Крохмаль помістіть на дно хімічного стакана, вилийте в нього воду та перемішайте речовини скляною паличкою. Після перемішування залиште су- Виготовте крохмальний клейстер.
Виготовте крохмальний клейстер. Проведіть взаємодію крохмального клейстеру з йодом.
Проведіть взаємодію крохмального клейстеру з йодом. Проведіть взаємодію порошку крохмалю з йодом.
Проведіть взаємодію порошку крохмалю з йодом. Проведіть випробування білого хліба та сирої картоплі на наявність у них крохмалю.
Проведіть випробування білого хліба та сирої картоплі на наявність у них крохмалю. Розробіть план добування крохмалю з бульб картоплі в домашніх умовах та реалізуйте його практично.
Розробіть план добування крохмалю з бульб картоплі в домашніх умовах та реалізуйте його практично. Назвіть формулу та відомі вам фізичні властивості крохмалю та целюлози.
Назвіть формулу та відомі вам фізичні властивості крохмалю та целюлози. За допомогою яких якісних реакцій можна розпізнати: а) глюкозу; б) сахарозу; в) крохмаль?
За допомогою яких якісних реакцій можна розпізнати: а) глюкозу; б) сахарозу; в) крохмаль? Оцініть значення деревини у природі та господарській діяльності людини.
Оцініть значення деревини у природі та господарській діяльності людини.
 одна чи кілька аміногруп — NH
одна чи кілька аміногруп — NH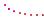 вості й кислоти, й основи, тобто виявляють амфотерні властивості.
вості й кислоти, й основи, тобто виявляють амфотерні властивості.